氨测定过程中质量保证措施
2018-05-11张静
张 静
(山西省环境监测中心站,山西 太原 030027)
氨是室内空气污染的重要组成物质,建筑施工混凝土中加入的含有尿素的防冻剂可以释放氨,进入室内空气中;室内使用的板材制品,有的含有脲醛树脂黏合剂,在室温条件下缓慢释放氨,进入室内空气中;生物性废弃物,如粪便、尿、人呼出气和汗液,也不同程度地释放氨气[1]。
氨是无色而具有刺激性气味的气体,以气体形式吸入肺泡,与血红蛋白结合,破坏运氧功能;氨是一种碱性物质,对动物或人体的上呼吸道有刺激和腐蚀作用,使组织蛋白变性,使脂肪皂化,破坏细胞膜结构,减弱人体对疾病的抵抗力。尽管文献[2]详细介绍了氨测定纳氏试剂分光光度法的原理及操作步骤,但在实际工作中的情况较为复杂。由于空气中普遍存在氨,所以氨的监测分析过程,包括采样、运输、分析过程都要严格控制。根据日常监测的工作经验,本文将上述可能影响测定结果的步骤进行了总结,以期更好地指导实际工作,保证出具合格有效的数据[2-3]。
1 方法原理
用硫酸溶液吸收的氨,在碱性条件下与纳氏试剂反应生成黄棕色络合物。该络合物的色度与氨的含量成正比,在420nm波长进行分光光度测定。
2 仪器与试剂
2.1 仪器
721分光光度计。
2.2 试剂
吸收液:0.01mol/L硫酸,临用现配。
纳氏试剂:溶解17g氯化汞于30mL水中,另将3.5g碘化钾溶于10mL水中,搅拌下将氯化汞溶液慢慢加入碘化钾溶液中至形成红色不溶的沉淀为止。然后,加入60mL 20g/L氢氧化钾溶液及剩余的氯化汞溶液,暗处静置24h。倾出上清液,储于棕色瓶中,用橡皮塞塞紧,避光保存。
酒石酸钾纳溶液:称取50g酒石酸钾钠(KNaC4H4O6·4H2O)溶于100mL水中,加热煮沸以除去氨,放冷,定容至100mL。
标准储备液1.00mg/mL:称取 0.314 2g经105℃干燥1h的优级纯氯化铵(G.R.)溶于水中,移入1 000mL容量瓶中,稀释至标线。此溶液每毫升含1.00mg氨氮。
标准使用液20.00μg/mL:吸取5.00mL氨标准储备液于250mL容量瓶,稀释至标线,摇匀,临用现配。
无氨水经实验证明,新制的蒸馏水可满足实验要求。
3 结果与讨论
3.1 标准曲线的绘制
吸取标准溶液0.00、0.10、0.30、0.50、0.70、1.00、2.00mL,在 各 管 中 分 别 加 入 酒 石 酸 钾 钠0.5mL,摇匀。再加入纳氏试剂0.5mL,摇匀。放置10min后,在420nm下,用1cm比色皿,以水作参比,测定各管的吸光度,测定曲线见第46页表1。
3.2 实验用水的影响
本实验室采用蒸馏水集中制备供应系统,保证了实验用水新鲜,避免了因存放过程中吸收氨引起的空白增高。实验中用每天新制的蒸馏水与超纯水进行连续7d的对比,结果见第46页表2。表明新制的蒸馏水可以满足要求。

表1 测定曲线
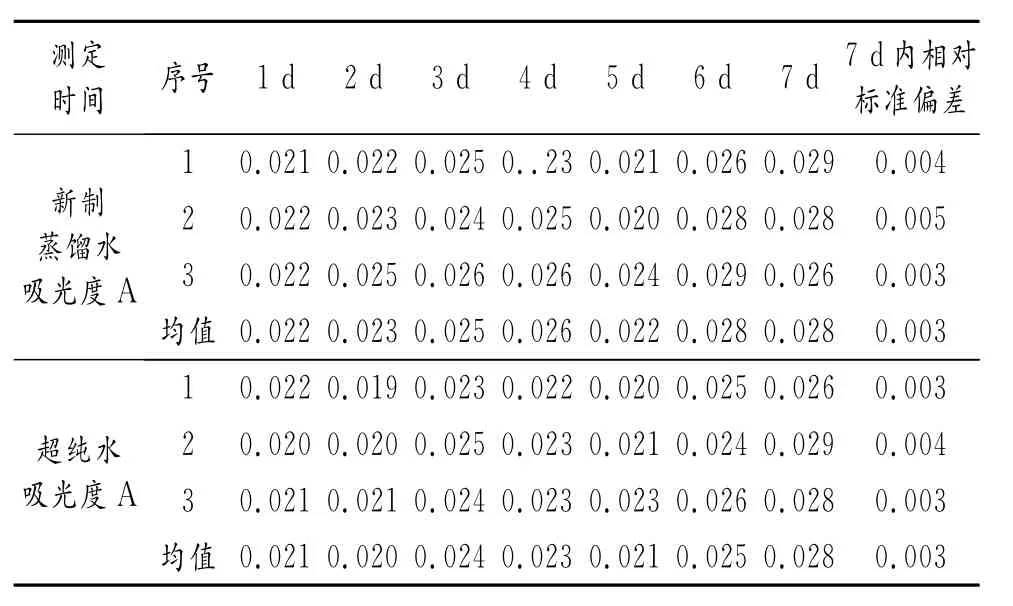
表2 实验用水对空白值的影响
3.3 吸收液的影响
由于氨在空气中普遍存在,因此,硫酸吸收液必须密封保存,且存放的时间不宜过长。经实验确定吸收液的保质期在1周内,超过1周后应重新配制。否则,零管过高,影响测定结果。连续7d测定的空白值见表3。

表3 吸收液保存时间对空白值的影响
3.4 吸收管清洗方法的影响
用洗洁精清洗吸收管,并与用硫酸清洗(1+9)盐酸浸泡进行比较。由于空气中氨无所不在,因此,要尽量避免使用长时间放置的吸收管,洗净后的吸收管用铝箔将2个口封好保存,或在采样前清洗吸收管,最大限度地避免吸收管吸附氨带来的影响。
连接吸收管应使用聚四氟乙烯管。采集氨用的吸收管尽量实现专管专用,避免因项目不同引起的交叉污染。实验结果见表4。

表4 清洗方式对空白值的影响
3.5 化学试剂的影响
本实验纳氏试剂的配制是关键,这是因为纳氏试剂对比色的影响很大。在配制纳氏试剂时,将氯化汞溶液滴入碘化钾溶液中至形成红色不溶的沉淀为止是关键的关键,应在刚刚形成不溶的红色沉淀时立即停止滴入氯化汞溶液。若氯化汞溶液滴入过量,影响纳氏试剂的澄清度。溶液静置数日后,溶液上层会出现一层薄膜状漂浮物,在吸取溶液时膜状物质会吸附在管壁上,在加入纳氏试剂时会带入试管内,影响比色结果的测定,使结果偏高。
酒石酸钾钠溶液在配制过程中去除试剂中的铵盐很关键。某些市售分析纯的酒石酸钾钠试剂中的铵盐有时含量较高,按国标方法配制时仅靠加热煮沸并不能完全除去铵盐,可采用称取50g酒石酸钾钠加100mL无氨水中,再加入0.5mol/L氢氧化钠溶液1.0mL煮沸蒸发至溶液剩一半,冷却后用无氨水稀释至原体积,即能有效去除氨,并放置于冰箱冷藏保存。
3.6 显色温度的影响
国标HJ533-2009中规定显色时间为10min,在实际的监测工作中,受各种因素的影响,显色时间具有一定的不确定性,因此探讨合理的显色时间非常重要。在室温25℃下,进行了显色时间与吸光度关系的研究,实验结果见表5。从表5可以看出,显色时间不足10min,显色不完全;显色时间10min~30min,显色稳定;超过30min,吸光度有增大的趋势。因此,显色时间可以选定10min~30min。

表5 显色时间与吸光度的关系
3.7 显色温度的影响
实验温度影响氨与纳氏试剂的反应速度,显色温度的控制直接影响数据的准确度。本文对显色温度与吸光度的关系进行了考察,实验结果见表6。实验发现,5℃~15℃较低的显色温度,反应不完全;20℃~25℃,吸光度稳定;25℃~35℃时,吸光度又下降。在具体的分析工作中,可以通过控制室内温度来达到理想的效果。
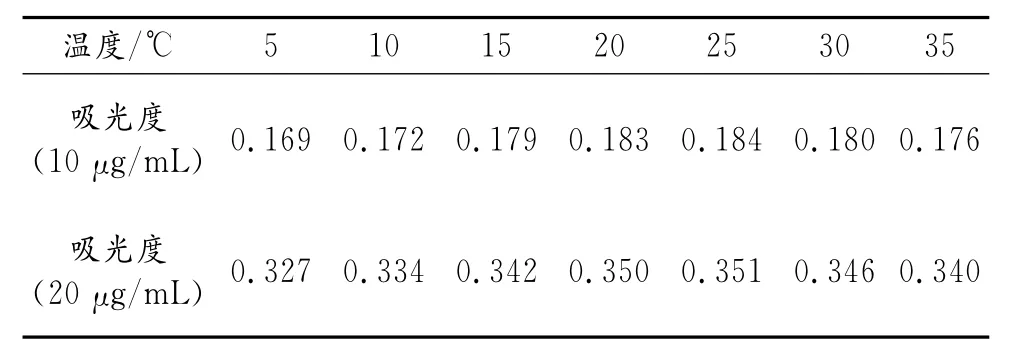
表6 显色温度与吸光度的关系
3.8 实验场所
测定氨的实验中,要避开厕所、使用氨水等的实验区域,或与产生干扰的项目错时进行分析。
4 结论
由于氨测定纳氏试剂分光光度法非常灵敏,在实际的工作中应特别注意实验用水、采样器皿清洁、试剂配制与储存、实验温度和反应时间控制等问题。本文对上述条件逐一进行了详细的讨论,以期更好地指导实际的环境监测工作,保证提供更为准确合理的实验数据。
参考文献:
[1] 邓大跃,王俊,吴丽萍,等.室内空气中氨的标准测定方法的比较分析[J].北京联合大学学报,2006,20(3),69-72.
[2] 国家环境保护部.空气和废气监测分析方法[M].第四版(增补版).北京:中国环境科学出版社,2007:158-160.
[3] 沈阳市环境监测站.环境空气氨的测定纳氏试剂分光光原法:HJ 533-2009[S].北京:中国环境出版社,2009:1-5.
