HAV疫苗干预对哮喘患儿治疗效果的影响
2018-05-10陈建平何念海
余 丹,陈建平,何念海△
(1.陆军军医大学西南医院儿科,重庆 400038;2.西安天佑儿童医院儿科,西安 710065)
近年来,以咳嗽和喘息为主要症状的儿童哮喘的发病率逐年增加,严重影响了患儿的生长发育,给家庭和社会带来了不小的经济负担[1]。重庆因受当地气候和环境的影响,儿童哮喘患病率在全国排在前位[2],这提示重庆儿童哮喘的防控任重而道远。笔者前期对儿童哮喘危险因素的Logistic回归分析发现,母乳喂养和甲型肝炎病毒(HAV)感染是儿童哮喘的保护因素,故提倡并鼓励母乳喂养[3]。可能由于HAV疫苗并非国家一类疫苗,接种的人数较少,所以导致在婴幼儿期HAV抗体阳性率较低,只有10%~40%;之后由于隐性感染等原因在成年后HAV抗体阳性率明显提高,甚至可以达到90%~100%[4],而成年后哮喘的发病率逐年减少,由此可见HAV感染率与哮喘的发病率正好相反,提示HAV感染可能对哮喘的控制有保护作用。本研究利用HAV疫苗接种模拟HAV感染,观察其对哮喘儿童症状控制及肺功能的影响,为儿童哮喘的防治提供参考。
1 资料与方法
1.1一般资料 选择2013年6月至2015年6月陆军军医大学西南医院儿科哮喘门诊及住院部收治的患儿,均符合儿童哮喘诊断标准[5]。所有患儿均同意HAV减毒活疫苗接种并检测HAV IgM抗体(HAV-IgM抗体)。HAV-IgM抗体阳性为干预组(n=78),其中女43例,男35例,平均年龄5.8岁;HAV-IgM抗体阴性为对照组(n=80),其中女47例,男33例,平均年龄5.4岁。两组患儿均属于哮喘缓解期,给予糖皮质激素吸入治疗及孟鲁司特钠咀嚼片口服控制症状。纳入标准:(1)肺部查体有哮鸣音或临床出现喘息、气短、胸闷的发作史大于或等于3次;(2)使用平喘药物(支气管扩张剂)可使喘息症状减轻和缓解。排除标准:患有严重的心血管及呼吸系统疾病,伴有其他慢性疾病。所有研究对象均来自中国西南地区,并且获得儿童及家长的知情同意。这项研究获得解放军陆军军医大学伦理委员会的批准。
1.2方法
1.2.1哮喘控制情况评估方法 哮喘控制情况评估[6]: (1)控制,近2周未出现夜间或者日间症状;(2)部分控制,近2~4 周出现日间或夜间症状的时间大于或等于2 d,日常生活受到影响,使用全身皮质激素,每周超过2次应用应急缓解药物改善症状;(3)未控制,近2~4周内出现“部分控制”的特征大于或等于3项。
1.2.2HAV-IgM抗体检测 HAV疫苗干预2周后检测干预组血清样品,采用酶联免疫吸附法(ELISA,北京科卫临床诊断试剂有限公司)HAV-IgM抗体检测试剂盒检测,HAV-IgM抗体阳性归为干预组,阴性为对照组。
1.2.3肺功能检测 按照欧洲呼吸学会(ERS)推荐标准[7],采用德国Master Screen 脉冲震荡(IOS)型肺功能仪(Jaeger公司)检测患儿肺功能。要求受试患儿检测时取坐位,头稍微后仰并夹上鼻夹,双手掌压住腮帮,用牙齿咬住塑料口器,不要漏气,通过塑料口器用嘴平静呼吸,同时避免过紧的腰带和衣服。待患儿呼吸平稳后仪器自动采集数据,记录1 min。测定参数为呼吸总阻抗(Zrs)、共振频率 (Fres)、周边弹性阻力(X5,反映周边顺应性)、总呼吸黏性阻力(R5)、中心气道黏性阻力(R20)及周边气道黏性阻力(R5-R20,反映小气道阻力)。
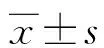
2 结 果
2.1哮喘患儿干预1年内疾病控制情况比较 哮喘患儿HAV疫苗干预后6个月,干预组症状控制与部分控制率(89.8%)高于对照组(86.3%),但比较差异无统计学意义(P>0.05);干预12个月后,干预组症状控制与部分控制率(92.3%)与对照组(87.6%)相比明显升高,哮喘症状控制情况明显好转,比较差异有统计学意义(P<0.05),见表1。

表1 哮喘患儿干预1年内疾病控制情况比较[n(%)]

表2 两组干预前后的IOS肺功能各指标比较
2.2两组干预前后的IOS肺功能指标比较 哮喘患儿HAV疫苗干预后6个月,干预组IOS肺功能R5-R20低于对照组,但比较差异无统计学意义(P>0.05);干预12个月后,干预组Zrs、Fres、R5均低于对照组,比较差异有统计学意义(P<0.05),见表2。
3 讨 论
随着经济状况的提高、卫生条件的改善及家庭规模的缩小,欧美发达国家的HAV感染率降至25%~30%,而变应性哮喘的发病率却增高了2~3倍[8]。许多研究表明HAV感染对哮喘具有保护作用[9],这种HAV感染与变应性哮喘表现的流行病学负相关,提示HAV感染可能对变应性哮喘产生影响,具体的作用机制虽不清楚,但合理解释了HAV感染与变应性哮喘这种流行病学负相关现象[10-11]。MATRICARDI等[12]报道HAV感染与哮喘等变应性疾病呈负相关,随后用流行病学与实验研究的方法,通过分子遗传学验证了这一假说[13]。此前笔者对中国西南地区儿童哮喘的病例对照研究结果也验证了这一假说[14]。可能的机制是HAV 侵入机体后优先与表达在 Th2细胞上的 T细胞免疫球蛋白黏蛋白分子-1(TIM-1) 结合,当二者结合后干扰 TIM-1与其配体的结合,从而阻断 TIM-1 与其配体结合后提供的向Th2细胞诱导的信号转导,抑制对 Th2 细胞的激活,促进向Th1细胞分化的信号从而促进 Th1 细胞的生长[15]。人HAV受体为HAVCR1,也就是TIM-1,表达在肝细胞和肠上皮细胞等表面,是目前所知HAV唯一的细胞受体,介导HAV脱包膜进入细胞的全过程[16]。UMETSU等[17]和SONAR等[18]在哮喘小鼠模型中应用TIM-1抗体干预结果显示其对哮喘及其他免疫性疾病有潜在的治疗作用。
本研究发现HAV疫苗干预后6个月,干预组虽然哮喘症状均有所好转,但与对照组比较差异无统计学意义,可能的原因是机体产生免疫应答需要一定的时间;朱奕奕[19]的研究表明,HAV解毒活疫苗接种后,Th1 细胞分泌的干扰素-γ(IFN-γ)在前4周水平较低,4~6周呈现较快的上升趋势,24~25周达到较高水平并维持不变,提示前6个月HAV疫苗干预对Th1 细胞影响较小,对哮喘的临床症状无明显改善。干预12个月后,干预组与对照组相比哮喘症状控制情况明显好转,就此可以看出HAV干预模拟了自然隐性感染的过程,对儿童哮喘起到了保护作用,安全性还较自然感染高,不会引起HAV爆发,又能提高对儿童哮喘的症状控制。IOS肺功能指标可用于儿童哮喘疗效监测,是一种无创、简便、无需特殊配合的好方法[20]。哮喘患儿HAV疫苗干预后6个月,干预组IOS肺功能部分指标有所改善,与哮喘症状控制情况相似;干预12个月后,干预组与对照组相比IOS肺功能Zrs、Fres和R5均明显降低,提示HAV疫苗干预对哮喘患儿Zrs、Fres及R5改善明显,对哮喘患儿的肺功能有部分改善。
虽然有一部分哮喘患儿到成年后哮喘会自愈,但尚有很大一部分患儿会发展为成人哮喘,需要终身治疗。韩文等[21]对212例儿童哮喘进行随访研究发现,如果把持续2年以上无喘息发作(包括过敏原和感染诱发的哮喘)视为停止发作,则有91例(42.9%)的患儿仍有哮喘发作,可见儿童哮喘的防治任重而道远。HAV疫苗干预对儿童哮喘疾病控制情况及肺功能的影响,目前尚未见研究报道。虽然本研究发现其对儿童哮喘临床症状及肺功能有所改善,对儿童哮喘有保护作用,但是样本量偏少,缺乏多中心的研究。期望后续有大样本多中心的研究报道,为儿童哮喘的预防控制及发展个体化治疗策略提供可靠依据。
[1]PEDERSEN S E,HURD S S,LEMANSKE R F,et al.Global strategy for the diagnosis and management of asthma in children 5 years and younger[J].Pedia Pulmonol,2011,46(1):1-17.
[2]刘传合,洪建国,尚云晓,等.中国16城市儿童哮喘患病率20年对比研究[J].中国实用儿科杂志,2015,29(8):596-600.
[3]陈建平,赵婉莹,何念海,等.413例儿童哮喘危险因素Logistic回归分析[J].第三军医大学学报,2011,33(17):1862-1864.
[4]张嘉民,孙玉波.2008年新疆昌吉市学龄前儿童甲肝感染调查分析[J].地方病通报,2010,25(3):49.
[5]中华医学会儿科学分会呼吸学组.儿童支气管哮喘防治常规(试行)[J].中华儿科杂志,2004,42(2):24-30.
[6]邵双珠.孟鲁斯特钠联合布地奈德治疗缓解期哮喘患儿临床疗效评估[J].临床肺科杂志,2016,21(3):556-558.
[7]NAJI N,KEUNG E,KANE J,et al.Comparison of changes in lung function measured by plethymography and IOS after bronchoprovocation[J].Resp Med,2013,107(4):503-510.
[8]GONZALEZ-QUINTELA A,GUDE F,BOQUETE O,et al.Association of hepatitis A virus infection with allergic sensitization in a population with high prevalence of hepatitis A virus exposure[J].Allergy,2005,60(1):98-103.
[9]LINNEBERG A,OSTERGAARD C,TVEDE M,et al.IgG antibodies against microorganisms and atopic disease in Danish adults:the copenhagen allergy study[J].J Allergy Clin Immun,2003,111(4):847-853.
[10]MATRICARDI P M.99th Dahlem conference on infection,inflammation and chronic inflammatory disorders:controversial aspects of the ′hygiene hypothesis′[J].Clin Exp Immunol,2010,160(1):98-105.
[11]VON MUTIUS E.99th Dahlem conference on infection,inflammation and chronic inflammatory disorders:farm lifestyles and the hygiene hypothesis[J].Clin Exp Immunol,2010,160(1):130-135.
[12]MATRICARDIPM,ROSMINIF,FERRIGNOL,etal.Crosssectionalretrospectivestudyof
prevalence of atopy among Italian military students with antibodies against hepatitis A virus[J].Brit Med J,1997,314(7086):999-1003.
[13]MCINTIRE J J,UMETSU D T,DEKRUYFF R H.TIM-1,a novel allergy and asthma susceptibility gene[J].Springer Semin Immun,2004,25(3/4):335-348.
[14]CHEN J P,ZHAO WL,HE N H,et al.Association of hepatitis A exposure and TIM-1 with childhood allergic asthma[J].J Asthma,2012,49(7):697-702.
[15]MCINTIRE J J,UMETSU S E,AKBARI O,et al.Identification of Tapr (an airway hyperreactivity regulatory locus) and the linked Tim gene family[J].Nat Immunol,2001,2(12):1109-1116.
[16]SILBERSTEIN E,XING L,DE BEEK W V,et al.Alteration of hepatitis A virus (HAV) particles by a soluble form of HAV cellular receptor 1 containing the immunoglobulin- and mucin-like regions[J].J Virol,2003,77(16):8765-8774.
[17]UMETSU S E,LEE W L,MCINTIRE J J,et al.TIM-1 induces T cell activation and inhibits the development of peripheral tolerance[J].Nat Immunol,2005,6(5):447-454.
[18]SONAR S S,HSU Y M,CONRAD M L,et al.Antagonism of TIM-1 blocks the development of disease in a humanized mouse model of allergic asthma[J].J Clin Invest,2010,120(8):2767-2781.
[19]朱奕奕.上海市甲型病毒性肝炎免疫策略评价研究[D].上海:复旦大学,2012.
[20]李航,蔡金龙,曲书强.脉冲振荡技术在支气管哮喘治疗效果评价中的临床应用[J].临床肺科杂志,2016,21(1):119-120,176.
[21]韩文,谢勇,周新龙,等.212例儿童哮喘预后的5年随访研究[J].中国当代儿科杂志,2011,13(11):870-872.
