强化教育对维持性血液透析患者高磷血症影响的Meta分析
2018-05-05许明杰孟祥龙赵玉容洪大情李贵森
任 松 许明杰 孟祥龙 赵玉容 洪大情 张 渊 李贵森
慢性肾脏病(CKD)是影响人类健康的最主要的慢性疾病之一,其病程长,花费大,已成为全球性的健康问题。部分CKD患者逐渐进展至终末期肾病(ESRD)并出现高钾血症、高磷血症、贫血、高血压、酸中毒等并发症,有调查发现,约90%的CKD患者合并上述2~4个并发症[1]。维持性血液透析(MHD)是ESRD患者最主要的治疗方式,尽管可清除患者体内大部分毒素,但代谢性骨病(MBD)依然是MHD患者最常见的并发症之一。
高磷血症作为代谢性骨病的始动因素,越来越受到医务人员和患者的重视。长期高磷血症可导致继发性甲状旁腺功能亢进,进而出现矿物质及骨代谢异常[2],还有研究发现高磷血症可增加患者发生心血管事件的风险[3]。饮食是导致患者高磷血症的最主要原因,近年来,对于多种慢性病管理中,都特别强调生活方式改变。对于ESRD高磷血症患者,生活方式改变,尤其是加强饮食管理,是磷管理的重要内容。由于磷管理中涉及的知识专业性较强,需要对患者进行系统性地教育培训。有研究发现强化饮食教育可降低患者出现高磷血症的风险,本文将使用Meta分析的方法探讨强化教育对MHD患者高磷血症影响。
资料与方法
纳入排除标准纳入标准:根据国际循证医学/Cochrane 协作网工作手册标准,制定本研究的纳入标准为:(1)试验设计类型为临床随机对照试验(RCTs)。(2)研究对象均为维持性血液透析患者,且透析时间>6个月,同时合并高磷血症。(3)干预措施:强化患者的饮食教育,包括医护人员定期开展讲座、发放宣传手册及营养师制定营养计划等对患者饮食进行教育。(4)观察指标:治疗前后患者血清钙、磷、钙磷乘积和知识评分等相关指标。
排除标准:研究类型非RCTs;研究对象为非透析患者;试验组的干预措施除了患者教育以外,还给予了对照组未使用的其他方法;统计方法不恰当;数据不完整;重复发表的文章。
检索策略计算机检索Medline、Embase、Cochrane图书馆等数据库系统,检索的时间范围为建库至2018-01-15,检索词包括“patient education”、“hemodialysis”、“hyperphosphatemia”和“randomized controlled trial”等。
文献筛选及质量评价由两名研究者独立对检索的文献进行筛选,在排除明显不符合纳入标准的试验后,对可能符合纳入标准的文献阅读全文,以确定是否真正符合纳入标准。使用Jadad量表对纳入的研究进行方法学质量评价,评分1~2分为低质量文献,3~5分则为高质量文献。
数据收集制定统一的数据提取表对纳入的文献进行数据提取,由两名研究者独立进行,若存在分歧,则由第三名研究者裁决。提取内容包括:文献作者及发表时间、试验设计、研究对象的基本资料、干预的具体措施、结局指标等。
统计分析采用 Cochrane协作网推荐的Review Manager 5.3软件对数据进行分析,对纳入的文献进行异质性检验,采用χ2检验来判断各个临床试验是否存在异质性,若I2≤50%,认为各个研究间同质性较好,使用固定效应模型进行Meta分析,若I2>50%,则认为研究间异质性较大,使用随机效应模型进行Meta分析,并根据异质性来源进一步行行亚组分析或敏感度分析。
二分类变量用相对危险度(RR)及95%置信区间(95%CI)作为统计效应量,连续型变量则根据测量尺度相同与否分别采用加权均数差(WMD)或标准均数差(SMD)及其95%置信区间作为统计量。
结 果
文献筛选结果共检出相关文献173篇,按照纳入排除标准,通过阅读标题及摘要,排除无关的研究后,纳入26篇文献,进一步阅读全文,最终纳入10篇文献[4-13](文献筛选流程见图1)。

图1 文献筛选流程图
10篇文献均以英文的方式发表,共包括908例患者,其中强化教育组525例,对照组383例。有两篇文献[11,13]将患者分为三组,其中有两组同为强化
教育组,仅教育方式不同,故将其数据进行合并。10篇文献中仅一篇文献Jadad评分为2分,为低质量文献,其余9篇均为高质量文献,10篇文献的基本信息详见表1。10篇文献中有两篇文献[8,12]提及血样本采集时间为透析前,另一篇文献[4]为透析后2天,其余7篇文献未提及样本采集时间。
meta分析结果
强化教育对维持性血液透析患者血钙的影响 异质性检验结果:χ2=5.12,I2=22%,P=0.27。异质性检验无统计学意义。采用固定效应模型进行meta分析,结果显示,和对照组相比,强化教育能显著提升维持性血液透析患者血钙离子水平0.07 mmol,两组之间差异具有统计学意义(P=0.007),根据教育实施者不同进行亚组分析结果显示两亚组之间患者差异不明显(P=0.13)(图2)。

表1 纳入研究的基本特征
Ca:钙;P:磷;Ca×P:钙磷乘积;knowledge score:知识得分
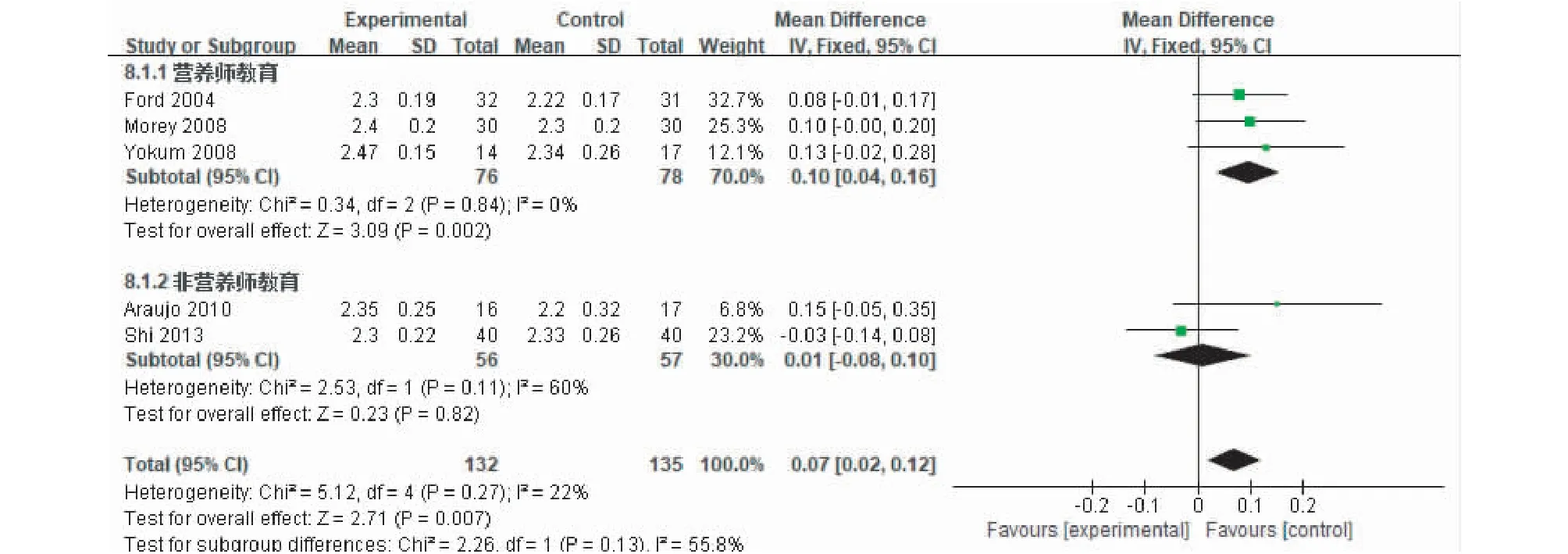
图2 强化教育对维持性血液透析患者血清钙离子影响的森林图
强化教育对MHD患者血磷的影响 异质性检验结果:χ2=21.72,I2=59%,P=0.01。异质性检验有统计学意义。采用随机效应模型进行meta分析,结果显示,和对照组相比,强化教育能显著降低患者血清磷水平(WMD=-0.20,95%CI:-0.32~-0.09,P<0.01),两组之间差异具有统计学意义,根据教育实施者不同进一步行亚组分析,结果显示和非营养师教育相比,营养师教育组患者在降低血磷方面效果更佳,两亚组之间差异具有统计学意义(P=0.03)(图3)。
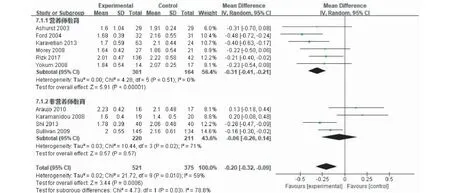
图3 强化教育对维持性血液透析患者血清磷影响的森林图
强化教育对MHD患者钙磷乘积的影响 异质性检验结果:χ2=7.40,I2=32%,P=0.19。异质性检验无统计学意义。采用固定效应模型进行Meta分析,结果显示,强化教育能显著降低患者钙磷乘积水平(WMD=-0.62,95%CI:-0.86~-0.38,P<0.01),两组之间差异具有统计学意义,而根据教育实施者不同行亚组分析差异无统计学意义(图4)。

图4 强化教育对维持性血液透析患者钙磷乘积影响的森林图
强化教育对MHD患者知识得分的影响 异质性检验结果:χ2=16.04,I2=88%,P<0.01。异质性检验具有统计学意义。采用随机效应模型进行Meta分析,结果显示,强化教育组患者知识得分较对照组明显提升(SMD=0.78,95%CI:0.06~1.51,P=0.03),两组之间差异具有统计学意义(图5)。
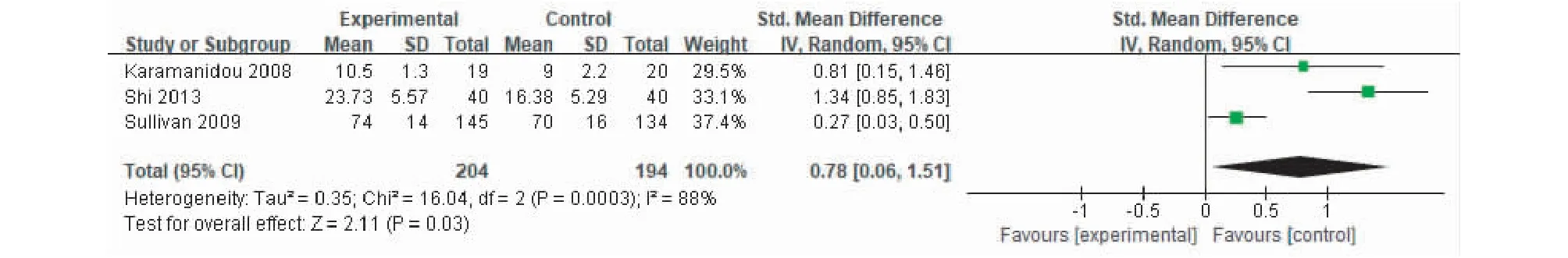
图5 强化教育对维持性血液透析患者知识得分影响的森林图
讨 论
慢性肾脏病矿物质与骨异常(CDK-MBD)是维持性血液透析患者最常见的并发症之一,2009年,改善全球肾脏病预后组织(KDIGO)颁布了适用于全球的CKD-MBD 的临床实践指南[14],为CKD-MBD的诊断、预防和治疗提供和参考。指南建议CKD 3~5D 期的患者应进行低磷饮食,同时联合其他降磷治疗(充分透析,磷结合剂的使用),即3D(diet, dialysis, drug)降磷治疗,其中饮食控制是磷管理的基础。
磷主要来源于食物,经过消化道吸收进入体内,并由肾脏排出体外,CKD患者由于肾功能不全,磷排出减少,因此常出现高磷血症。持续性的高磷血症可刺激甲状旁腺分泌大量的甲状旁腺激素(PTH),导致甲状旁腺功能亢进,并出现肾性骨病等一系列继发性并发症[15]。高磷血症还可增加患者出现心血管事件的风险,其可通过破坏细胞骨架,促使钙沉积于血管平滑肌细胞,从而促进血管钙化[16]。
大量的研究还发现,严重的高磷血症与患者出现全因死亡密切相关。Palmer等[17]纳入47篇研究进行Meta分析结果显示,血清磷水平每升高10 mg/L,患者死亡率增加18%。Floege等[18]则发现血磷水平和患者死亡率呈U型关系,当血磷水平<1.13 mmol/L,或>1.78 mmol/L时,患者死亡率明显升高。
大部分患者由于缺乏CKD-MBD相关的知识,因此容易忽视该并发症。患者教育是CKD-MBD长期管理的重要组成部分,教育的方式多样化,包括制作宣传手册、定期举行讲座、制定饮食计划等,而教育的实施人员包括医生、护士和营养师等,长期患者教育可减低患者出现CKD-MBD的风险。营养师由于接受过更加专业的学习,其在食物成分,营养搭配等方面更具有优势,因此更适合进行患者饮食教育工作。
本研究纳入10篇随机对照试验进行Meta分析,结果表明,对于MHD患者,强化教育可升高患者血钙水平,降低血磷和钙磷乘积的水平,并显著提高患者知识水平,营养师教育在改善患者高磷血症方面较非营养师教育效果更佳。由于本文纳入的研究随访时间差异较大,进一步根据随访时间不同(<6个月和≥6个月)行亚组分析,结果显示差异无统计学意义。
尽管本文纳入分析的各研究间观察指标的基线数据差异较大,但在同一研究的两个组中基线数据差异无统计学意义,因此本文的阳性分析结果仍具有意义。本研究纳入的文献中有4篇文献提及PTH,但使用的单位不尽相同,经换算后差异巨大,同时文献中的PTH结果数据均以中位数表示,提示该数据呈偏态分布,在缺乏原始数据情况下不宜直接转换为均数及标准差进行比较,故本文未对PTH进行数据分析。
本文的局限性:(1)纳入的研究较少,总样本量偏少,从而影响证据的力量;(2)纳入研究的各试验干预措施差异较大,导致各研究间异质性较大;(3)部分研究数据不完整,势必会影响研究的结果;(4)本研究纳入的文献随访时间均较短,大部分文献随访时间<6个月,影响需长时间观察指标如全因死亡等终点事件的结果。综上所述,强化教育可显著降低MHD患者血清磷水平,同时提高血清钙水平和患者知识得分,提高患者对疾病的认知程度,有助于改善患者生活质量,营养师教育在改善患者高磷血症方面较非营养师教育效果更佳,在后期的患者管理中可进一步推广。
1 Tuot DS,Plantinga LC,Hsu CY,et al.Chronic kidney disease awareness among individuals with clinical markers of kidney dysfunction.Clin J Am Soc Nephrol,2011,6(8):1838-1844..
2 Voormolen N,Noordzij M,Grootendorst DC,et al.High plasma phosphate as a risk factor for decline in renal function and mortality in pre-dialysis patients.Nephrol Dial Transplant,2007,22(10):2909-2916.
3 Mucsi I,Hercz G,Uldall R,et al.Control of serum phosphate without any phosphate binders in patients treated with nocturnal hemodialysis.Kidney Int,1998,53(5):1399-1404.
4 Ashurst IB,Dobbie H.A randomized controlled trial of an educational intervention to improve phosphate levels in hemodialysis patients.J Ren Nutr,2003,13(4):267-274.
5 Ford JC,Pope JF,Hunt AE,et al.The effect of diet education on the laboratory values and knowledge of hemodialysis patients with hyperphosphatemia.J Ren Nutr,2004,14(1):36-44.
6 Karamanidou C,Weinman J,Horne R.Improving haemodialysis patients′ understanding of phosphate-binding medication:a pilot study of a psycho-educational intervention designed to change patients′ perceptions of the problem and treatment.Br J Health Psychol,2008,13(Pt 2):205-214.
7 Morey B,Walker R,Davenport A.More dietetic time,better outcome? A randomized prospective study investigating the effect of more dietetic time on phosphate control in end-stage kidney failure haemodialysis patients.Nephron Clin Pract,2008,109(3):c173-180.
8 Yokum D,Glass G,Cheung CF,et al.Evaluation of a phosphate management protocol to achieve optimum serum phosphate levels in hemodialysis patients.J Ren Nutr,2008,18(6):521-529.
9 Sullivan C,Sayre SS,Leon JB,et al.Effect of food additives on hyperphosphatemia among patients with end-stage renal disease:a randomized controlled trial.JAMA,2009,301(6):629-635.
10 de Araujo LP,Figueiredo AE,d′Avila DO.[Evaluation of an educational program on calcium and phosphorus metabolism for patients on hemodialysis].Rev Esc Enferm USP,2010,44(4):928-932.
11 Karavetian M,Ghaddar S.Nutritional education for the management of osteodystrophy (nemo) in patients on haemodialysis:a randomised controlled trial.J Ren Care,2013,39(1):19-30.
12 Shi YX,Fan XY,Han HJ,et al.Effectiveness of a nurse-led intensive educational programme on chronic kidney failure patients with hyperphosphataemia:randomised controlled trial.J Clin Nurs,2013,22(7-8):1189-1197.
13 Rizk R,Karavetian M,Hiligsmann M,et al.Effect of stage-based education provided by dedicated dietitians on hyperphosphataemic haemodialysis patients:results from the Nutrition Education for Management of Osteodystrophy randomised controlled trial.J Hum Nutr Diet,2017,30(5):554-562.
14 KDIGO clinical practice guideline for the diagnosis,evaluation,prevention,and treatment of Chronic Kidney Disease-Mineral and Bone Disorder (CKD-MBD).Kidney Int Suppl,2009,(113):S1-130.
15 Waheed AA,Pedraza F,Lenz O,et al.Phosphate control in end-stage renal disease:barriers and opportunities.Nephrol Dial Transplant,2013,28(12):2961-2968.
16 Burger D,Levin A.'Shedding' light on mechanisms of hyperphosphatemic vascular dysfunction.Kidney Int,2013,83(2):187-189.
17 Palmer SC,Hayen A,Macaskill P,et al.Serum levels of phosphorus,parathyroid hormone,and calcium and risks of death and cardiovascular disease in individuals with chronic kidney disease:a systematic review and meta-analysis.JAMA,2011,305(11):1119-1127.
18 Floege J,Kim J,Ireland E,et al.Serum iPTH,calcium and phosphate,and the risk of mortality in a European haemodialysis population.Nephrol Dial Transplant,2011,26(6):1948-1955.
