川牛膝和怀牛膝多糖抗炎 免疫调节活性研究*
2018-04-28王媛媛张雪芹袁菲菲余培凡吴飘扬
王媛媛 张雪芹 袁菲菲 余培凡 吴飘扬 田 宇
(蚌埠医学院公共基础学院,蚌埠 233030)
川牛膝为苋科植物川牛膝(CyathulaofficinalisKuan)的干燥根,气微、味甜,功能为逐瘀通经,通利关节,利尿通淋。怀牛膝为苋科植物牛膝(AchyranthesbidentataB1.)的干燥根,气微、味微甜而稍苦涩,功能为逐瘀通经,补肝肾,强筋骨,利尿通淋,引血下行[1]。川牛膝和怀牛膝多糖由两种植物通过提取分离获得,具备较高的生物活性,如抗炎、增强免疫、抗肿瘤等,临床上被用于免疫调节及肿瘤治疗[2-6]。目前,国内外研究关于川牛膝和怀牛膝多糖的药理活性区别报道较少,本文采用ELISA技术[7-9],通过检测两种多糖对小鼠腹腔来源巨噬细胞中PGE2、TNF-α、IL-12因子分泌的影响,探究两种多糖的抗炎、免疫调节活性,为后期两种多糖的临床选用研究提供支持。
1 仪器与实验材料
1.1 仪器
CO2培养箱(HF151型,力康生物医疗有限公司);酶标仪(Multiskan FC型,美国Thermo Fisher公司);流式细胞仪(FACSCanto II型,美国BD公司);超净工作台(RL119952型,上海荣丰仪器公司);低温高速离心机(TGL-16k型,常州国华科学仪器有限公司)。
1.2 实验材料
胎牛血清(批号:10099-141,Gibco公司);1640培养基干粉(批号:31800022,Gibco公司);胰酶干粉(批号:25200056,Gibco公司);PBS缓冲液(批号:SH30256.01B,HyClone公司)。
两种多糖由实验室通过水提醇沉法[10]制备。
2 方法
2.1 Ana-1细胞的培养
取Ana-1细胞,在37 ℃、5%CO2条件下,用含10%的小牛血清、青霉素(1 ×105U/L)及链霉素(100mg/L)的DMEM培养液进行培养。待细胞基本长满后,用胰酶消化,细胞计数器或细胞板计数,调整细胞浓度为2.5×104/ml。接种于96孔培养板,每孔接种200μl细胞悬液。接种24h后把培养孔分为空白对照组、各浓度的两种牛膝多糖溶液受试组,每个样品设3复孔,用培养液洗涤3次,然后空白对照组更换含10%小牛血清的DMEM培养基,受试组更换含10%小牛血清及各浓度多糖样品的DMEM培养基,放入培养箱中继续培养48h。
2.2 ELISA法检测两种多糖的抗炎、免疫调节活性
取细胞上清液,用ELISA试剂盒方法测定空白对照组和受试组各样品细胞培养上清液中PGE2、TNF-α、IL-12的水平,于450nm波长处测定OD值。计算两种多糖样品各浓度溶液抑制Ana-1细胞产生PGE2的抑制率及促进Ana-1细胞分泌TNF-α、IL-12的增值率,做出抑制率及增值率/%-浓度/μg·ml-1曲线。
2.3 统计学方法
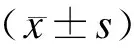
3 结果
3.1 两种多糖对Ana-1细胞产生PGE2的影响
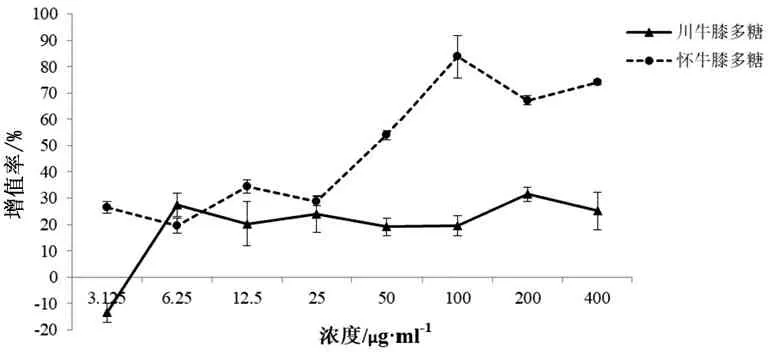
图1 两种多糖抑制Ana-1细胞产生PGE2的抑制率-浓度曲线
由抑制率-浓度曲线可以看出,两种多糖对Ana-1产生PGE2具有不同程度的影响,且怀牛膝多糖在一定浓度范围内对Ana-1细胞产生PGE2的抑制率与其浓度呈正相关;对抑制率-浓度曲线进行拟合并计算结果表明,怀牛膝多糖抑制Ana-1细胞产生PGE2的IC50值为(46.151±1.408)μg/ml;川牛膝多糖抑制Ana-1细胞产生PGE2的能力较弱,并未计算出IC50值,在此模型下,怀牛膝多糖显示出一定的抗炎活性优势。
3.2 两种多糖对Ana-1细胞分泌TNF-α、IL-12的影响
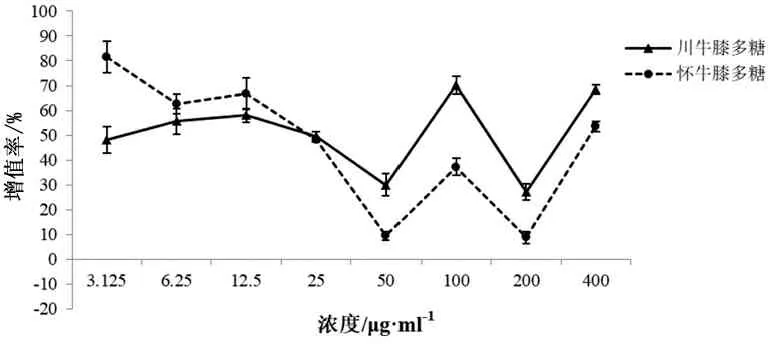

图2 两种多糖促进Ana-1细胞分泌TNF-α的增值率-浓度曲线

图3 两种多糖促进Ana-1细胞分泌TNF-α的EC50值
图4 两种多糖促进Ana-1细胞分泌IL-12的增值率-浓度曲线
由增值率-浓度曲线可以看出,两种多糖对Ana-1细胞分泌TNF-α具有一定的促进作用,对曲线进行拟合并计算结果表明,川牛膝多糖、怀牛膝多糖促进Ana-1细胞中TNF-α因子分泌的EC50值分别为(21.247±3.521)μg/ml、(23.532±1.160)μg/ml,经t检验两者无显著性差异(P>0.05);川牛膝和怀牛膝多糖促进Ana-1细胞分泌IL-12因子的能力不明显,均未算出EC50值。
4 讨论
本文通过ELISA技术检测川牛膝和怀牛膝多糖对Ana-1细胞分泌PGE2、TNF-α、IL-12因子的作用,评价两种多糖的抗炎、免疫调节活性。研究结果显示,两种多糖对Ana-1细胞分泌PGE2、TNF-α、IL-12因子具有不同程度的影响,在抑制Ana-1细胞产生PGE2的测试模型中,怀牛膝多糖显示出一定的抗炎活性优势;在促进Ana-1细胞分泌TNF-α、IL-12的测试模型中,两种多糖主要通过促进Ana-1细胞中TNF-α因子分泌的途径产生免疫活性,且在此模型下川牛膝多糖和怀牛膝多糖无显著性差异,揭示两者的免疫调节活性无统计学差异。
炎症和免疫作为机体对外来入侵物质的两种不同反应,它们的作用机制涉及很多共同的细胞因子、化学介质,所以在疾病发生的过程中相互联系,如免疫可以增强炎症反应、调节炎症过程。相对于川牛膝多糖而言,怀牛膝多糖不仅表现出免疫调节活性,还表现出较好的抗炎活性,它可以通过多途径多通路发挥药理活性,并有可能通过免疫调节功能强化抗炎作用,发挥抗炎、免疫协同作用。因此,其在抗炎、免疫调节活性方面呈现出更强的优势。本文结果为牛膝多糖工业生产中的原料选择及两种多糖的临床选用提供了参考依据。
参考文献:
[1] 国家药典委员会.中华人民共和国药典(2015年版一部)[M].北京:中国医药科技出版社,2015:38,72.
[2] Feng H,Du X,Liu J,et al.Novel polysaccharide from Radix Cyathulae officinalis Kuan can improve immune response to ovalbumin in mice[J].International Journal of Biological Macromolecules,2014,65(5):121-128.DOI:10.1016/j.ijbiomac.2014.01.017.
[3] Feng H,Jing F,Yang S,et al.Antiviral activity of phosphorylated Radix Cyathulae officinalis polysaccharide against Canine Parvovirus in vitro[J].International Journal of Biological Macromolecules,2017,99:511-518.DOI:10.1016/j.ijbiomac.2017.02.085.
[4] Feng H,Mcdonough S P,Fan J,et al.Phosphorylated Radix Cyathulae officinalis Polysaccharides act as Adjuvant via promoting dendritic cell maturation[J].Molecules,2017,22(1):106-122.DOI:10.3390/molecules22010106.
[5] Weng X,Lin P,Liu F,et al.Achyranthes bidentata polysaccharides activate the Wnt/β-catenin signaling pathway to promote chondrocyte proliferation.[J].International Journal of Molecular Medicine,2014,34(4):1045-1050.DOI:10.3892/ijmm.2014.1869.
[6] 徐小娟.山慈菇多糖、牛膝多糖对H22小鼠肝癌抑制作用及其抗肿瘤机制研究[D].长沙:湖南农业大学,2015.
[7] 马兴铭,丁剑冰.医学免疫学[M].北京:清华大学出版社,2013:223.
[8] Knepper T A,Duncan E H,Savransky T,et al.Novel ELISA method as exploratory tool to assess immunity induced by radiated attenuated sporozoites to decipher protective immunity[J].Malaria Journal,2017,16(1):484.DOI:10.1186/s12936-017-2129-9.
[9] Ye C,Luo J,Wang X,et al.Development of a peptide ELISA to discriminate vaccine-induced immunity from natural infection of hepatitis A virus in a phase IV study[J].European Journal of Clinical Microbiology,2017,36(11):2165-2170.DOI:10.1007/s10096-017-3040-6.
[10] 王媛媛,张梦凡,查丽丽,等.川牛膝和怀牛膝提取工艺比较[J].长春师范大学学报,2016,35(10):77-81.
