超精煤热解行为及动力学研究
2018-04-21郭龙飞左海滨王亚杰王静松
郭龙飞,左海滨,赵 骏,王亚杰,王静松
(北京科技大学钢铁冶金新技术国家重点实验室,北京 100083)
0 引 言
目前,煤炭资源仍是世界能源消费的主体[1],对不同品级煤炭能源的高效利用始终是研究的热点。近年来通过可循环有机溶剂对劣质煤进行热熔萃取处理[2]成为煤炭资源综合利用的研究热点。Takanohashi等[3]使用1-甲基萘对不同煤阶煤在不同温度条件下进行处理,发现高温条件有利于提高产率,而且低阶煤处理后具有更高的热塑性。Shui等[4]在室温条件下使用CS2/NMP混合有机溶液处理非炼焦煤,有效提高了其黏结性指数,进行混煤炼焦时其焦炭强度显著提高。通过可循环有机溶剂对煤进行高温萃取,萃取混合液经分离有机溶剂后所得的萃取物称为超精煤(hyper coal,HPC)[5]。HPC具有低灰、低硫的特点,作为清洁能源使用可以有效减少污染物排放,减少对反应容器的损害。樊丽华等[5]对无灰煤的热解行为进行研究,发现无灰煤中中小型分子增多,热解初始温度降低,热失重量增加。目前对于HPC的研究主要集中在热熔萃取的机理研究和较好炼焦能力的应用上,而对于热解过程尤其是热解动力学研究相对较少。煤的热解是煤炭气化与燃烧等煤资源转换方式的初始阶段[6],并且对产物反应活性和转化有重要影响[7]。热解过程的内在机理通过宏观反应动力学的方式表现出来[8]。在热重分析仪器上采用程序升温法研究煤热解过程中的失重现象是一种成熟的手段,其具有试验量小,操作周期短,获得信息多等特点[9]。在对热解过程失重数据进行处理时,将其看为一个整体并不能真正反映煤复杂的热解过程,因此对热解过程分阶段研究可以更好地描述热解过程[10]。平传娟等[7]利用热天平试验测试数据对混煤热解动力学进行研究,发现对混煤热解分段拟合可以很好地描述不同温度段热解机制。
本文采用升温热重分析法在氩气下,对原煤和超精煤热解特性和动力学进行研究。根据热解特征参数对热解过程进行分段处理。采用分段模型拟合法研究确定热解不同阶段的动力学模型及其对应的热解动力学参数。
1 试 验
1.1 样品制备
以岢岚(KL)煤为试验用煤。使用可循环有机溶剂(N-甲基吡咯烷酮,NMP)在高压反应釜内对KL煤粉进行热萃取处理。试验所选高压反应釜有效容积为1 L,按煤粉与溶剂比为8 g∶400 mL,准确称取相应量的KL煤粉和NMP溶剂加入高压反应釜。首先向反应釜内以400 mL/min的速率通入高纯氮气20 min,排除空气后关闭进气口和出气口,此时釜内为大气压力。设置程序控制反应釜升温至350℃后恒温1 h。整个试验过程反应釜内桨叶以100 r/min转速搅拌,使煤粉与有机溶剂两相充分接触。在350℃下保温1 h后关闭控温程序,取下加热套空冷至室温,取出反应物。使用布氏漏斗和滤纸分离萃取混合液,获得液相和残渣。将滤液通过真空旋转蒸发仪回收有机溶剂和析出固体产物。固体产物经酒精和去离子水反复冲洗后放入真空干燥箱(80℃)真空干燥12 h,干燥后产物即为超精煤。将原煤和超精煤分别标记为KL-RAW和KL-HPC。相应煤样的工业及元素分析见表1。样品均研磨至粒度<0.074 mm,以备热重分析使用。
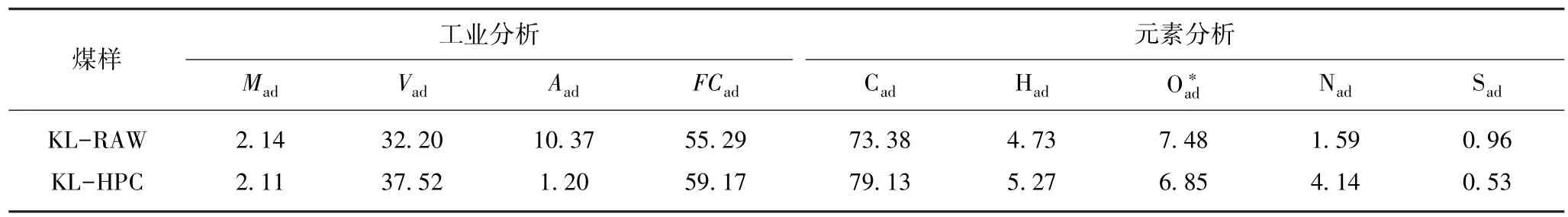
表1 煤样的工业及元素分析Table 1 Proximate and ultimate analysis of coal samples %
1.2 试验仪器及过程
试验设备为美国TA仪器的SDT-600系列热重分析仪。试验过程:温度范围为室温至1 500℃,升温速率0.1~50 K/min,样品容量200 mg,天平灵敏度 0.1 μg,DTA 灵 敏 度 0.001 K。 每 次 取 样 品10.0 mg(粒径<0.074 mm)。 反应温度为室温至1 000℃,采用高纯氩(99.999%)为载气,流量为100 mL/min,升温速率分别为 5、10、20 K/min。
1.3 动力学模型
煤热解动力学的研究目的在于定量表征反应过程及确定反应过程中遵循的最佳机理函数,求出动力学参数和,算出速率常数k,提出模拟TA(thermal analysis)曲线的反应速率表达式。通常煤热解过程表示为

基于质量作用定律和Arrhenius方程,均相反应的动力学方程为

对于非等温、非均相反应的动力学方程为

式中,α为转化率;A为指前因子,min-1;E为活化能,kJ/mol;R为气体常数;T为反应温度,K。
根据热重分析数据,热解转化率α为
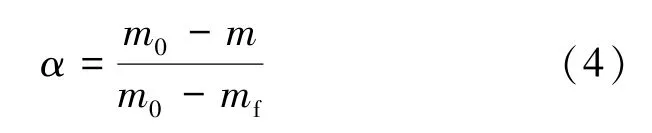
式中,m为样品质量,mg;m0为样品初始质量,mg;mf为样品反应终止质量,mg。
f(α)为热解反应动力学机理函数,表示物质反应速率与反应转换率α之间所遵循的某种函数关系。相应的积分形式定义为

其中,P(u)为温度积分,其没有解析解,只有数值解。动力学方程的求解最终归结在对P(u)的处理上,本文采用Coasts-Redfern法[11]对P(u)进行近似,即
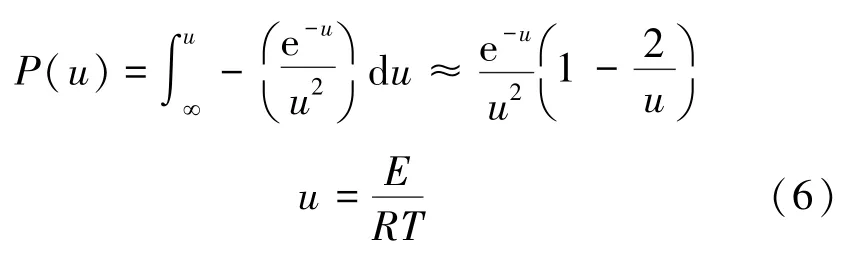
将式(6)代入式(5)得
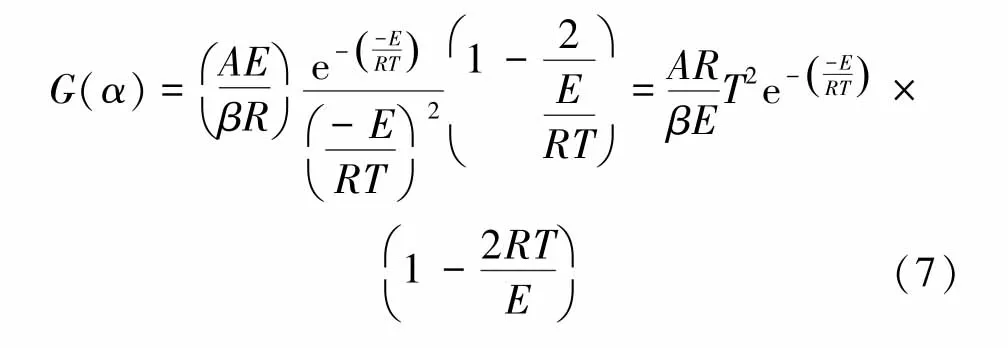
对式(7)两边取自然对数,得到Coats-Redfern方程为

对于一般的反应温度区与大部分的E值来说所以式(8)变为
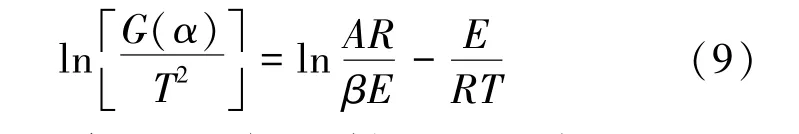
对于正确的反应机制f(α)或G(α),,因此对1/T是一条直线,可判定反应模型是否正确,常见反应机理函数的微分和积分形式见表2[12-13],包括扩散模型,随机成核模型、收缩核模型和反应级数模型。
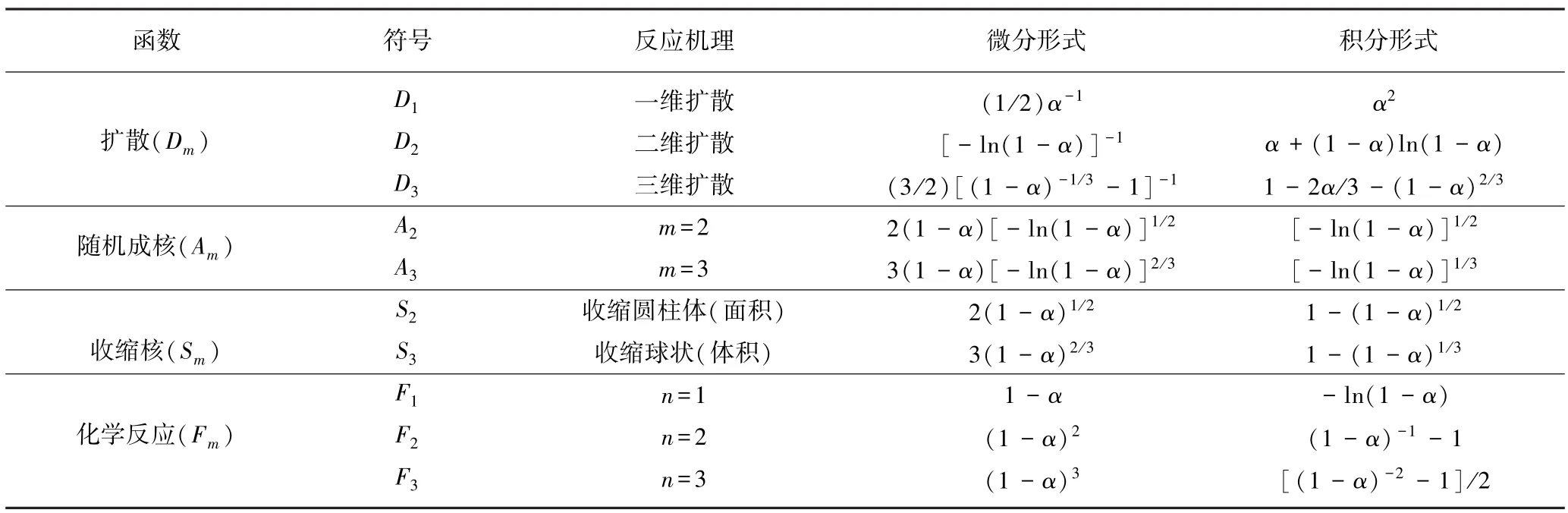
表2 常用气固反应动力学函数[12-13]Table 2 Basic gas-solid reaction kinetics function[12-13]
2 试验结果与讨论
2.1 不同样品热解特性
KL-RAW和KL-HPC煤在20℃/min升温下热解的TG和DTG曲线如图1所示。可以看出,2种煤的热解失重过程具有类似的特征,失重速率先增大后减小。所以煤的热解过程主要分为3个阶段:结晶水和吸附气体脱除阶段,热解气体和半焦生成阶段以及半焦缩聚焦化阶段。从DTG曲线可知,KL-RAW煤热解过程仅在500℃附近存在1个失重速率较大的失重峰,为热解过程热解气体大量生成阶段;KL-HPC煤热解过程除在与KL-RAW煤相近温度存在1个失重速率较大的失重峰外,在较低温度存在2个失重峰。超精煤制备过程中,高温下有机溶剂对煤结构产生溶胀作用,使煤结构疏松,制取的KL-HPC空隙中吸附有少量NMP有机溶剂;另一方面,KL煤粉经有机溶剂高温萃取后,大分子聚合结构打开、断裂,产生较多的芳香自由基碎片,主要以中、小分子量的状态存在。导致超精煤中易挥发组分含量增大,因此在KL-HPC煤粉热解过程DTG图的较低温度存在2个失重峰。
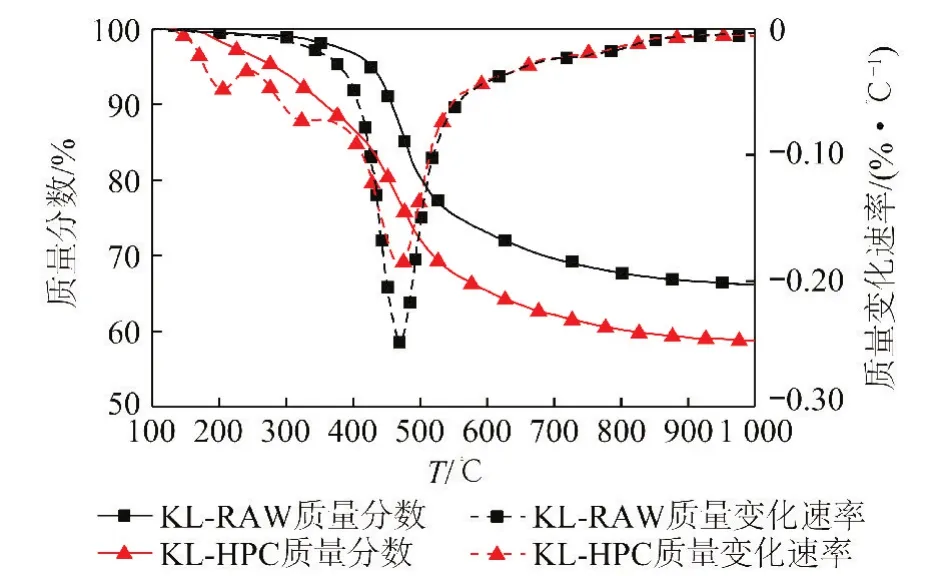
图1 KL-RAW和KL-HPC在20℃/min升温下TG和DTG曲线Fig.1 TG and DTG curves of pyrolysis of KL-RAW and KL-HPC at 20℃/min
2种样品的热解特征参数见表3。其中,热解开始温度Ts为转化率随温度变化中,转化率5%与50%的连线与横坐标的交点所对应的温度;热解最大质量变化速率温度Tmax为热解速率随温度变化中,质量变化速率最大的点对应的温度,对应热解最大质量变化速率为(dw/dT)max;热解终温Tf根据文献定义为Tf=2Tmax-Ts[14]。可以看出,虽然 KLHPC煤的最大质量变化速率低于KL-RAW煤,但是KL-HPC煤的起始热解温度更低,热解终温更高,导致其有更宽的热解温度区间,因此KL-HPC在整个热解过程中表现出更大的质量变化速率。

表3 不同样品热解特征参数Table 3 Characteristic parameters of different samples pyrolysis reaction
2.2 加热速率对热解影响
不同升温速率下样品热解失重过程如图2所示,其特征参数见表4。可以看出,升温速率的提高对KL-RAW和KL-HPC热解过程的影响类似,随着升温速率的提高,热解失重曲线向高温区移动,对应的Ts、Tm和Tf值均增大,表现出热滞后性[9]。但是相应的增幅KL-RAW较大,因此加热速率对其影响较大。升温速率的提高对样品最大热解速率的影响不大,主要是因为其表达为单位温度的质量变化分数(%/℃),若将其单位转化为单位时间的质量变化分数(%/min),可以看出随着升温速率的提高单位时间内失重量显著增多,这样的单位表达更具有实际意义。
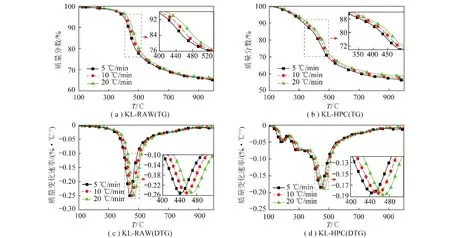
图2 不同升温速率TG和DTG曲线Fig.2 TG and DTG curves of pyrolysis at different heating rates

表4 不同升温速率条件下热解特征参数Table 4 Characteristic parameters of pyrolysis reaction at different heating rates
由于煤热解过程的复杂性,不同温度阶段内其热解过程存在差异。一般地,根据热解过程和质量变化速率的不同,将整个热解温度范围划分为不同阶段。本文主要采用Ts和Tmax为节点,将整个热解温度区间划分为低温、中温和高温段,见表5,此区间的划分同样也是动力学参数求解的依据。

表5 不同升温速率温度范围Table 5 Temperature ranges at different heating rates
2.3 动力学参数的求解
采用模型拟合法对煤热解动力学研究时,将整个热解过程视为一个整体有时不能很好地分析热解过程的机理,因此应对热解反应过程依据表5进行分段处理,对不同速率条件下热解过程每个阶段分别进行模型拟合。根据表2中所列动力学机理函数,结合式(9)进行线性拟合,热解过程的机制为拟合过程中相关系数R2最大的机理函数所描述的动力学模型。根据最佳机理函数的拟合直线所对应的斜率和截距分别计算得到活化能E和指前因子A,即可获得“热解动力学三因子”。结合表6,分析KL-RAW和KL-HPC煤在升温速率10℃/min下热解不同温度阶段的动力学参数,可以看出,KLRAW煤的第2个阶段的活化能最高,其次是第3阶段,而第1个阶段的活化能最低。这主要是因为煤的热解过程主要发生在第2阶段,而第1阶段主要发生结晶水的脱除和脱气,随着温度的升高,第3阶段主要发生半焦缩聚焦化过程,这与前文所阐述的热解过程相符。对于KL-HPC,第1阶段活化能最高,随着反应的进行活化能逐渐降低,这可能主要是在制备KL-HPC时存在未完全分离出去的有机溶剂导致的活化能升高。
不同升温速率下热解过程的最佳动力学机理函数见表6,其中的动力学参数可以很好地反映出随升温速率的提高,所出现的“热滞后”现象。在不同升温速率条件下,相应阶段的最佳动力学机理函数并不发生变化,对于不同升温速率条件下KL-RAW煤热解过程,低温段和中温段热解机制均为一维扩散模型,高温段热解机制为二级化学反应模型;对于KL-HPC煤热解过程,3个温度阶段热解机制分别为一维扩散模型、三维扩散模型、二级化学反应模型。对于KL-HPC煤,随着升温速率的变化,每个温度阶段的活化能发生变化,但活化能总和基本保持不变,这与文献[15]中结论一致。不同温度区间活化能的变化情况可以看出,升温速率增大对KLRAW煤中温段和KL-HPC煤低温段影响较大。
3 结 论
1)原煤和超精煤热解过程主要分为3个阶段:结晶水和脱气阶段,热解气体和半焦生成阶段以及半焦缩聚焦化阶段。尽管原煤的最大热解失重速率比超精煤大,超精煤具有更高的热解温度区间,造成更大的最终失重率。
2)随着升温速率的提高,热解失重曲线向高温区移动,对应的Ts、Tmax和Tf值均增大,表现出热滞后性,且对原煤影响较大。以Ts和Tmax为节点可以将热解过程划分为3个阶段:低温、中温和高温段。划分同样适用热解动力学求解过程。

表6 不同升温速率条件下KL-RAW和KL-HPC热解动力学参数Table 6 Kinetics parameters of the pyrolysis of KL-RAW and KL-HPC at different heating rates
3)分段模型拟合法可以很好地解释煤热解过程机理。原煤的低温和中温段的热解机制均为一维扩散模型,高温段热解机制为二级化学反应模型;超精煤的3个温度段分别为一维扩散模型、三维扩散模型和二级化学反应模型。升温速率的提高对原煤热解的中温段影响较大,而对超精煤热解的低温过程影响较大;同时加热速率的提高对超精煤3个温度段的活化能总和并无影响。
参考文献(References):
[1]樊东黎.世界能源现状和未来[J].金属热处理,2011,36(10):119-131.FAN Dongli.World energy:Present and future[J].Heat Treatment of Metals,2011,36(10):119-131.
[2]赵雪飞,吴凯,赖仕全,等.热解温度条件下溶剂萃取煤技术及应用[J].辽宁科技大学学报,2012,35(2):113-117.ZHAO Xuefei,WU Kai,LAI Shiquan,et al.Application of solvent extraction coal technology under pyrolytic temperature condition[J].Journal of University of Science and Technology Liaoning,2012,35(2):113-117.
[3]TAKANOHASHI T,SHISHIDO T,KAWASHIMA H,et al.Characterisation of hyper coals from coals of various ranks[J].Fuel,2008,87(4-5):592-598.
[4]SHUI H,YE W,WANG Z,et al.Hydrothermal treatment of a subbituminous coal and its use in coking blends[J].Energy&Fuels,2013,27(1):138-144.
[5]樊丽华,杜敬文,梁英华,等.无灰煤的热解行为及其在配煤中的添加效果[J].煤炭科学技术,2017,45(3):185-190.FAN Lihua,DU Jingwen,LIANG Yinghua,et al.Pyrolysis behavior of hypercoal and its adding effect in blending coal[J].Coal Science and Technology,2017,45(3):185-190.
[6]SOLOMON P R,FLETCHER T H,PUGMIRE R J.Progress in coal pyrolysis[J].Fuel,1993,72(5):587-597.
[7]平传娟,周俊虎,程军,等.混煤热解反应动力学特性研究[J].中国电机工程学报,2007,27(17):6-10.PING Chuanjuan,ZHOU Junhu,CHENG Jun,et al.Research on the pyrolysis kinetics of blended coals[J].Proceeding of the CSEE,2007,27(17):6-10.
[8]赵毅,汪黎东,王小明,等.烟气脱硫产物-亚硫酸钙非催化氧化的宏观反应动力学研究[J].中国电机工程学报,2005,25(8):116-120.ZHAO Yi,WANG Lidong,WANG Xiaoming,et al.Study on the macroscopical uncatalyzed oxidation kinetics of desulfurization residual product-calcium sulftte[J].Proceeding of the CSEE,2005,25(8):116-120.
[9]DONG K S,SANG S P,YONG T K,et al.Study of coal pyrolysis by thermo-gravimetric analysis(TGA)and concentration measurements of the evolved species[J].Journal of Analytical&Applied Pyrolysis,2011,92(1):209-216.
[10]DU R,WU K,ZHANG L,et al.Thermal behavior and kinetic study on the pyrolysis of Shenfu coal by sectioning method[J].Journal of Thermal Analysis&Calorimetry,2016,125(2):959-966.
[11]COATS A W,REDFERN J P.Kinetic parameters from thermogravimetric data[J].Nature,1964,201:68-69.
[12]NIU Z,LIU G,HAO Y,et al.Investigation of mechanism and kinetics of non-isothermal low temperature pyrolysis of perhydrous bituminous coal by in-situ FTIR[J].Fuel,2016,172:1-10.
[13]VLAEV L T,MARKOVSKA I G,LYUBCHEV L A.Non-isothermal kinetics of pyrolysis of rice husk[J].Thermochimica Acta,2003,406(1/2):1-7.
[14]朱丰.COREX熔融气化炉内块煤裂解机理及喷煤燃烧行为研究[D].重庆:重庆大学,2013:11.
[15]何佳佳,邱朋华,吴少华.升温速率对煤热解特性影响的TG/DTG 分析[J].节能技术,2007,25(4):321-325.HE Jiajia,QIU Penghua,WU Shaohua.Study on the effects of heating-up speed to coal pyrolysis with TG/DTG analysis[J].Energy Conservation Technology,2007,25(4):321-325.
