6-羧基壳寡糖螯合钙制备工艺与络合性能研究
2018-04-19胡雪芳田志清张志民王士奎
胡雪芳 田志清 梁 亮 张志民 王士奎
(1.农业部规划设计研究院, 北京 100125; 2.农业部农产品产后处理重点实验室, 北京 100121)
0 引言
钙是人体必需营养元素之一,参与人体的整个生命过程[1-2],我国以植物性膳食为主,补钙是我国膳食营养研究中的重要课题[3]。在实际饮食中钙含量十分充足的情况下,缺钙仍是普遍发生的问题,这是因为仅补充钙量达标是不行的,还需要将钙转化为可吸收的形式。目前常见补钙制剂如碳酸钙等无机钙及柠檬酸钙、葡萄糖酸钙等有机钙,由于其生物效价低、溶解性差,人体对其的吸收利用率有限。另外,人体吸收环境过酸,肠道对Ca2+的通透性差等对钙的吸收也有着重要影响。因此开发一种具有多重功能的螯合钙制剂具有重要意义。
目前钙螯合制剂作为广大学者的研究热点,其制备原料、制备方法丰富多样,产品也有很多种[4-8],其研究主要是从农渔产品加工副产物综合利用角度出发,开发肽-钙、氨基酸-钙螯合物,有相当一部分都是粗品,其成分和作用机制复杂,且作为动物性蛋白质存在潜在过敏原,产品纯化难度大,产品检测、安全管理等难以形成统一标准,另外人体对氨基酸类的需求是有一定数量和比例要求的,多肽及氨基酸类螯合钙制剂的长期服用对其他代谢途径、生理功能也存在潜在影响[9]。
壳寡糖(COS)是壳聚糖经过降解以后得到的聚合度2~20的产物,不仅具有与壳聚糖相似的性质,而且水溶性大大提高,且更容易被吸收,一些生理活性也更加显著,具有提高机体免疫、抗肿瘤、调节血脂、促进双歧杆菌的生长、调节肠道内微生物的代谢活动等功能[10],尤其在促进成骨细胞增殖、增加骨密度、促进骨折愈合、提高骨骼再建能力等骨关节疾病领域具有独特应用价值[11]。6-羧基壳寡糖(CCOS)是壳寡糖分子第6位羟基直接羧基化后生成的一种壳寡糖衍生物,其分子中除了含有—OH和—NH2外,还有—COOH,是一种两性电解质,液态下粘度小,除具有与壳寡糖相似生理功能外,还能有效提高壳寡糖络合金属离子的能力。本文通过TEMPO催化氧化法制备6-羧基壳寡糖,利用该分子特性,与Ca2+形成稳定络合体系,制备CCOS-Ca(Ⅱ)配合物,使Ca2+随之进入机体,同时改善Ca2+的人体吸收环境,充分发挥壳寡糖和钙金属离子对人体双重营养功能特性,探究其合成的最佳工艺条件,对其进行红外表征和元素分析,探讨其配位机理,旨在为开发壳寡糖基金属配合物和高效补钙制剂提供新的思路,为进一步研究壳寡糖及金属配合物在医药保健食品以及生物医学领域的应用提供一定的理论依据。
1 试验材料与方法
1.1 材料与设备
原材料:壳寡糖(分子量500~1 500,脱乙酰度90%以上,山东奥康生物科技有限公司),CaCl2(分析纯,天津市科密欧化学试剂有限公司);无水乙醇(分析纯,天津市化学试剂有限公司);NaOH(分析纯,天津市百世化工有限公司);TEMPO (Sigma 公司);HCI、Na2SO3、NaClO、NaBr(分析纯,国药集团化学试剂有限公司);EDTA(分析纯,国药集团化学试剂有限公司);TEOA(分析纯,国药集团化学试剂有限公司);钙指示剂(分析纯,天津市河东区红岩试剂厂)。
主要设备:FA1204B型电子天平(上海精密科学仪器有限公司);DF-101S型集热式恒温加热磁力搅拌器(郑州科丰仪器设备有限公司);TGL-16C型离心机(上海安宁科学仪器);冷冻干燥机(北京博医康试验仪器有限公司);GZX-GF-MBS-1型电热恒温鼓风干燥器(上海跃进医疗器械厂);PHS-25型PH计(上海精密雷磁);Perkin-Elmer 2400型元素分析仪(美国PE公司);AA300型原子吸收分光光度计 (美国Perkin Elmer公司);Nicolet 6700型傅里叶红外光谱仪(美国Perkin Elmer公司)。
1.2 试验方法
1.2.16-羧基壳寡糖的制备
在500 mL三口烧瓶中加入200 mL蒸馏水和10 g壳寡糖,充分溶解,低温浴槽控制体系温度10℃,加入1 g TEMPO和5 g NaBr,通过滴液漏斗以1~2滴/s的速度滴加质量分数为30%(基于壳寡糖质量)的NaClO溶液,并滴加0.5 mol/L的NaOH溶液维持反应介质的pH值在10~10.5之间,反应2 h。反应结束后,向反应液中加入适量饱和Na2SO3溶液终止反应,静置片刻,将混合液搅拌加入到乙醇中沉淀,过滤,并使用去离子水充分滤洗氧化产物至中性;所得6-羧基壳寡糖质量分数在95%以上。在50℃下真空干燥后,4℃条件下储存备用。
1.2.2螯合率测定方法
CCOS和CaCl2在一定条件下反应一定时间后,移取一定量的反应液两份,一份稀释后直接用0.05 mol/L的EDTA溶液滴定(不需要标定),记录所消耗EDTA体积V0,另一份蒸干,加入无水乙醇进行振荡洗涤,分离出乙醇后加水溶解,再 EDTA滴定,消耗体积记录为V1。
螯合率计算公式为
a=V1/V0×100%
1.2.36-羧基壳寡糖螯合钙的工艺流程
工艺流程为:一定质量比的CCOS和CaCl2→溶于200 mL去离子水中→搅拌→调节溶液pH值(pH值3~10)→一定温度下反应(40~80℃)一定时间→乙醇沉淀(乙醇质量分数90%以上,静置3 h)→离心并收集沉淀(8 000 r/min,15 min)→溶解沉淀物并透析→冷冻干燥(-26℃预冻,工作压力100~110 Pa,升华温度45~55℃)→CCOS-Ca(Ⅱ)成品→测定螯合率。
1.2.4单因素试验
据对壳寡糖(氨基酸、多肽)对金属离子(钙、铁、锌等)螯合工艺参数的相关研究,影响合成反应的主要因素有:pH值、反应时间、反应温度、配体质量比等。
(1)固定反应温度在40℃,反应时间30 min, CCOS与CaCl2质量比为10,pH值2、4、6、8、10、12,考察pH值对螯合率的影响。
(2)固定反应pH值在8,反应时间30 min,CCOS与CaCl2质量比为10,反应温度分别为30、40、50、60、70、80℃,考察反应温度对螯合率的影响。
(3)固定反应温度在50℃、pH值在8,CCOS与CaCl2质量比为10,反应时间20、40、60、80、100、120 min,考察反应时间对螯合率的影响。
(4)固定反应温度50℃,反应时间60 min,反应pH值为8,CCOS与CaCl2质量比分别为5、10、15、20、25、30,考察质量比对螯合率的影响。
1.2.5响应面法优化螯合工艺
采用三因素五水平的响应面优化试验,选取体系pH值、反应温度、CCOS与CaCl2质量比3个因素,设计二次通用回归试验。试验设计如表1所示。
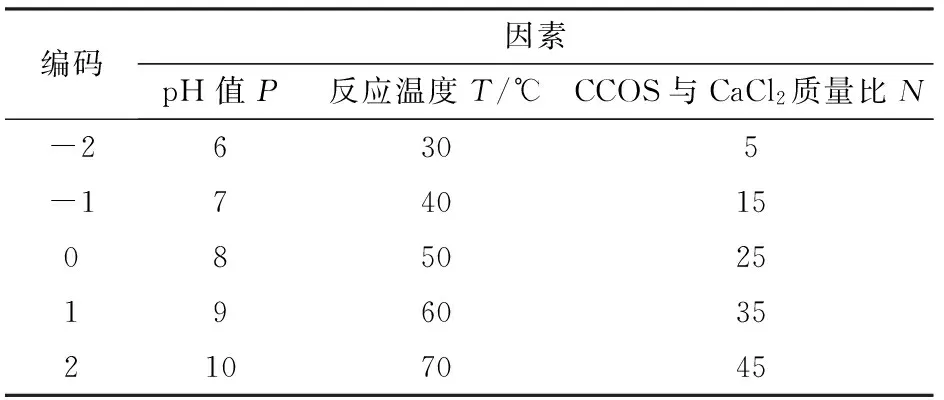
表1 中心组合设计各因素编码Tab.1 Range of different factors investigated with CCRD design
1.2.66-羧基壳寡糖螯合钙红外光谱分析
取样品5 mg,与500 mg的KBr一起放入干燥的研钵中,在红外灯下混合研磨均匀,使其颗粒粒径在2.5pm以下,装入压片模具,制得透明的KBr样品片。利用傅里叶红外光谱仪进行定性分析,在4 000~500 cm-1条件下扫描得到光谱图。按同样方法对6-羧基壳寡糖进行红外光谱测定。
1.2.7元素分析
用元素分析仪分别检测样品中C、H、N的质量分数,用原子吸收分光光度计测定Ca2+的含量。
1.3 数据统计分析
试验结果测定3次,用Sigma Plot 12.5进行数据处理与制图,Design-Expert(Version 8.0.6,美国,Stat-Ease公司)软件对试验数据进行拟合与统计分析。
2 结果与分析
2.1 单因素试验
(1)pH值
由图1可知,pH 值对于螯合率有较大影响,在酸性条件下,螯合率随着pH值的升高而迅速升高,而当体系pH值大于8,螯合率随着体系pH值升高而缓慢下降。究其原因,在酸性条件下,溶液中H+大量存在,H+将会与Ca2+争夺供电子基团,—COOH的离解受到抑制,—COO-减少,且—NH2容易被质子化,氨基及羧基配位能力较弱,不利于螯合物的形成;随着pH值的增加,—COOH的离解增加,—COO-对Ca2+的络合作用增强,而在碱性条件下(pH值大于8),OH-与供电子基团争夺Ca2+而形成羟桥化物,生成了氢氧化钙沉淀[12],且H+对螯合率的影响大于OH-的作用,在相对中性条件下,配体受 H+和OH-影响较小,提供了充分的供电子基团,从而有利于钙通过配位键形成螯合物。本试验在pH值为8时,螯合率与螯合物中钙的含量最高。优化试验中,选取pH值8作为设计中点。
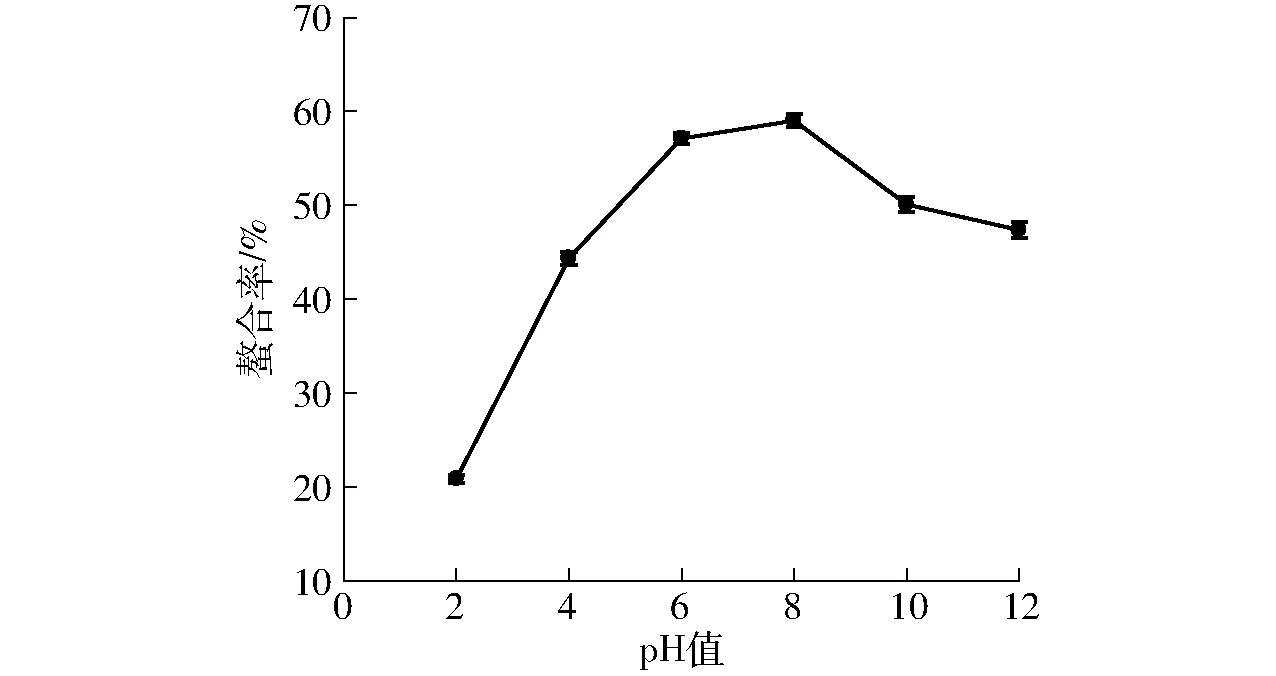
图1 pH值对螯合率的影响Fig.1 Effect of pH value on rate of chelation rate
(2)体系温度
由图2可知,随着反应温度的增加,产物螯合率呈现先上升后下降的趋势,螯合率在50℃达到最大,此后随着温度的升高,螯合率和螯合物中钙含量逐渐降低。分析原因,可能是由于该螯合反应为放热反应,适当升高温度能够促进反应的进行,但提高过度会使反应逆向进行,温度过高,使聚合物分解或使螯合物解离[13],在优化试验中,选择50℃为反应体系温度设计中点。
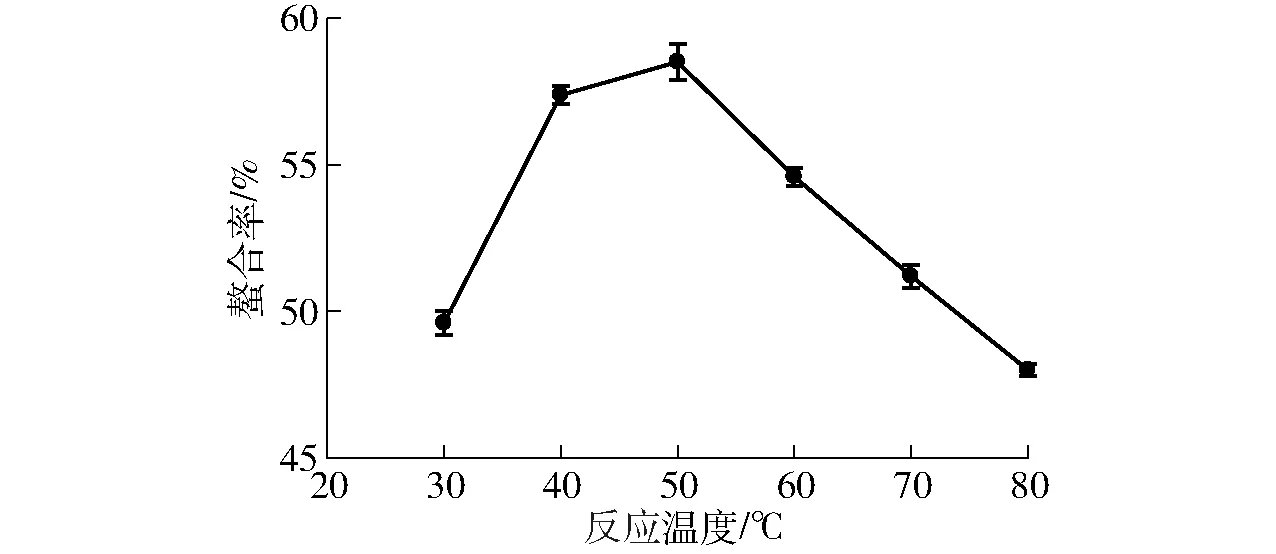
图2 反应温度对螯合率的影响Fig.2 Effect of reaction temperature on rate of chelation rate
(3)反应时间
由图3可知,选取的反应时间范围内,随着反应时间的延长,螯合率变化趋势不明显,采用SPSS 19.0进行方差分析结果显示,在60~100 min时间范围内,反应时间对螯合率影响差异不显著(p<0.01),螯合率虽然随着时间的改变有上下浮动,应属于随机波动,无统计学意义,在100 min后螯合率显著下降,这是由于随着反应时间的延长,一部分螯合物不稳定被分解。总体上反应时间对螯合率影响不大,在响应面试验中固定在60 min。
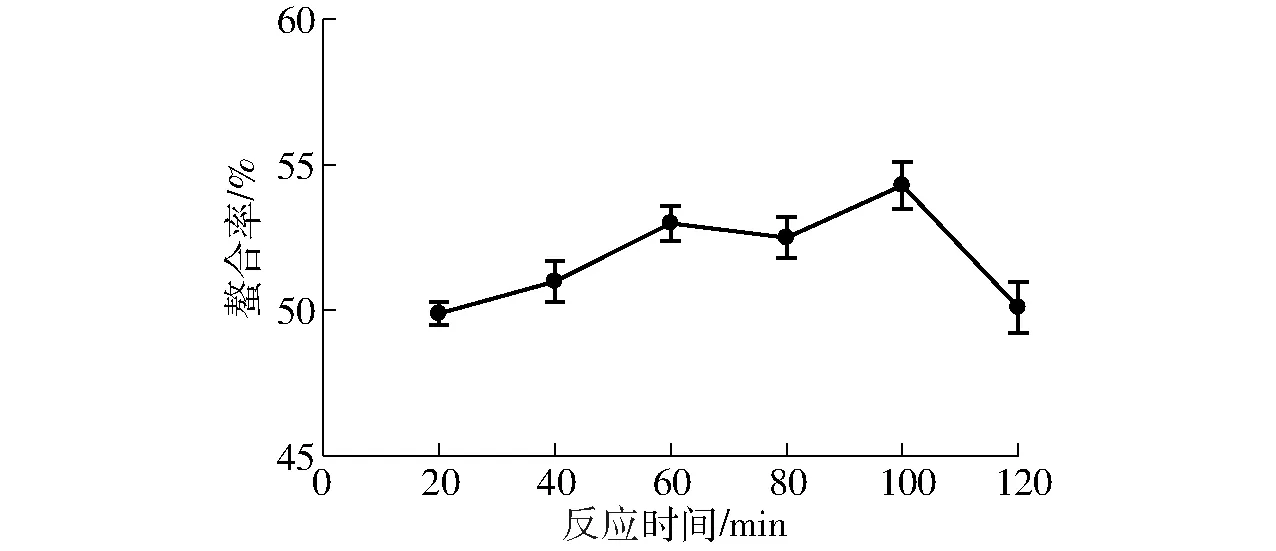
图3 反应时间对螯合率的影响Fig.3 Effect of reaction time on chelation rate
(4)CCOS与CaCl2质量比
配体质量比是指配位体与金属离子的质量之比,是影响鳌合反应的一个重要因素。配位比过高,会使6-羧基壳寡糖的利用率下降,配位体过低,鳌合物不稳定。由图4可以看出,CCOS与CaCl2质量比对螯合率有非常显著的影响,随着质量比的不断增加螯合率不断升高,当质量比为25时,产物螯合率在85%左右,且此时钙源和6-羧基壳寡糖的利用率都比较高,当质量比进一步增加,螯合率升高的趋势并不明显。说明增大配位比可以推动螯合反应向有利的方向进行,但过大的配位比显然会造成配体的浪费。因此,选择CCOS与CaCl2质量比25作为优化试验中质量比设计中点。
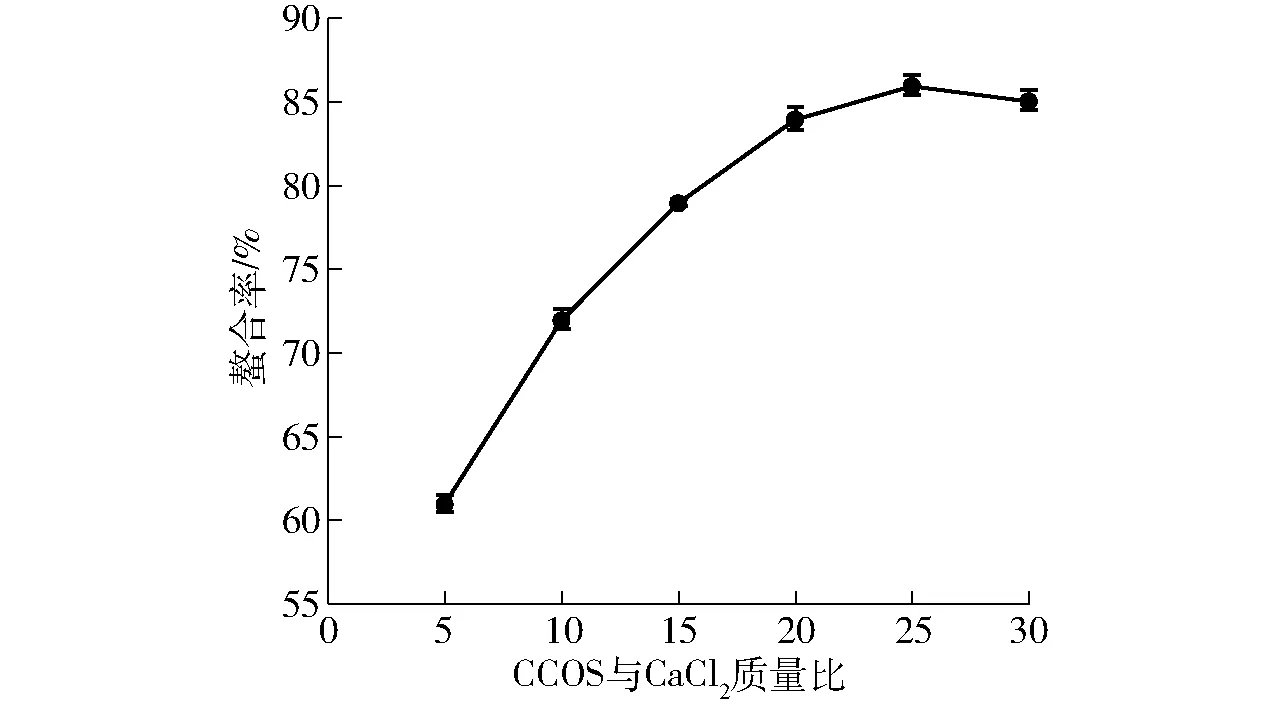
图4 CCOS与CaCl2质量比对螯合率的影响Fig.4 Effect of CCOS and CaCl2 mass ratio on chelation rate
2.2 试验结果
试验方案设计与结果如表2所示,表中A、B、C分别为pH值、反应温度、CCOS与CaCl2质量比的编码值。

表2 试验方案与结果Tab.2 CCRD experiment design and response values
2.3 模型的建立与检验
利用Design-Expert 8.0.6数据处理系统对试验结果进行方差统计分析,结果如表3所示。
由表3的方差分析可以看出,回归模型高度显著(p<0.001),模型R2=0.945 5,矫正R2=0.920 9,说明模型拟合良好;模型失拟项表示模型预测值与实际值不拟合的概率,表3中模型失拟项的p值大于0.05表明模型失拟项不显著,回归方程能较好地解释响应结果并预测最佳螯合工艺条件,图5~7直观地反映了各因素对CCOS-Ca(Ⅱ)螯合率的影响。
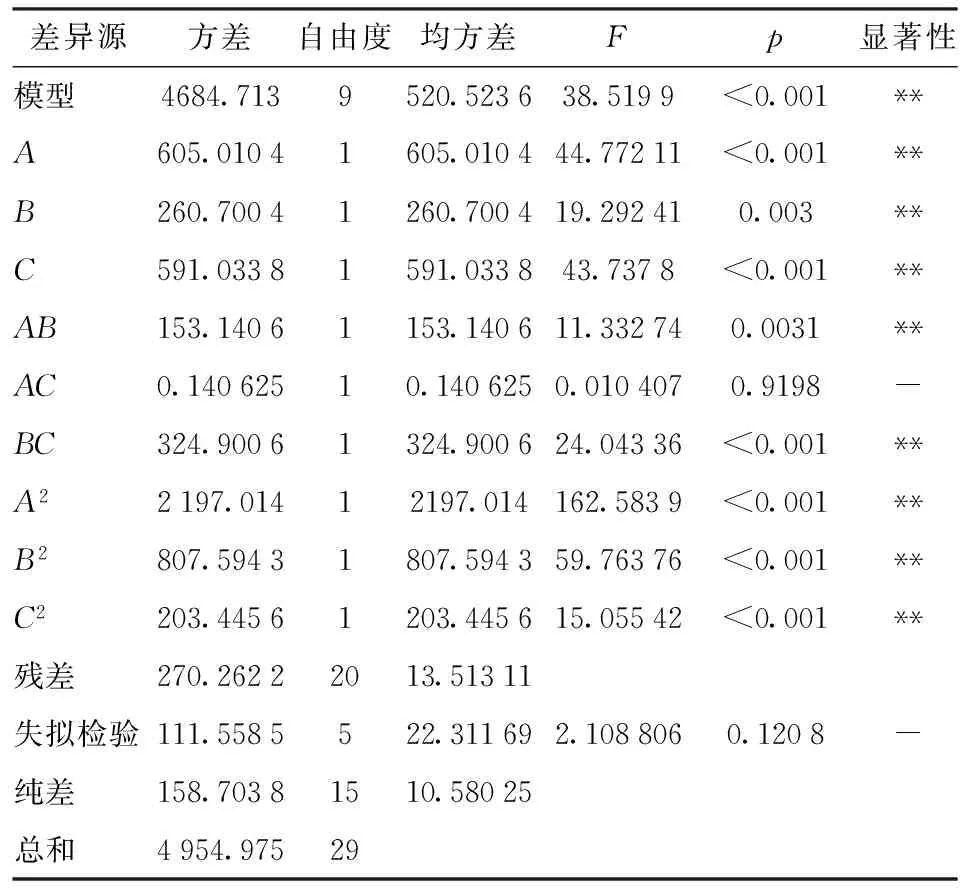
表3 螯合率回归方程方差分析Tab.3 Variance analysis of chelating rate
注:** 表示极显著,-表示不显著。

图5 反应温度和pH值对螯合率的影响Fig.5 Effect of reaction temperature and pH value on chelation rate
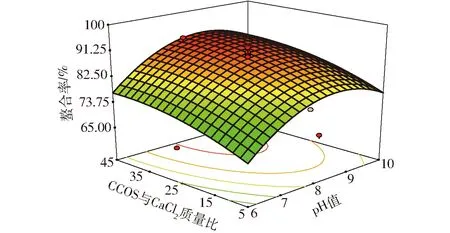
图6 CCOS与CaCl2质量比和pH值对螯合率的影响Fig.6 Effect of pH value and mass ratio on chelation rate

图7 CCOS与CaCl2质量比和反应温度对螯合率的影响Fig.7 Effect of reaction temperature and mass ratio on chelation rate
从表3回归方程系数显著性检验可知,该模型A、B、C、A2、B2、C2、AB、BC对产品螯合率的影响均达到了极显著的水平(p<0.01),而AC(p=0.919 8)对螯合率的影响作用不显著。在试验的范围内,对CCOS-Ca(Ⅱ)螯合率的影响从大到小依次为:pH值、质量比、反应温度。根据方差分析和回归方程系数显著性检验结果,将差异不显著因子剔除后的回归方程为
Y=88.89+5.02A-3.30B+4.96C-3.09AB+
4.51BC-8.86A2-5.37B2-2.70C2
得到CCOS-Ca(Ⅱ)螯合率与真实值之间关系的回归方程为
Y=-730.77+161.98P+6.39T-0.48NP+
0.05TN-8.85P2-0.05T2-0.03N2
模型预测最高螯合率为91.91%,对应pH值为8.29,温度为49.97℃,CCOS与CaCl2质量比为34.24,考虑到实际操作的简便性,将参数修正为:pH值8.3,反应温度50℃,CCOS与CaCl2质量比34。在此优化后工艺条件下,验证试验螯合率为88.86%,验证试验值与预测值误差较小,不存在显著性差异(p>0.05),说明优化试验较为成功。验证试验值与预测值误差较小,说明模型拟合较好。
2.4 CCOS-Ca(Ⅱ)红外光谱分析

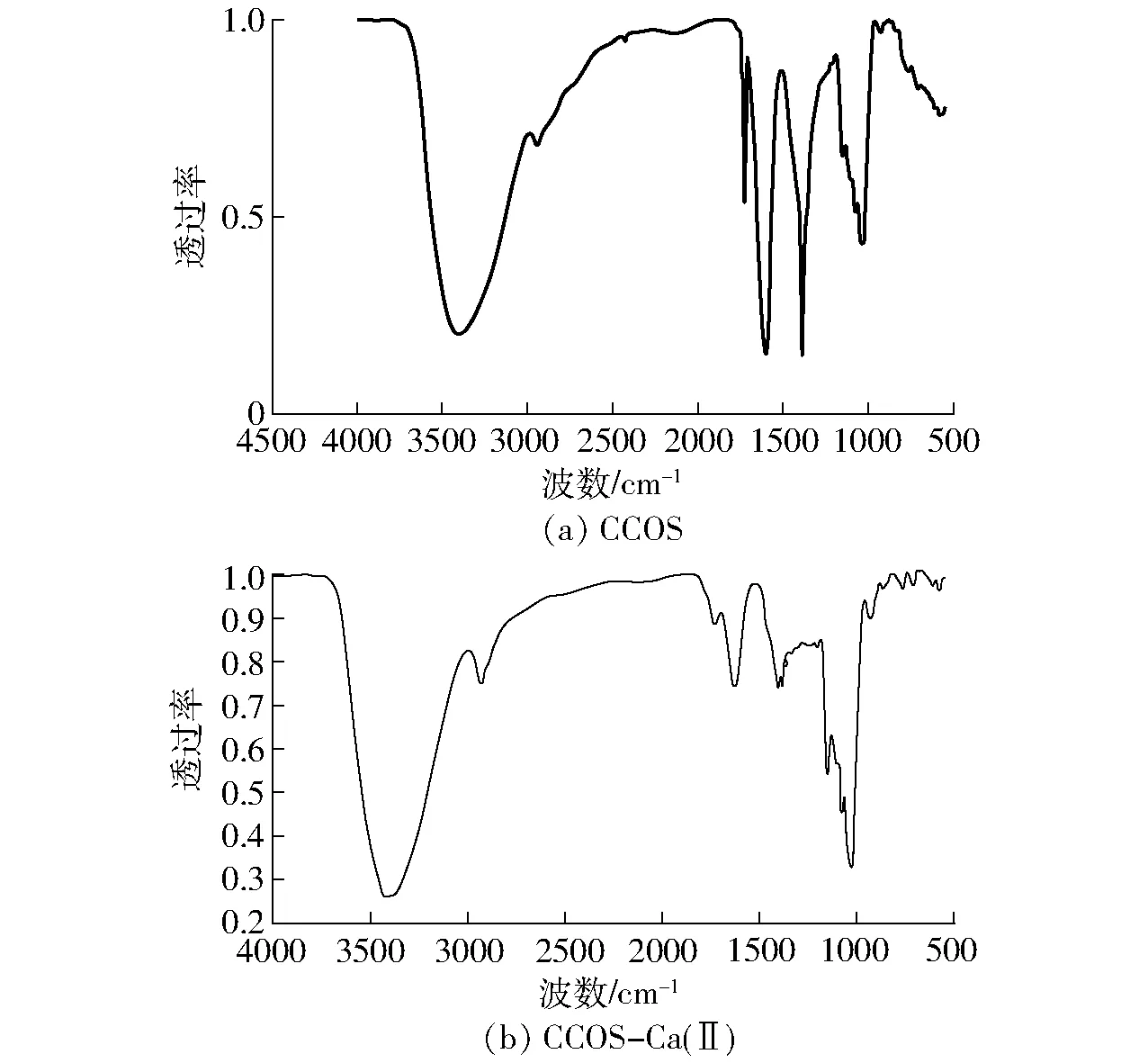
图8 CCOS和CCOS- Ca(Ⅱ)红外光谱图Fig.8 Infrared spectra of CCOS and CCOS- Ca(Ⅱ)
2.5 螯合物元素分析
表4列出了6-羧基壳寡糖、6-羧基壳寡糖合钙的元素分析数据。可计算出6-羧基壳寡糖分子中各个元素的原子个数比为5.95∶9.16∶1∶8.16,单元残基的分子组成接近于C6H9O5N, 6-羧基壳寡糖螯合钙各个原子数比为11.75∶18.41∶1.97∶1,由此可推算出配合物中6-羧基壳寡糖与Ca2+的大致配位比为2∶1,即相当于6-羧基壳寡糖分子中的2个氨基葡萄糖单元残基与1个Ca2+配位。

表4 螯合物的元素分析Tab.4 Elements analysis of 6-carboxy-chitooligosaccharide chelated calcium %
3 讨论
壳寡糖/壳聚糖及其衍生物中因存在着有良好配位能力的氨基和羟基以及羧基,对金属具有良好的配位作用。以壳寡糖或者改性壳寡糖为基体络合金属离子所得金属配合物材料具有许多独特的物理、化学性质,比如抗氧化[19-20]、抗菌[21]、脱除动物体内重金属[22-23]等功能,另外壳寡糖及其衍生物良好的生物相容性和可降解性使其有望成为人体微量元素钙、铁、锌等的补给剂[24-26]。为了提高壳寡糖对金属离子的吸附、螯合能力,近年来有学者通过引入羧基对其改性,杨华[24]研究发现,壳寡糖改性后所得的羧甲基壳寡糖对锌的吸附能力明显提高,许聪等[25]、许才利等[26]研究发现,羧甲基壳寡糖对稀土元素钆和金属元素铁的络合能力强于壳寡糖且热稳定性更好。
本研究通过直接对壳寡糖C6位羟甲基氧化生成羧基,较引入乙酸对其进行羧基化改性工艺更具经济性,经过螯合工艺优化后,通过元素分析初步推断CCOS与Ca2+摩尔比为2∶1,即2个CCOS分子螯合1个Ca2+,高于田金花等[27]、王金明等[28]研究中壳寡糖对同样价态的锌离子的络合能力。本文研究发现CCOS对金属的配位能力受体系pH值影响最为显著,在pH值相对中性条件下螯合率较高,体系过酸,H+过多,影响—NH2和—COOH在体系中的存在状态,进而影响螯合产物的形成,而体系过碱,OH-过多而与钙形成沉淀,而降低螯合率,刘艳如等[29]也研究发现壳寡糖与金属钙离子发生配位反应时,当溶液的pH值呈酸性时,溶液中的—NH3+浓度增大,—NH2浓度减小,平衡朝锌络合物解离方向移动;螯合率受体系温度的影响也较为明显,反应温度50℃附近,螯合产物最为稳定,温度过高会使得已经形成的螯合物发生解离;受反应时间影响不显著,螯合过程迅速,这与赵丽娜等[30]、桑亚新等[31]研究结果一致,本文研究所得最高螯合率为88.86%,高于骨胶原、多肽、氨基酸等[4-5,14-15,32]对钙离子的螯合能力。
4 结论
(1)利用壳寡糖(COS)制备6-羧基壳寡糖(CCOS),将壳寡糖C6位上的羟甲基直接氧化成为羧基,研究了CCOS对钙离子的络合性能,考察了体系pH值、反应温度、反应时间、CCOS与CaCl2质量比对螯合率的影响规律,研究结果表明,体系pH值、反应温度对螯合率影响显著,反应时间对螯合率影响不显著。
(2)通过中心复合旋转设计优化确定了CCOS-Ca(Ⅱ)制备的最终工艺参数为:反应pH值为8.3,反应时间60 min,反应温度50℃,CCOS与CaCl2质量比为34。在此优化工艺条件下,验证试验螯合率为88.86%。方差分析与检验结果表明,pH值、反应温度、CCOS与CaCl2质量比以及3个因素的平方项,pH值和反应温度、pH值和质量比的交互作用对产品螯合率的影响均达到了极显著的水平(p<0.01)。
(3)对产物进行傅里叶变换红外光谱扫描及元素分析,结果表明,螯合前后两者在化学结构上存在一定的变化,较好地证明了钙螯合物的形成,CCOS-Ca(Ⅱ)配合物的的结构初步认为CCOS与Ca2+摩尔比为2∶1。
1朱晓霞,汪国英,朱贤英. 钙的作用机理及如何安全补钙的研究现状[J]. 保健医学研究与实践,2014,11(1):91-94.
ZHU Xiaoxia, WANG Guoying, ZHU Xianying. The research reality on the functioning mechanism of calcium and the safe supplementation of calcium[J]. Health Medicine Research and Practice, 2014,11(1): 91-94. (in Chinese)
2ROBERT P H,BESS D H,GALLAGHER J C, et al. The role of calcium in peri-and postmenopausal women: consensus opinion of the North American Menopause Society[J].The Journal of the North American Menopause Society,2001,8(2): 84-95.
3宋俊梅, 曲静然. 促进骨钙生物可利用性的研究[J].食品科技,2002(2): 60-62.
SONG Junmei, QU Jingran. Study on the enhancement of bone calcium [J]. Food Science and Technology, 2002 (2): 60-62. (in Chinese)
4赵妍嫣,胡林林,姜绍通. 猪骨粉制备胶原多肽螯合钙工艺优化[J]. 农业工程学报,2011,27(增刊2):277-281.
ZHAO Yanyan, HU Linlin, JIANG Shaotong. Optimum conditions of producing collagen polypeptide chelated Ca using pig bone[J]. Transactions of the CSAE, 2011, 27(Supp.2): 277-281. (in Chinese)
5陆剑锋,孟昌伟,李进,等. 斑点叉尾鱼骨胶原多肽螯合钙的制备及其特征[J].水产学报,2012,36(2):314-320.
LU Jianfeng, MENG Changwei, LI Jin, et al. Preparation and characterization of collagen polypeptide chelated calcium from fish bone powder of channel catfish (Ictaluruspunctatus) [J]. Journal of Fisheries of China, 2012, 36(2): 314-320. (in Chinese)
6张凯,侯虎,彭喆,等. 鳕鱼骨明胶多肽螯合钙制备工艺及其在体外模拟消化液中的稳定性[J].食品科学,2016,37(24):1-7.
ZHANG Kai, HOU Hu, PENG Zhe, et al. Optimization of preparation of calcium-chelated cod bone gelatin peptide and its stability in simulated gastrointestinal system[J]. Food Science, 2016,37(24): 1-7. (in Chinese)
7NARIN C, BENJAMAS C, NUALPUN S, et al. Calcium-peptides derived from tilapia(Oreochromisniloticus) protein hydrolysate[J].European Food Research and Technology,2013,236: 57-63.
8胡振珠,杨贤庆,马海霞,等.罗非鱼骨粉制备氨基酸螯合钙及其抗氧化性研究[J].食品科学,2010,31(20):141-145.
HU Zhenzhu, YANG Xianqing, MA Haixia, et al. Preparation, indentifi cation and antioxidant activity of Tilapia fish skin collagen polypeptide chelated calcium[J]. Food Science, 2010,31(20): 141-145. (in Chinese)
9薛荣涛,李翠芹,何腊平. 复合氨基酸螯合钙的研究进展[J].食品工业科技,2014,35(21):390-394.
XUE Rongtao, LI Cuiqin, HE Laping. Research progress in compound amino acid chelated calcium[J]. Science and Technology of Food Industry, 2014,35(21): 390-394. (in Chinese)
10张新娜,孙君社,王淑豪,等. 羧甲基壳聚糖亚铁配合物的表征及其对CO的吸附研究[J]. 高校化学工程学报,2011,25(1):91-95.
ZHANG Xinna, SUN Junshe, WANG Shuhao, et al. Study on the N-O-Carboxymethyl Chitosan-Fe2+complex and its adsorption of CO[J]. Journal of Chemical Engineering of Chinese Universities, 2011,25 (1): 91-95. (in Chinese)
11乔莹,恽小婧,白雪芳,等. 壳寡糖与骨关节病相关性研究进展[C]∥全国第八届中西医结合风湿病学术会议论文汇编,2010.
12杨文炳,姚芬英.复合氨基酸铁合成及其鳌合反应研究[J].化学通报,1991(1):46-47.
13窦丽娜. 低聚谷氨酸钙的制备条件及功能特性研究[D].郑州:河南工业大学,2010.
DOU Li’na. The study on preparation and functional properties of oligomeric glutamate calcium[D].Zhengzhou:Henan University of Technology, 2010. (in Chinese)
14韩克光,甄守艳,范华,等.钙螯合羊骨胶原多肽的制备及表征分析[J].农业工程学报,2015,31(21):301-307.
HAN Keguang, ZHEN Shouyan, FAN Hua, et al. Preparation and characteristic analysis of calcium-chelated ossein peptide[J]. Transactions of the CSAE, 2015, 31(21): 301-307. (in Chinese)
15张妹,过世东.氨基酸多肽螯合钙的制备及其工艺优化[J]. 食品与生物技术学报,2014,33(4):422-425.
ZHANG Shu, GUO Shidong. Study on preparation and optimization of amino acid chelated calcium[J]. Journal of Food Science and Biotechnology, 2014,33(4): 422-425. (in Chinese)
16王伟. 固相法制备壳聚糖羧酸盐及其结构、性质和应用研究[D].南宁:广西大学,2008.
WANG Wei. The chitosan carboxylic acid saits: preparation by solide-phase way, structure, properties and application[D].Nanning:Guangxi University,2008. (in Chinese)
17回瑞华,关崇新,侯冬岩. 羧酸及其盐红外光谱特性的研究[J]. 鞍山师范学院学报,2001,3(1):95-98.
HUI Ruihua, GUAN Chongxin, HOU Dongyan. Study on IR characteristics of carboxylic acid and their salts[J]. Journal of Anshan Normal University,2001,3(1):95-98. (in Chinese)
18于世林, 李寅蔚,夏心泉,等.波谱分析[M].重庆:重庆大学出版社,1991
19吕新刚,刘兴华,蔡露阳.壳聚糖涂膜对苹果虎皮病防治效果与机理研究[J].农业机械学报,2011,42(3):131-135.
LÜ Xin’gang, LIU Xinghua, CAI Luyang. Effects and mechanism of chitosan coatings in the control of superficial scald in apples[J]. Transactions of the Chinese Society for Agricultural Machinery, 2011,42(3):131-135. (in Chinese)
20罗自生,徐晓玲,徐庭巧,等.壳聚糖添加纳米碳酸钙助剂对鲜切山药品质的影响[J].农业机械学报,2009,40(4):125-128.
LUO Zisheng, XU Xiaoling, XU Tingqiao, et al. Effect of chitosan coating with nano-CaCO3appendix on quality of fresh cut yam [J]. Transactions of the Chinese Society for Agricultural Machinery, 2009,40(4):125-128. (in Chinese)
21杨楠,徐翠莲,杨国玉,等. 壳寡糖希夫碱金属配合物的合成及其对烟草花叶病毒的抑制活性[J]. 农药学学报,2010,12(1):31-36.
YANG Nan, XU Cuilian, YANG Guoyu, et al. Synthesis and biologicalactivity of chitooligosaccharides Schiff base metal complexes[J]. Chinese Journal of Pesticide Science,2010,12(1):31-36. (in Chinese)
22孙继鹏,汪东风,李国云,等. 壳寡糖钙、镁配合物对栉孔扇贝体内镉的脱除[J]. 中国海洋大学学报:自然科学版,2010,40(2):33-37.
SUN Jipeng, WANG Dongfeng, LI Guoyun, et al. The removal of cadmium from chlamys ferrari by chitosan oligosaccharide complexes with Ca and Mg[J]. Periodical of Ocean University of China: Natural Science Edition, 2010,40(2): 33-37. (in Chinese)
23黄国清,李志茹,朱常龙,等. 壳寡糖-金属配合物对太平洋牡蛎体内中Cd脱除效果的研究[J]. 中国食品学报,2012,12(4):121-126.
HUANG Guoqing, LI Zhiru, ZHU Changlong, et al. Effect of chitosan oligosaccharide-metal complex on cadmiun removal from oyster crassostrea gigas[J]. Journal of Chinese Institute of Food Science and Technology, 2012,12(4):121-126. (in Chinese)
24杨华. 壳寡糖和羧甲基壳寡糖对Zn(Ⅱ)的络合性能研究[C]∥2012年中国药学大会暨第十二届中国药师周论文集,2012.
25许聪,杨华,黄杨. 羧甲基壳寡糖与钆配合物的制备[J]. 功能高分子学报,2013,26(1):104-108.
XU Cong, YANG Hua, HUANG Yang. Preparation of coordination compound of carboxymethyl chitooligosaccharides and gadolinium nitroxide[J]. Journal of Functional Polymers, 2013,26(1): 104-108. (in Chinese)
26许才利,唐星华. 新型补铁剂羧甲基壳寡糖-亚铁的制备研究[J]. 南昌航空工业学院学报:自然科学版,2006,20(1):43-45.
XU Caili, TANG Xinghua. Study on the preparation of the ferrous carboxymethyl chitooligosaccharides for a new ferruginous[J]. Journal of Nanchang Institute of Aeronautical Technology:Natural Science Edition, 2006,20(1): 43-45. (in Chinese)
27田金花,杨华,迟光伟,等. 壳寡糖锌(Ⅱ)配合物的合成与结构表征[J]. 高分子通报,2011(1):71-74.
TIAN Jinhua, YANG Hua, CHI Guangwei, et al. Synthesis and characterization of chitooligosaccharides-zinc complex[J]. Chinese Polymer Bulletin, 2011(1): 71-74. (in Chinese)
28王金明,黄卫红,闫永胜,等.壳寡糖锌配合物的合成、表征及动力学研究[J]. 食品科技,2010,35(5):244-247.
WANG Jinming, HUANG Weihong, YAN Yongsheng, et al. Synthesis, characterization and adsorptive kinetics of the chitooligosaccharide-Zn coordination[J]. Food Science and Technology, 2010,35(5): 244-247. (in Chinese)
29刘艳如,陈盛,余萍.水溶性壳聚糖的制备及其钙离子的络合[J].福建师范大学:自然科学版,1997,13(3): 67-70.
LIU Yanru, CHEN Sheng, YU Ping. The preparation of water-soluble low-molecular weight chitosan and the complex with calcium ions[J]. Fujian Normal University:Natural Science Edition, 1997,13(3): 67-70. (in Chinese)
30赵立娜,汪少芸,张亚娇,等. 响应面法优化乳清蛋白肽螯合钙离子的研究[J]. 中国食品学报,2014,14(4):64-71.
ZHAO Li’na, WANG Shaoyun, ZHANG Yajiao, et al. Optimization of chelation of whey protein peptides with calcium using response surface method[J]. Journal of Chinese Institute of Food Science and Technology, 2014,14(4):64-71. (in Chinese)
31桑亚新,王昌禄,王苏,等. 利用扇贝壳制备胶原螯合钙的研究[J]. 中国食品学报,2012,12(5):49-55.
SANG Yaxin, WANG Changlu, WANG Su, et al. Study on the preparation of collagen chelating calcium using shellfish[J]. Journal of Chinese Institute of Food Science and Technology,2012,12(5):49-55. (in Chinese)
32高菲,王维有,鲁军,等. 海洋鱼骨胶原肽钙螯合物的制备及红外光谱表征[J]. 中国海洋大学学报:自然科学版,2015,45(1):47-54.
GAO Fei, WANG Weiyou, LU Jun, et al. Preparation and infrared spectrum identification for marine fish ossein peptide chelated calcium[J]. Periodical of Ocean University of China:Natural Science Edition, 2015,45(1): 47-54. (in Chinese)
