满山香片的质量标准提高研究Δ
2018-04-17章光文殷海霞1段和祥杨毅生
钱 媛,洪 挺,章光文,殷海霞1,,段和祥,黄 东,杨毅生#
(1.江西中医药大学药学院,江西 南昌330004; 2.江西省药品检验检测研究院/江西省药品与医疗器械质量工程技术研究中心,江西 南昌 330029; 3.江西省食品药品监督管理局规划财务处,江西 南昌 330029)
*硕士研究生。研究方向:药学。E-mail:chain8@163.com
#通信作者:副主任中药师。研究方向:中药活性成分和质量控制研究。E-mail:1020115850@qq.com
满山香片由满山香单味中药组成,具有清热解表之功效,用于外感风热,发热头痛、咽痛及身痛。在江西民间,满山香药材常用于治疗流行性感冒,此外还用于风湿痛、月经不调、神经衰弱、补虚及驱蛔等[1]。近年来,其抗肿瘤活性成分的研究越来越受到关注[2]。该制剂现行质量标准为国家食品药品监督管理局国家药品标准颁布件[批件号:(2012)国药标字ZD-0 674号],标准编号:WS-11216(ZD-1216)-2002-2012Z,其质量标准正文收载了性状、槲皮素的薄层色谱鉴别、片剂常规检查项及高效液相色谱法测定山柰素的含量。由于质量标准较简单,并仅用山柰素这一常见化合物来控制产品质量,不能全面地反映制剂质量,不利于制剂质量的准确控制;同时,含量方法操作复杂,重现性不好。为更有效地控制制剂质量,参考相关文献[3],本研究建立了以满山香对照药材、山柰素和槲皮素对照品的薄层色谱鉴别法,修订了高效液相色谱法测定制剂中山柰素的含量方法,以保证药品的有效性和安全性。
1 材料
1.1 仪器
SHIMADZU LC-2010AD型高效液相色谱仪(四元泵;二极管阵列检测器;LC solution色谱工作站;自动进样器)(日本岛津公司);Sartorius BT25S型电子天平(德国赛托利斯公司);Sartorius BSA 124S-CW型电子天平(德国赛托利斯公司);KQ5200B型超声波清洗机(昆山市超声仪器有限公司);TLC Visualzer薄层成像系统(瑞士卡玛公司)。
1.2 药品与试剂
满山香片(江西本真药业有限责任公司,批号:20131101、20140801和20150301,规格:0.34 g/片);槲皮素对照品(批号:100081-200907,纯度:96.5%)、山柰素对照品(批号:110861-201209,纯度:93.2%),均购自中国药品生物制品检定所;对照药材(江西本真药业有限责任公司提供,经江西省药品检验检测研究院万林春副主任中药师鉴定为正品);羟甲基纤维素钠(批号:110819)、硅胶G(青岛海洋化工厂分厂,批号:20160812);甲醇为色谱纯,其余试剂均为分析纯,水为超纯水。
2 方法与结果
2.1 定性鉴别
2.1.1槲皮素、山柰素的薄层色谱法的建立:参考相关文献[4-6],取本品5片,除去包衣,研细,取约0.6 g,置于圆底烧瓶中,加入甲醇-盐酸(V∶V=10 ∶1)混合溶液50 ml,混匀,加热回流1 h,冷却,滤过,滤液蒸干,残渣加甲醇1 ml使溶解,作为供试品溶液。另取槲皮素、山柰素对照品,加甲醇分别制成每1 ml含0.1、1.0 mg的溶液,作为对照品溶液。按满山香片处方和工艺分别制备缺满山香药材的单一阴性样品,并按供试品溶液制备方法制成阴性对照溶液。照薄层色谱法[《中华人民共和国药典:四部》(2015年版)通则0502]试验,吸取上述4种溶液各5 μl,分别点于同一硅胶G薄层板上,以环己烷-乙酸乙酯-甲酸(V∶V∶V=10 ∶8 ∶1)为展开剂,展开,取出,晾干,喷以1%三氯化铝乙醇溶液,105 ℃下加热至斑点显色清晰,置于紫外光灯(365 nm)下检视。结果显示,在供试品色谱中,在与对照品色谱相应的位置上,显相同颜色的荧光斑点,阴性对照无干扰,见图1。
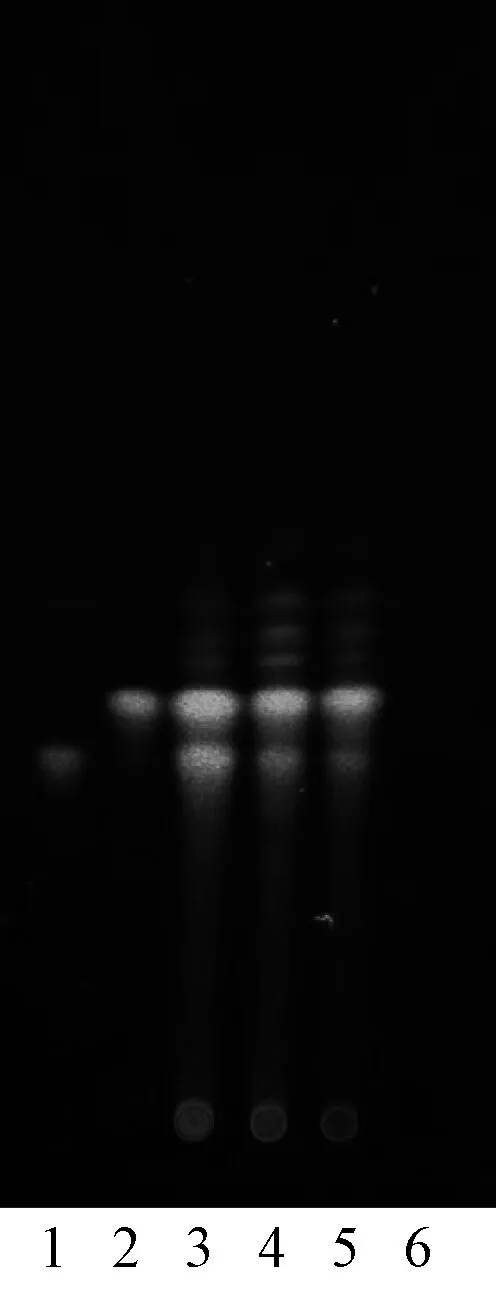
1.槲皮素对照品溶液;2.山柰素对照品溶液;3.供试品溶液 (批号:20131101);4.供试品溶液(批号:20140801);5.供试品溶液 (批号:20150301);6.阴性对照溶液 1.reference substance solution of kaempferide; 2.reference substance solution of quercetin; 3.test solution (batch number:20131101); 4.test solution(batch number: 20140801); 5.test solution(batch number:20150301); 6.negative control solution 图1 槲皮素、山柰素的薄层色谱图Fig 1 TLC chromatograms of kaempferide and quercetin
2.1.2满山香:取“2.1.1”项下供试品溶液,作为供试品溶液。参考相关文献[7-9],另取满山香对照药材0.3 g,加水50 ml煎煮2次,1次1 h,合并煎液,放冷、离心(转速为3 000 r/min),去除药渣,溶液减压浓缩至近干,加入70%乙醇溶液100 ml,搅匀,冷藏静置24 h,滤过,滤液回收乙醇至干,残渣加甲醇1 ml使溶解,作为对照药材溶液。照薄层色谱法[《中华人民共和国药典:四部》(2015年版)通则0502]试验,分别吸取上述对照品和供试品溶液各5 μl,分别点于同一硅胶G薄层板上,以三氯甲烷-乙酸乙酯-甲醇-水(V∶V∶V∶V=15 ∶40 ∶22 ∶10)于5~10 ℃放置12 h的下层溶液为展开剂,展开,取出,晾干,再喷以10%硫酸乙醇溶液,在105 ℃下加热数分钟至斑点显色清晰,分别在日光和紫外光(365 nm)下检视。结果显示,供试品色谱中,在与对照药材色谱相应的位置上,日光下显相同颜色的主斑点,紫外光下显相同颜色的荧光主斑点,见图2。
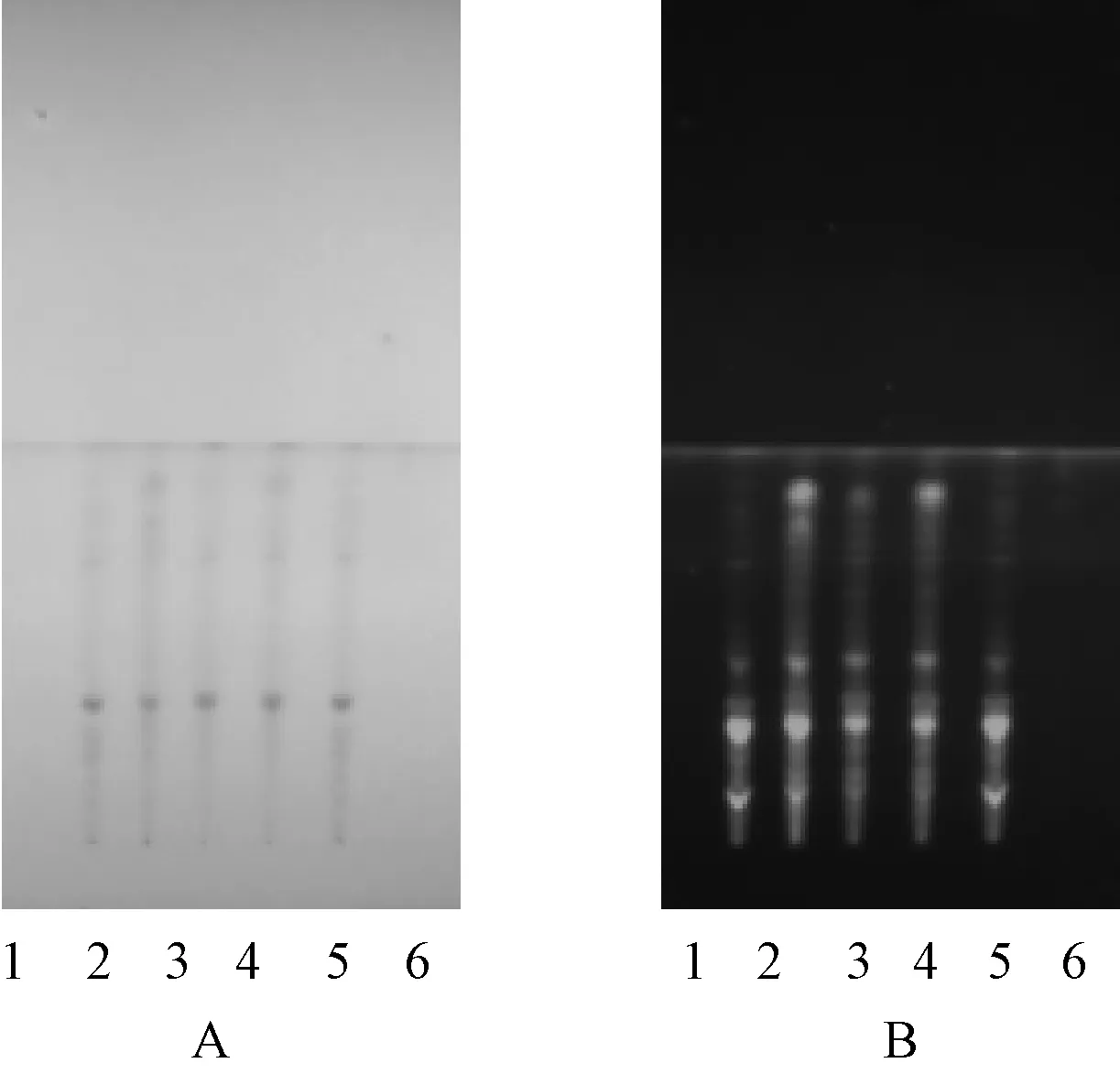
A.日光;B.紫外光(365 nm);1.满山香对照药材溶液; 2.供试品溶液(批号:20131101);3.供试品溶液(批号:20140801); 4.供试品溶液(批号:20150301);5.满山香对照药材溶液; 6.阴性对照品溶液 A.sunlight;B.ultraviolet light(365 nm);1.reference substance solution of Manshanxiang;2.test solution(batch number:20131101);3.test solution(batch number:20140801); 4.test solution(batch number:20150301);5.reference substance solution of Manshanxiang;6.negative control solution 图2 满山香的薄层色谱图Fig 2 TLC chromatograms of Manshanxiang
2.2 含量测定
2.2.1对照品溶液的制备:精密称取山柰素对照品11.11 mg,置于50 ml容量瓶中,加甲醇溶解并稀释至刻度,摇匀,即得对照品母液。精密量取上述对照品母液1 ml,置于10 ml容量瓶中,加甲醇至刻度,摇匀,即得对照品溶液。
2.2.2供试品溶液的制备:参考相关文献[10],取本品10片,除去包衣,精密称定,研细,取约0.6 g,精密称定,置于具塞锥形瓶中,精密加入甲醇50 ml,称定质量;超声处理(功率:500 W,频率:40 kHz)30 min,放冷,再称定质量,用甲醇补足减失质量;摇匀,滤过,精密量取续滤液20 ml,置于100 ml圆底烧瓶中,加盐酸3 ml,混匀,热回流1 h,然后迅速冷却至室温(25 ℃),再减压浓缩至约10 ml,转移至25 ml容量瓶中,用少量甲醇分数次洗涤容器,洗液并入容量瓶中,加甲醇稀释至刻度,摇匀,即得。
2.2.3阴性对照溶液的制备:按处方取不含满山香药材,照本制剂的制备工艺制成阴性对照样品,再按“2.2.2”项下方法制成阴性对照品溶液。
2.2.4色谱条件与系统适用性试验:色谱柱为YMC-Pack ODS-A C18柱(250 mm×4.6 mm,5 μm);流动相为甲醇-0.2%磷酸溶液(V∶V=47 ∶53);流速为1 ml/min;检测波长为365 nm;柱温为40 ℃;进样量为10 μl;在上述色谱条件下,理论板数以山柰素峰计>3 000。结果显示,各成分基线分离良好,分离度>1.5[11-12],见图3。
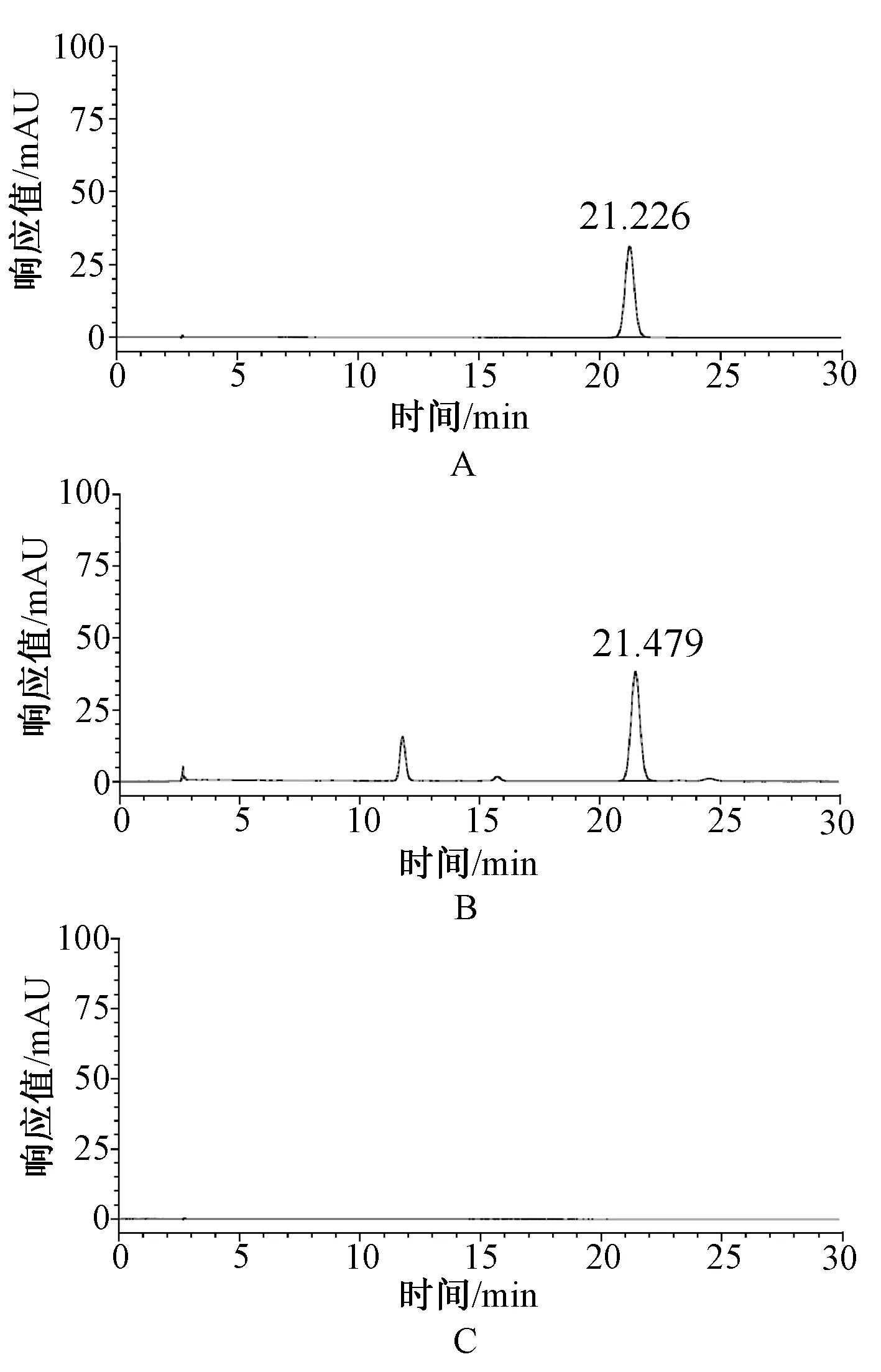
A.山柰素对照品溶液;B.供试品溶液;C.阴性对照溶液 A.reference substance solution of kaempferide; B.test solution;C.negative control solution 图3 高效液相色谱图(365 nm)Fig 3 HPLC chromatograms(365 nm)
2.2.5线性关系考察:分别吸取“2.2.2”项下对照品溶液2、5及10 μl,对照品母液2、4 μl,注入液相色谱仪中,按上述色谱条件测定对照品峰面积,以进样量为横坐标(X)、峰面积为纵坐标(Y)进行回归处理,回归方程为Y=4 104 447.089 2X-4 905.265 7(r=0.999 8),计算得山柰素对照品进样量在0.041 4~0.828 4 μg范围内与峰面积呈良好的线性关系。
2.2.6精密度试验:精密吸取“2.2.2”项下对照品溶液10 μl,按“2.2.1”项下色谱条件,重复进样6次,测定山柰素峰面积值。结果显示,重复进样6次的峰面积值分别为856 383、857 217、857 435、856 089、859 188和859 261,平均峰面积值为857 993,RSD为0.18%,表明仪器精密度良好。
2.2.7稳定性试验:精密吸取供试品溶液(批号:20150301)10 μl,按“2.2.1”项下色谱条件,分别在0、1、2、3、6、9、12和24 h,测定供试品溶液中山柰素峰面积值。结果显示,各时间点供试品山柰素峰面积值分别为960 229、961 579、962 262、960 771、962 112、960 794、962 154和963 920,平均峰面积值为962 245,RSD为0.13%,表明供试品溶液在室温(25 ℃)放置24 h内稳定性良好。
2.2.8重复性试验:取批号为20150301的样品,照“2.2.3”项下方法制成6份供试品溶液,按“2.2.1”项下色谱条件进行测定,计算山柰素含量。结果显示,山柰素含量的RSD为1.28%,表明本方法重复性良好,见表1。
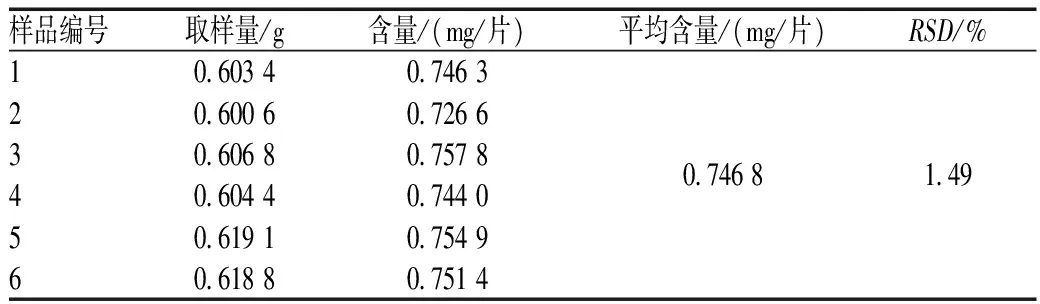
表1 重复性试验结果Tab 1 Results of repeatability tests
2.2.9加样回收率试验:取已知含量样品(批号:20150301,山柰素含量为2.422 7 mg/g)适量,除去包衣,精密称定,研细,取6份,每份约0.3 g,精密称定,置于具塞锥形瓶中,精密加入甲醇25 ml,再分别精密加入含山柰素(质量浓度为0.031 8 mg/ml)对照品溶液25 ml,称定质量;超声处理(功率:500 W,频率:40 kHz)30 min,放冷,再称定质量,用甲醇补足减失质量,摇匀,滤过;精密量取续滤液20 ml,置于圆底烧瓶中,加盐酸3 ml,混匀,加热回流1 h,迅速冷却至室温(25 ℃),减压浓缩至约10 ml,移至25 ml容量瓶中,用少量甲醇分数次洗涤容器,洗液并入量瓶中,加甲醇至刻度,摇匀,即得。再按“2.2.1”项下色谱条件进样测定,记录峰面积并计算加样回收率,结果见表2。
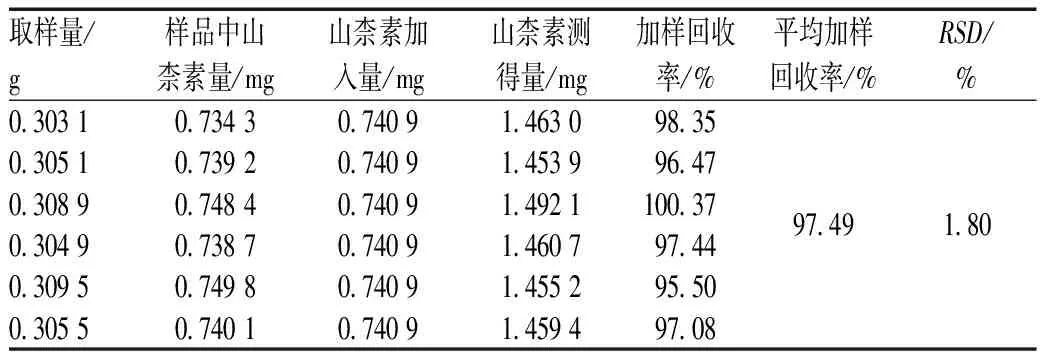
表2 加样回收率试验结果(n=6)Tab 2 Results of sample recovery tests(n=6)
2.2.10耐用性试验:取本品(批号:20150301),照“2.2”项下方法制备,分别用A[Agilent Eclipse Plus C18柱(250 mm×4.6 mm,5 μm)]、B[SHIMADZU Inertsil ODS-SP柱(250 mm×4.6 mm,5 μm)]和C[COSMOSIL 5C18-AR-Ⅱ柱(250 mm×4.6 mm,5 μm)]三种品牌的色谱柱,按正文中的色谱条件对其进行测定。结果显示,山柰素含量的RSD为0.91%,三种品牌色谱柱无明显差别。
2.2.11样品含量测定:取3批样品各适量,分别按“2.2.2”项下方法制备供试品溶液,于“2.2.1”项下色谱条件进样测定,记录峰面积并计算样品含量,结果见表3。
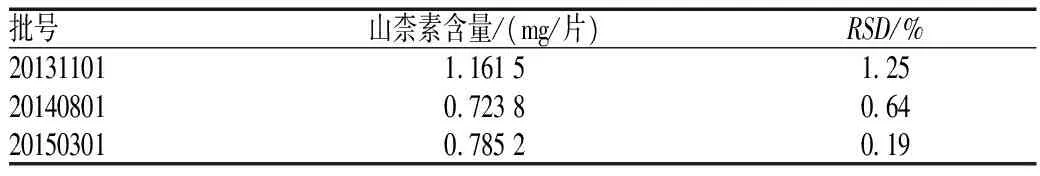
表3 样品含量测定结果(n=3)Tab 3 Results of content determination of samples(n=3)
3 讨论
满山香具有广泛而显著的药理作用,在民间具有悠久的使用历史,其治疗感冒发热具有良好的临床效果,因而具有很大的潜在药用价值,其已被开发出满山香片制剂,临床用于外感风热,发热头痛、咽痛及身痛等。采用满山香对照药材薄层色谱法鉴别控制满山香片的质量,确保原料的质量,可以大幅度提高药品的质量,保证药品的有效性,从而确定满山香片的疗效;通过山柰素的含量测定严格控制药品质量,山柰素类化合物亦是满山香片的主要有效成分之一,可以严格控制药品质量,保证药品安全、有效。
本研究仅对山柰素进行含量测定是因为经过多次实验发现槲皮素在制剂中的含量比较低,而且较不稳定,含量差异较大,推测槲皮素可能是以结合形式存在于制剂中,故未选用槲皮素进行含量鉴别。原质量标准中,在山柰素含量测定方面,通过超声提取后加酸水解,最后使用聚酰胺住富集山柰素的含量制得供试品。但经过多次实验发现,过聚酰胺柱并没有起到富集作用,且对山柰素在制剂中的含量影响较大,方法复杂,重现性差,对质量控制不利,故本研究仅通过考察酸水解等因素简化实验步骤,方法稳定可控,利于山柰素含量测定。
3.1 定性指标的选择
本研究分别优化了供试品与对照品的点样量,比较了预制板和自制板对斑点的影响,考察了不同温湿度下的展开情况,充分查阅文献,通过优化显色剂,得到清晰的薄层色谱斑点,充分验证了薄层色谱鉴别法的重现性和耐用性。在满山香药材薄层色谱中,对满山香对照药材处理方法也进行了考察,对比了药材用甲醇直接超声和按照处方工艺处理的差异。结果表明,按照处方工艺来处理,使满山香对照药材和供试品色谱斑点基本相同,更能真实客观地反应出满山香药材的色谱行为,能系统地评价所使用满山香药材的质量,从而准确反应出满山香片的质量。
3.2 含量测定条件的选择
按原质量标准对3批供试品进行含量测定检验时,发现测定结果不准确,重现性较差,且操作较复杂。查阅文献发现,满山香药材中山柰素主要是以结合苷的形式存在,游离量非常少,考虑到可能是盐酸用量和酸水解时间对其含量的影响[13-16]。因此,本研究针对性地对山柰素的含量测定条件进行摸索:首先,考察了超声时间对含量的影响。分别超声20、30、40及50 min,结果显示,山柰素的含量分别为0.60、0.76、0.75及0.76 mg/片,表明超声30 min已经超声完全,故选择超声30 min。其次,考察了盐酸用量情况。盐酸加入量分别为0.5、1.0、2.0、3.0及4.0 ml,结果显示,山柰素的含量分别为0.46、0.56、0.72、0.76及0.76 mg/片,可见盐酸用量对结果影响较大,且盐酸用量3.0与4.0 ml时的测定结果无显著差异,表明酸水解基本完全,故盐酸用量选取3.0 ml。再次,考察了水解时间的影响。分别加热回流20、30 min和1、2、3 h,结果显示,山柰素的含量分别为0.41、0.74和0.75、0.73、0.61 mg/片,表明加热回流30 min与1 h的测定结果无显著差异,而2、3 h的测定结果呈下降趋势,考虑到样品批次间差异,为保证酸水解完全,故加热回流时间选取1 h。最后,考察了水浴温度对水解的影响。分别采用60、80及100 ℃的水浴温度,结果显示,山柰素的含量分别为0.52、0.70及0.75 mg/片,表明水浴温度为100 ℃时酸水解最为彻底,故采用水浴100 ℃。另外,原标准中需要对水解后的溶液进行聚酰胺柱纯化,经研究发现,在高效液相色谱图谱中山萘素色谱峰旁边未有其他色谱峰干扰,且峰面积在聚酰胺柱纯化前后差异不大,故删除该聚酰胺纯化过程。
[1]田景奎,邹忠梅,徐丽珍,等.细梗香草化学成分的研究[J].中国药学杂志,2006,41(3):171-173.
[2]徐燕,荣语媚,刘小保,等.细梗香草总皂苷的抗肿瘤活性研究[J].中国药理学通报,2012,28(4):545-549.
[3]林贵兵,罗光明,许燕萍,等.HPLC法对细梗香草中槲皮素和山奈酚含量的测定[J].湖北农业科学,2014,53(23):5848-5850,5854.
[4]李彩丽,平欲晖.HPLC测定芒萁中槲皮素和山柰素的含量[J].中国实验方剂学杂志,2015,21(19):64-66.
[5]郝庆秀,刘超,金艳,等.彝药满山香的资源调查和鉴别研究[J].中国现代中药,2015,17(7):698-703.
[6]李刚,封传华,张静,等.HPLC法测定山柰药材中山柰素的含量[J].中国药房,2016,27(18):2558-2559.
[7]陈吓俤,谢淑芳,郑小珍,等.金线莲中槲皮素的超声提取及HPLC法测定[J].湖北农业科学,2016,55(20):5324-5326.
[8]应弘梅.细梗香草总皂苷制备工艺及质量标准研究[D],杭州:浙江大学,2011.
[9]兰霞,王洪新.比色法测定甘草中总皂苷的含量[J].时珍国医国药,2007,18(4):886-887.
[10]梁莹莹,张淑君,赫军,等.痛块消口服液的质量标准研究[J].中国药房,2017,28(3):374-376.
[11]万德光,裴瑾,唐远,等.分光光度法测定威灵仙中总皂昔的含量[J].成都中医药大学学报,2007,30(3):52-53.
[12]陈希,万林春,张文婷.抗骨增生片的质量标准提高研究[J].中国药房,2017,28(6):838-841.
[13]李喜香,李兴勇,包强,等.骨痹止痛液的质量标准提高研究[J].中国药房,2017,28(9):1249-1253.
[14]郑云枫,李家春,彭国平.高效液相色谱法测定柘木中山柰素含量[J].医药导报,2007,26(2):191-192.
[15]刘知远,沈廷明,吴仲玉.RP-HPLC法同时测定福建产金线莲中槲皮素、山柰素、异鼠李素的量[J].中草药,2015,46(3):432-434.
[16]杜安全,王先荣,周正华,等.银杏叶总黄酮苷的HPLC法分析水解条件[J].安徽医药,2001,5(3):164-165.
