针铁矿和针铁矿—胡敏酸复合体对Se(Ⅳ)吸附机制*
2018-04-13许海娟魏世勇杨小洪
王 锐 许海娟 魏世勇 方 敦 杨小洪
(湖北民族学院化学与环境工程学院,恩施 445000)
硒是人类和动物必需的微量元素,适量的硒具有提高人体免疫机能、抗癌和抗衰老等功能[1-3]。硒的摄入量不足可引起克山病、大骨节病等疾病,而过量的硒会出现脱发、指甲变脆、肝增大等中毒症状[2-3]。表生环境中不同形态的硒具有不同的环境行为和生物有效性[4-7]。可见,人畜体内硒的供应状况受制于环境中硒的总量和赋存形态。亚硒酸盐(Se(IV))是土壤最常见的硒形态,其生物有效性较高,是植物的主要硒营养源[1,5-6]。土壤金属氧化物、有机质等固相组分可与硒相互作用,影响土壤硒的赋存形态和生物有效性[8-9]。氧化铁和腐殖酸是土壤的重要固相组分,可与不同形态的硒发生多种界面作用,从而改变土壤硒的形态分布[7,10-13]。土壤中氧化铁和腐殖酸通常紧密相伴,并通过一定的作用力结合形成复合体[14-15]。土壤腐殖质—氧化物复合体是土壤肥力的基础物质,又是土壤中营养元素和环境污染物迁移转化的重要影响因子[16-18]。因此,研究氧化铁—腐殖酸复合体与硒相互作用的过程和机制,有助于深入认识土壤硒的地球化学行为。
针铁矿是最常见的土壤晶质氧化铁,广泛分布于各类土壤中。针铁矿对Se(IV)的吸附数据符合Langmuir方程,而Freundlich方程适合描述铁/铝复合氧化物的吸附过程[19-20]。针铁矿对Se(IV)的吸附约3 h即可平衡,吸附过程符合二级动力学模型,其平衡吸附数据符合扩散双电层模型(DDLM)[21-22]。针铁矿和赤铁矿对Se(IV)的吸附类型主要为单齿内圈配位,而非晶质氧化铁对Se(IV)的吸附以双齿内圈配位为主[10,23-24]。X-射线吸收精细结构(XAFS)分析表明,Se(IV)和Se(VI)均可与针铁矿表面两个单配位的羟基形成双核桥联配合,其有效位点主要位于针铁矿(010)面[21,25]。腐殖酸是土壤有机质的主体,可与土壤营养元素和污染物相互作用形成稳定性的络合物[26-27]。Coppin等[28]研究显示,相同条件下土壤腐殖酸对硒的吸附量低于铁/铝氧化物。腐殖酸对硒的吸附量随其分子质量减小而逐渐升高[29]。羧基、羟基、芳香碳含量高及C/O比例低的腐殖酸与硒有较强的结合能力[29-30]。研究显示,腐殖酸中芳香碳和含氧基团在吸附硒的过程中起重要作用,而表面负电荷会在一定程度上抑制吸附作用[29-30]。腐殖酸吸附硒的机制主要为表面配位,Se(IV)和Se(VI)能够在腐殖酸结构中相邻的两个羧基、羟基或羧基及羟基间螯合成键,也可与一个羧基或羟基形成单齿配合物[30-31]。
可见,有关氧化铁和腐殖酸与硒的相互作用已有较多研究成果。土壤中氧化铁和腐殖酸很少单独存在,它们往往通过多种微观作用彼此胶结而复合[14-15]。研究表明,氧化铁—腐殖酸复合体中腐殖酸可包被于氧化铁表面,显著影响氧化铁的表面性质[14]。土壤腐殖酸通过改变氧化铁的表面理化性质,影响矿物表面的吸附、溶解、沉淀等过程,从而控制一些营养元素和环境污染物在土壤中的赋存形态、化学行为和生物有效性[14,32-33]。可以推断,氧化铁—腐殖酸复合体对硒的吸附作用应该不同于两种单体的独立效应,然而,迄今尚未见有关这方面的研究报道。为此,本研究制备了针铁矿和针铁矿—胡敏酸复合体,以对比的方式研究了它们与Se(IV)相互作用的机制。这些研究有助于深入理解土壤氧化铁—腐殖酸复合体与硒的相互作用过程,以期为土壤硒生物有效性的合理调控提供基础资料和科学依据,这在土壤化学、环境化学、农业科学等领域均有重要意义。
1 材料与方法
1.1 试验材料
所用试剂均为分析纯级。超纯水由超纯水机(HK-UP-11-20,浩康科技,成都)制备。腐殖酸钠购自阿拉丁试剂(上海)有限公司。胡敏酸的提取程序见文献[14],主要步骤为:用0.1 mol L-1NaOH溶液将腐殖酸悬浮液调至pH=10.0,搅拌至悬浮液溶解,静置2 h,弃去不溶物;将所得棕褐色溶液继续静置2 h,取上层棕褐色溶液,重复操作3次;用0.1 mol L-1HCl溶液将所得棕褐色溶液调节至pH=1.0,静置1 d,弃去上清液,沉淀物用超纯水洗涤并离心两次,所得胡敏酸50℃真空干燥、研磨保存。
1.2 样品制备
针铁矿的制备:根据文献[14]中的方法合成针铁矿,主要步骤为:取50 ml 1 mol L-1Fe(NO3)3溶液于1 L塑料烧杯中,搅拌条件下迅速加入90 ml 5 mol L-1NaOH溶液,加超纯水至总体积为1 000 ml,用保鲜膜将烧杯密封,置于70℃油浴中老化60 h。将所得样品悬浮液冷却至室温,充分搅拌悬浮液,并将其分成两份。一份用超纯水洗涤并离心2次,沉淀物50℃真空干燥、研磨、保存备用。另一份悬浮液用于合成针铁矿—胡敏酸复合体。
针铁矿—胡敏酸复合体的制备:根据文献[14]中的方法合成针铁矿—胡敏酸复合体,主要步骤为:取胡敏酸0.9 g于50 mL超纯水中,用1 mol L-1NaOH溶液调节至pH=12.0,搅拌至胡敏酸全部溶解。将已制备的针铁矿悬浮液超声分散处理10 min,磁力搅拌状态下将胡敏酸溶液缓慢滴加至针铁矿悬浮液中,继续搅拌2 h,并用1 mol L-1HCl和NaOH溶液调节悬浮液至pH=4.0,室温静置2 d,离心分离。沉淀物即为针铁矿—胡敏酸复合体,50℃真空干燥、研磨、保存备用。
1.3 样品的表征方法
2种样品的X-射线衍射(XRD)和透射电镜(TEM)分析及其结果见文献[14]。胡敏酸和针铁矿—胡敏酸复合体的总有机碳(TOC)在总有机碳分析仪(TOC-L,岛津,日本)上采用高温催化燃烧氧化法测定,测试结果为腐殖酸样品的TOC含量为463.4 g kg-1,复合体样品的TOC含量为96.5 g kg-1,通过计算可得复合体中胡敏酸的理论含量为208.2 g kg-1。
样品表面电位用马尔文纳米粒度电位仪(Nano-ZS,马尔文,英国)测定。称取若干份0.01 g的供试样品,加入15 mL 0.01 mol L-1KCl溶液,超声分散后,用0.01 mol L-1KOH和HCl溶液反复将样品悬浮液的pH分别调至预先设定的值,用0.01 mol L-1KCl溶液定容至20 mL,再次超声分散后取2 ml悬液测定其Zeta电位。
样品表面X—射线光电子能谱(XPS)数据在X—射线光电子能谱仪(Escalab 250XI,赛默飞,美国)上测试。X射线源为单色Al Kα(hv=1 486.6 eV),功率150 W,500 μm束斑,标准镜头模式,元素扫描步幅0.05 eV,实验中以C1s (284.6 eV)为标准进行能量校正。用XPSPEAK41软件进行数据处理,背景信号用Shirley方法扣除,采用Lorentzian-Gaussian方法进行分峰拟合。
1.4 吸附实验
储备液制备:称取3.0 g样品于500 ml烧杯中,加入400 ml 0.01 mol L-1KCl溶液,超声分散30 min,搅拌条件下用1 mol L-1KOH或HCl溶液将悬浮液的pH调至4.0,并在12 h内使其pH稳定在4.0。将悬浮液全部转入500 ml容量瓶中,用0.01 mol L-1KCl溶液定容至500 ml,获得6.0 g L-1样品悬浮液。称取1.729 4 g Na2SeO3于100 ml聚乙烯烧杯中,加入90 ml 0.01 mol L-1KCl溶液,搅拌条件下用1 mol L-1KOH或 HCl溶液将其pH调至4.0,并在12 h内使其pH稳定在4.0。将悬浮液全部转入100 ml容量瓶中,定容至100 ml,获得Se(Ⅳ)浓度为0.1 mol L-1的储备溶液。使用前将0.1 mol L-1Se(Ⅳ)储备溶液稀释20倍,得Se(Ⅳ)浓度为5 mmol L-1的使用溶液。
样品对Se(Ⅳ)的等温吸附实验:取若干份6.0 g L-1的样品悬浮液5 ml注入50 ml聚乙烯离心管中,加入不同体积的Se(Ⅳ)使用溶液,用0.01 mol L-1KCl溶液调至总体积为30 ml,使悬浮液中样品浓度均为1.0 g L-1,Se(Ⅳ)初始浓度依次为0.05、0.1、0.2、0.3、0.4、0.5、0.7、1.0、1.5和2.0 mmol L-1。在25℃、转速250 r min-1条件下震荡24 h。将震荡后的悬浮液在12 000 r min-1的转速下离心分离,分别得到上清液和沉淀物。测定上清液的pH,用氢化物发生—原子荧光分光光度计(AFS-8330,北京吉天,中国)测量上清液中Se(Ⅳ)浓度。实验设置重复3次,取平均值。沉淀物在50℃鼓风干燥箱中烘干,取Se(Ⅳ)初始浓度为2.0 mmol L-1的沉淀物进行Zeta电位和XPS测试。
1.5 数据处理
样品对S e(Ⅳ)的吸附量计算表达式见式(1):

式中,Q表示吸附剂对吸附质的吸附量,mmol g-1;C为吸附体系中吸附质的平衡浓度,mmol L-1;C0为吸附体系中吸附质的初始浓度,mmol L-1;Cs为吸附体系中吸附剂的浓度,g L-1;V为吸附体系的体积,L。
用Langmuir和Freundlich模型对样品吸附Se(Ⅳ)的等温吸附数据进行拟合,2种模型的表达式分别见式(2)和式(3):

Langmuir模型中Qm表示吸附剂对吸附质的最大吸附容量,mmol g-1;b为与吸附亲和力及结合能有关的常数,L mmol-1。Freundlich模型中k为与吸附容量有关的常数,mmol1-(1/n)L1/ng-1;1/n为与吸附强度相关的系数。
使用Origin 8.0软件对样品吸附Se(Ⅳ)的等温吸附数据模型进行拟合;用XPSPEAK41软件对样品的XPS数据作分析处理,背景信号用Shirley方法扣除,采用Lorentzian-Gaussian方法进行分峰拟合。
2 结果与讨论
2.1 样品对Se(Ⅳ)的等温吸附及模型拟合
针铁矿和复合体对Se(Ⅳ)的等温吸附曲线见图1。可见,在吸附体系初始pH为4.0的条件下,当Se(Ⅳ)的平衡浓度相同时,针铁矿的吸附量明显高于复合体,且2种样品的吸附等温线类型差异较大。针铁矿吸附Se(Ⅳ)时,当Se(Ⅳ)的平衡浓度从0升高至0.22 mmol L-1时,吸附量也随之明显增加;当Se(Ⅳ)的平衡浓度从0.22 mmol L-1升高至0.77 mmol L-1时,吸附量的增加趋势明显减缓;当Se(Ⅳ)的平衡浓度达0.77 mmol L-1时,吸附量逐渐趋于饱和。复合体吸附Se(Ⅳ)时,当Se(Ⅳ)的平衡浓度从0升高至1.31 mmol L-1时,吸附量一直呈明显增加趋势;当Se(Ⅳ)的平衡浓度达1.31 mmol L-1以后,吸附量趋于稳定而不再增加。
2种样品吸附Se(Ⅳ)的实验数据Langmuir和Freundlich模型拟合参数列于表1。Langmuir模型的拟合结果中,针铁矿和复合体对Se(Ⅳ)的最大吸附容量Qm分别为0.202 mmol g-1和0.159 mmol g-1,常数b分别为34.72和5.42,拟合度(R2)分别为0.970和0.932。Freundlich模型的拟合参数中,常数k分别为0.206和0.132,与二者对Se(Ⅳ)的吸附容量趋势一致,与吸附强度相关的系数1/n分别为0.179和0.308,R2分别为0.914和0.980。可见,与针铁矿比较,复合体对Se(Ⅳ)的最大吸附容量和吸附亲和力均明显减小。根据文献[34-35],针铁矿表面的正电荷位、铁原子和两性羟基均为吸附Se(Ⅳ)的有效位点。王锐等[14]研究显示,针铁矿—胡敏酸复合体中部分胡敏酸颗粒包被在针铁矿表面。这种包被作用降低了针铁矿表面吸附位点的有效性,致使复合体的表面吸附容量降低。2种等温吸附模型的拟合度表明,针铁矿对Se(Ⅳ)的等温吸附数据更适合用Langmuir模型拟合,而Freundlich模型适合描述复合体对Se(Ⅳ)的等温吸附过程。这表明针铁矿对Se(Ⅳ)的等温吸附属于匀质性表面单层吸附模式,而异质性表面的多层吸附是复合体吸附Se(Ⅳ)的重要模型。

图1 针铁矿和复合体对Se(Ⅳ)的等温吸附曲线Fig. 1 Adsorption isotherms of Se(Ⅳ) by goethite and goethitehumic acid complex

表1 针铁矿和复合体吸附Se(Ⅳ)的等温吸附模型拟合参数Table 1 Fitting parameters of isothermal adsorption models of Se(Ⅳ) by goethite and goethite-humic acid complex
2.2 吸附体系的pH和Zeta电位
根据文献[36],亚硒酸的一级、二级电离表达式及平衡常数分别见反应式(4)和式(5):


样品表面的Zeta电位—pH关系曲线见图2。吸附Se(Ⅳ)以前,针铁矿的等电点(IEP)为7.0,复合体的IEP < 3.0;pH=4.0时,两种样品的Zeta电位分别为46.6 mV和-40.5 mV(图2a)。可见,吸附过程中针铁矿表面与阴离子之间存在较强的静电引力,而复合体表面与阴离子之间有明显的静电排斥作用,这也是复合体对Se(Ⅳ)的吸附容量低于针铁矿的原因之一。吸附Se(Ⅳ)以后,针铁矿表面的IEP降低至4.5,复合体的IEP仍然低于3.0;pH=4.0时,其Zeta电位分别为7.52 mV和-38.7 mV(图2b)。在吸附体系的初始pH=4.0的条件下,吸附Se(Ⅳ)以后针铁矿表面Zeta电位降低了39.08 mV,表明HSeO3-与针铁矿表面之间的静电引力是重要吸附机制。然而,pH=4.0时复合体吸附Se(Ⅳ)以后的表面Zeta电位反而升高了1.8 mV。这是由于HSeO3-与带负电荷的复合体表面活性羟基之间可能存在双齿配位,导致吸附过程中脱离复合体表面的OH-为被吸附的HSeO3-的2倍。因此,吸附作用导致复合体表面的Zeta电位略有升高。
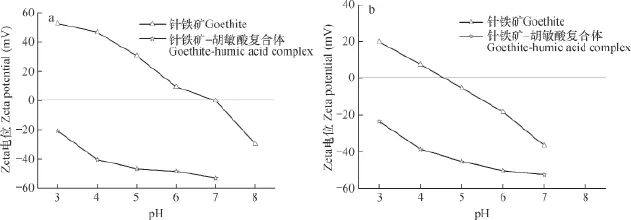
图2 样品的Zeta电位—pH关系曲线(a为吸附Se(Ⅳ)以前的样品,b为吸附Se(Ⅳ)以后的样品)Fig. 2 Relationship curve of pH-Zeta potential of the samples (a. Samples before Se(Ⅳ) adsorption, and b. Samples after Se(Ⅳ)adsorption)
2.3 样品的X—射线光电子能谱
2.3.1针铁矿吸附Se(Ⅳ)前后的X—射线光电子能谱 图3为吸附Se(Ⅳ)前后针铁矿表面Fe2p3/2的XPS谱图,分峰拟合数据及归属列于表2。吸附Se(Ⅳ)前针铁矿表面Fe2p3/2的XPS谱图(图3a)中,Fe的电子结合能(B.E.)的峰值为711.4 eV,表明针铁矿表面Fe均为正三价铁Fe(III)。根据Fe(Ⅲ)的核外电子云密度的差异,可将针铁矿表面的Fe(Ⅲ)分为3种不同的化学环境,分别为本征Fe(Ⅲ)、氧化态偏低Fe(Ⅲ) 和氧化态偏高Fe(Ⅲ)[37-40]。分峰拟合曲线中,B.E.峰值为711.5 eV的Fe(Ⅲ)可归属针铁矿表面本征Fe(Ⅲ),其含量为49.1%。与本征Fe(Ⅲ)相比,B.E.峰值为710.5 eV的Fe(Ⅲ)的核外电子云密度增大,为氧化态偏低Fe(Ⅲ),其含量为13.6%;713.8 eV的Fe(Ⅲ)核外电子云密度减小,为氧化态偏高Fe(Ⅲ),其含量为37.3%。
针铁矿吸附Se(Ⅳ)以后表面Fe2p3/2的XPS谱图(图3b)中,Fe2p3/2的B.E.峰值为711.0 eV,表明吸附Se(Ⅳ)以后样品表面的Fe仍为Fe(Ⅲ)。分峰拟合曲线中,氧化态偏低、本征和氧化态偏高Fe(Ⅲ)的B.E.峰值分别为710.0、711.2和713.1 eV,其相对含量分别为13.3%、46.1%和40.6%。与吸附前相比,吸附Se(Ⅳ)以后针铁矿表面氧化态偏低、本征和氧化态偏高Fe(Ⅲ)的B.E.峰值分别降低了0.5、0.3和0.7 eV。可见,针铁矿与Se(Ⅳ)的相互作用增加了表面Fe的电子云密度。根据文献[41-43],针铁矿与HSeO3-之间的相互作用机制主要包括表面≡FeOH中Fe与HSeO3-中Se或O之间的配位作用、带正电荷的针铁矿表面与HSeO3-之间的静电引力、表面吸附态阴离子与HSeO3-之间的离子交换以及氢键作用(针铁矿表面羟基H原子与HSeO3-中羟基O原子之间的氢键Ⅰ或针铁矿表面羟基O原子与HSeO3-中羟基H原子之间的氢键Ⅱ)等,其中,表面配位、静电引力和氢键Ⅰ可导致针铁矿表面Fe的电子云密度增加,而阴离子交换和氢键Ⅱ可降低表面Fe的电子云密度。可见,针铁矿吸附Se(Ⅳ)时,有多种作用机制可引起表面Fe的B.E.发生不同的变化。图3中的数据显示,针铁矿吸附Se(Ⅳ)以后,表面Fe的表观B.E.值有所降低。这表明表面配位、氢键Ⅰ和静电引力对针铁矿吸附Se(Ⅳ)有重要贡献。
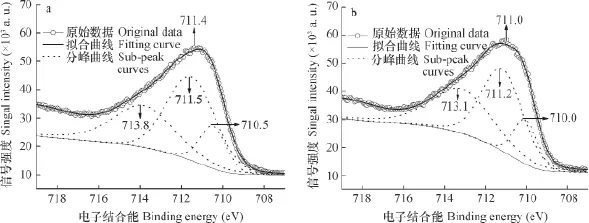
图3 针铁矿表面Fe2p3/2的X—射线光电子能谱谱(a为吸附Se(Ⅳ)以前的样品,b为吸附Se(Ⅳ)以后的样品)Fig. 3 X-ray photoelectric spectroscopy (XPS) spectra of Fe2p3/2 on the surface of goethite (a. Samples before Se(Ⅳ) adsorption, and b.Samples after Se(Ⅳ) adsorption)

表2 针铁矿表面Fe2p3/2的分峰拟合数据Table 2 Fitting data of sub-peaks of Fe2p3/2 XPS spectra of the surface of goethite
图4为亚硒酸钠和针铁矿表面吸附态硒的Se3d5/2的XPS谱图。亚硒酸钠和吸附态Se的Se3d5/2B.E.峰值均为58.7 eV,为正四价硒。Das等[10]研究表明,针铁矿吸附Se(Ⅵ)时在其表面形成了键长为0.31 nm的Fe-Se键。本研究也表明针铁矿表面的Fe与HSeO3-中的Se之间存在配位作用。这类作用可降低Se的电子云密度,导致3d5/2的B.E.峰值升高。图4显示,吸附在针铁矿样品表面Se3d5/2的B.E.峰值几乎未发生变化。这表明针铁矿吸附Se(Ⅳ)时还存在其他作用机制(如针铁矿表面羟基O原子与HSeO3-中羟基H原子之间的氢键Ⅱ)可使Se3d5/2的B.E.峰值降低。可见,尽管吸附态Se3d5/2的表观B.E.峰值未变化,但并不能说明HSeO3-中的Se原子在吸附过程中未直接参与作用。

图4 亚硒酸钠和针铁矿表面吸附态硒的Se3d5/2的XPS谱图Fig. 4 Se3d5/2 XPS spectra of Na2SeO3 and Se(Ⅳ) adsorbed on the surface of goethite
2.3.2针铁矿—胡敏酸复合体吸附Se(Ⅳ)前后的X—射线光电子能谱 图5为针铁矿—胡敏酸复合体表面Fe2p3/2的XPS谱图。吸附Se(Ⅳ)以前,复合体表面Fe的B.E.峰值为711.5 eV,较针铁矿表面Fe升高了0.1 eV,但仍然为Fe(Ⅲ)。分峰拟合曲线中,复合体表面氧化态偏低、本征和氧化态偏高Fe(Ⅲ)的B.E.峰值分别为710.5、711.8和713.7 eV,其相对含量分别为18.1%、37.9%和44.1%。与针铁矿比较,复合体表面本征Fe(Ⅲ)的B.E.峰值升高了0.3 eV,含量降低了11.2%;氧化态偏低Fe(Ⅲ)的含量增加了4.5%;氧化态偏高Fe(Ⅲ)的B.E.峰值降低了0.1 eV,其含量增加了为6.8%。总体而言,针铁矿与胡敏酸复合后其表面Fe的氧化态有所升高。根据文献[14,41],其原因主要有2个:①针铁矿表面≡FeOH与胡敏酸中羧酸基团的脱水作用,致使复合体表面出现了形态为Fe—O—C=O的Fe(Ⅲ);②针铁矿表面的活性氧与胡敏酸表面的活性氢之间存在氢键作用,其诱导效应可导致复合体表面Fe的电子云密度降低。
吸附Se(Ⅳ)以后,复合体表面Fe2p3/2的B.E.峰值为711.2 eV,较吸附前降低了0.3 eV,但仍为Fe(III)。分峰拟合曲线中,复合体氧化态偏低、本征和氧化态偏高Fe(Ⅲ)的B.E.峰值分别为710.4、711.3和713.2 eV,其相对含量分别为10.6%、45.4%和44.0%。与吸附前相比,吸附Se(Ⅳ)以后样品表面氧化态偏低、本征和氧化态偏高Fe(III)的B.E.峰值分别降低了0.1、0.5和0.5 eV;氧化态偏低Fe(III)的含量降低了7.5%,本征Fe(III)的含量升高了7.5%,氧化态偏高Fe(III)的含量无变化。可见,复合体和针铁矿吸附Se(Ⅳ)以后,样品表面Fe2p3/2的B.E.峰值的变化较为类似。
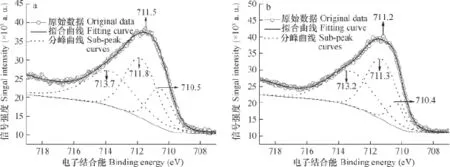
图5 针铁矿—胡敏酸复合体表面Fe2p3/2的XPS谱图(a为吸附Se(Ⅳ)以前的样品,b为吸附Se(Ⅳ)以后的样品)Fig. 5 Fe2p3/2 XPS spectra of goethite-humic acid complex ( a. Samples before Se(Ⅳ) adsorption, and b. Samples after Se(Ⅳ)adsorption)
图6为针铁矿—胡敏酸复合体表面C1s的XPS谱图。吸附Se(Ⅳ)前,复合体表面C1s的B.E.峰值为284.8 eV。复合体表面C1s的分峰拟合曲线中出现了明显的3个拟合峰,B.E.峰值分别为284.7、285.7和288.7 eV,相对含量分别为61.4%、25.8%和12.8%。根据文献[37,44-48],胡敏酸中的C1s按电子结合能由低至高可依次分为C=C、C-C、C-O和O-C=O/O-C-O共4种,其B.E.峰值分别在284.4~284.8、285.1~285.5、285.7~287.5和288.4~289.5 eV范围内。图6中,复合体表面C1s的B.E.峰值为285.7 eV的拟合峰的峰形较宽(半高宽为3.0 eV),且峰位与文献中C-C和C-O中C1s的B.E.峰值较接近。因此,复合体表面C1s的B.E.峰值为285.7 eV的C可归属为C—C和C—O中的混合形态, 284.7 eV的C为C=C形态,288.7 eV的C为O-C=O/O-C-O形态。
样品吸附Se(Ⅳ)以后的分峰拟合曲线中,出现了一个强峰和两个强度较弱的峰,其B.E.峰值分别为284.8、286.5和288.6 eV,相对含量分别为68.9%、6.4%和24.7%。与吸附前复合体表面C1s的XPS拟合数据相比,吸附Se(Ⅳ)以后样品表面C-O中C的B.E.峰值升高了0.8 eV,导致C-O与C-C中C的拟合峰分离而形成了独立的峰,且其相对含量明显减少;由于C=C和C-C中C的拟合峰重叠,导致其B.E.峰值略高于吸附前C=C中C的B.E.峰值,且相对含量也有所增加;O-C=O/O-C-O中C的B.E.峰值降低了0.1 eV,其相对含量增加了11.9%。可见,复合体与Se(Ⅳ)之间的作用明显降低了C-O中C的电子云密度,其原因可归属为复合体表面C-O中O原子(酚羟基氧、醌基氧等)与HSeO3-中的H发生了氢键作用。此外,吸附作用略微降低了复合体表面O-C=O/O-C-O中C的电子云密度,其原因可归属为O-C=O/O-C-O中呈正电性的C与HSeO3-之间存在静电引力作用。
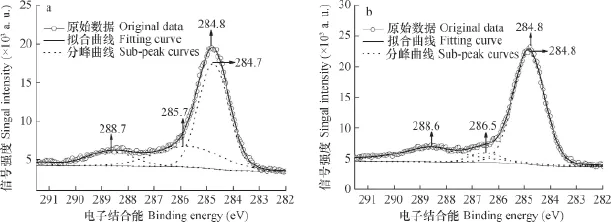
图6 针铁矿—胡敏酸复合体表面C1s的XPS谱图(a为吸附Se(Ⅳ)以前的样品,b为吸附Se(Ⅳ)以后的样品)Fig. 6 C1s XPS spectra of goethite-humic acid complex ( a. Samples before Se(Ⅳ) adsorption, and b. Samples after Se(Ⅳ)adsorption)
图7为吸附Se(Ⅳ)以后,针铁矿—胡敏酸复合体表面Se3d5/2的XPS谱图。Se3d5/2的XPS数据中,拟合峰的B.E.值为59.3 eV。根据文献[49-50],复合体表面吸附态Se仍为正四价硒,表明复合体与HSeO3-之间并未发生明显的氧化还原作用。与亚硒酸钠中Se3d5/2的B.E.比较,复合体表面吸附态Se3d5/2的B.E.升高了0.6 eV,表明复合体与HSeO3-之间的作用明显降低了Se的电子云密度。根据文献[10],导致吸附态Se的电子云密度减小的因素主要有:①复合体表面Fe与HSeO3-中Se之间的配位作用,②复合体表面铁羟基中H原子与HSeO3-中O原子之间的氢键Ⅰ,③复合体表面活性氧(针铁矿的羟基氧和胡敏酸的酚羟基、羧基、醌基氧等)与HSeO3-中H之间的氢键Ⅱ,④复合体表面呈正电性的Fe和C与HSeO3-之间的静电作用。与针铁矿单体表面吸附态Se相比,复合体表面吸附态Se3d5/2的B.E.峰值变化更大,这表明复合体表面吸附态Se(Ⅳ)同时与针铁矿和胡敏酸组分发生了作用,形成了针铁矿—Se(Ⅳ) —胡敏酸三元体。结果显示,针铁矿表面被胡敏酸包被以后不仅降低了针铁矿表面对Se(Ⅳ)的吸附容量,而且影响了样品表面与Se(Ⅳ)的作用方式。可见,针铁矿—胡敏酸复合体对硒的吸附容量和吸附机制均不同于针铁矿单体。这些研究结果可为认识土壤环境中Se(Ⅳ)的迁移转化和形态分布提供基础资料,也可为硒的生物有效性调控提供一定的科学依据。

图7 针铁矿—胡敏酸复合体吸附Se(Ⅳ)以后表面Se3d5/2的XPS谱图Fig. 7 XPS spectra of Se3d5/2 on the surface of goethite-humic acid complex after adsorbing Se(Ⅳ)
3 结 论

[ 1 ] Lanctôt C M,Cresswell T,Callaghan P D,et al.Bioaccumulation and biodistribution of selenium in metamorphosing tadpoles. Environmental Science &Technology,2017,51(10):5764—5773
[ 2 ] Fernández-Martínez A,Charlet L. Selenium environmental cycling and bioavailability:A structural chemist point of view. Reviews in Environmental Science and Bio/Technology,2009,8(1):81—110
[ 3 ] Winkel L H,Johnson C A,Lenz M,et al.Environmental selenium research:From microscopic processes to global understanding. Environmental Science & Technology,2011,46(2):571—579
[ 4 ] Lessa J H L,Araujo A M,Silva G N T,et al.Adsorption—desorption reactions of selenium(VI)in tropical cultivated and uncultivated soils under Cerrado biome. Chemosphere,2016,164:271—277
[ 5 ] Weng L,Vega F A,Supriatin S,et al. Speciation of Se and DOC in soil solution and their relation to Se bioavailability. Environmental Science &Technology,2010,45(1):262—267
[ 6 ] Wang S S,Liang D L,Wang D,et al. Selenium fractionation and speciation in agriculture soils and accumulation in corn(ZeamaysL.)under field conditions in Shanxi Province,China. Science of the Total Environment,2012,427/428:159—164
[ 7 ] Chen S S,Sun Y,Tsang D C W,et al. Insights into the subsurface transport of As(V)and Se(VI)in produced water from hydraulic fracturing using soil samples from Qingshankou Formation,Songliao Basin,China. Environmental Pollution,2017,223:449—456
[ 8 ] Söderlund M,Virkanen J,Holgersson S,et al.Sorption and speciation of selenium in boreal forest soil. Journal of Environmental Radioactivity,2016,164:220—231
[ 9 ] Li Z,Liang D,Peng Q,et al. Interaction between selenium and soil organic matter and its impact on soil selenium bioavailability:A review. Geoderma,2017,295:69—79
[10] Das S,Hendry M J,Essilfie—Dughan J. Adsorption of selenate onto ferrihydrite,goethite,and lepidocrocite under neutral pH conditions. Applied Geochemistry,2013,28:185—193
[11] Szlachta M,Chubar N. The application of Fe—Mn hydrous oxides based adsorbent for removing selenium species from water. Chemical Engineering Journal,2013,217:159—168
[12] Li J,Peng Q,Liang D,et al. Effects of aging on the fraction distribution and bioavailability of selenium in three different soils. Chemosphere,2016,144:2351—2359
[13] Jones C P,Grossl P R,Amacher M C,et al.Selenium and salt mobilization in wetland and arid upland soils of Pariette Draw,Utah(USA).Geoderma,2017,305:363—373
[14] 王锐,朱朝菊,向文军,等. 针铁矿与胡敏酸的交互作用及其复合物的稳定性. 环境科学,2017,38(11):4860—4867 Wang R,Zhu C J,Xiang W J,et al. Interactions between goethite and humic acid and stability of goethite—humic acid complex(In Chinese).Environmental Sciences,2017,38(11):4860—4867
[15] Chen K Y,Chen T Y,Chan Y T,et al. Stabilization of natural organic matter by short—range—order iron hydroxides. Environmental Science & Technology,2016,50(23):12612—12620
[16] 黄玉芬,刘忠珍,魏岚,等. 土壤不同粒径有机无机复合体对丁草胺的吸附特性. 土壤学报,2017,54(2):400—409 Huang Y F,Liu Z Z,Wei L,et al. Effect of soil orango—inorganic compounds different in particle size on butachlor sorption(In Chinese). Acta Pedologica Sinica,2017,54(2):400—409
[17] 周俊,刘兆云,孟立丰,等. 土壤性质对土壤—水稻系统中硒迁移的影响. 土壤,2016,48(4):734—741 Zhou J,Liu Z Y,Meng L F,et al. Selenium transport in soil—paddy system influenced by soil properties(In Chinese). Soils,2016,48(4):734—741
[18] 郑学博,樊剑波,周静,等. 沼液化肥配施对红壤旱地土壤养分和花生产量的影响. 土壤学报,2016,53(3):675—684 Zheng X B,Fan J B,Zhou J,et al. Effects of combined application of biogas slurry and chemical fertilizer on soil nutrients and peanut yield in upland red soil(In Chinese). Acta Pedologica Sinica,2016,53(3):675—684
[19] Goh K H,Lim T T. Geochemistry of inorganic arsenic and selenium in a tropical soil:Effect of reaction time,pH,and competitive anions on arsenic and selenium adsorption. Chemosphere,2004,55(6):849—859
[20] Nie Z,Finck N,Heberling F,et al. Adsorption of selenium and strontium on goethite:EXAFS study and surface complexation modeling of the ternary systems.Environmental Science & Technology,2017,51(7):3751—3758
[21] Rovira M,Giménez J,Martínez M,et al. Sorption of selenium(IV)and selenium(VI)onto natural iron oxides:Goethite and hematite. Journal of Hazardous Materials,2008,150(2):279—284
[22] Sheha R R,El-Shazly E A. Kinetics and equilibrium modeling of Se(IV)removal from aqueous solutions using metal oxides. Chemical Engineering Journal,2010,160(1):63—71
[23] Zelmanov G,Semiat R. Selenium removal from water and its recovery using iron(Fe3+)oxide/hydroxide—based nanoparticles sol(NanoFe)as an adsorbent.Separation and Purification Technology,2013,103(15):167—172
[24] Börsig N,Scheinost A C,Shaw S,et al. Uptake mechanisms of selenium oxyanions during the ferrihydrite—hematite recrystallization. Geochimica et Cosmochimica Acta,2017,206:236—253
[25] Ling L,Pan B C,Zhang W X. Removal of selenium from water with nanoscale zero-valent iron:Mechanisms of intraparticle reduction of Se(IV).Water Research,2015,71(15):274—281
[26] Liu J F,Zhao Z S,Jiang G B. Coating Fe3O4magnetic nanoparticles with humic acid for high efficient removal of heavy metals in water. Environmental Science & Technology,2008,42(18):6949—6954
[27] Lenoble V,Dang D H,Cazalet M L,et al.Evaluation and modelling of dissolved organic matter reactivity toward As(III)and As(V)—Implication in environmental arsenic speciation. Talanta,2015,134:530—537
[28] Coppin F,Chabroullet C,Martin—Garin A. Selenite interactions with some particulate organic and mineral fractions isolated from a natural grassland soil.European Journal of Soil Science,2009,60(3):369—376
[29] Kamei-Ishikawa N,Nakamaru Y,Tagami K,et al.Sorption behavior of selenium on humic acid under increasing selenium concentration or increasing solid/liquid ratio. Journal of Environmental Radioactivity,2008,99(6):993—1002
[30] Tolu J,Thiry Y,Bueno M,et al. Distribution and speciation of ambient selenium in contrasted soils,from mineral to organic rich. Science of the Total Environment,2014,479:93—101
[31] Dinh Q T,Li Z,Tran T A T,et al. Role of organic acids on the bioavailability of selenium in soil:A review. Chemosphere,2017,184:618—635
[32] 王磊,应蓉蓉,石佳奇,等. 土壤矿物对有机质的吸附与固定机制研究进展. 土壤学报,2017,54(4):805—818 Wang L,Ying R R,Shi J Q,et al. Advancement in study on adsorption of organic matter on soil minerals and its mechanism(In Chinese). Acta Pedologica Sinica,2017,54(4):805—818
[33] 扬子,刘晓光,宁静,等. 典型黑土垄作区耕地沟蚀对土壤养分的影响研究. 土壤,2017,49(2):379—385 Yang Z,Liu X G,Ning J,et al. Effects of gully erosion on soil nutrients in ridge area of typical black soil(In Chinese). Soils,2017,49(2):379—385
[34] Cornell R M,Schwertmann U. The iron oxides:Structure,properties,reactions occurences and uses.Weinheim,Germany:Wiley—VCH,2003
[35] Liu H,Chen T,Frost R L. An overview of the role of goethite surfaces in the environment. Chemosphere,2014,103:1—11
[36] Petrucci R H,Harwood W S,Herring F G. General chemistry:Principles and modern applications. 8th ed.Upper Saddle River,NJ:Prentice Hall,2002
[37] The U.S. Secretary of Commerce on behalf of the United States of America. http://srdata.nist.gov/xps/selEnergyType.aspx,2012—09—15
[38] Bhargava G,Gouzman I,Chun C M,et al.Characterization of the “native” surface thin film on pure polycrystalline iron:A high resolution XPS and TEM study. Applied Surface Science,2007,253(9):4322—4329
[39] Descostes M,Mercier F,Thromat N,et al. Use of XPS in the determination of chemical environment and oxidation state of iron and sulfur samples:Constitution of a data basis in binding energies for Fe and S reference compounds and applications to the evidence of surface species of an oxidized pyrite in a carbonate medium. Applied Surface Science,2000,165(4):288—302
[40] Grosvenor A P,Kobe B A,Biesinger M C,et al.Investigation of multiplet splitting of Fe2p XPS spectra and bonding in iron compounds. Surface and Interface Analysis,2004,36(12):1564—1574
[41] Mikutta C,Kretzschmar R. Spectroscopic evidence for ternary complex formation between arsenate and ferric iron complexes of humic substances. Environmental Science & Technology,2011,45(22):9550—9557
[42] Chubar N,Gerda V,Szlachta M. Mechanism of selenite removal by a mixed adsorbent based on Fe—Mn hydrous oxides studied using X—ray absorption spectroscopy. Environmental Science & Technology,2014,48(22):13376—13383
[43] Martin R R,Smart R S C. X—ray photoelectron studies of anion adsorption on goethite. Soil Science Society of America Journal,1987,51(1):54—56
[44] Xiong J,Koopal L K,Weng L,et al. Effect of soil fulvic and humic acid on binding of Pb to goethitewater interface:Linear additivity and volume fractions of HS in the stern layer. Journal of Colloid and Interface Science,2015,457:121—130
[45] Mangolini F,Rossi A,Spencer N D. Chemical reactivity of triphenyl phosphorothionate(TPPT)with iron:An ATR/FT—IR and XPS investigation.The Journal of Physical Chemistry C,2010,115(4):1339—1354
[46] Tan X,Fan Q,Wang X,et al. Eu(III)sorption to TiO2(anatase and rutile):Batch,XPS,and EXAFS studies. Environmental Science & Technology,2009,43(9):3115—3121
[47] Okpalugo T I T,Papakonstantinou P,Murphy H,et al. High resolution XPS characterization of chemical functionalised MWCNTs and SWCNTs. Carbon,2005,43(1):153—161
[48] Fan Q H,Tan X L,Li J X,et al. Sorption of Eu(III)on attapulgite studied by batch,XPS,and EXAFS techniques. Environmental Science &Technology,2009,43(15):5776—5782
[49] 付茂,吴德礼,张亚雷,等. 多羟基结构态亚铁化合物预处理含亚硒酸盐工业废水的影响机制. 高等学校化学学报,2016,37(12):2221—2227 Fu M,Wu D L,Zhang Y L,et al. Removal research of selenite in wastewater with the ferrous hydroxyl complex(FHC)(In Chinese). Chemical Journal of Chinese Universities,2016,37(12):2221—2227
[50] Papelis C. X—ray photoelectron spectroscopic studies of cadmium and selenite adsorption on aluminum oxides. Environmental Science & Technology,1995,29(6):1526—1533
