一步溶剂热法合成CoO/Ti3C2复合材料及其电化学性能研究
2018-04-11朱建锋吕文静任莹莹李学林
朱建锋, 吕文静, 任莹莹, 李学林
(陕西科技大学 材料科学与工程学院, 陕西 西安 710021)
0 引言
二维层状材料即电子仅可在两个维度的非纳米尺度上自由运动的材料,如石墨烯、二硫化物和金属氧化物或氢氧化物等[1].这类二维层状材料与其他纳米结构相比,具有比表面积大,表面载流子传输速率高等优异的性能.二维材料独特的形态结构能加快离子扩散并提供离子插入通道,使其成为备受瞩目的锂离子电池和超级电容器电极材料[2].
二维过渡金属碳化物MXene是一种具有类石墨烯结构的新型二维晶体化合物.通过选择性腐蚀剥离母体MAX相而获得.MXene的化学式为Mn+1Xn,其中n=1,2,3;X=C、N;M为前过渡金属[3].目前已成功制备的MXene包括Ti3C2、Ti2C、TiNbC、V2C和Ti3CN等.其中,Ti3C2作为的MXene材料的一种,因为其独特的层状结构、良好的亲水性、优异的电子电导以及适应不同电解质离子插层(H+、Na+、K+、Li+、Al3+、Mg2+)等的特点,受到科研工作者的极大关注[4,5].然而,与其他材料相比,Ti3C2理论比容量较低且片层之间容易堆叠,导致其电化学性能不理想.
为了提高Ti3C2材料的电化学性能,研究人员进行了一系列的探索,例如液相剥离法[6],金属或金属氧化物负载法[7],原子掺杂等.金属氧化物负载法是通过不同方法将不同尺寸及形貌的过渡金属氧化物与Ti3C2材料进行复合,由于协同作用与界面相互作用的结果,氧化物与Ti3C2的复合材料可以改善电池的充放电比容量、倍率特性以及循环稳定性.然而,由于Ti3C2在水溶液中容易原位氧化生成二氧化钛颗粒,使得复合材料出现TiO2杂相,一定程度破坏层状结构,导致材料储能机理不明确,电化学性能降低[8].
通过金属氧化物CoO对二维层状材料Ti3C2基体进行负载改性,不仅可以改善CoO的导电性、缓解充放电过程中的体积膨胀,而且可以改善Ti3C2的堆叠情况,增加层间距扩大其与锂离子的接触途径,从而提高材料的循环性能与比容量.本文采用溶剂热法一步合成CoO/Ti3C2复合材料,分析合成机理,通过X射线衍射(XRD)、扫描电镜(SEM)、透射电镜(TEM)对材料的结构及形貌进行了表征,并考察了其作为锂离子电池负极材料的比容量及循环性能.
1 实验部分
1.1 Ti3C2基体材料的制备
将5 gTi3AlC2粉体缓慢加入80 mL40 wt.%的HF中,温室下磁力搅拌24 h.用去离子水清洗反应产物,离心后上清液pH>6,接着用无水乙醇清洗3次,之后将产物置于真空烘箱中,40 ℃下烘12 h,即得到Ti3C2基体材料.
1.2 CoO/Ti3C2复合材料的制备
将取制得的Ti3C2粉体200 mg分散到40 mL的N,N-二甲基甲酰胺中(DMF),磁力搅拌下1 h得到均匀的悬浮液,随后加入0.334 g的四水醋酸钴,并搅拌1 h,放入反应釜中,150 ℃保温12 h.接着用无水乙醇清洗6次,去除未反应的离子,待清洗完毕后将反应产物放入真空干燥箱中60 ℃下干燥24 h制得CoO/Ti3C2复合材料.为了进行对比试验,上述步骤不加入Ti3C2粉体,得到单一的CoO纳米球.最后进行性能的测试.
1.3 CoO/Ti3C2复合材料的物理表征
使用X射线衍射仪(XRD,D/Max-2200pc Rigaku,Japan)对所制备的复合材料进行结构表征,以CuKa为靶源(波长0.154 18 nm),扫描方式采用步进式扫描,歩宽为0.02 °,扫描角度2θ为5 °~80 °.材料表面的结构以及元素分析通过X射线光电子能谱(XPS,VG Thermo ESCALAB 250,Al Kα离子源)测试.材料的形貌结构由扫描电子显微镜(SEM,S4800,HITACHI)和透射电子显微镜(TEM JEM2100F)来表征.利用N2吸附/脱附仪(Micromeritics ASAP2460,USA)进行N2吸附/脱附实验,得到材料的比表面积和孔容孔径.
1.4CoO/Ti3C2复合材料电极的制备及电化学性能测试
采用涂膜法制备电极:将制备好的活性粉体与乙炔黑、PVDF按质量比8∶1∶1混合并加适量氮基吡咯烷酮研磨制成浆状物,均匀涂于铜箔上,在真空箱中120 ℃干燥12 h,切成直径14 mm的圆形电极片在真空手套箱中组装电池(CR2032纽扣电池).以金属锂片为对电极,使用1 mol/L LiPF6在碳酸亚异酯:碳酸二甲酯溶剂的质量比为1∶1的溶液做电解液.采用蓝电电池测试仪CT2001A的恒电流充放电测试系统进行充放电性能测试,电压范围0.01~3 V,电流密度100 mA/g.循环伏安测试和电化学阻抗谱(EIS)的测试通过Ametek PARSTAT4000电化学工作站在0.1 mV s-1的扫速,电压为0.01~3 V的条件下进行测试.
2 结果与讨论
2.1 机理分析
CoO/Ti3C2复合材料一步溶剂热合成的示意图如图1所示.当Ti3C2粉末加入到DMF溶液中,Ti3C2表面的氧、羟基、氟官能团基团与DMF结合.在溶剂热过程中,大部分的F杂质都是被氧或羟基取代,因为没有添加任何还原剂,因此推断在CoO合成中N,N-二甲基甲酰胺(DMF)作为一种弱的还原剂存在,其反应式如下[9]:
4HCON(CH3)2+H2O→HCOOH+
NH(CH3)2
(1)
Co2++H2O+2NH(CH3)2→ CoO(s)+
2NH2(CH3)2+
(2)

图1 CoO/Ti3C2复合材料合成示意图
2.2 物相分析
图2 (a)为CoO、Ti3C2和CoO/Ti3C2复合材料XRD图.从图2(a)可以看出,CoO的XRD与CoO(JCPDS 43-1004)相吻合,且2θ位于36.5 °、42.7 °、61.5 °、73.7 °、77.5 °分别对应立方相CoO的(111)、(200)、(220)、(311)、(222)晶面[10].层状Ti3C2的特征峰为(002),(006),(008)和(0010)等(00l)方向的衍射峰,与之前文献相一致[4].CoO/Ti3C2复合材料的XRD图中,其所有的衍射峰与立方相CoO和Ti3C2的衍射峰吻合,因此从物相分析上可以看出所制备的CoO/Ti3C2为立方相CoO和Ti3C2共存相.
图2(b)为XRD图谱的局部放大图,CoO/Ti3C2复合材料的(002)衍射峰较Ti3C2相(002)衍射峰向左偏移了2.1 °,对应于晶面间距增大了0.074 nm.

(a) Ti3C2、CoO和CoO/Ti3C2复合材料 (b)为(a)的局部放大图图2 产物XRD图
图3(a)为所制备的Ti3C2的SEM图.从图3(a)可以看出,基体Ti3C2呈现明显的类石墨烯层状结构;图3(b)为所制备CoO的SEM图.从图3(b)可以看出CoO呈圆球状,粒径尺寸约为100 nm,且团聚现象严重;图3(c)和图3(d)为所制备CoO/Ti3C2复合材料的SEM图.从图3(c)、(d)中可以看出,大量的纳米球均匀的分布在Ti3C2片层表面上和层间隙中.与纯CoO相比,CoO纳米球的尺寸减小,粒径尺寸约为50 nm,团聚现象也显著降低;图3(e)为所制备CoO/Ti3C2复合材料的TEM图.从图3(e)中可以看出,Ti3C2表面复合了大量的球状物质;由样品高倍下的TEM图3(f)可以看出,复合的球状物质为立方相CoO,0.214 nm和0.242 nm的晶格条纹间距分别对应于CoO的(200)和(111)晶面.表明通过一步水热法成功制备了CoO/Ti3C2复合材料.

(a)Ti3C2的SEM图 (b)CoO的SEM图

(c)、(d)CoO/Ti3C2的SEM图

(e)、(f) CoO/Ti3C2的TEM图图3 材料的SEM图和TEM图
2.3 比表面积及孔径分布分析
图4(a)为所制备Ti3C2和CoO/Ti3C2的N2吸附/脱附曲线.从图4(a)可以看出,在相对压力0.45~1.0范围内,两个曲线均存在明显的滞后环,这表明Ti3C2和CoO/Ti3C2这两个样品中均存在介孔和大孔.根据BET公式计算可得Ti3C2和CoO/Ti3C2的比表面积分别为8.428 1 m2g-1和44.005 1 m2g-1.显然,CoO/Ti3C2具有更高的比表面积,这可归因于均匀分布的CoO纳米微球防止了Ti3C2片层的堆积并扩大片层之间的距离.另外,孔径的尺寸以及孔径分布也是决定材料电化学性能的重要因素之一.
图4(b)为所制备Ti3C2和CoO/Ti3C2的N2脱附曲线通过Barrett-Joyner-Halenda(BJH)模型估算的孔径分布曲线.从图4(b)可以看出,CoO/Ti3C2的孔径尺寸约为10.0~25.0 nm,且孔体积约为Ti3C2的两倍,这表明CoO/Ti3C2拥有更多介孔.高的空隙体积有利于增加电极材料与电解液的接触面积并缩短了离子从材料表面扩散到内部的距离,为高倍率存储性能提供了保障[11].因此,推断CoO/Ti3C2复合材料的电化学性能将优于Ti3C2.

(a)Ti3C2和CoO/Ti3C2的N2吸附/脱附曲线
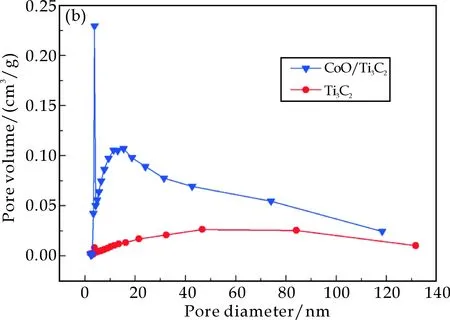
(b)Ti3C2和CoO/Ti3C2的孔径分布曲线图4 Ti3C2和CoO/Ti3C2的N2吸附/脱附曲线与孔径分布曲线
2.4 电化学性能分析
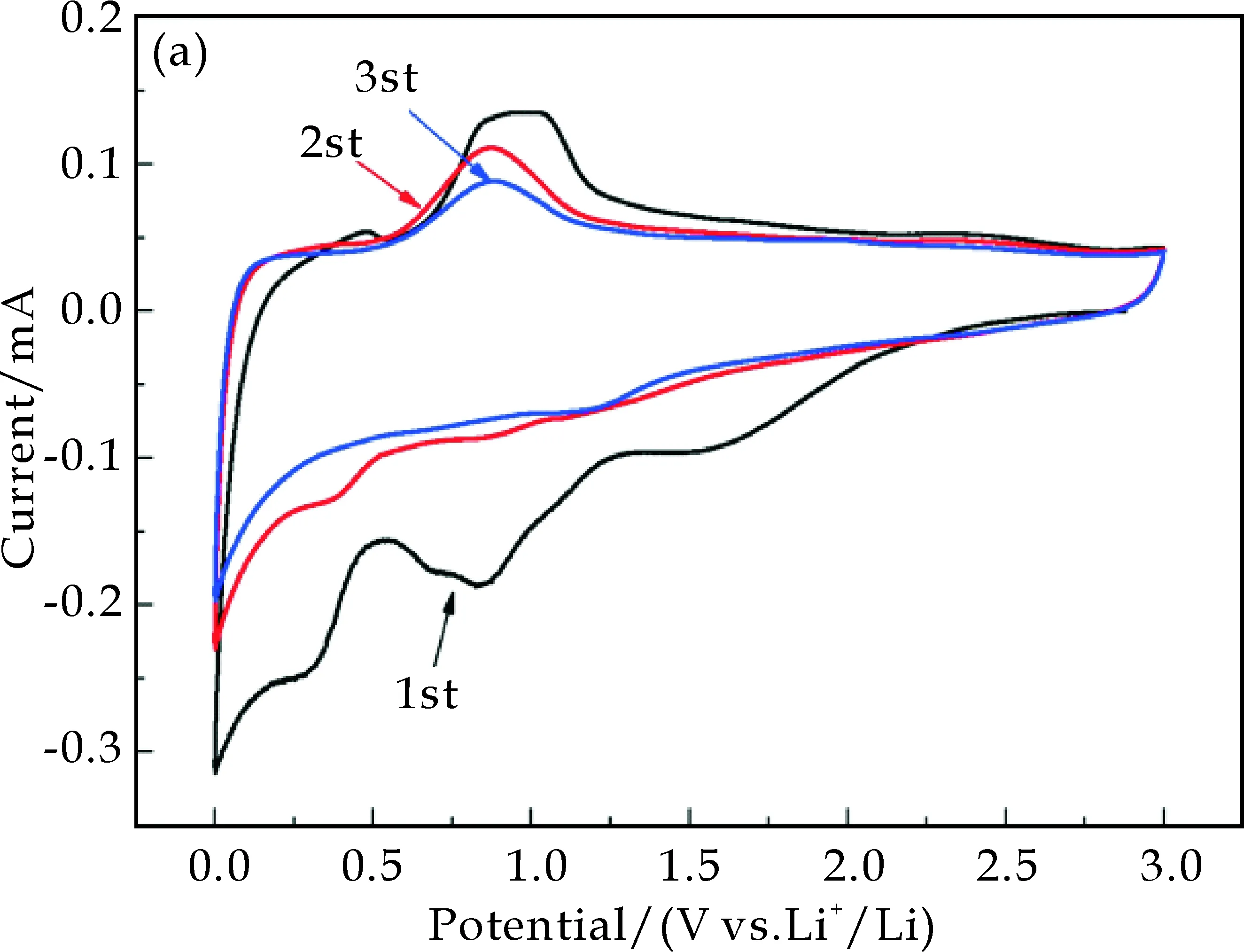
为了研究电极材料的储锂性能和机理,把材料作为锂离子电池的负极材料进行电化学测试.图5(a)为Ti3C2电极在扫描速率为10 mV s-1下在第一圈的嵌锂阶段,0.01 V的峰位对应的是乙炔黑的嵌锂电位.0.8 V的峰位在后续的循环中消失了,这应该是因为锂与电极材料形成了SEI膜.在1.2 V和0.75 V的位置,对应的是脱嵌锂的峰位[12].其电化学反应如下所示:
Ti3C2+xLi++xe-=Ti3C2Lix
(3)
在后续的循环中,与第一圈相比,除了SEI膜的形成电位以外,别的峰位没有变化,说明Ti3C2的储锂机理是锂离子的插入到层间,而不是转化反应.
图5(b)为CoO/Ti3C2电极在扫描速率为10 mV s-1下的循环伏安CV曲线图.从图5(b)中可以看出,在首次锂化过程中,在0.75 V出现宽的不可逆峰,随后在剩下的几次循环中消失.这是由于在电极材料中的Ti3C2的层间捕获了Li+,从而形成了固态电介质SEI膜.从第二次循环开始出现了钴的电化学氧化还原过程,1.0 V左右出现钴的还原峰,而2.3 V对应于钴的氧化过程[13].根据循环伏安曲线可知,CoO在电池充放电过程中发生了电化学氧化还原,对应于活性位对锂离子的脱嵌,表现出典型的含钴电极的循环伏安特性.同时,从该曲线可以发现,第二次与第三次的循环伏安扫描曲线较好吻合,说明SEI膜已经很好地生成,电池容量趋于稳定.其电化学反应如下所示:
CoO+2Li++2e-=2Co+Li2O
(4)
图5(c)为Ti3C2、CoO和CoO/Ti3C2三种电极在不同电流密度下的倍率性能图.从图5(c)中可以看出,电流密度为100 mA g-1、300 mA g-1、500 mA g-1、700 mA g-1和1 000 mA g-1时,CoO/Ti3C2电极材料的可逆比容量分别为398 mAh g-1、283 mAh g-1、171 mAh g-1、156 mAh g-1和136 mAh g-1,随着电流密度的增加,容量呈稳定下降趋势.当电流密度返回100 mA g-1时,容量达到250 mAh g-1,明显高于单独的Ti3C2和CoO电极.表明了CoO/Ti3C2复合材料较好的倍率性能.
图5(d)为Ti3C2、CoO和CoO/Ti3C2电极在100 mA g-1的电流密度下充放电300次的充放电比容量和CoO/Ti3C2电极材料的容量保持率图.从图5(d)中可以看出,CoO的比容量衰减较快,循环100次之后容量低于100 mAh g-1,循环150次之后容量仅为56 mAh g-1.CoO/Ti3C2复合材料第一次的充电容量和放电容量分别为456和915 mAh g-1,首次库伦效率为48.08%.其较大的不可逆容量损失可以归因于固态电介质SEI膜的形成以及Ti3C2表面官能团的不可逆反应[14].循环十次以后,CoO/Ti3C2电极的库仑效率基本维持在99%左右,充放电循环300次后仍能够获得415 mAh g-1的可逆比容量.这明显高于Ti3C2电极充放电循环300次后的可逆比容量157 mAh g-1.表明CoO/Ti3C2复合材料具有较高可逆比容量的同时其循环稳定性也很优异.这主要归功于复合材料的结构,均匀分布的CoO纳米微球防止了Ti3C2片层的堆积并扩大片层之间的距离.从而提高了电极与电解提高液的接触面积,使得在充放电中更多的锂离子能够在CoO/Ti3C2纳米复合材料脱嵌,因而提高锂离子电池的性能.
(a)Ti3C2循环伏安CV曲线

(b)CoO/Ti3C2循环伏安CV曲线
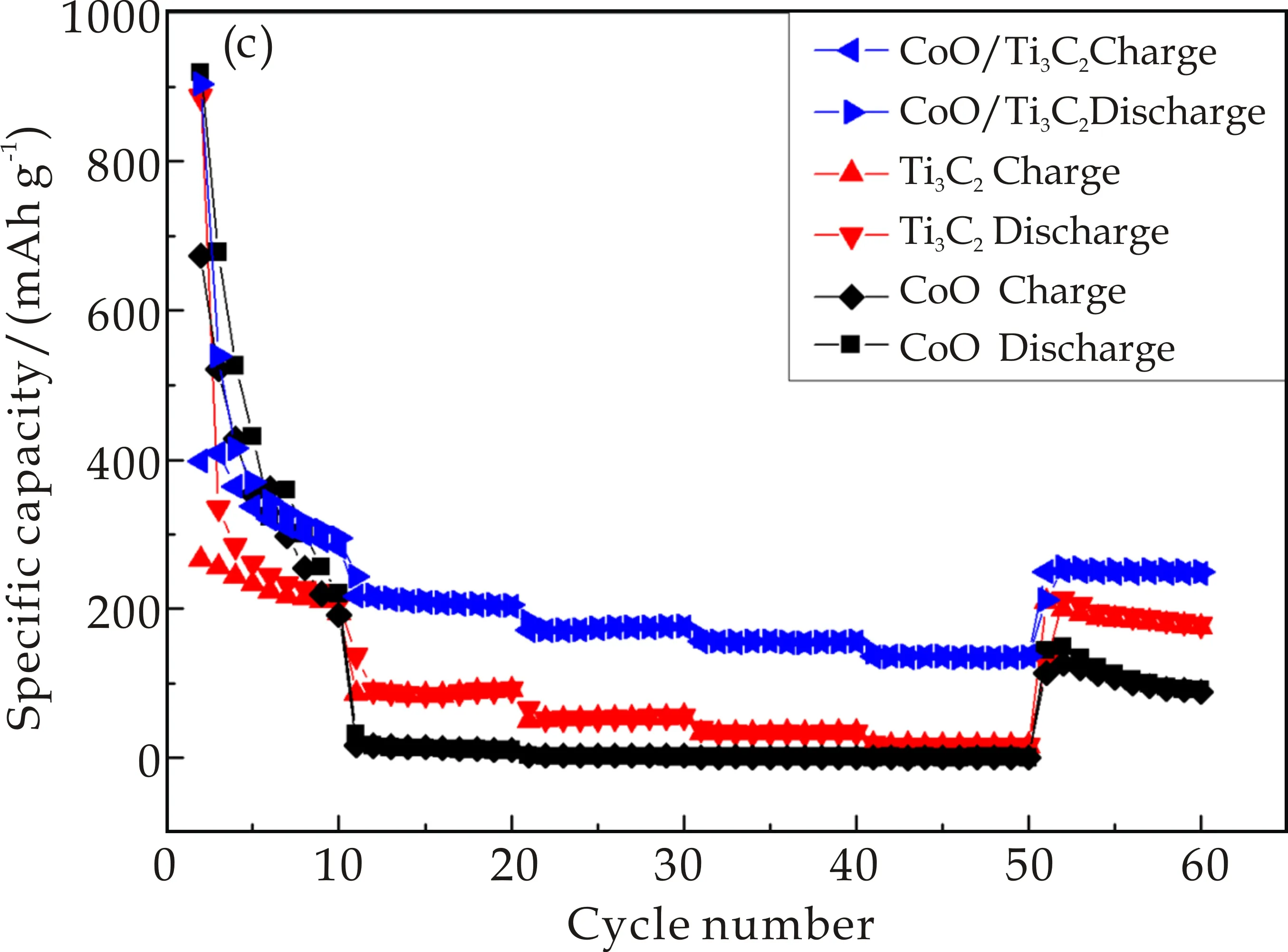
(c)Ti3C2、CoO和CoO/Ti3C2倍率性能图
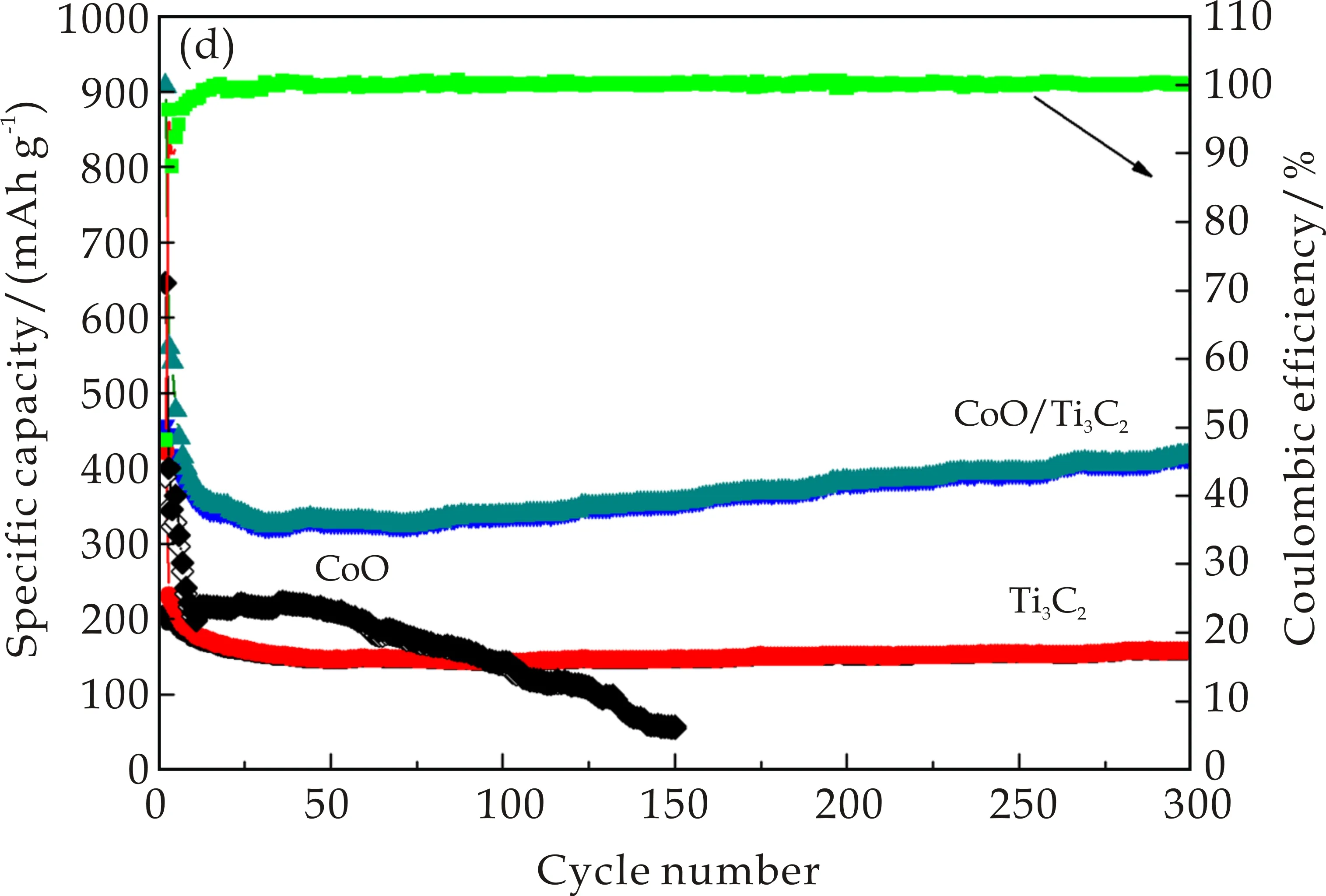
(d)Ti3C2、CoO和CoO/Ti3C2循环性能图图5 Ti3C2、CoO和CoO/Ti3C2电化学性能图
电化学阻抗谱(EIS)是电极材料的内部电阻和容量的测试方法.图6为纯相的CoO、Ti3C2和CoO/Ti3C2的交流阻抗图,可以看到电化学阻抗谱图是由高频区域的半圆和低频区域的直线两部分构成,位于高频区的半弧代表接触电阻和电荷转移电阻,半圆的直径越小说明阻抗越小.而在低频区倾斜的直线代表锂离子扩散电阻,直线的斜率越小,说明材料的锂离子扩散阻抗越大,反之,则越小[15].由此图中高频区半圆的大小和低频区直线的斜率可以看出,CoO/Ti3C2复合负极材料的接触阻抗、电荷传递阻抗以及Li+在电极材料中的扩散阻抗都小于纯CoO和Ti3C2,这说明CoO/Ti3C2电极材料具有更大的电活性表面,更好的导电性.这是由于一氧化钴纳米球均匀的负载在Ti3C2的表面和层间,有效的防止了Ti3C2层间的堆叠增加了电解液与材料的接触面积,同时较大的层间距有利于锂离子的扩散,提高电子电导率.

图6 Ti3C2、CoO和CoO/Ti3C2复合材料的交流阻抗图
3 结论
通过简单的溶剂热法在Ti3C2片层上以及片层之间引入大量CoO纳米微球,从而制备出CoO/Ti3C2纳米复合材料.实验结果表明:通过CoO纳米球的负载改性可显著增加Ti3C2的电化学性能.CoO/Ti3C2复合材料第一次的充电容量和放电容量分别为456和915 mAh g-1,首次库伦效率为48.08%.充放电循环300次后仍能够获得415 mAh g-1的可逆比容量,是Ti3C2电极材料的2.5倍(157 mAh g-1).并且其具有优良的倍率性能及循环稳定性(循环十次以后,CoO/Ti3C2电极的库仑效率基本维持在99%左右).CoO/Ti3C2电极优良的电化学性能是由于:CoO纳米微球的引入增加了材料的比表面积,提供了更多的活性位点,增大了层间距使得锂离子的插层更容易.同时,大量的CoO纳米微球可以提供额外的离子扩散路径.以上研究表明,所制备的CoO/Ti3C2纳米复合材料作为锂离子电池负极材料具有潜在的应用前景.因此,金属氧化物均匀的负载分布在Ti3C2二维纳米片层表面是一个非常有前景的锂离子电池负极材料.
[1] Poizot P,Laruelle S,Grugeon S,et al.Nano-sized transition-metal oxides as negative-electrode materials for lithium-ion batteries[J].Nature,2000,407 (6 803):496-499.
[2] Bonaccorso F,Colombo L,Yu G H,et al.Graphene,related two-dimensional crystals,and hybrid systems for energy conversion and storage[J].Science,2015,347(6 217):1 246 501.
[3] Naguib M,Kurtoglu M,Presser V,et al.Two-dimensional nanocrystals produced by exfoliation of Ti3AlC2[J].Adv.Mater.,2011,23(37):4 248-4 253.
[4] Feng A H,Yu Y,Wang Y,et al.Two-dimensional MXene Ti3C2produced by exfoliation of Ti3AlC2[J].Mater.Design,2017,114:161-166.
[5] Sun D D,Wang M S,Li Z Y,et al.Two-dimensional Ti3C2as anode material for Li-ion batteries[J].Electrochem.Comm.,2014,47:80-83.
[6] Mashtalir O,Lukatskaya M R,Kolesnikov A I,et al.The effect of hydrazine intercalation on the structure and capacitance of 2D titanium carbide (MXene)[J].Nanoscale,2016,8(17):9 128-9 133.
[7] Meng J K,Zhao Q Q,Ye W H,et al.Facile assembly and electrochemical properties of alpha-Fe2O3@graphene aerogel composites as electrode materials for lithium ion batteries[J].Mater.Chem.Phys.,2016,182:190-199.
[8] Zhu J F,Lu X,Wang L.Synthesis of a MoO3/Ti3C2Tx composite with enhanced capacitive performance for supercapacitors[J].RSC Adv.,2016,6(100):98 506-98 513.
[9] Zhang H,Dong H,Zhang X,et al.Cu2O hybridized titanium carbide with open conductive frameworks for lithium-ion batteries[J].Electrochim.Acta,2016,202:24-31.
[10] Yao Y F,Zhu Y H,Shen J H,et al.CoO nanosheets derived from electrodeposited cobalt metal towards high performance lithium ion batteries[J].Electrochim.Acta,2016,222:1 300-1 307.
[11] Wang R,Han M,Zhao Q N,et al.Construction of 3D CoO quantum dots/graphene hydrogels as binder-free electrodes for ultra-high rate energy storage applications[J].Electrochim.Acta,2017,243:152-161.
[12] Zou G D,Zhang Z W,Guo J X,et al.Synthesis of MXene/Ag composites for extraordinary long cycle lifetime lithium storage at high rates[J].ACS Appl.Mater.Inter.,2016,8(34):22 280-22 286.
[13] Ma J J,Wang J L,He Y S,et al.A solvothermal strategy:One-step in situ synthesis of self-assembled 3D graphene-based composites with enhanced lithium storage capacity[J].J.Mater.Chem.A,2014,2(24):9 200-9 207.
[14] Naguib M,Mochalin V N,Barsoum M W,et al.25 th Anniversary article:MXenes:A new family of two-dimensional materials[J].Adv.Mater.,2014,26(7):992-1 005.
[15] Yuan W W,Zhang J,Xie D,et al.Porous CoO/C polyhedra as anode material for Li-ion batteries[J].Electrochim.Acta,2013,108:506-511.
