2,3-二氟甲苯用作锂离子电池防过充添加剂的研究
2018-04-11李志健史凤兰黄东海
李志健, 史凤兰, 张 宏, 黄东海, 余 乐
(1.陕西科技大学 轻工科学与工程学院, 陕西 西安 710021; 2.陕西科技大学 机电工程学院, 陕西 西安 710021; 3.广州天赐高新材料股份有限公司, 广东 广州 510760)
0 引言
锂离子电池广泛应用于各个领域[1],其安全问题已经成为人们关注的重点.由于三元材料在高电压下的安全性能较差[2],故当锂离子电池过充时,电池的电压随着极化增大而迅速上升,引发正极活性物质结构的不可逆变化以及电解液氧化分解,进而产生大量气体、热量,致使电池存在燃烧、爆炸等安全隐患[3].
在早期研究的安全添加剂中,甲苯作为防过充添加剂[4],当电池充到4.5 V时,会发生聚合反应,降低了充电电流,达到了防过充的效果.而在4.3 V高电压电池50次循环内,其容量迅速下降[5].其原因是由于在4.3 V高电压电池满电状态下,甲苯已开始分解,致使电池内阻增大,不适用于高电压电池.为了解决这一问题,Taggougui M等[6]提出采用氟原子等吸电子基团取代苯环上的氢原子,可有效地提高芳香族化合物的氧化电位.
本文选用2,3-二氟甲苯作为锂离子电池电解液的防过充添加剂,研究了其防过充效果以及对LiNi0.5Co0.2Mn0.3O2电池循环的影响.
1 实验部分
1.1 电解液的配制
在氮气手套箱中(H2O<0.1 ppm、O2<0.1 ppm),将1 mol/L LiPF6/EC+EMC(广州天赐公司产,99.99%)按质量比1∶3混合,定义为Control.Control作为溶剂,甲苯(阿拉丁,99%)、2,3-二氟甲苯(阿拉丁,98%)作为添加剂.配制6%甲苯(阿拉丁,99%)、6%的2,3-二氟甲苯(阿拉丁,98%)电解液,分别记为6Toluene和6Di-Ftoluene,待其完全混合使用,具体配方见表1所示.

表1 电解液添加剂的配方
1.2 实验方法与仪器
1.2.1量子化学理论计算
在Gaussian软件中,采用密度泛函理论(DFT)中的B3LYp/6-311G++d方法对添加剂甲苯、2,3-二氟甲苯进行几何构型的全优化[7],确定最高占据轨道(HOMO)和最低占据轨道(LUMO)能量.
1.2.2电化学性能测试
(1)线性扫描伏安法(LSV)测试:在CHI604C电化学工作站(上海辰华)上进行测试,CR2025扣式电池,正极材料为LiNi0.5Co0.2Mn0.3O2材料,扫速为0.02 mV/s,电压范围为3~6 V.
(2)交流阻抗测试:在Solartron1470E电化学工作站(英国产)上对电池进行交流阻抗测试,频率为10-2~105Hz,交流振幅为10 mV.
(3)充放电性能测试:将编号Control,6Toluene和6Di-Ftoluene的电解液注入注液量为5.5 g、容量为1 750 mAh的高电压三元材料(LiNi0.55Co0.2Mn0.3O2)电池(广州天赐公司产)中[8].采用CT-3008-5V3A- A1型充放电测试柜(深圳产)对电池进行测试.
室温循环性能测试以容量1C,电压3~4.4 V充放循环100圈;过充性能测试是电池在4.4 V满电状态下,1C恒流充电6.35 V.
1.2.3表征
在手套箱中,用工具将充满电的电池拆开,取出隔膜.将隔膜在DMC溶剂中冲洗,除去残留的电解液,真空干燥2 h.采用日本Hitachi SU8010高分辨冷场发射扫描电子显微镜及其能谱分析表征形貌、尺寸及元素组成.
2 结果与讨论
2.1 前线分子轨道能量计算
添加剂甲苯和2,3-二氟甲苯的结构区别是:2,3-二氟甲苯的邻位和间位上各有一个强电负性取代基——氟原子,如图1所示.
图1 甲苯和2,3-二氟甲苯的结构式
分子的HOMO能量越高,轨道中的电子越不稳定,越容易被氧化夺去;而分子的LUMO能量越低,则还原性越好[9].在表2中,2,3-二氟甲苯的HOMO能量比甲苯的HOMO能量低,说明在甲苯上引入两个氟原子的2,3-二氟甲苯,其抗氧化能力更强、更稳定.

表2 前线分子轨道能量计算结果
2.2 线性扫描伏安测试
图2为不同电解液在LiNi0.5Co0.2Mn0.3O2/Li扣式电池中的线性扫描伏安法(LSV)曲线.由图2可知,Control电解液除了在4.7 V左右出现少量电解液分解外,仅在电压超过5 V时才开始剧烈分解反应.而6Toluene和6Di-Ftoluene电解液的氧化反应分别是从4.5 V、4.85 V开始出现,表明添加剂2,3-二氟甲苯的氧化稳定性更好,其初始氧化电位比甲苯提高了0.35 V,验证了表2前线分子轨道能量的结果,同时均符合氧化电位的理想区间(高于电池的满电电压,小于电解液氧化分解电压).
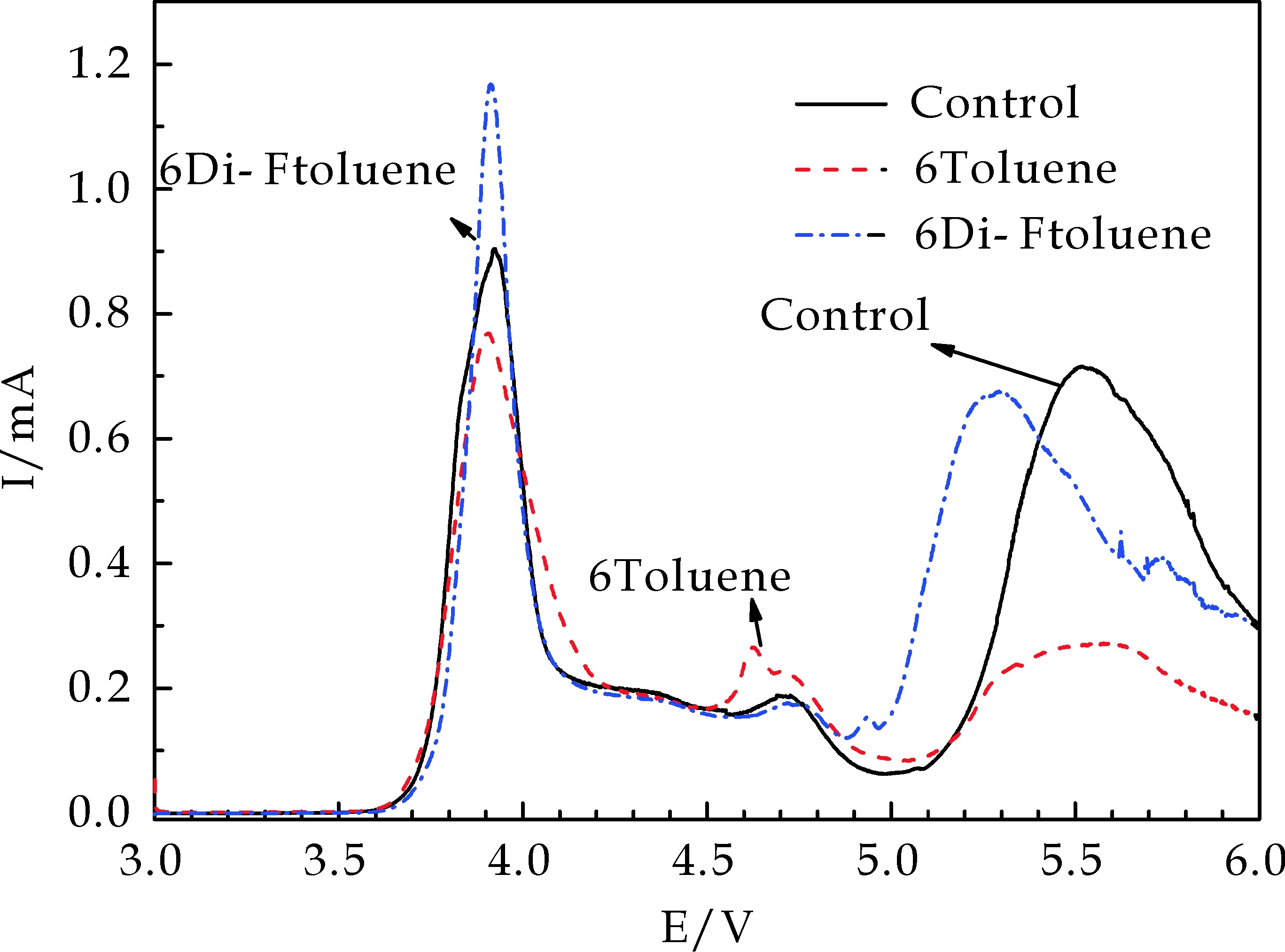
图2 不同电解液在LiNi0.5Co0.2Mn0.3O2/Li扣式电池中的线性扫描曲线
2.3 过充实验
图3为LiNi0.5Co0.2Mn0.3O2/Li扣式电池采用不同组分电解液的过充测试曲线.由图3可知,电池在Control电解液中迅速上升至5 V.而加入甲苯、2,3-二氟甲苯后则分别在电压为4.5 V、4.85 V时出现平台,并在很长时间后达到6.35 V.

图3 LiNi0.5Co0.2Mn0.3O2/Li扣式电池采用不同组分电解液的过充测试曲线
2.4 隔膜形貌及EDS分析
样品a、b、c、d依次为原始隔膜、Control电解液的电池过充后的隔膜、6Toluene电解液的电池过充后的隔膜、6Di-Ftoluene电解液的电池过充后的隔膜.图4为不同电解液中隔膜过充前后的扫描电镜图(SEM).与原始隔膜图4(a)相比[10],采用Control电解液的电池过充后的隔膜图4(b)无明显变化,仅存在少量的电解液氧化分解产物,而加入添加剂的电池过充后的隔膜图4(c)和图4(d)则表面变厚,似乎覆盖一层膜,推测其为添加剂聚合反应的不可逆产物[11].

(a) 原始隔膜 (b) Control电解液
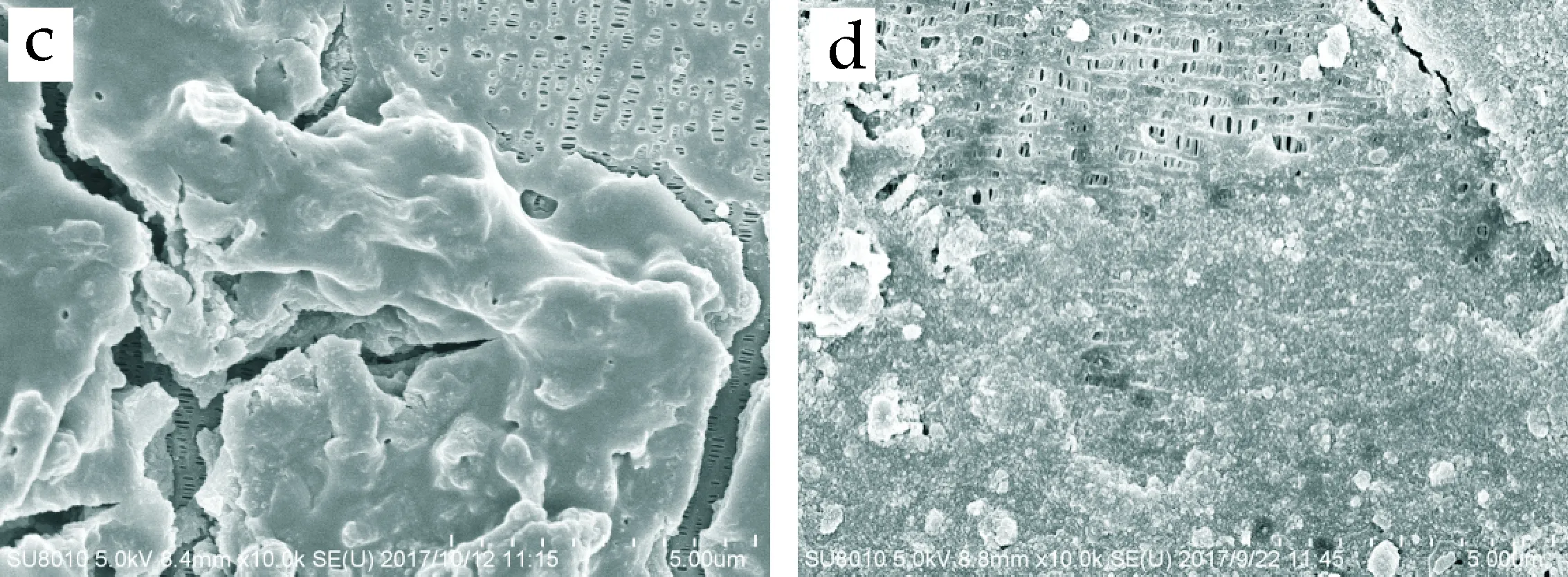
(c) 6Toluene电解液 (d) 6Di-Ftoluene电解液图4 不同电解液中隔膜过充前后的扫描电镜图
表3为不同电解液中隔膜过充前后的能谱分析.由表3可知,隔膜的主要成分为C、O、Mn,过充后Control、6Toluene电解液电池中的隔膜表面则多出了F元素,说明隔膜表面存在电解液的分解产物;过充后6Di-Ftoluene电解液隔膜表面的F元素增多,说明隔膜表面存在大量的2,3-二氟甲苯聚合产物,从而验证了图4扫描电镜结果.

表3 不同电解液中隔膜过充前后的能谱(EDS)分析
2.5 过充前后交流阻抗影响
图5为在不同电解液的电池过充前后的交流阻抗.由图5可知,电池过充前阻抗基本接近,过充后阻抗与过充前相比明显增大,Control电解液的电池过充后阻抗略有增大,而6Toluene和6Di-Ftoluene电解液的电池过充后阻抗则变化很大.含有添加剂的电池过充后阻抗明显增大的原因,验证了图4结果.添加剂的聚合反应的不可逆产物沉积在正极片表面,引起电荷传递阻抗增大,阻碍了离子迁移、电荷传递等,从而使电池的整体阻抗变大[12].
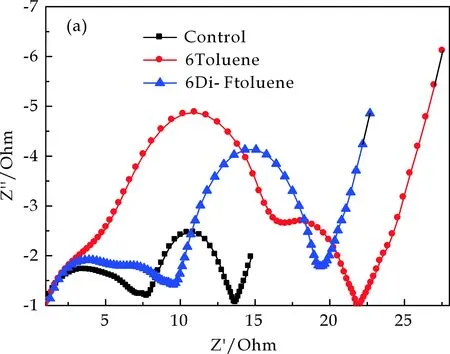
(a)过充前交流阻抗
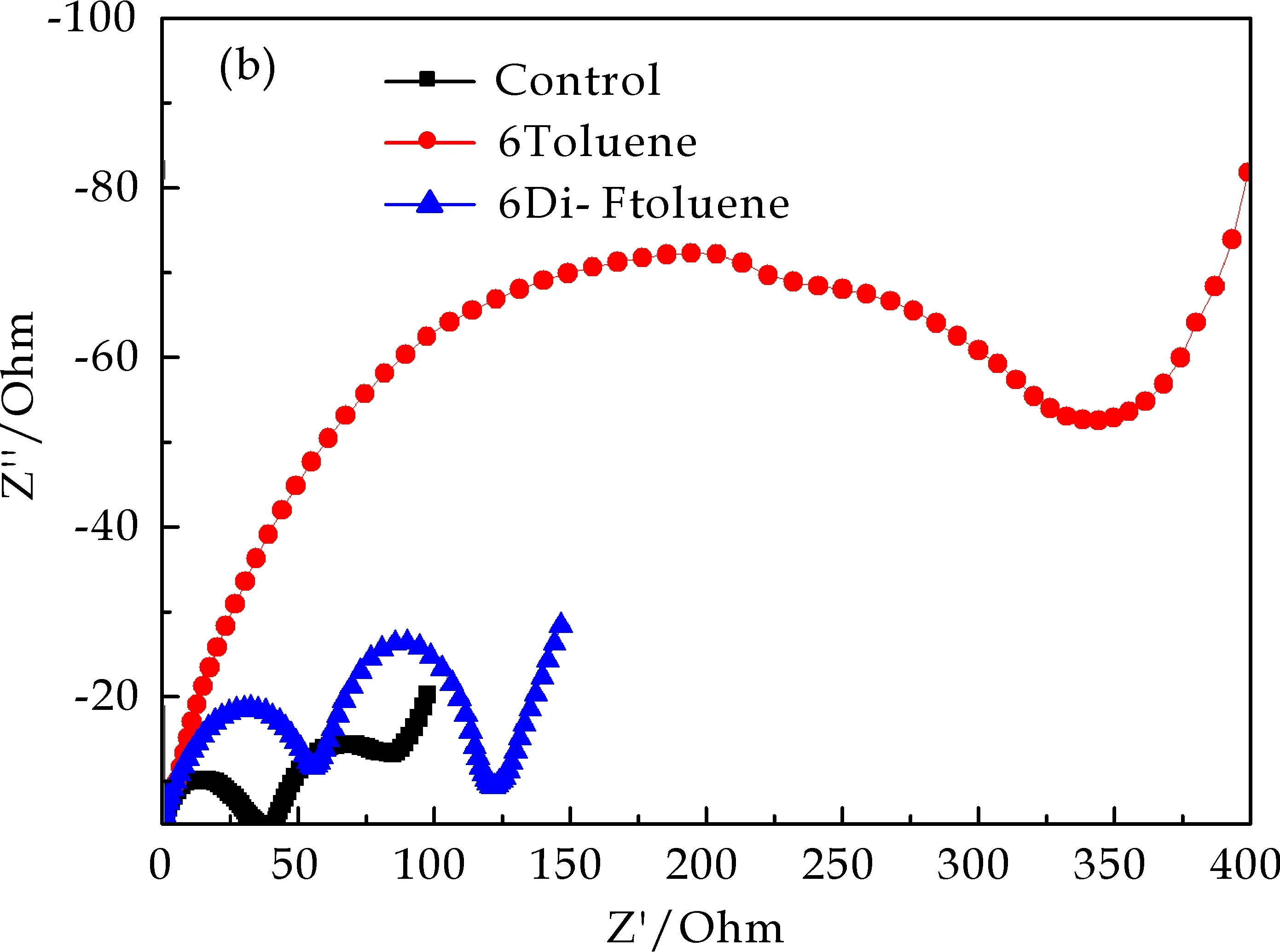
(b)过充后交流阻抗图5 不同电解液电池过充前后的交流阻抗
2.6 电池循环性能
图6为不同电解液电池室温循环性能.由图6可知,使用Control电解液的电池循环100圈后容量保持率为69.8%,与之相比,加入6Di-Ftoluene电解液的电池循环100圈后容量保持率为67.5%,与Control电解液的电池相比差异不大,而6Toluene电解液的电池在循环10圈后容量保持率急速下降.这表明加入2,3-二氟甲苯的电池优于加入甲苯添加剂的电池,含有甲苯电解液的电池呈现快速递减的趋势.推测是因为甲苯在4.4 V下产生副反应,在正极形成聚合物,导致循环性能劣化.
2.7 循环前后交流阻抗的变化
图7为不同电解液电池循环前后的交流阻抗.由图7可知,电池循环前阻抗基本接近,而循环后阻抗与循环前相比明显增大,其中,Control、6Di-Ftoluene电解液的电池循环后的阻抗略有增大,而6Toluene电解液的电池循环后的阻抗变化很大.推测含有甲苯添加剂的电池循环后阻抗明显增大的原因是:甲苯的氧化电位较低,在高电压4.4 V下发生副反应,分解产生高阻抗特性的聚合物,使得电池性能劣化,验证了图6的推测.结合图6、图7可知,添加剂2,3-二氟甲苯与甲苯相比,其氧化电位高,且在4.4 V电压下对电池的负面影响小.

图6 不同电解液电池的室温循环性能
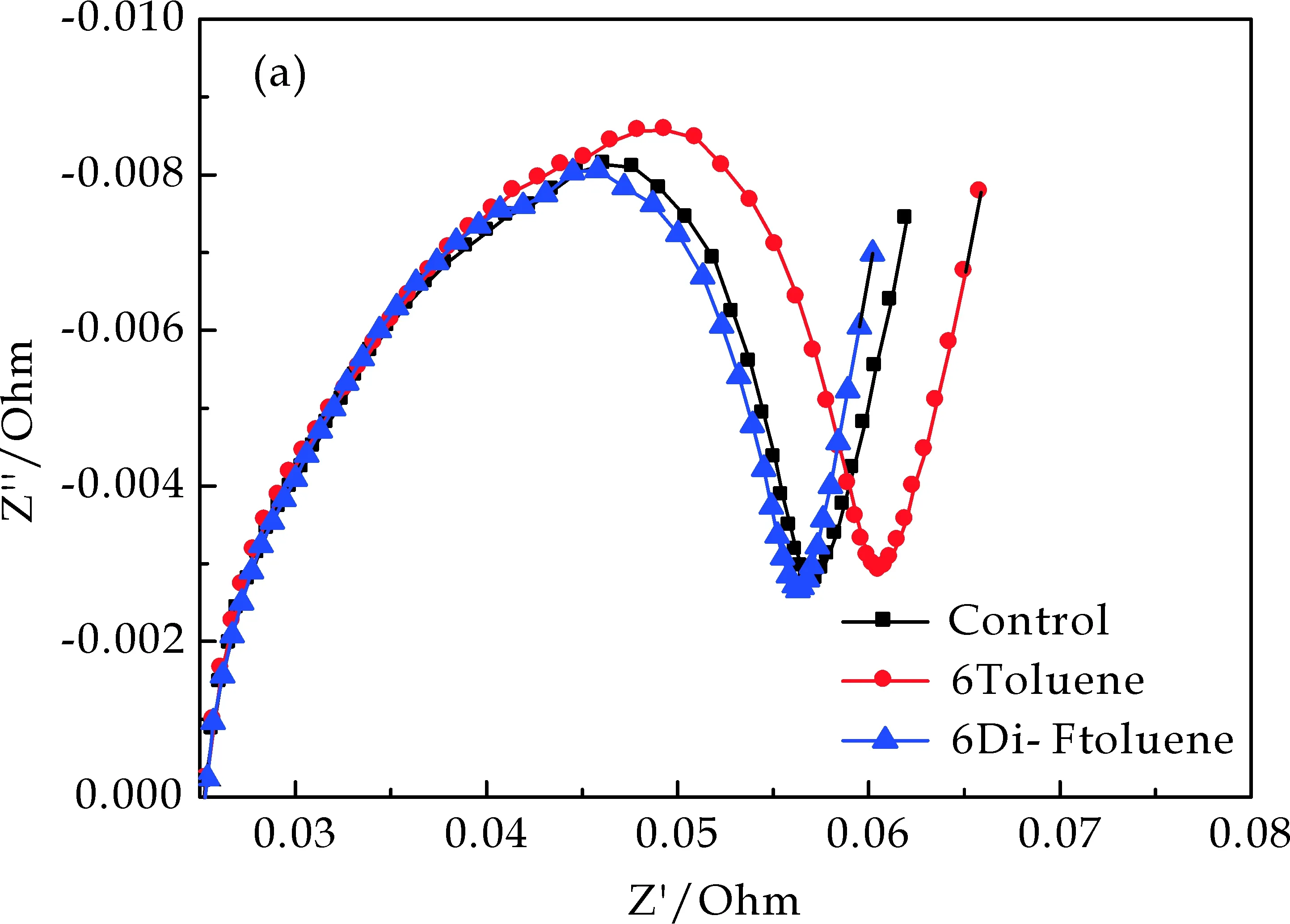
(a)循环前交流阻抗

(b)循环后交流阻抗图7 不同电解液电池循环前后的交流阻抗
3 结论
综上所述,在甲苯上引入具有较强电负性氟原子的2,3-二氟甲苯,与甲苯相比,降低了HOMO和LUMO能量,从而使初始氧化电位提高了0.35 V;含有2,3-二氟甲苯的电解液在高电压三元正极材料锂离子电池中,过充至4.85 V时发生电聚合反应,形成了高阻抗特性的含氟聚合物膜,有效限制了充电电流,达到防过充效果;同时,2,3-二氟甲苯在4.4 V高电压三元材料电池中的室温循环良好.
[1] 戴永年,杨斌,姚耀春,等.锂离子电池的发展状况[J].电池,2005,35(3):193-195.
[2] 沈恒冠,戚洪亮,佘圣贤,等.单晶高电压三元的制备及性能研究[J].电源技术,2016,40(7):1 356-1 358.
[3] Arora P,White R E,Doyle M.Capacity fade mechanisms and side reactions in lithium-ion batteries[J].Chem Inform,1998,145(10):3 647-3 667.
[4] 崔明,许汉良,黄赛先,等.一种锰酸锂为正极材料的锂离子电池用电解液[P].中国专利:CN101504992,2009-08-12.
[5] Feng X M,Ai X P,Yang H X.Possible use of methylbenzenes as electrolyte additives for improving the overcharge tolerances of Li-ion batteries[J].Journal of Applied Electrochemistry,2004,34(12):1 199-1 203.
[6] Taggougui M,Carré B,Willmann P,et al.2,5-Difluoro-1,4-dimethoxybenzene for overcharge protection of secondary lithium batteries[J].Journal of Power Sources,2007,174(2):1 069-1 073.
[7] Pople J A.Gaussian 03,revision C.02[J].Journal of the Royal Asiatic Society of Great Britain & Ireland,2004(1):91.
[8] 凌国维,唐致远,薛建军.软包装锂离子电池的研制[C]//化学与物理电源学术年会.广东惠州:中国电子学会,2002:105-106.
[9] 谢晓华,陈立宝,高阳,等.锂离子电池电解液功能组分的设计[J].电池,2006,36(6):435-437.
[10] 李素丽.电势敏感隔膜的制备及其在锂离子电池中的应用[D].武汉:武汉大学,2011.
[11] 叶佳娜.锂电子电池过充电和过放电条件下热失控(失效)特性及机制研究[D].合肥:中国科学技术大学,2017.
[12] 黄东海,刘蕊,范伟贞,等.2,4-二氟联苯用作高电压锂离子电池防过充剂[J].电池,2017,47(4):223-225.
