“初高中化学衔接”视角下的“氧化还原反应”教学设计
2018-03-19于斌
于 斌
(南京市秦淮高级中学,江苏 南京)
“氧化还原反应”是高中化学必修课程中的核心概念,它不仅是一种十分重要的化学反应类型,而且在生产、生活等各个方面具有广泛的应用。同时,这一概念是连接义务教育阶段化学与高中化学的纽带和桥梁,对于发展学生的科学素养、引导学生有效地进行高中阶段的化学学习具有承前启后的作用。根据自己多年的教学经验谈一下具体的做法和体会。
一、从“初高中内容衔接”的角度分析“氧化还原反应”
人教版九年级化学在第二单元“我们周围的空气”的“课题2氧气”中介绍了化学反应、氧化反应,出现了氧化性和氧化剂概念。人教版高中化学1在第二单元“化学物质及变化”第三节“氧化还原反应”中,首先以木炭还原氧化铜为例,从得氧、失氧角度判断氧化铜发生了还原反应、碳发生了氧化反应的基础上,说明氧化反应和还原反应是同时的。这样的反应称为氧化还原反应。接着通过分析氧化还原反应中某些元素的化合价在反应前后发生的变化。然后从原子核外电子的运动情况对物质的化学反应有非常大的影响,要想深刻地揭示氧化还原反应的本质,需要从微观角度来认识电子转移与氧化还原反应的关系。
二、从“初高中内容衔接”的角度构建“氧化还原反应”教学目标
1.知识层面
初中阶段对氧化还原反应的认识介绍比较简单,不够全面不够本质。而高中阶段的教学需要从本质上认识氧化还原反应。同时在初中直观地学习了化合价,理解了化合价的变化,但并没有了解化合价变化的实质以及化合价的变化与得失电子之间的关系。基于此,知识层面上教学目标设计是:(1)使学生理解氧化反应和还原反应必然同时发生在一个氧化还原反应中。(2)通过分析化学反应中元素化合价的变化,使学生建立氧化还原反应的概念。(3)使学生认识到化合价变化,电子转移是反应分类的标准之一,也是研究物质性质的重要思考角度。
2.方法层面
初中化学课程,注重化学教学的基础性和启蒙性,其知识层次要求学生“知其然”为主,在能力培养方面注重定性分析和形象思维。而高中化学更加注重学习的主动性和能动性,逐渐向系统化和理论化靠近,要求“知其所以然”。因此在教学“氧化还原反应”时,要注意方法的选择,确定方法的教学目标。(1)注重学生认识思路的结构化和显性化。(2)注重真实问题情境的设计、引导思考、实验探究、分析得出结论。(3)注重“教、学、评”一体化,提高学生分析、联想、类比、迁移以及概括能力。
3.情感层面
初高中化学所学内容差别很大,如果教师不注重从情感方面与学生沟通,那么高一化学学习时学生就会出现抵触的情绪。而“氧化还原反应”的内容正是进行辩证唯物主义教育的好教材。确定情感的教学目标。(1)通过交流、讨论活动,探究、加强学生之间的合作学习。(2)在理解电子得失、氧化和还原的相互依存和相互对立的关系上,感知事物的现象与本质之间的关系。
三、教学过程设计
【学习任务1】:
1.初中阶段,我们有哪些途径获得单质铜

2.以反应(1)(2)为例完成表格
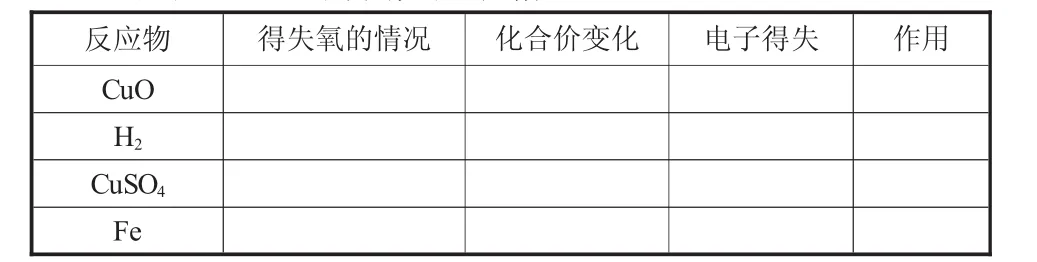
反应物 得失氧的情况 化合价变化 电子得失 作用CuO H2 CuSO4 Fe
3.分析反应(1)中反应物的得失氧情况,概括反应前后相关物质得失氧的关系
分析反应(1)(2)化合价变化情况,概括反应前后相关元素化合价升降的情况。
观察实验,分析反应(1)(2)中电子转移情况,概括反应前后相关物质电子得失的情况。
4.归纳:氧化还原反应的概念
从得失氧角度;
从化合价变化角度;
从电子得失角度。
【学习任务2】:分析H2和单质铁在(1)(2)两个反应中的作用
1.归纳H2和单质铁反应前后化合价变化情况。
2.概括氧化剂、还原剂在反应中的变化特点,填入下表。

氧化剂 氧化剂从得失氧角度从化合价升降角度从电子得失角度
【学习任务3】
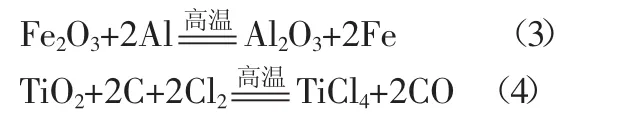
(1)双线桥分析(3)、(4)。
(2)归纳H2和单质铁反应前后电子转移的数目有何关系。
(3)电子得失情况。
氧化剂得到的电子总数_______,还原剂失去的电子总_______。
【拓展训练】
氧化还原反应在工农业生产和日常生活中有广泛应用。
(1)人通过呼吸作用吸入氧气,氧化体内的葡萄糖,提供能量以维持生命活动,反应为C6H12O6+6O2→6CO2+6H2O+能量,该反应中的还原剂是_______(填化学式)。
(2)罐头厂在装食物罐头时,通常要添加一些对人体无害的防腐剂,防止食物被空气中的氧气氧化而变质,此类食物防腐剂应具有 (填“氧化性”或“还原性”)。
四、结语
整节课通过一系列学习任务的解决使学生对氧化还原反应有了充分的认识,培养了积极探索科学问题的热情和解决生产生活中的化学问题的担当和能力,突出了化学学科对提高人类生活质量和促进人类社会发展的价值。
