基于硫代硫酸盐铜乙二胺浸金体系铜及乙二胺影响电化学研究*
2018-03-15项朋志叶国华
项朋志 刘 琼 黄 遥 叶国华
(1.云南开放大学化学工程学院;2.昆明理工大学国土资源工程学院)
氰化浸金工艺具有毒性,因此硫代硫酸盐浸金体系作为无毒非氰体系受到重视[1-2]。在近几十年来,很多研究团队致力于硫代硫酸盐浸金的研究。研究表明,该浸金体系常温下即可达到理想的金浸出效果[3-4],有研究表明利用乙二胺代替氨水也可取得不错的效果。乙二胺能够与许多过渡金属离子形成稳定的配位化合物,与铜相配合可以形成稳定的配合物,降低铜离子的氧化性,降低硫代硫酸钠的消耗,因此硫代硫酸盐铜乙二胺体系具有潜在的使用价值。
基于硫酸盐铜乙二胺体系电化学鲜有报道,基于分析化学角度,采用方波伏安法探究了硫酸盐铜乙二胺体系电化学行为,探究铜离子、乙二胺及添加剂EDTA对金溶出的影响,为硫代硫酸盐铜乙二胺浸金体系提供一定的理论基础。
1 试验部分
1.1 试验材料
所用试剂均为分析纯,试验用水为去离子水。
1.2 分析仪器
电化学分析采用mec-16多功能电化学分析仪(江苏江分电化学仪器公司), 采用三电极系统,其中铂丝电极作为辅助电极,饱和甘汞电极作为参比电极,金电极或铂电极作为工作电极。pH值采用PHS-25型pH计测定 (上海仪电科学仪器股份有限公司)。
1.3 浸出体系
结合文献,硫代硫酸钠浓度选择为0.08 mol/L,铜离子浓度选定为0.002~0.01 mol/L,乙二胺浓度选为0.02~0.1 mol/L,pH值调到10左右。
2 试验结果与讨论
2.1 浸出体系电化学行为
在硫代硫酸钠乙二胺铜浸金体系中铂电极和金电极的方波伏安曲线见图1。

图1 硫代硫酸钠乙二胺铜浸金体系中
由图1可见,曲线1对应为铂电极,曲线2对应为金电极,曲线2与曲线1最大的差别在于在电极电势为0.2 V处,有一金的氧化峰,在曲线2中,电极电势为-0.610 V对应于硫代硫酸钠还原峰,电极电势为-0.424 V对应于铜的还原峰,这两处峰相对于曲线1来说,更有特征性且电势朝正方向移动,这说明金电极对于硫代硫酸钠和铜的还原有良好的促进作用,所以在硫代硫酸钠乙二胺铜浸金体系中,金作为工作电极更具有特征性,在曲线2中出现的这3种峰可以作为该体系中监测各种因素的信号。
利用金电极,对硫代硫酸钠乙二胺铜浸金体系进行循环伏安分析,结果见图2。
由图2可见,图中出现了两对准可逆峰,其中峰b对应于金的溶出峰,峰c对应于硫代硫酸钠的还原峰,峰e对应于铜(II)的还原峰。
2.2 铜浓度对金的溶出影响

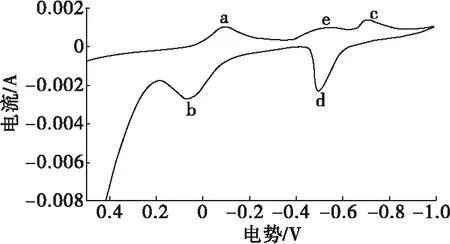
图2 硫代硫酸钠乙二胺铜浸金体系中
(1)
Cu2++ 2OH-→Cu(OH)2
(2)
(3)
(4)
en+Cu+→[Cu(en)]+
(5)
(6)
采用方波伏安法评价当条件一定时,铜的浓度对金的浸出影响,对金的溶出影响结果见图3。
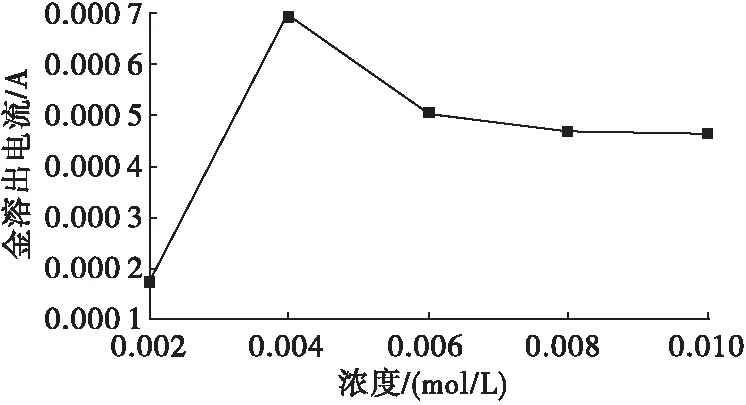
图3 铜离子对金的溶出电流的影响
(Cen=0.06 mol/L,CS2O32-=0.08 mol/L,pH=10)
由图3可见,随着铜浓度的增加,金的溶出峰先增加后减小,当铜的浓度为0.004mol/L时,金的溶出峰最大,铜的浓度增大对反应(1)、(6)有促进作用,但反应(2)、(3)、(4)显然对金的溶出是不利的。一般说来,基于铜在溶出过程中具有催化作用,铜的浓度增加对金的溶出是有利的[6],但当铜的浓度超过0.004mol/L时候,从图3可以看出,金的溶出下降,原因可能是铜离子浓度更高将会消耗更多的硫代硫酸盐,另外反应(2)、(3)、(4)将会在金表面产生钝化作用。
铜的还原电流与铜的浓度关系见图4。

图4 铜的浓度对铜的还原峰电流的影响
(Cen=0.06 mol/L,CS2O32-=0.08 mol/L,pH=10)
由图4可见,在浓度为0.002~0.010mol/L时,铜的还原电流与铜的浓度关系线性关系较差,其方程为y=0.658 1x+0.000 29(R=0.937 2),铜离子浓度超过0.004 mol/L时,其还原峰将下降,这说明增加的铜离子并没有转化成可被还原的形态,有可能转化成难溶物,导致其还原峰下降;从图3,图4可以充分说明,在该浸体系中铜的浓度并非越大越好,其最佳浓度可以控制在0.004 mol/L左右。
2.3 乙二胺浓度对金的溶出影响
关于乙二胺(en)的作用,Xia[5]认为在整个浸出过程中,乙二胺(en)参与了以下反应:
(7)
(8)
(9)
(10)
根据方程式(7)~(10),按理论来讲,较大浓度的乙二胺(en)浓度对浸出浓度有利。乙二胺浓度对金的溶出峰的影响见图5。

图5 乙二胺浓度对金的溶出峰的影响
CS2O32-=0.08 mol/L,pH=10)
由图5可见,当乙二胺(en)浓度为0.02~0.06mol/L时,金的溶出峰电流增大,当其浓度增大至0.10mol/L时,金的溶出峰电流反而下降,即当乙二胺(en)浓度为0.06mol/L时,金的溶出峰最大,这说明乙二胺(en)浓度在一定范围内增加是有利于金的溶出,但过高的乙二胺(en)浓度有可能对金的溶出不利,原因可能是过高的乙二胺(en)浓度可能使溶液的pH值偏高,而pH值又影响到铜(II)和硫代硫酸钠的浓度,这一点也可以从图5中同样可以看出;当乙二胺(en)浓度为0.06~0.10mol/L时,不但金的溶出峰下降,铜(II)和硫代硫酸钠的还原峰均下降;基于此,选择合适的乙二胺(en)浓度是有必要的,从电化学角度所筛选的条件与文献中实际工艺最佳条件基本相似[7]。
2.4 添加剂EDTA溶液对金的溶出影响
乙二胺四乙酸俗称为EDTA,文献表明适量的EDTA的加入可促进金的溶解。在含0.1mol/L硫代硫酸钠、0.06mol/L乙二胺(en)和0.08mol/L硫代硫酸钠的溶液中,考查不同浓度EDTA对金的溶出影响,结果见图6。

图6 添加剂EDTA浓度对金的溶出电流的影响
由图6可见,适量的EDTA可以提高金的溶出,原因可能是铜离子与EDTA相结合,生成更加稳定的Cu(EDTA)2-降低了氧化电势,从而降低了对硫代硫酸钠的氧化,减少了氧化产物的生成,避免了金溶出时产生钝化现象,另外也可以使硫代硫酸钠保持较高的浓度[5],从而增加对溶出金的络合作用。
总而言之,在该浸金体系中,适度的EDTA对铜离子有稳定作用,减少了硫代硫酸钠的消耗,减少了钝化现象的产生,从而提高了金的溶出。这一点与许姣[8]所研究的硫代硫酸钠铜氨体系中EDTA 影响是类似的。
3 结 论
采用方波伏安曲线研究了硫代硫酸钠乙二胺铜浸金体系中铜离子浓度、乙二胺浓度、添加剂EDTA浓度各因素的影响,得出以下结论:
(1)在该浸金体系中,采用金电极作为工作电极不但出现了金的溶出峰,而且对于硫代硫酸钠和铜的还原具有良好的促进作用。
(2)铜的浓度超过0.004 mol/L时候,金的溶出下降。
(3)当乙二胺(en)浓度为0.06 mol/L时,金的溶出峰最大,较高的乙二胺(en)浓度有可能对金的溶出不利。
(4)在该浸金体系中,适度的EDTA对铜离子有稳定作用,可减少硫代硫酸钠的消耗,减少钝化现象的产生,从而提高金的溶出。
[1] 鲁顺利.非氰化法提金工艺研究现状[J].云南冶金,2011,40(3):32-36.
[2] 钟 晋,胡显智,字富庭,等.硫代硫酸盐浸金现状与发展[J].矿冶,2014,23(2):65-69.
[3] BREUER P,JEFFREY M.An electrochemical study of gold leaching in thiosulfate solutions containing copper and ammonia[J].Hydrometallurgy,2002,65(2):145-157.
[4] AYLMORE M G,MUIR D M.Thermodynamic analysis of gold leaching by ammoniacal thiosulfate using Eh/pH and speciation diagrams [J].Minerals & metallurgical processing,2001,18(4):221-227.
[5] XIA,C THI FENG D,DEVENTER J S J V.Thiosulphate leaching of gold in the presence of ethylenediaminetetraacetic acid (EDTA)[J].Minerals Engineering,2010,23(2):143-150.
[6] AYLMORE,M G,D M MUIR.Thiosulfate leaching of gold-A review[J].Minerals Engineering,2001,14(2):135-174.
[7] 高 鹏,唐道文,唐攒浪.用硫代硫酸钠从某卡林型金矿石中浸出金试验研究[J].湿法冶金,2017,36(1):12-15.
[8] 许 姣,胡显智,杨 朋,等.氨性硫代硫酸盐体系中金溶解过程的腐蚀电化学行为[J].昆明理工大学学报(自然科学版),2004(2):126-129.
