一次性使用湿化瓶不良事件处理的全流程控制实践
2018-03-13彭俊彦陈爽张雷钱建国
彭俊彦,陈爽,张雷,钱建国
复旦大学附属华山医院 装备科,上海 200040
引言
一次性使用湿化瓶作为医院临床病人吸氧过程中对氧气经行湿化的常规耗材,具有使用面广、使用量大、操作方便等特点,在我院临床使用量极大。近年来我院在临床应用中陆续发生了3起一次性使用湿化瓶在使用中爆裂的事件,为保证临床治疗时病人的安全,遵循JCI持续改进原则,在此次事件发生后我院设备管理部门立即组织力量深入调研,提出整改方案并实施[1-3]。
1 方法
1.1 调研
我院使用的一次性湿化瓶共有两个品牌,其中一个品牌仅在手术室使用,另一品牌的产品在病房、急诊等处使用,本次发生爆裂的湿化瓶来源于为病房、急诊提供湿化瓶的厂商。3起爆裂中有两起分别是在做超声雾化和正常吸氧湿化时发生的(19病房和37病房),另一个则是在充氧气袋时发生的(13病房)(表1)。

表1 我院发生的3起一次性使用湿化瓶爆裂事件的基本情况
根据厂商有关湿化瓶的工艺说明,一旦发生瓶内压力过大,为了保证病人安全,该一次性使用湿化瓶会在临界压力下自动上下脱开,防止因爆裂产生碎片飞溅伤害病人的事件发生。但通过观察湿化瓶爆炸后遗留残片发现其中两起爆炸是符合厂家所说的安全设计要求的,湿化瓶由中间断裂,上下脱开,保护了病人的安全;而另一个不符合安全爆裂,发生不规则爆裂,湿化瓶碎片向四周扩散飞溅,碎片飞溅距离约为10 cm。
集中出现问题的湿化瓶均为最新采购的批号为0110620的湿化瓶,由于数量不多,在不影响临床正常使用的情况下我方紧急通知临床,要求临床暂停使用该批次湿化瓶并封存所有相关湿化瓶,联系供应商紧急调拨新一批次的湿化瓶给临床使用。但第二天,新的一批次批号为0111128的湿化瓶在临床使用过程中又发生了多次爆裂现象,其中一次爆裂碎片飞溅到病人脸上,造成病人脸部受伤,于是应急召回小组召开紧急会议,评估风险后决定启动召回程序召回两个批次的湿化瓶,并根据封存的事故产品,请专业质量检测部门对供应商提供的湿化瓶进行检测[4]。
1.2 启动召回程序
1.2.1 风险评估
供应商产品专家、质量检测部门权威专家初步判断爆裂的两个批次湿化瓶在生产工艺、材质等方面存在缺陷,故根据我院《医院装备科工作手册》质量控制规程及制度中的条款,由科长、副科长、库房主管、帐务管理员组成应急召回小组,按照召回流程展开具体实施和全过程评估[5]。根据应急召回小组的风险评估意见,认为此批次湿化瓶爆裂问题集中,继续使用存在安全风险,需要根据工作手册要求实施院内召回[6-7]。
1.2.2 召回启动
确认召回启动后,我科第一时间向医务处递交不良反应事件报告及评估结果[8-9]。应急召回小组确认召回数量和批号,通过我科和供应商的出库入库登记单据,定位所有该批次的一次性使用湿化瓶去向,通过临床使用单位的使用登记信息,核对数量并封存(表2)。将该问题批次的湿化瓶召回(其中5病房少召回一只,6病房多召回前一批次的10只)。与供应商提供的出库单据吻合,与装备科领物清单吻合[10]。
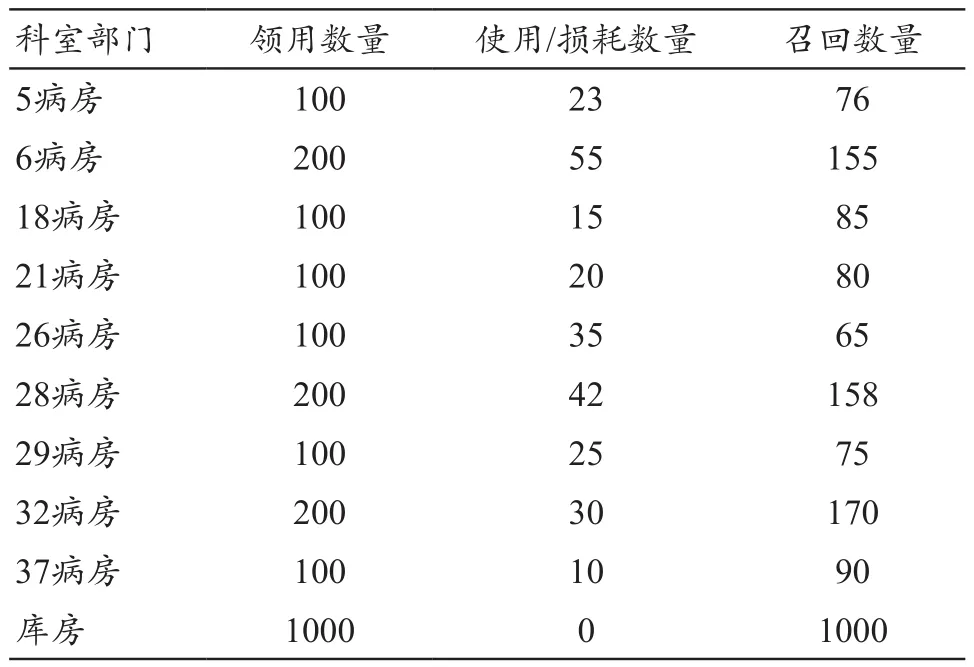
表2 各科室召回湿化瓶情况(只)
1.2.3 召回处置
召回耗材由临床签字确认,装备科统一收集,再交付供应商悉数召回[11]。
1.2.4 流程评估
应急小组评估整个召回实施,整个召回流程共召回生产批号为0110620、0111128两个批次的一次性使用湿化瓶共1954只,已使用(损坏)湿化瓶255只,未召回湿化瓶为1只,基本免除该批次湿化瓶在临床产生的风险。
1.2.5 结果上报
将召回结果上报医务处,经医务部门上报相关不良事件上报中心,科室内做好备案工作[12-13]。
2 结果分析
装备科按工作手册要求对供应商产品的事故原因进行分析,可能有以下原因引起一次性湿化瓶发生爆炸[14]。
2.1 吸氧湿化
对比上海各大医院的不良事件资料发现,在正常使用过程中湿化瓶发生爆裂的情况非常罕见。质检部门的最终检测报告结果显示,该批次湿化瓶绝大部分在<0.4 Mpa(出厂标准)的压力下情况不会发生爆裂,但部分产品对氧气压力实际承受极限值存在10%左右的误差(只有0.36 Mpa左右)[15-16]。
2.2 驱动超声雾化
国家食品药品监督管理局在2006年发过《关于正确使用浮标式氧气吸入器的紧急通知》,在通知中写明“禁止利用浮标式氧气吸入器进行氧气雾化吸入治疗”的条款(详见国食药监办[2006]155号)。北京也有因使用湿化瓶做雾化治疗引发湿化瓶爆裂,飞溅的碎片划伤病人眼睛造成严重的病人伤害的案例。
使用雾化器时在雾化器的雾化腔内混合使用液态和粉剂药物,由于要产生较高的压力差引流药物通过氧气出口,雾化腔内的氧气出口必须极细小(图1),非常容易被粉剂药物阻塞,一旦阻塞就会使得整个上游气路压力骤升[17-18]。

图1 雾化器孔
2.3 充氧气袋
临床用液氧经湿化瓶充氧气袋,有时临床或病人家属为了多充一点氧气就会用力挤压氧气袋,导致整条气路承受更大的压力。
2.4 安全脱开失效
湿化瓶的瓶身上有一圈薄弱圈,该部分的受压能力要明显弱于湿化瓶的其他部分,当瓶内压力到达某个临界值得时候该圈上的某个薄弱点会比其他部位优先断开,防止湿化瓶爆裂。但我院发生的3次爆裂中有一次爆裂并没有按照预设的安全防护原则进行,存在碎片飞溅伤害病人的风险。
3 改进措施
3.1 采用全新模具
3.1.1 加大瓶身
对湿化瓶内特定质量的气体为研究对象,由简单的理想气体状态方程:


图2 理想气态方程曲线
当出气端氧气流通不畅时,相对入气端较大的氧气流速,可定性认为出气端阻塞,气体相对体积变化的压力变化随该气体的多少而变化,故空腔越大气体的量越多,承受的压力变化就越少,也越安全。
按照以上分析,厂商对其产品生产线进行了升级改进,加大了湿化瓶身。更大的湿化瓶也拥有更大空腔,抵抗压力突变的能力也更强。使其对氧气压力的承受力增大到0.5 MPa(经第三方检测)。
3.1.2 改进材料
厂商更换了原材料的供应商,使用了纯净度更高的PVC粒子,材质中的杂质浓度将直接影响材料表面张力,瓶身的材料张力正是影响湿化瓶强韧的主要因素。
3.1.3 增厚瓶壁
在改变了湿化瓶大小的基础上,厂商增加了瓶身的厚度,以此增加湿化瓶的抗摔能力,减少使用湿化瓶过程中的碰、摔使瓶身受伤的可能。
3.1.4 安全脱开机制
原模具的薄弱点部分因为长时间的使用已经磨损,薄弱点已经无法有效形成,故趁此次更换新磨具的机会将之前已经磨损的旧磨具淘汰,并规定当模具使用一定年数时必须强制报废。
3.2 加强培训
临床在正确使用湿化瓶中仍存在一些不良习惯,我科室人员将会协同供应商对临床护士进行详细的产品培训,并在病房显著位置粘贴湿化瓶使用注意事项。
3.3 加示标贴
在病房等需要使用湿化瓶的醒目部位粘贴标贴,提醒临床正确使用一次性湿化瓶。防止因粗心大意或培训不到位导致的湿化瓶误操作。
4 总结讨论
在对两个批次湿化瓶的召回过程中,未能将所有湿化瓶一次性如数召回,其主要原因在于临床对不安全产品的召回流程普遍缺乏认识,急需加强培训。其次是问题湿化瓶的数量较大、批次多、时间间隔长,临床虽有每次领用的湿化瓶批号,但没有做到每次都能正确登记和标示,造成遗漏和错登记现象,这些都影响了召回的速度和准确性,下步改进措施是在临床引入计算机系统加强医用耗材的批号登记和管理。
[1]彭磷基.国际医院管理标准(JCI)中国医院实践指南[M].北京:人民卫生出版社,2008.
[2]刘少杰.浅析计量检测在保证医疗设备质量中所起的作用[J].科技创新与应用,2015(20):296.
[3]郑盘根,郜宝成.浅谈医疗设备的科学管理[J].总装备部医学学报,2010,(3):132-133.
[4]汤黎明,吴敏,陈锐华.医院医疗设备企业化管理探索[J].医疗卫生装备,2007,28(9):46-47,50.
[5]杨晓慧.医疗设备风险评估与安全管理[J].健康界,2012,9(4):36-38.
[6]国家食品药品监督管理局.医疗器械监管技术基础[M].北京:中国医药科技出版社,2008.
[7]郑骏,陈斯尧.JCI体系中医疗设备风险管理的实践和探讨[J].中国医疗设备,2014,29(6):78-80.
[8]谢松城.医疗器械临床使用风险及其对护理质量的影响[J].中国护理管理,2010,10(10):5-7.
[9]Clark T, Perron E.临床工程指引——医疗仪器设备临床应用分析评估[M].北京:中国计量出版社,2009.
[10]范明利,范兴.对在用医疗设备的质量控制的几点具体做法[J].现代科学仪器,2010,(5):138-139.
[11]Claycamp HG, Rahaman F, Urban JM.The reliability-quality relationship for quality systems and quality risk management[J].PDA J Pharm Sci Technol,2012,66(6):512-517.
[12]GB/T 7826-87,系统可靠性分析技术-失效模式和效应分析(FMEA)程序[S].2009.
[13]中华人民共和国卫生部,医疗器械召回管理办法(试行)(卫生部令第82号)[S].2011.
[14]周琳,陈奕霖,梁庆宇.FMEA与RCA在骨科风险管理中的综合应用[J].成都医学院学报.2012,7(2):166-169.
[15]米永巍,李怡勇,郭赤.医疗设备质量控制体系的建立与实施[J].中国医疗设备,2010,26(11):94-96.
[16]国家食品药品监督管理局.《医疗器械不良事件监测和再评价管理办法(试行)》(国食药监械[2011]425)[S].2011.
[17]赵燕,郑立,王刚,等.医疗器械召回典型案例研究[J].中国药物警戒,2011,8(12):722-724.
[18]Karaarslank.Joint commission on international accreditation workshop: planning, development and provision of laboratory services[J].Clin Biochem,2009,42(4):284-287.
