DSA三维重建后处理技术在颈内动脉海绵窦瘘治疗中的应用价值
2018-03-08胡威陈如东杨洪宽于加省
胡威, 陈如东, 杨洪宽, 于加省
颈内动脉海绵窦瘘(carotid-cavernous fistula,CCF)是颈内动脉海绵窦段及其分支与海绵窦异常沟通而引起的一组临床综合征,可分为外伤性和自发性,多因外伤引起。经血管内栓塞技术来封堵瘘口是近年来治疗CCF的主要方法,而寻找瘘口是治疗的关键[1]。多平面重组(MPR)技术可多平面、多角度的显示瘘口的位置及大小。本文拟探讨DSA三维血管重建技术在CCF治疗中的应用价值,为临床治疗方案的选择提供参考。
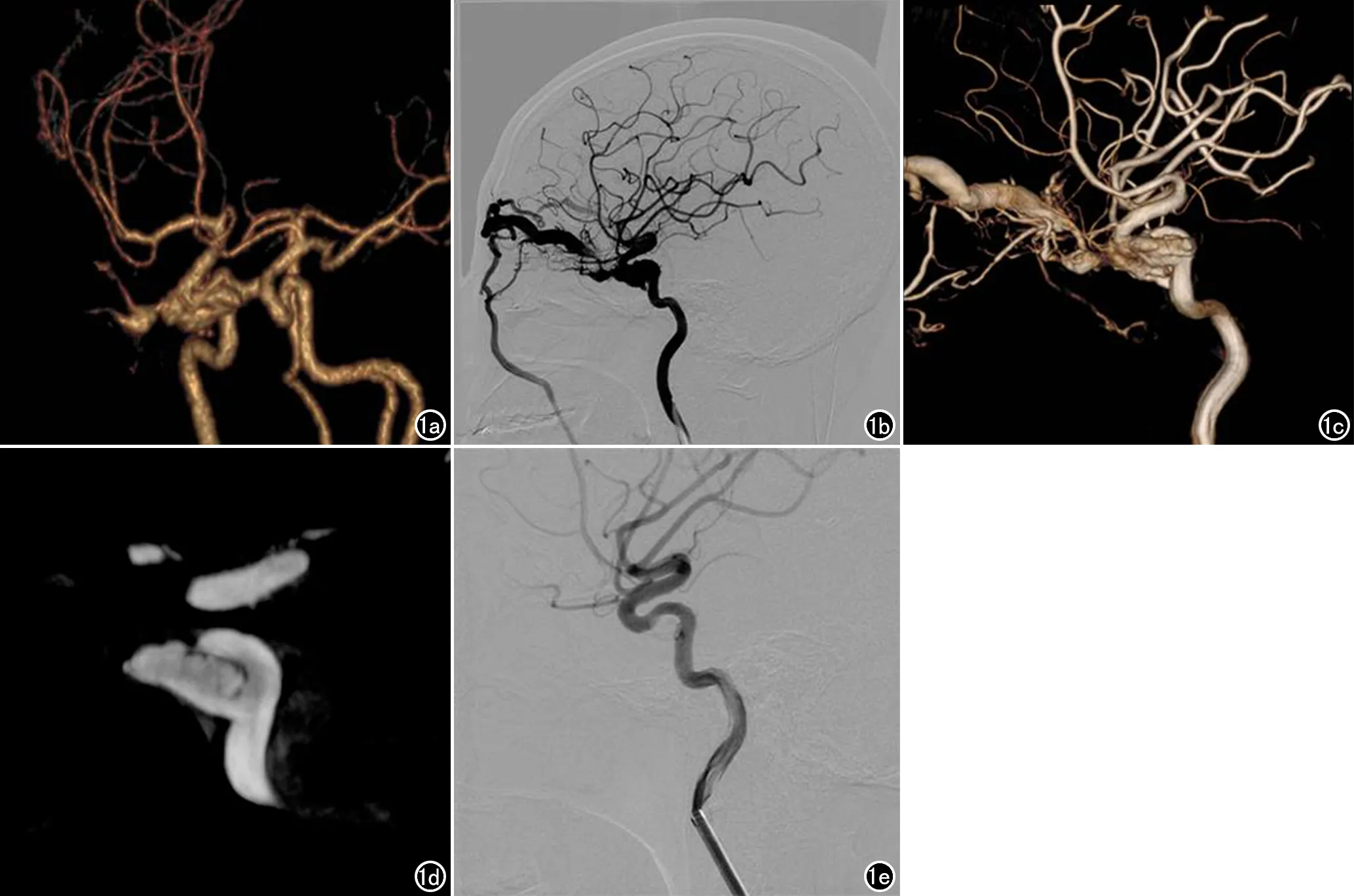
图1 患者,女,65岁,外伤性CCF。a) CTA示瘘口显示不清; b) DSA侧位造影提示瘘口显示不清,对比剂经眼上静脉引流; c) 3D VR图显示海绵窦包绕颈内动脉,无法显示瘘口位置与颈内动脉关系; d) MPR显示瘘口较小,可选择可解脱球囊闭塞瘘口; e) DSA示经可解脱球囊闭塞瘘口后瘘口未再显影,颈内动脉通畅。
材料与方法
1.临床资料
收集2009年1月-2016年6月本院收治的67例CCF患者(男47例,女20例),其中外伤性59例(男46例,女13例),自发性6例(男1例,女5例),医源性损伤2例(女2例)。临床表现为眼球突出及球结膜水肿65例,颅内搏动性杂音10例,视力下降8例,眼球外展受限7例,单纯复视1例,鼻出血1例。
2.仪器设备及造影过程
机器型号为美国GE Innova-3131 IQ双平板DSA。工作站GE ADW 4.5(Advantage Workstation 4.5)。高压注射器为美国 Medrad MarkⅤ。
患者于术前4 h禁食、水。双侧腹股沟区备皮,采用Seldinger技术穿刺右侧股动脉,置入Cordis 5F造影导管行双侧颈内动脉、颈外动脉及椎动脉造影(先行患侧颈内动脉正侧位及3D血管成像,再按压患侧颈总动脉并分别行健侧颈内动脉正位和椎动脉侧位造影,全面评估脑血管代偿情况)。2D造影参数设置:颈内动脉对比剂流率6 mL/s,总量9 mL,注射延迟0.5 s,压力上限300PSI,采集帧数双C为4 fps,单C为7.5 fps;颈外动脉对比剂流率3 mL/s,总量5 mL,注射延迟0.5 s,压力上限300PSI,采集帧数为4 fps;椎动脉对比剂流率4 mL/s,总量7 mL,注射延迟0.5 s,压力上限300PSI,采集帧数双C为4 fps,单C为7.5 fps。3D血管成像参数设置:进入3D模式,选择FOV 20 cm×20 cm(放大一档),以海绵窦为中心正、侧位校对后,持续按压操作面板set按钮,进行3D曝光前的自检,直到显示屏左下角出现Ready后松开按钮开始曝光。对比剂注射流率5 mL/s,总量25 mL,曝光延迟1.5 s,压力上限300 PSI。C型臂以40°每秒的转速,旋转5 s完成曝光采集。
3.3D血管成像后处理
3D血管成像完成后将原始数据自动传输到ADW4.5工作站,工作站自动生成3D图像,图像后处理采用容积再现(volume rendering,VR)、多平面重组(multi-planar reformation,MPR)技术,在VR Preset选择预设窗宽、窗位或在Advanced VR Settings里手动调节窗宽、窗位。此时的3D VR图像,无法判断瘘口的位置和大小,进一步利用MPR技术寻找瘘口。工作站分6个小窗口(3D、3D VR、轴位、矢状位、冠状位、斜位),首先把光标定位在3D VR图像正侧位海绵窦的中心位置,然后把3D图像调成标准侧位,采用多窗口光标联动技术,在斜位窗口放大图像,选择合适的窗宽、窗位及层厚,通过鼠标和滚轴在断层图像上逐层寻找瘘口,发现瘘口后测量瘘口的大小,判断其在颈内动脉上具体的位置,并分析瘘口与海绵窦的关系。
4.治疗方法
通过对瘘口的分析后选择不同的血管内介入治疗方式(单纯球囊封堵、弹簧圈加Onxy胶栓塞、血流导向装置、覆膜支架、闭塞颈内动脉等),以达到最佳的治疗效果。

图2 患者,女,52岁,外伤性CCF。a) CTA示瘘口显示不清; b) DSA侧位造影提示瘘口显示不清,对比剂主要经岩下窦、部分经眼上静脉引流; c) 3D VR图显示海绵窦包绕颈内动脉,不能显示瘘口位置与颈内动脉关系; d) MPR显示瘘口较大,可选择球囊辅助弹簧圈加Onyx胶栓塞; e) 栓塞术后侧位DSA显示瘘口未再显影,颈内动脉通畅。
结 果
67例CCF患者均能清晰显示瘘口的大小及位置。3例属于小瘘口,即微导管不能通过颈内动脉进入瘘口,最终经静脉途径弹簧圈加Onyx胶栓塞;45例属于较小瘘口(图1),即微导管能够通过颈内动脉进入瘘口,最终行单纯球囊封堵瘘口(其中3例在术后1周内复发,再次行弹簧圈加Onyx胶栓塞);18例属于较大瘘口(图2),即微导管通过颈内动脉进入瘘口,球囊不能封堵瘘口,最终采用经动脉途径弹簧圈加Onyx胶栓塞;1例属于大瘘口,即球囊和弹簧圈加胶都不能封堵住瘘口,最终选择闭塞患侧颈内动脉。所有患者术后即刻造影均可见瘘口完全消失,66例颈内动脉通畅。所有患者均接受临床随访,随访时间为3个月~6年,均无复发。
讨 论
海绵窦部位解剖复杂,颈内动脉呈“S”形走行其中,是人体中唯一的、动脉穿过静脉的结构[2]。颈内动脉海绵窦段及其分支破裂均可引起动静脉瘘,进而导致海绵窦及临近静脉结构压力增高,临床主要表现为以下症状:头痛、颅内杂音、搏动性突眼、球结膜充血水肿、眼球运动障碍、视力减退甚至失明、脑缺血发作等[3,4],严重者可出现鼻腔大出血而危及生命[5]。
CTA和MRA对于CCF的早期筛查和诊断有一定价值,在显示血管的同时亦可显示复杂海绵窦区骨性结构,但MRA对于小瘘口容易漏诊;而DSA二维及三维重建后处理技术可提供影像细节,如结合DSA观察血流的动态变化。
CCF的治疗经历了早期的颈内动脉结扎术,外科开颅颈动脉瘘口修补术等方法,但缺点较多,效果差。随着介入神经外科的飞速发展,血管内栓塞手术闭塞瘘口成为治疗CCF的理想方法[6],文献报道90%的CCF瘘口可经可解脱球囊闭塞,但也存在球囊移位、脱落等诸多风险[7]。Wang等[8]采用栓塞海绵窦来达到闭塞CCF瘘口的目的,效果较好。对于复杂的CCF,覆膜支架的应用为闭塞瘘口提供了新思路[9]。
然而,所有技术的选择及治疗策略的确定,需要术前详细了解CCF瘘口、引流静脉及海绵窦解剖等信息。普通VR技术对瘘口位置的判断较差,且无法较好的显示血管与周围颅骨、脑组织的位置关系,而这些信息在瘘口栓塞过程中至关重要。MPR技术可多角度观察感兴趣区,多层面显示CCF瘘口位置及大小,从而便于微导管顺利到位,缩短手术时间,降低患者和手术医生受到的辐射剂量,提高栓塞治疗的成功率。本组CCF病例采用DSA三维MPR技术后,均可多角度、多方位的显示瘘口,为后续治疗方案的选择提供了重要的参考信息。
由于CCF瘘口的存在,颈内动脉造影后,对比剂被快速的抽吸进海绵窦,导致图像重叠,难以观察到瘘口的具体位置和大小,因此常规正、侧位造影对CCF瘘口的判断较为困难。压迫患侧颈内动脉分别行对侧颈内动脉正位及椎动脉侧位造影,使对比剂由前交通动脉及后交通动脉进入患侧颈内动脉逆行进入瘘口,有助于瘘口位置的判断[10],但瘘口大小及治疗工作角度的选择仍无法确定。3D VR图像因海绵窦包绕颈内动脉导致瘘口显示不清,而MPR技术对CCF瘘口的显示非常清晰。本研究中,笔者采用MPR技术,通过定位瘘口处的颈内动脉为中心,在斜位上选择合适的窗宽、窗位,使图像只显示血管断层,选择最小层厚0.2 mm,在不同的角度对颈内动脉断面进行360°旋转,找到海绵窦与颈内动脉相连的断面,显示瘘口后测量瘘口的宽度和瘘口相连海绵窦的大小,同时,适当的增加层厚可显示海绵窦的引流静脉。
通过三维重建MPR技术,找到显示瘘口的最佳层面,结合2D造影图像对瘘口与海绵窦的引流方向(常见眼上静脉、岩下窦、岩上窦、皮层静脉引流),瘘口的大小、位置的研究,可为下一步介入治疗方案的选择提供参考。如瘘口很小,微导管不能通过颈内动脉进入瘘口,可通过术前对海绵窦引流方向的判断,选择微导管从静脉(常见眼上静脉或岩下窦)途径进入与瘘口相连的海绵窦进行弹簧圈加胶栓塞从而闭塞瘘口。如瘘口较小,微导管通过颈内动脉进入瘘口,可选择可解脱球囊闭塞瘘口。如瘘口较大,可解脱球囊不能封堵住瘘口,可选择动脉途径球囊辅助弹簧圈加胶栓塞海绵窦闭塞瘘口。如瘘口很大,可解脱球囊和弹簧圈加胶栓塞都不能封堵住瘘口,且瘘口处的血管不是特别弯曲时,可考虑使用覆膜支架覆盖瘘口;而对于血管特别弯曲处的大瘘口,不适合使用覆膜支架,可先评估脑血管代偿情况,再选择是否闭塞患侧颈内动脉。
综上所述,DSA三维重建后处理技术可以在行常规DSA的同时,清晰显示CCF瘘口的具体位置、大小以及静脉的引流方向,为血管内介入治疗方案的选择提供参考,对治疗CCF具有很好的临床应用价值。
[1] YU JS,Lei T,Chen JC,et al.Diagnosis and endovascular treatment of spontaneous direct carotid-cavernous fistula[J].Chin Med J (Engl),2008,121(16):1558-1562.
[2] Ringer AJ,Salud L,Tomsick TA.Carotid cavernous fistulas:anatomy,classification,and treatment[J].Neurosurg Clin N Am,2005,16(2):279-295.
[3] Spektor S,Pointer I,Umansky F.Orbital venous draionage into the anterior cavernous sinus space:microanatomic relationships[J].Neurosurgery,1997,40(3):532-539.
[4] Théaudin M,Saint-Maurice JP,Chapot R,et al.Diagnosis and treatment of dural carotid-cavernous fistulas:a consecutive series of 27 patients[J].J Neurol Neurosurg Psychiatry,2007,78(2):174-179.
[5] 吴中学,王忠诚,李佑祥.520例外伤性颈动脉海绵窦瘘的血管内栓塞治疗[J].中华神经外科杂志,1999,15(3):135.
[6] Annesley-Williams DJ,Goddard AJ,Brennan RP,et al.Endovascular approach to treatment ofindirect carotico-cavernous fistulae[J].Br J Neurosurg,2001,15(3):228-233.
[7] Luo CB,Teng MM,Chang FC,et al.Transarterial balloon-assisted nbutly-2-cyanoacrylate embolization of direct carotid cavernous fistulas[J].AJNR,2006,27(7):1535-1540.
[8] Wang W,Li MH,Li YD,et al.Endovascular treatment of post-traumatic direct carotid-cavernous fistulas:A single-centerexperience[J].J Clin Neurosci,2011,18(1):24-28.
[9] Li MH,Li YD,Tan HQ,et al.Treatment of distal internalcarotid artery aneurysm with the Willis covered stent:aprospective pilot study[J].Radiology,2009,253(2):470-477.
[10] 于加省,胡道予,李振强,等.动脉瘤性颈内动脉海绵窦瘘的临床与影像学表现[J].放射学实践,2011,26(10):1085-1088.
