酮咯酸氨丁三醇复合右美托咪定对瑞芬太尼致妇科腹腔镜患者术后痛觉过敏的影响
2018-03-06唐志清陈治军
石 泉, 李 敏, 唐志清, 谭 洪, 陈治军
瑞芬太尼为超短效阿片类镇痛药物,被广泛应用于临床麻醉,具有起效快、连续注射无蓄积等优点,但易诱发痛觉过敏[1]。痛觉过敏不仅大大降低阿片类药物镇痛效果,还易引起全麻苏醒期躁动,影响临床预后[2]。因此,如何减轻瑞芬太尼所诱发的术后痛觉过敏是临床麻醉工作者共同面临的一大挑战。研究表明,单独应用酮咯酸氨丁三醇或右美托咪定均可有效减轻瑞芬太尼所诱发的术后痛觉过敏[3-4]。值得注意的是,单独应用酮咯酸氨丁三醇可引起胃肠道出血等不良反应,单独应用右美托咪定则易引起血流动力学波动,导致低血压及心动过缓。酮咯酸氨丁三醇和右美托咪定抑制痛觉过敏的机制并不相同,二者复合抑制痛觉过敏的有效性及安全性尚未可知。本研究旨在探讨酮咯酸氨丁三醇复合右美托咪定对瑞芬太尼诱发术后痛觉过敏的效果,以期为临床提供依据。
1 对象与方法
1.1对象 选取2016年7月—2017年5月笔者医院收治的择期全麻下行妇科腹腔镜手术患者共120例为研究对象,年龄(44.1±12.4)岁(18~60岁),ASA分级Ⅰ~Ⅱ级。排除麻醉药过敏史、长期应用阿片类药物史、药物成瘾及酗酒、肝肾功能不全、胃肠道疾病、严重血液系统疾病史及术前48 h使用阿片类药物等。按随机数字表法将入组患者分为4组,即对照组(C组),酮咯酸氨丁三醇组(K组)、右美托咪定组(D组)及酮咯酸氨丁三醇联合右美托咪定组(K+D组),每组30例。
1.2方法 术前禁食12 h,麻醉前30 min肌内注射(肌注)阿托品0.5 mg。入室后面罩吸氧,O2流量为6 L/min,监测无创血压(non invasive blood pressure,NBP)、心率(heart rate,HR)、心电图(electrocardiograph,ECG)和血氧饱和度(oxyhemoglobin saturation,SpO2)。麻醉诱导前,K组静脉推注酮咯酸氨丁三醇(批号:035160602,山东新时代药业有限公司)30 mg;D组于静注右美托咪定(批号:16032032,江苏恒瑞药业有限公司)1.0 μg/kg;K+D组于静注右美托咪定0.5 μg/kg,静注酮咯酸氨丁三醇15 mg。麻醉诱导:依次静注咪达唑仑(江苏恒瑞药业有限公司;批号:20160618)0.05 mg/kg、舒芬太尼(批号:1160302,宜昌人福药业有限责任公司)0.6 μg/kg、异丙酚(批号:1607152,四川国瑞药业有限公司)2.0 mg/kg及罗库溴铵(批号:160418,浙江仙琚药业股份有限公司)0.7 mg/kg,气管插管后行机械通气,维持呼气来二氧化碳分压(end expiratory carbon dioxie partial pressure, PETCO2)35~40 mmHg(1 mmHg=0.133 kPa)。麻醉维持:静注瑞芬太尼0.2~0.3 μg·kg-1·min-1、异丙酚4~6 mg·kg-1·h-1。术中持续监测麻醉深度,维持BIS值至40~60。间断静注罗库溴铵0.1~0.3 mg/kg维持肌松。术中发生低血压[(平均动脉压(mean arterial blood pressurs, MAP)<60 mmHg]时静注去氧肾上腺素10 μg,心动过缓(HR<45次/min)时静注阿托品0.5 mg。术毕停止输注异丙酚和瑞芬太尼,静注阿托品0.01 mg/kg、新斯的明0.02 mg/kg;待自主呼吸恢复、且潮气量>8 mL/kg,满足气管拔管指征后,拔除气管导管。生命体征平稳后,送至PACU留观至少1 h。PACU期间,若视觉模拟评分(visual analogue scale,VAS)≥4分,则给予静注舒芬太尼0.04 μg /kg,每间隔3 min评估1次。出PACU后行PCIA:生理盐水稀释舒芬太尼至100 mL,浓度为1 μg/mL,背景输注速率2 mL/h,PCA剂量0.5 mL,锁定时间15 min,维持VAS评分<4分。
1.3观察指标 (1)一般情况及手术相关指标:收集患者一般情况及手术相关指标,包括年龄、身高、体质量、ASA分级、手术时间、瑞芬太尼输注时间及拔除气管导管时间;(2)舒芬太尼用量:记录各组患者术后30 min,60 min,6 h,12 h,24 h时舒芬太尼用量,舒芬太尼用量=PACU期间用量+出PACU后背景输注量+出PACU后按压量,出PACU后按压泵次数由患者及其家属记录;(3)不良反应:恶心呕吐、低血压、心动过缓、嗜睡、胃肠道出血。

2 结 果
2.1一般情况及手术相关指标 各组患者的年龄、身高、体质量、ASA分级、手术时间、瑞芬太尼输注时间及拔除气管导管时间比较,差别无统计学意义(P>0.05,表1)。
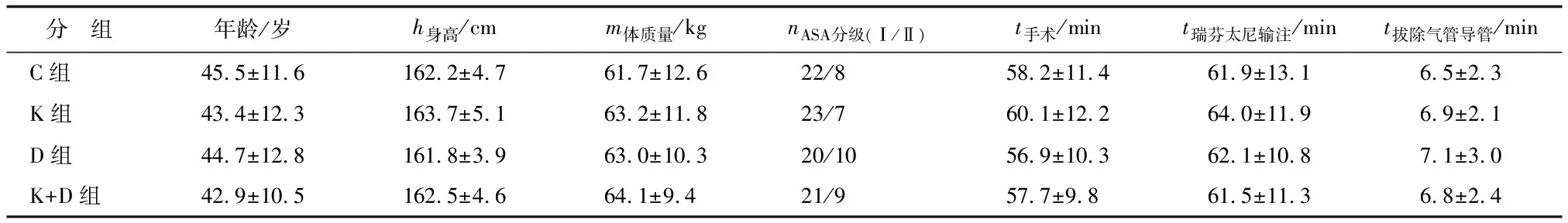
表1 各组患者一般情况及手术相关指标比较
C组:对照组; K组:酮咯酸氨丁三醇组; D组:右美托咪定组; K+D组:酮咯酸氨丁三醇联合右美托咪定组.
2.2舒芬太尼用量 在不同时间点,各组舒芬太尼用量比较,差别具有统计学意义(P<0.05)。与C组比较,K,D组及K+D组术后各时点舒芬太尼用量均显著降低(P<0.05);K,D组及K+D组术后各时点舒芬太尼用量比较无统计学意义(P>0.05)(表2)。

表 2 各组患者术后不同时点舒芬太尼用量比较
C组:对照组; K组:酮咯酸氨丁三醇组; D组:右美托咪定组; K+D组:酮咯酸氨丁三醇联合右美托咪定组. 与C组比较,△:P<0.05.
2.3不良反应 不同分组患者的恶心呕吐、低血压、心动过缓发生率比较,差别具有统计学意义(P<0.05)。与C组比较,K,D组及K+D组恶心呕吐率显著降低(P<0.05),D组低血压、心动过缓率显著增高(P<0.05),K组胃肠道出血率显著显著增高(P<0.05);相较于K组,K+D组胃肠道出血率显著降低(P<0.05);与D组比较,K+D组低血压、心动过缓率显著降低(P<0.05);各组嗜睡率、胃肠道出血率比较,差别无统计学意义(P>0.05,表3)。

表3 各组患者不良反应发生率比较
C组:对照组; K组:酮咯酸氨丁三醇组; D组:右美托咪定组; K+D组:酮咯酸氨丁三醇联合右美托咪定组. 与C组比较,△:P<0.05.
3 讨 论
瑞芬太尼所诱发的痛觉过敏是指其引起的中枢性敏感化,主要表现为疼痛敏感性增高、疼痛阈值降低[5-6]。本研究结合临床经验,选择瑞芬太尼剂量0.2~0.3 μg·kg-1·min-1进行麻醉,结果显示C组患者术后需要较大剂量舒芬太尼方可达到满意镇痛效果,提示瑞芬太尼诱发了术后过敏,与张麟临等研究结论一致[7]。
酮咯酸氨丁三醇属于非甾体类抗炎药物,可降低环氧化酶-1(cyclooxygenase-1,COX-1)和COX-2表达,抑制前列腺素合成,从而降低传入神经末梢对疼痛递质刺激的敏感性;此外,酮咯酸氨丁三醇还可干扰脊髓N-甲基-D-天门冬氨酸(N-Methyl-D-aspartic acid or N-Methyl-D-aspartate,NMDA)受体激活后诱发的伤害性反应,抑制脊髓伤害感受性信息传递,从而发挥中枢镇痛作用[8-9]。本研究选择麻醉诱导前静注酮咯酸氨丁三醇30 mg以抑制瑞芬太尼诱导的痛觉过敏,结果发现,K组术后舒芬太尼用量较C组显著降低(P<0.05),提示采用酮咯酸氨丁三醇30 mg预防瑞芬太尼诱导术后痛觉过敏是有效的。通过比较各组不良反应情况发现,K组胃肠道出血率高于C组、D组及K+D组(P<0.05)。由于酮咯酸氨丁三醇为非选择性COX抑制剂,易引起胃肠出血、溃疡甚至穿孔等不良反应,用药量超过90 mg时尤为明显。
右美托咪定为高选择性α2肾上腺素能受体激动剂,可通过刺激交感神经末梢突触前α2肾上腺素能受体,调控ATP和肾上腺素释放,从而产生镇静、镇痛效应。研究发现,右美托咪定缓解瑞芬太尼诱发的痛觉过敏机制可能与其抑制NMDA受体介导的突触后电位及抑制脊髓背角NMDA受体亚基磷酸化水平有关[10-13]。本研究选择麻醉诱导前静注右美托咪定1.0 μg/kg可降低D组患者术后舒芬太尼用量,与C组比较差别显著(P<0.05),与田立东等研究结果一致[14],提示使用该剂量右美托咪定可有效预防瑞芬太尼诱导术后痛觉过敏;且D组患者术后舒芬太尼用量与K组比较,差别无统计学意义(P>0.05),提示酮咯酸氨丁三醇与右美托咪定对瑞芬太尼所诱导的痛觉过敏具有相似的抑制作用。但值得注意的是,使用该剂量右美托咪定可引起较高的低血压及心动过缓发生率。
酮咯酸氨丁三醇与右美托咪定所引起的上述不良反应主要与其使用剂量有关。故本研究在复合应用时,选择较低的药物剂量,酮咯酸氨丁三醇剂量降至15 mg,右美托咪定剂量降至0.5 μg/kg。在此复合剂量下,K+D组术后舒芬太尼用量与K,D组比较无统计学差别(P>0.05),提示二者复合用药可获得与单纯用药相似的抗瑞芬太尼诱发痛觉过敏作用。此外,K+D组低血压、心动过缓发生率较D组显著降低(P<0.05),胃肠道出血发生率较K组显著降低(P<0.05),提示二者复合用药可减轻不良反应。
综上所述,酮咯酸氨丁三醇与右美托咪定复合使用时,其降低术后痛觉过敏的作用并不优于两者单独使用,但可减少右美托咪定单独使用时的并发症。但本研究未能对酮咯酸氨丁三醇、右美托咪定不同剂量复合应用的效果进行对比研究,二者复合应用的适宜剂量仍需进一步探讨。
