超声降解落叶松中阿拉伯半乳聚糖及其活性的研究
2018-03-06郭怡帆林圣翔刘焕燕贺亮
郭怡帆 ,林圣翔,刘焕燕,贺亮*
(1.浙江省萧山中学,杭州 311201;2.CATS Academy Boston,Massachusetts 02184;3.浙江省森林资源生物与化学利用重点实验室,浙江省林业科学研究院森林食品所,杭州 310023)
各种降解方法中,物理法降解最为简单、绿化、无污染。超声降解作为一种物理降解法已在环境、化工、食品等领域得到高度关注[8]。本文以落叶松林木采伐加工后的剩余木屑为原料提取出阿拉伯半乳聚糖并进行超声降解,通过测定降解后多糖的·OH清除率变化来探究超声功率、降解温度、降解时间、料液比对多糖降解过程的影响,并确定最适宜降解条件,进而比较多糖降解前后体外抗氧化效果,为后续阿拉伯半乳聚糖的开发研究奠定了基础。
1 材料与方法
1.1 材料与仪器
落叶松林木采伐加工后的剩余木屑,来自中国大兴安岭;500Da透析袋。
30%H2O2、FeSO4、水杨酸、DPPH、乙醇,购自国药集团化学试剂有限公司,均为分析纯。
旋转蒸发器RE-52AA,上海亚荣生化仪器厂;BS224S电子天平,北京塞多利斯仪器系统有限公司;UV-9100紫外可见分光光度计,北京瑞利分析仪器公司;台式高速冷冻离心机,美国Thermo公司;真空冷冻干燥机,美国LABCONCO公司;超声波细胞破碎仪,昆山市超声仪有限公司。
1.2 方法
1.2.1 阿拉伯半乳聚糖(AG)的提取
称取20g松针木屑,以料液比1∶200、提取温度70℃、浸提取时间1h,提2次。将粗提液抽滤,合并两次滤液并浓缩,以1∶4(V/V)的比例加入95%的乙醇,在4℃的环境下静置20h,离心,取出沉淀冻干,得松针粗糖。
1.2.2 阿拉伯半乳聚糖降解的单因素试验
通过单因素试验考察超声功率、降解温度、降解时间、料液比对松针多糖清除·OH能力的影响。降解反应后,离心除去沉淀,取上清液;考察其抗氧化活性,初步确定适宜多糖降解的相应水平范围。
1.2.2.1 超声功率对抗氧化活性的影响。称取0.5g松针多糖,放入圆底烧瓶中,溶于100mL蒸馏水中,在温度为60℃的条件下,分别以50W、100W、150W、200W、250W超声降解1h。
1.2.2.2 降解温度对抗氧化活性的影响。称取0.5g松针多糖,放入圆底烧瓶中,溶于100mL蒸馏水中,在超声功率为150W的条件下,分别以温度40℃、50℃、60℃、70℃、80℃、90℃超声降解1h。
1.2.2.3 降解时间对抗氧化活性的影响。称取0.5g松针多糖,放入圆底烧瓶中,溶于100mL蒸馏水中,在超声功率150W、温度70℃的条件下,分别降解0.5h、1h、1.5h、2h、2.5h。
1.2.2.4 料液比对抗氧化活性的影响。按照料液比1∶100、1∶150、1∶200、1∶250、1∶300称取0.5g松针多糖,放入圆底烧瓶中,在超声功率为150W、温度70℃的条件下降解2h。
1.2.3 阿拉伯半乳聚糖降解的正交试验
根据单因素试验结果,建立正交试验L9(34)的因素水平表(表1)进行正交试验,以降解松针多糖对自由基的清除能力为检测指标,确定最佳降解工艺参数,计算最佳得率,其计算公式如下:

多糖得率
1.2.4 降解阿拉伯半乳聚糖对·OH清除率的测定
试剂配置:8.8mmol/L的H2O2溶液100mL ;9.0mmol/L的FeSO4溶液50mL;9.0mmol/L的水杨酸乙醇液50mL,0.5g/mL降解前后阿拉伯半乳聚糖溶液各100mL。
对于高分子溶液,在一定的超滤压力下,随着凝胶层厚度的增加,超滤通量会不断减少。如图5所示,本实验的超滤通量-超滤时间的关系基本符合这一规律。在超滤运行的初期,因为膜表面无其他物质,阻力较小,因此超滤通量维持较稳定状态;随着超滤的不断进行,在膜表面迅速吸附有机胶体等物质,超滤通量下降较快[21,22]。综合考虑超滤通量及压力,试验选择两条曲线交点的时间,即超滤时间60 min。
试验步骤:分别取降解前后阿拉伯半乳聚糖样品液1mL,FeSO4溶液1.0mL,水杨酸乙醇液1.0mL,H2O2溶液1.0mL混合均匀,37℃水浴30min,510nm处测定吸光值。
·OH清除率计算公式如下:
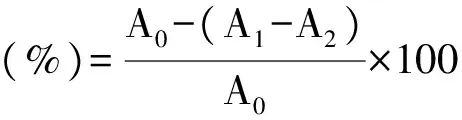
1.2.5 降解阿拉伯半乳聚糖对DPPH自由基清除率的测定
试剂配置:0.075mmol/L的DPPH乙醇液100mL,0.5g/mL的降解前后阿拉伯半乳聚糖溶液各100mL;
试验步骤:分别取降解前后阿拉伯半乳聚糖溶液各0.5mL;添加DPPH乙醇液3mL,混 合均匀,置于黑暗处放置30min,517nm处测定吸光值。
DPPH自由基清除率计算公式如下:
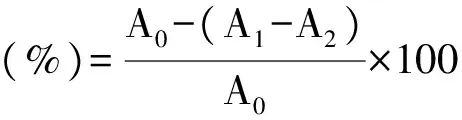
2 结果与分析
2.1 降解阿拉伯半乳聚糖工艺的优化
2.1.1 单因素试验
2.1.1.1 降解温度对阿拉伯半乳聚糖·OH清除率的影响。
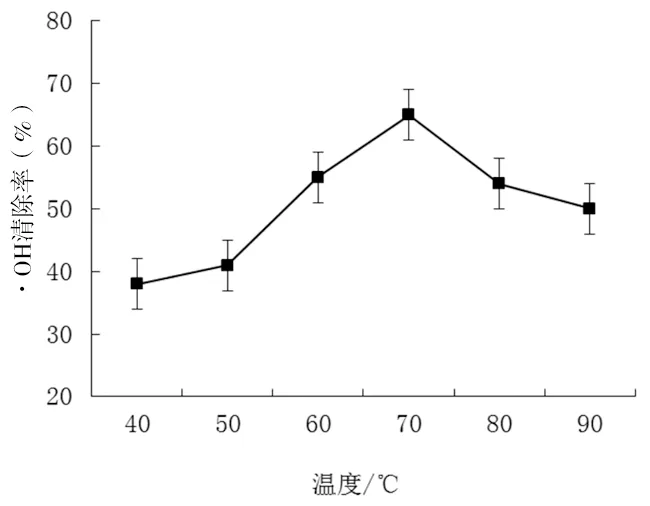
图1 (a)不同降解温度对阿拉伯半乳聚糖·OH清除率的影响
由图1(a)可以看出:随着温度的升高,降解阿拉伯半乳聚糖对·OH清除率呈先升高后降低的趋势。当温度为70℃时,清除率最高为65.05%;当温度高于70℃时,清除率开始下降。虽然温度能提高化学反应的速度,但当降解温度过高时,具有活性的多糖片段减少,降解效果降低,故其最适宜温度为70℃[4]。
2.1.1.2 降解时间对阿拉伯半乳聚糖·OH清除率的影响。
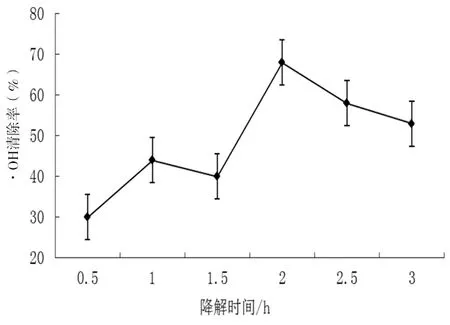
图1 (b)不同降解时间对阿拉伯半乳聚糖·OH清除率的影响
由图1(b)可以看出:随着降解时间的延长,对·OH清除率呈先升高后降低的趋势;当时间达到2h时,清除率达到最大值为62.12%,之后开始下降,为此最适宜降解时间为2h。
2.1.1.3 料液比对阿拉伯半乳聚糖·OH清除率的影响。
由图1(c)可以看出:随着料液比增加,对·OH清除率呈先升高后降低的趋势;当料液比为1∶250时,清除率最高。提取液用量比较少时,由于多糖高分子之间相互作用形成胶团,影响多糖降解效果;提取液用量过多时,多糖降解程度增大,部分多糖被降解为小分子质量的多糖、寡糖等,由于透析时损失,保留下的活性多糖含量低,综合考虑选用1∶250为最佳料液比[4]。
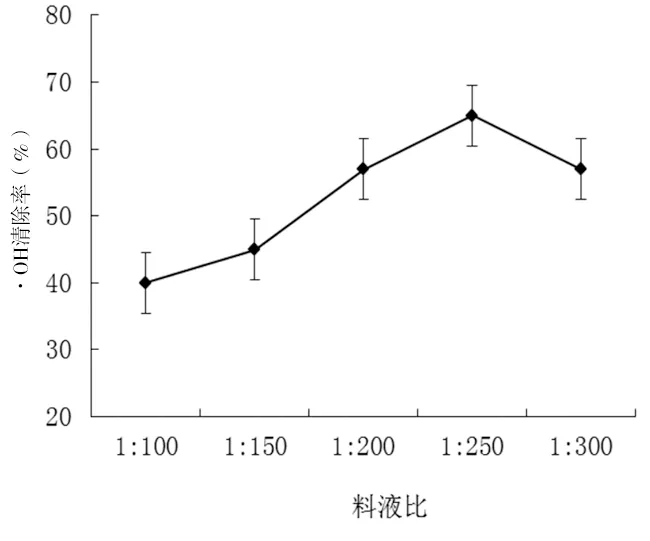
图1 (c)不同料液比对阿拉伯半乳聚糖·OH清除率的影响
2.1.1.4 超声功率对阿拉伯半乳聚糖·OH清除率的影响
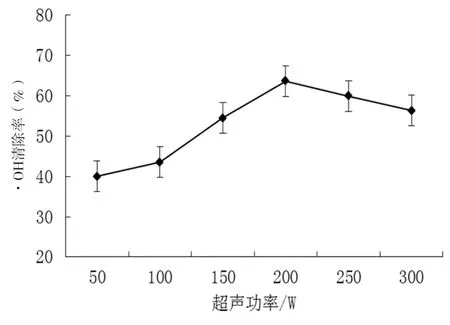
图1 (d)不同超声功率对阿拉伯半乳聚糖·OH清除率的影响
由图1(d)可以看出:随着超声功率增大,对·OH清除率呈先升高后降低的趋势;当超声功率达到150W时,对·OH清除率达到最高值为60.07%,而后缓慢降低。其原因可能是超声功率的增加能强化空化效应,从而增加了断裂生物大分子化学键的能量,引起降解作用加强[3]。而超声功率超过150W时,随着超声功率的继续增大,超声的巨大能量可能会破坏多糖的活性部位,或者将有抗氧化活性的多糖键打断变成较小分子而使得活性降低,从而引起降解作用的减弱[21]。
2.1.2 正交试验
由于提取效果受到降解温度、降解时间、降解功率、料液比四个因素的影响,为确定更适宜的提取条件,采用4因素3水平正交试验L9(34)对超声降解落叶松中阿拉伯半乳聚糖的工艺条件进行优化,具体结果见表2。
根据极差R的大小,进行因素的主次排列:极差越大,说明该因子水平变动时,实验结果的变动越大,即该因子对实验结果的影响越大。因此,在本实验中,这个因素就越重要;反之,R越小,这个因素就越不重要。由表2 可知,本实验各因素对降解效果的影响主次顺序为:B>D>C>A,即降解温度>料液比>降解时间>降解功率。
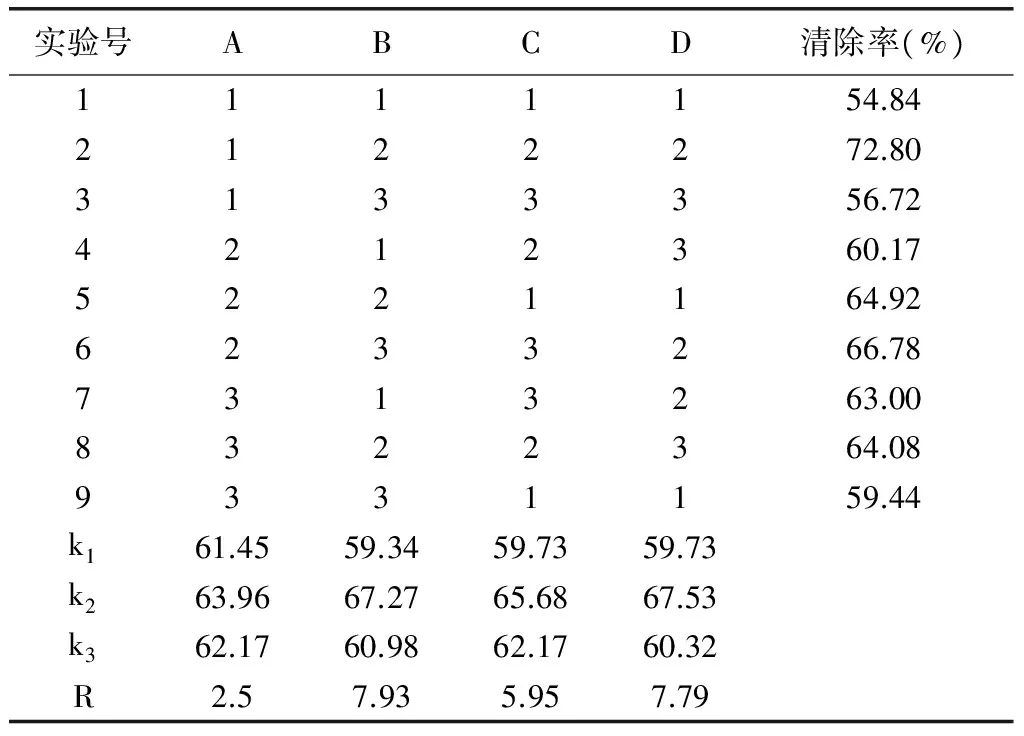
表2 L9(34)正交试验设计分析结果表
K1、K2、K3反映了试验因子各水平对实验结果的影响,因而最大的K值对应于最好的水平,通过表2正交试验结果分析,可以看出本实验最适宜的降解条件为B2D2C2A2,即料液比1∶250、降解温度70℃、降解时间2.0h、降解功率150W。
2.2 降解前后阿拉伯半乳聚糖抗氧化活性的比较
2.2.1 清除羟自由基
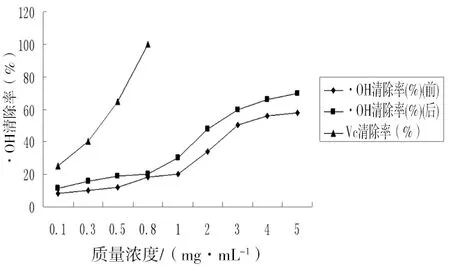
图2 不同质量浓度的阿拉伯半乳聚糖降解前后对·OH清除效果比较
羟自由基的化学性质极为活泼,也是毒性最大的自由基,可以与多种有机物或无机物反应[5]。由图2可知,超声法降解前后阿拉伯半乳聚糖对·OH都有一定清除作用,降解后清除·OH能力明显增强,而且均呈随质量浓度提高而增强的趋势,且增速先慢后快。通过与VC进行比较,当VC浓度达到0.8mg/mL时,清除率达到100%;而超声法降解前后清除率均低于VC清除率,当质量浓度达到5mg/mL时,超声法降解后多糖对·OH清除率达到70.32%。
2.2.2 清除DPPH
DPPH是一种稳定的有机自由基,通过检测抗氧化剂对DPPH的清除能力,可以表示其抗氧化性的强弱[6]。由图3可知,超声法降解前后对DPPH都有一定清除作用,降解后阿拉伯半乳聚糖清除DPPH能力明显增强,而且均呈随质量浓度提高而增强的趋势,增速先慢后快。通过与VC进行比较,当VC浓度达到0.8mg/mL时,清除率达到100%;而超声法降解前后清除率均低于VC清除率,当质量浓度达到5mg/mL,超声法降解后多糖对DPPH清除率达到80.16%。
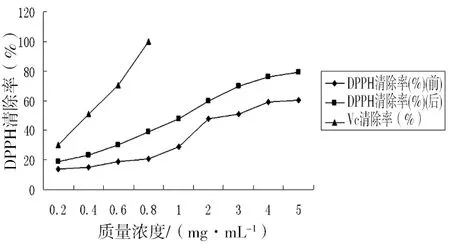
图3 不同质量浓度阿拉伯半乳聚糖降解前后对DPPH清除效果比较
由以上分析可知,在实验质量浓度范围内,降解前后的阿拉伯半乳聚糖都有一定的抗氧化活性。经回归分析可知,抗氧化活性顺序为降解前<降解后,即超声法有利于提高阿拉伯半乳聚糖的抗氧化活性。
3 结论
用物理法中的超声降解法来降解阿拉伯半乳聚糖,以降解松针多糖对自由基清除率为检测指标,通过单因素试验考察超声功率、降解温度、降解时间、料液比对松针多糖体外抗氧化活性的影响,利用正交试验确定最佳降解条件为降解温度70℃、降解时间2.0h、料液比1∶250、超声功率150W。在抗氧化活性方面,降解后的阿拉伯半乳聚糖较未降解前在清除·OH和DPPH上都有一定提高。
本试验对超声降解最佳工艺和抗氧化活性变化做了初步研究,但是其作用机制还有待进一步深入探讨,今后应着重微观机理的研究,探明超声降解多糖生物大分子键断裂机制和自由基反应机理,建立相应的物理数学模型,从根本上解决该技术产业化的科技问题[20]。
[1]Hauer J, Anderer F A. Mechanism of stimulation of human natural killer cytotoxicity by arabinogalactan from Larix occidentalis[J].Cancer Immunology,Immunotherapy,1993,36(4):237-244.
[2]Chandrasekaran R, Janaswamy S. Mophology of Western larch arabinogalactan[J].Carbohydrate Research,2002,337(21-23):2211-2222.
[3]任瑞,马海乐,刘斌,等.超声降解香菇多糖及其体外抗氧化活性的研究[J].安徽农业科学,2008,36(17):7061-7062,7065.
[4]高玉杰,吕海涛. 酸法降解浒苔多糖及其清除羟自由基活性研究[J].食品科学,2013,34(16):62-66.
[5]魏涛,何培新,郑俊丽. 铁棍山药水溶性多糖的超声波提取工艺及体外抗氧化活性的研究[J].河南工业大学学报(自然科学版),2010,31(6):25-28.
[6]阿吉姑·阿布都热西提,买尔旦·马合木提,马合木提·乌斯满,等.维生素C清除自由基能力3种检测方法的比较[J]. 新疆医科大学学报,2008,31(5):578-579,582.
[7]李坚斌,李琳,李冰,等.超声降解多糖研究进展[J].食品工业科技,2006,27(9):181-184.
[8]马艳丽,方桂珍,等.超声波法提取木材中阿拉伯半乳聚糖的工艺参数优化[J].林产化工通讯,2004,38(5):6-7.
[9]方桂珍,马艳丽,徐凤英.等超声波法提取木材中的阿拉伯半乳聚糖的研究[J]. 林产化学与工业,2004,24(4):104-106.
[10]Thompson L H, Doraiswamy L K.Sonochemistry:science and engineering[J] .Industrial & Engineering Chemistry Research,1999,38(4):1215-1249.
[11]方桂珍,黄占华,李淑君.微波法提取木材中阿拉伯半乳聚糖[J].林产化学与工业,2003,23(3):81-84.
[12]冯若,赵逸云,李化茂.超声在生物技术中应用的研究进展[J].生物化学与生物物理进展,1994,21(6):500-503,562.
[13]DORAISWAMYLKTH.Science and engineering industrial &engineering chemistry research[J] .Sonochemistry ,1999,38(4):1215.
[14]苟劲.超声波在化学化工中的应用研究[J] .重庆工学院学报,2002,16(3):76.
[16]GOELLNER E M, UTERMOEHLEN J, KRAMER R, et al.Structure of arabinogalactan from Larix laricina and its reactivitywith antibodies directed against type-Ⅱ-arabinogalactans[J].Carbohydrate Polymers,2011,86(4):1739-1744.
[17]黄桂东,钟先锋.阿拉伯半乳聚糖的研究进展[J].食品与机械,2006,22(4):141-144.
[18]任瑞,马海乐,刘斌,等.超声降解香菇多糖及其体外抗氧化活性的研究[J].安徽农业科学,Journal of Anhui Agri. Sci. 2008,36 (17):7061- 7062,7065.
[19]龚淑俐,邓放明.真菌多糖的生物活性研究进展 [J].食物与营养,2006 (1) :27- 28.
[20]闵婷,孙杰,黄菲,等.超声处理对龙眼果肉多糖理化特征及免疫调节活性的影响[J] .现代食品科技,2016,32 (5):125-125.
[21]王小梅,薛慧君,孙润广,等.超声提取功率对麦冬多糖体外清除羟自由基作用影响的研究[J] .食品工业科技,2011,32(04):73-74.
