掺杂态聚苯胺的乳液聚合及其与环氧树脂所制涂层的耐蚀性
2018-03-01宋航王华钱晨
宋航,王华*,钱晨
(大连理工大学化工学院,辽宁 大连 116023)
金属腐蚀带来的经济损失、安全事故、能源浪费、环境污染等问题阻碍了生产发展和科技进步,在金属表面覆盖一层涂层是防腐蚀最有效的办法之一。自 MacDiarmid等[1]发现聚苯胺(PANI)掺杂可形成优良导体后,国内外的学者开始对其进行深入研究。掺杂态聚苯胺及聚苯胺衍生物作为导电高分子聚合物,能有效降低不锈钢[2-3]、低碳钢[4-5]、铜[6-7]、铝[8-9]等金属的腐蚀速率。Deberry等[10]还发现导电聚苯胺可以促进不锈钢钝化。多种防腐蚀机理促使聚苯胺被广泛地应用在防腐涂料中。聚苯胺的合成有化学法和电化学法[11-12]。化学聚合法中的乳液聚合法具有聚合速率快,产物形貌均一、分子量大等特点,应用广泛。在化学聚合过程中,反应物以及氧化剂的浓度,体系的pH,反应温度及时间都直接影响着合成出来的聚苯胺的形貌及性质。将盐酸、磷酸[13-14]等质子酸作为掺杂剂嵌入聚苯胺骨架中,可使合成的聚苯胺具有良好的导电性。大多数文献用十二烷基苯磺酸(DBSA)做乳化剂合成具有良好结构和稳定性的聚苯胺。而十二烷基苯磺酸钠(SDBS)不仅可以做乳化剂,而且在酸性条件下可以作为共掺杂剂参与合成聚苯胺。正丁醇作为助乳化剂的一种,可以参与乳化剂在油水界面的分子排列,减小乳液的粒径,加强乳化效果[15];同时它还可以作为多元醇类环氧稀释剂,降低环氧体系的黏度,增大其流动性。
本文分别选用盐酸和磷酸做质子酸掺杂剂,以十二烷基苯磺酸钠作乳化剂和共掺杂剂,正丁醇为助乳化剂,采用低温慢速搅拌乳液聚合法制备了具有一定电导率的束状聚苯胺,并加入环氧树脂涂料中,涂覆在Q235低碳钢上。通过电化学阻抗谱和浸泡试验,考察了聚苯胺/环氧树脂复合涂层的耐蚀性。
1 实验
1.1 原料、基材及其预处理
苯胺(ANI,含量>99.8%,经二次减压蒸馏后使用)、过硫酸铵(APS)、十二烷基苯磺酸钠(SDBS)、浓磷酸、浓盐酸,上述试剂均为分析纯,由国药集团化学试剂有限公司提供。凤凰牌环氧树脂 E44,蓝星新材料无锡树脂厂;南亚牌固化剂593,昆山南亚环氧树脂公司。
基材为Q235低碳钢,用500目和800目的金相砂纸反复打磨至表面光亮,再进行除油,依次用丙酮、无水乙醇、去离子水冲洗,再超声洗净,氮气吹干。
1.2 聚苯胺乳液及其粉末的制备
配制质子酸(HCl或H3PO4)水溶液,分成等量两份,称为A、B液。先在A液中加入SDBS,充分搅拌至溶解,再缓慢滴入ANI至形成乳白色乳液,然后滴入2 ~ 5滴正丁醇,泡沫消除后静置。在B液中加入APS,充分搅拌至溶解。质子酸、APS、SDBS与ANI的摩尔比为1∶1∶1∶1,总摩尔浓度1 mol/L。将A、B液预冷至反应温度0 ~ 5 °C,随后在搅拌(150 r/min)下将B液缓慢滴入A液,0.5 h内滴完,反应6 h后保持反应温度静置12 h,使乳浊液静置破乳,得到共掺杂态的PANI溶液。
抽滤PANI溶液,再洗涤过滤物数遍至滤液无色,得到PANI滤饼,在60 °C下真空干燥24 h,最后研磨,即得共掺杂态的PANI粉末。分别用(HCl+DBSA)-PANI和(H3PO4+DBSA)-PANI代表盐酸和磷酸与十二烷基苯磺酸共掺杂的聚苯胺。
1.3 共掺杂态聚苯胺/环氧树脂复合涂层的制备
将环氧树脂与正丁醇按质量比3∶1混合均匀,再加入占体系质量分数1%的共掺杂态PANI粉末,充分搅拌1 h,超声10 min,再按m(环氧树脂)∶m(固化剂)= 3∶1加入固化剂,充分搅拌15 min,超声3 min,静置至气泡消散,得到PANI均匀分散的环氧树脂涂料。
用移液枪移取等量的涂料于碳钢试样上,用软毛刷单面涂覆均匀,膜厚控制在50 μm左右。电化学实验中的涂覆面积为10 mm × 10 mm,化学浸泡试验中的涂覆面积为40 mm × 30 mm,在30 °C下恒温干燥48 h。不加入共掺杂态PANI粉末即得纯环氧(EP)涂层。
1.4 表征与性能测试
1.4.1 聚苯胺的表征
采用德国布鲁克的EQUINOX55型傅里叶变换红外光谱仪(FT-IR),用KBr压片法制样,通过分析比对峰值来判断官能团类型以确定共掺杂态PANI的结构组成。用美国FEI公司的Quanta 450型扫描电镜(SEM)观察PANI的表面形貌,放大5 000倍,进一步确定PANI的微观形貌。用日本岛津的6000型X射线衍射仪(XRD)分析共掺杂态PANI的结晶度,扫描速率为0.02°/s,扫描范围5° ~ 40°。用北京菁美瑞科技公司的RTS-8型数显式四探针测试仪测量PANI片的电导率,压片直径10 mm。
1.4.2 复合涂层的表征
1.4.2.1 厚度与结合力
用TT260覆层测厚仪测得涂层的厚度平均为50 μm。参考GB/T 9286–1998《色漆和清漆 漆膜的划格试验》在涂层上纵横垂直交叉划格,间距1 mm,用胶带测得涂层的附着力为0级。
1.4.2.2 电化学性能
用上海辰华CHI750E型电化学工作站测量复合涂层的电化学阻抗谱(EIS)。采用三电极体系:工作电极为涂层试样,辅助电极为铂电极,参比电极为饱和甘汞电极(SCE)。腐蚀介质为3.5% NaCl溶液,在开路电位下测量,先稳定30 min再测,正弦波扰动电位幅值为5 mV,扫描频率100 000 ~ 0.01 Hz,共浸泡21 d。用ZSimpWin软件拟合数据。
1.4.2.3 耐蚀性
用刀片划透复合涂层,呈“×”形,浸泡在37 °C(水浴加热)的3.5% NaCl溶液中,7 d后观察涂层表面的变化,以判断腐蚀情况。
2 结果与讨论
2.1 红外光谱分析
由图1对照表1可知,3 445 cm-1处为N—H伸缩振动峰,1 127 cm-1和799 cm-1两处分别为苯环上═C—H面内和面外弯曲峰。1 570 cm-1和1 489 cm-1两处分别存在醌式结构和苯式结构中的C═C伸缩振动峰,1 298 cm-1处的峰则对应于C—N伸缩振动。而在1 031、665和578 cm-1处出现较强吸收峰,分别对应于S═O、C—S和S—O的伸缩振动,说明存在磺酸基团—SO3H;2 913 cm-1处有DBSA中烷烃的C—H伸缩振动峰,表明引入了十二烷基苯磺酸大分子。

图1 (HCl+DBSA)-PANI和(H3PO4+DBSA)-PANI的FT-IR谱图Figure 1 FT-IR spectra of (HCl+DBSA)-PANI and (H3PO4+DBSA)-PANI

表1 聚苯胺的部分特征吸收峰及其在红外谱图中的位置Table 1 Some characteristic absorption peaks of polyaniline and their locations in infrared spectrum(单位:cm-1)
2.2 扫描电镜分析
如图2所示,两种掺杂态PANI皆呈束状结构,直径0.5 ~ 1.0 μm,长度10.0 ~ 20.0 μm。这是因为在乳液聚合时,大分子磺酸基团与ANI分子相互作用,使ANI不再是直接聚合成单一的PANI单元,而变为沿着PANI分子链的纵向生长并延长。其中(H3PO4+DBSA)-PANI虽呈束状,但结构疏松凌乱,表面还有未参与纵向生长的PANI颗粒,而(HCl+DBSA)-PANI的束状结构均一、规整,层层叠加可使覆层变得严实致密,添加至涂料中能增大涂层的屏蔽效应。

图2 不同质子酸与十二烷基苯磺酸共掺杂的聚苯胺的SEM照片Figure 2 SEM images of polyaniline co-doped by dodecylbenzenesulfonic acid with different protonic acids
2.3 X射线衍射分析
观察图3可知,两种掺杂态PANI在2θ为20.5°和25.5°处均出现了较宽的衍射峰,说明它们具有一定的结晶度。这是因为在苯胺的聚合过程中,HCl和H3PO4质子化所产生的阳离子与溶液中的阴离子共同作用,使PANI分子链中的部分N原子形成了类似有机“季铵盐”的结构,加强了分子链间作用力,结晶取向增大[16]。另外,大分子酸DBSA的掺杂使更多的阳离子自由基电荷离域至苯环中的胺基(R—N—R)上,DBSA的支链阻断了致密的PANI链结构,使PANI分子链的排列变得规整[17]。

图3 (HCl+DBSA)-PANI和(H3PO4+DBSA)-PANI的XRD谱图Figure 3 XRD patterns of (HCl+DBSA)-PANI and (H3PO4+DBSA)-PANI
2.4 电导率分析
电子型导电高分子的载流子主要是电子,XRD的表征结果证实了HCl、H3PO4与DBSA共掺杂PANI均具有一定的结晶取向,分子紧密、整齐地堆砌排列,分子间键桥为电子提供了有利于传递的通道,电导率随晶体部分的有序排列程度而变化。(HCl+DBSA)-PANI和(H3PO4+DBSA)-PANI的结晶度相差不大,因此它们的电导率较为相近,前者为0.23 S/cm,后者为1.67 S/cm。但(HCl+DBSA)-PANI因分子链间距更大,减弱了分子链间作用力,降低了链间的电荷转移,故其电导率略小[18]。
2.5 电化学阻抗谱分析
2.5.1 不同掺杂酸对聚苯胺/环氧树脂(PANI/EP)复合涂层耐蚀性的影响
从图4可见,(HCl+DBSA)-PANI/EP复合涂层测得的Bode图中低频处模值和Nyquist曲线上半圆弧的直径远大于(H3PO4+DBSA)-PANI/EP复合涂层测得的结果。在等效电路图中,Rs是溶液电阻,Qc是涂层电容,Rc是涂层孔隙电阻,Qp是钝化层电容,Rp是钝化层电阻。由于电极表面存在弥散效应,引入常相位角元件Q来代替理想电容C,以弥补真实电容与理想电容之间的偏差[19]。鉴于膜层的特殊结构,用弥散指数n(取值在0 ~ 1之间)和Q共同表示不稳定电流引起的阻抗变化,n越趋于1越接近理想电容,越趋于0则越接近理想电阻[20]。Rc显示了离子在金属基体与涂层间传导的途径,它的值越大,离子越不容易渗透进涂层。复合涂层在浸泡前期显示了2个时间常数,第一个对应的是涂层电阻,第二个表明有少量离子通过孔隙进入了涂层内部并到达基体,但因为掺杂态PANI使基体表面存在钝化层,所以抑制了腐蚀的发生,Rp越大,抑制效果越强。如表2所示,(HCl+DBSA)-PANI/EP涂层的Rc和Rp均更大。这是因为(HCl+DBSA)-PANI粉末的束状结构更均一,加入环氧涂层后交叉层叠,迷宫效应优于(H3PO4+DBSA)-PANI,可减缓离子渗入的速率,所以屏蔽作用更好。另外,导电的掺杂态PANI具有可逆的氧化还原性,(HCl+DBSA)-PANI分子链间的结合力弱,更容易发生氧化还原反应,反复钝化可使金属表面形成新的钝化膜,从而增强了涂层的自愈合能力,也提高了防腐蚀效果。
综上所述,(HCl+DBSA)-PANI/EP涂层的屏蔽效应和钝化效应均优于(H3PO4+DBSA)-PANI/EP涂层,保护作用更为优异。
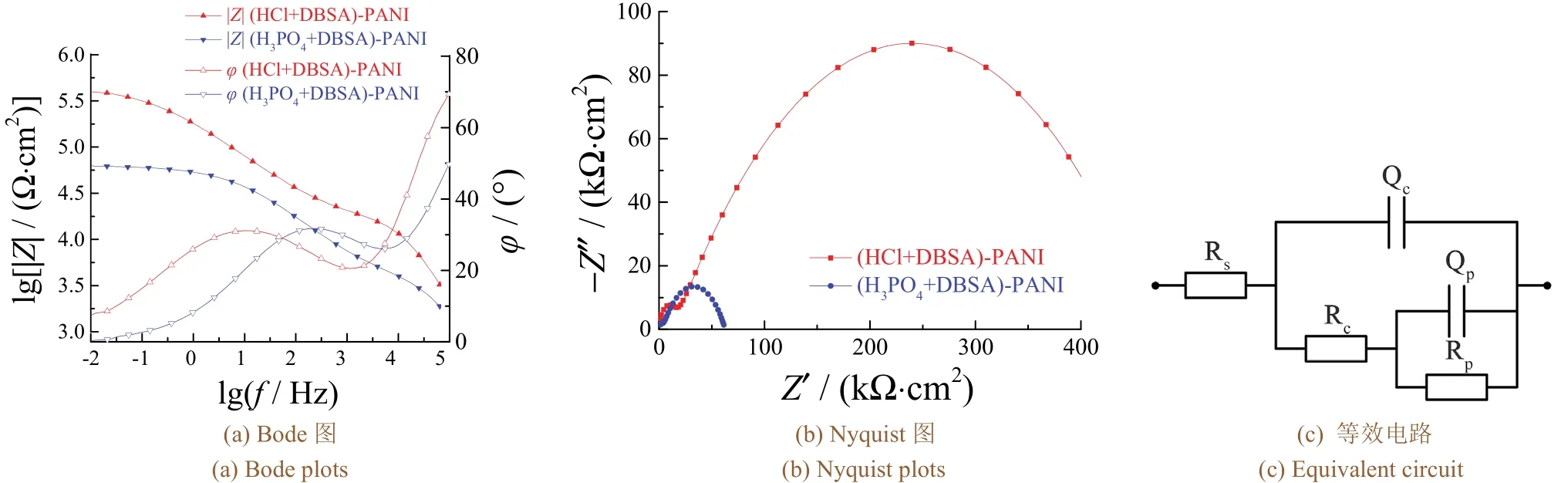
图4 不同掺杂聚苯胺/环氧树脂复合涂层在3.5%氯化钠溶液中的电化学阻抗谱和等效电路Figure 4 Electrochemical impedance spectra and equivalent circuit diagram for different doped PANI/EP composite coatings in 3.5% NaCl solution

表2 图4所示EIS谱图的拟合结果Table 2 Fitted results of the EIS spectra shown in Figure 4
2.5.2 (HCl+DBSA)-PANI/EP复合涂层与纯环氧树脂涂层的耐蚀性对比
选用防腐蚀效果较优的(HCl+DBSA)-PANI/EP涂层与纯 EP涂层进行对比。由图 5可见,(HCl+DBSA)-PANI/EP涂层的初始阻抗半弧比EP涂层大近2个数量级。而从表3可知,随着浸泡时间延长,(HCl+DBSA)-PANI/EP涂层的Rc从15 660 Ω·cm2逐渐减小至3 998 Ω·cm2。在浸泡中后期,其等效电路显示了3个时间常数,EIS低频区时间常数表明钝化层逐渐被破坏,腐蚀离子到达基体表面。Rct是电荷转移电阻,Qdl则是双电层电容,它们的存在表明了腐蚀发生的位置。Rc、Rp和Rct持续下降,说明腐蚀产物在基体表面累积,涂层逐渐失去作用。
纯环氧涂层主要以屏蔽作用为主。仅浸泡3 d,其Rc从6 395 Ω·cm2降至1 694 Ω·cm2,说明屏蔽作用减弱。在浸泡中后期的等效电路上显示了2个时间常数,EIS高频区的时间常数对应涂层电容Qc和涂层电阻Rc,在中低频区的时间常数则对应涂层与基体界面的双电层电容Qdl和电荷转移电阻Rct。到第5天,纯环氧涂层就失去了屏蔽作用,腐蚀离子到达基体表面。
因此,在环氧涂层中添加(HCl+DBSA)-PANI可显著提高其耐蚀性。

图5 不同涂层在3.5%氯化钠溶液中的电化学阻抗谱和等效电路Figure 5 Electrochemical impedance spectra and equivalent circuit diagram for different coatings in 3.5% NaCl solution
2.6 浸泡试验
如图6所示,浸泡实验前,涂层均光滑平整,无腐蚀存在。浸泡7 d后,EP涂层表面的锈蚀更多,且出现鼓泡现象,导致划痕宽度增大约1 mm。去掉涂层后,下方的碳钢基体不仅划伤处发生腐蚀,其他地方的腐蚀也很严重,这是因为 EP涂层有鼓泡,腐蚀介质更易渗入,涂层与碳钢基体之间的结合力下降,加速了碳钢的腐蚀。加入(HCl+DBSA)-PANI后,不管是涂层还是去除涂层后的基材,腐蚀情况明显得到改善。这映证了电化学测量的结果。
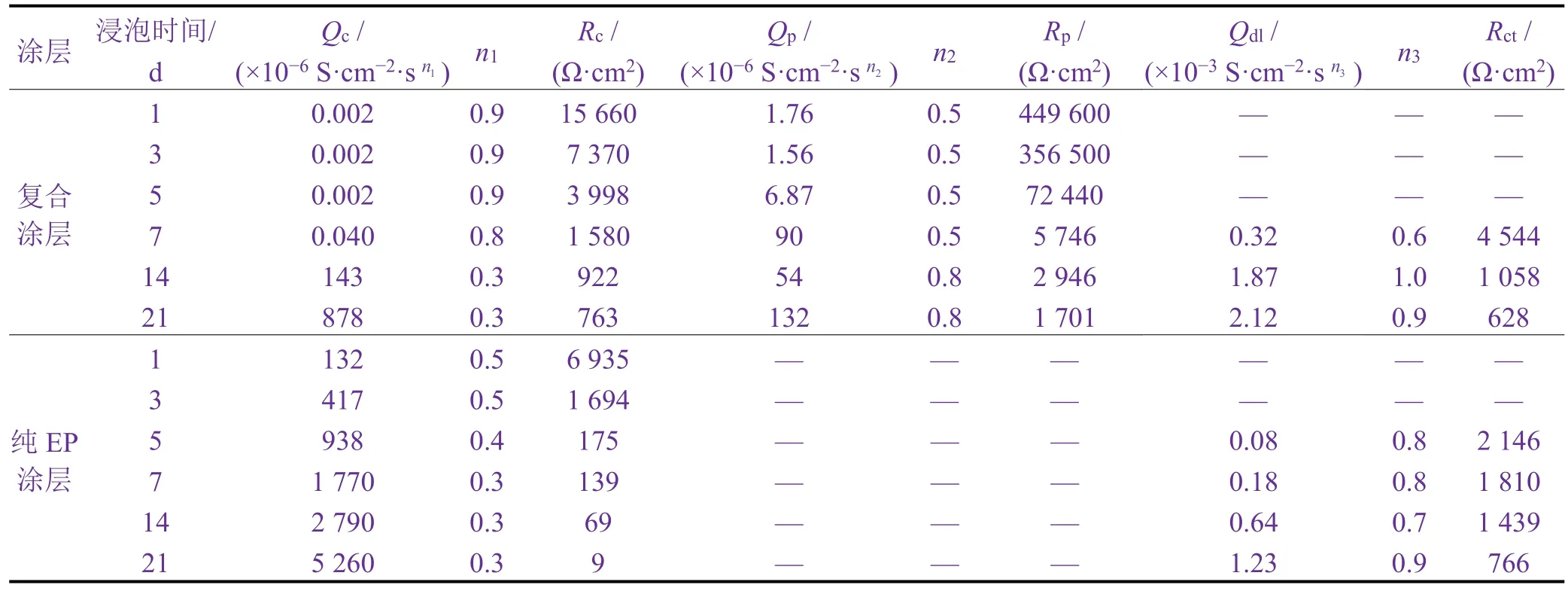
表3 图5所示EIS谱图的拟合结果Table 3 Fitted results of the EIS spectra shown in Figure 5

图6 涂覆不同涂层的碳钢试样在37 °C的3.5%氯化钠溶液中浸泡7 d后的情况Figure 6 Situations of carbon steel samples coated with different coatings after immersion in 3.5% NaCl solution at 37 °C for 7 days
3 结论
(1) 以HCl或H3PO4做质子酸,SDBS做乳化剂和共掺杂剂,用低温慢速搅拌乳液聚合法制得了共掺杂态的PANI,并在PANI链中引入了十二烷基苯磺酸大分子,呈现出大小均一的束状结构,具有一定的结晶度和电导率。
(2) 将共掺杂的PANI添加至环氧树脂涂料中,涂覆于Q235低碳钢表面,得到了致密度高,结合力好的复合涂层。不仅增强了涂层的屏蔽作用,而且对碳钢基体起到了一定的钝化作用,提高了环氧涂层的耐蚀性能。其中(HCl+DBSA)-PANI/EP涂层比(H3PO4+DBSA)-PANI/EP涂层具有更有效的保护作用。
(3) 添加了共掺杂PANI的环氧涂料具有良好的流动性,很好地解决了聚苯胺的分散问题,并完全发挥了PANI的优点,有效增强了涂层的耐蚀性,可广泛用于工业涂料中。
[1] CHIANG J C, MACDIARMID A G.Polyaniline-protonic acid doping of the emeraldine form to the metallic regime [J].Synthetic Metals, 1986, 13 (1/2/3)∶193-205.
[2] ABD-EL-NABEY B A, ABDULLATEF O A, EL-NAGGAR G A, et al.Effect of tween 80 surfactant on the electropolymerization and corrosion performance of polyaniline on mild steel [J].International Journal of Electrochemical Science, 2016, 11 (4)∶ 2721-2733.
[3] KUMAR A M, GASEM Z M.In situ electrochemical synthesis of polyaniline/f-MWCNT nanocomposite coatings on mild steel for corrosion protection in 3.5% NaCl solution [J].Progress in Organic Coatings, 2015, 78∶ 387-394.
[4] SHABANI-NOOSHABADI M, GHOREISHI S M, JAFARI Y, et al.Electrodeposition of polyaniline-montmorrilonite nanocomposite coatings on 316L stainless steel for corrosion prevention [J].Journal of Polymer Research, 2014, 21∶ 416-420.
[5] ZHANG Y Z, LUO H Q, LI N B.Polyaniline coating on 304 stainless steel by electropolymerisation from aqueous NaOH solution for corrosion protection in NaCl medium [J].Corrosion Engineering Science and Technology, 2011, 46 (4)∶ 580-584.
[6] JAFARI Y, GHOREISHI S M, SHABANI-NOOSHABADI M.Polyaniline/graphene nanocomposite coatings on copper∶ electropolymerization, characterization,and evaluation of corrosion protection performance [J].Synthetic Metals, 2016, 217∶ 220-230.
[7] SHABANI-NOOSHABADI M, MOLLAHOSEINY M, JAFARI Y.Electropolymerized coatings of polyaniline on copper by using the galvanostatic method and their corrosion protection performance in HCl medium [J].Surface and Interface Analysis, 2014, 46 (7)∶ 472-479.
[8] 王华, 宋航.铝表面聚苯胺的电化学合成与性能研究[J].表面技术, 2016, 45 (4)∶ 46-52.
[9] BANDEIRA R M, VAN DRUNEN J, GARCIA A C, et al.Influence of the thickness and roughness of polyaniline coatings on corrosion protection of AA7075 aluminum alloy [J].Electrochimica Acta, 2017, 240∶ 215-224.
[10] DEBERRY D W.Modification of the electrochemical and corrosion behavior of stainless-steels with an electroactive coating [J].Journal of the Electrochemical Society, 1985, 132 (5)∶ 1022-1026.
[11] POPOVIC M M, GRGUR B N.Electrochemical synthesis and corrosion behavior of thin polyaniline-benzoate film on mild steel [J].Synthetic Metals, 2004,143 (2)∶ 191-195.
[12] 王华, 宋航.聚吡咯/聚苯胺复合膜的制备及耐腐蚀性能[J].电镀与涂饰, 2015, 34 (22)∶ 1320-1326.
[13] KOHL M, KALENDOVA A.Effect of polyaniline salts on the mechanical and corrosion properties of organic protective coatings [J].Progress in Organic Coatings, 2015, 86∶ 96-107.
[14] CHEN X J, LUO C, ZHANG Z H, et al.Preparation and anticorrosion properties of polyaniline-containing coating on Mg–Li alloy [J].Anti-Corrosion Methods and Materials, 2012, 59 (6)∶ 291-298.
[15] 李俊.新型聚苯胺环氧树脂复合防腐涂料的制备及其涂覆体系防腐性能的研究[D].杭州∶ 浙江大学, 2016.
[16] 罗丞.掺杂聚苯胺/环氧树脂防腐涂料制备与防腐性能研究[D].哈尔滨∶ 哈尔滨工程大学, 2011.
[17] 贾艺凡, 刘朝辉, 廖梓珺, 等.不同质子酸二次掺杂聚苯胺的导电性能[J].机械工程材料, 2016, 40 (1)∶ 71-74.
[18] 孙通, 李晓霞, 郭宇翔, 等.不同酸掺杂聚苯胺的电化学聚合及性能[J].化工进展.2013, 32 (8)∶ 1870-1875.
[19] BARD A J, FAULKNER L R.Electrochemical methods∶ fundamentals and applications [M].New York∶ Wiley, 1980∶ 544-556.
[20] JAFARI Y, GHOREISHI S M, SHABANI-NOOSHABADI M.Polyaniline/graphene nanocomposite coatings on copper∶ electropolymerization,characterization, and evaluation of corrosion protection performance [J].Synthetic Metals, 2016, 217∶ 220-230.
