丽春红S探针双波长吸收光谱法测定食品中的Cu
2018-02-28江虹吴征真王芳冉纯民曾庆瑞程乙真
江虹,吴征真,王芳,冉纯民,曾庆瑞,程乙真
(长江师范学院 化学化工学院,武陵山片区绿色发展协同创新中心,重庆,408100)
Cu是人们熟知的一种金属元素,广泛存在于日常用品中。人体中的Cu主要来源于日常饮食,如蛋糕、面包、饼干、面条、豆制品以及奶制品等,尤其是婴儿配方奶粉、幼儿配方奶粉及儿童配方奶粉等系列奶制品在加工过程中都补充了一定量的矿物质元素;由于Cu对人体健康有着重要作用,它是人体内多种氧化还原酶的成分,参与人体造血,在造血过程中若缺少Cu,人体内的铁元素就不能合成血红蛋白,造血机能就会受到影响,由此就会出现缺Cu性贫血;除此之外,人体缺Cu,还会引起头晕、眼花、耳鸣、乏力、冠心病、糖尿病等疾病。若人体内Cu过量,则会引起恶心、呕吐、上腹疼痛、肝脏受损等[1]。而食品在生产加工过程中,可能因使用Cu器设备或环境污染而带入一定量Cu。鉴于此,对食品中Cu的研究有着重要意义。
目前,国内外对Cu的检测方法主要有:原子吸收法[2-5],电化学法[6-9],荧光法[10-12],电感耦合等离子体质谱法[13-15]和紫外-可见分光光度法[16-19]等。原子吸收法有较高的准确度,但所用仪器偏贵,分析成本偏高。电化学法、荧光法及电感耦合等离子体质谱法,要么分析成本高不易普及,要么选择性欠佳或条件要求较苛刻等。而分光光度法由于操作简便,仪器价廉,可普及到一般实验室,因此长期以来,这种方法受到人们的喜爱而得到不断的发展。虽然用紫外-可见分光光度法对金属离子的研究较多,而对Cu的研究较多的是采用催化光度法、萃取光度法及三元络合光度法,它们的灵敏度一般较低,如文献[17] 的灵敏度(κ)只有7.95×103L/(mol·cm),文献[18] 的灵敏度(κ)只有1.29×103L/(mol·cm)。鉴于此,本工作以酸性染料丽春红S为探针,在可见光区采用二元反应双波长吸收光谱法来研究饼干、面条与奶粉中Cu含量的定量检测方法,本法比一般紫外-可见分光光度有更高的灵敏度,且操作更简单,所用试剂更少,目前尚未见文献报道。
1 材料与方法
1.1 材料与试剂
丽春红S(99%),成都贝斯特试剂有限公司;Cu(NO3)2·3H2O(99.9%),国药集团化学试剂有限公司;三羟甲基氨基甲烷(99.9%),齐一生物科技(上海)有限公司;HCl(AR),重庆川东(化工)集团有限公司;HNO3(99%),成都化夏化学试剂有限公司;三乙醇胺(≥99.5%),上海麦克林生化科技有限公司;儿童营养饼干(1 #)、面条(2 #)、幼儿配方奶粉(3 #~4#),市售。
丽春红S(ponceau S,简写为POS)溶液:称取适量丽春红S,用水溶解后,配成1.00×10-3mol/L;Cu(Ⅱ) 标准溶液:准确称取适量的Cu(NO3)2·3H2O用水溶解后配成63.55 mg/L 贮备液,取此液稀释10倍即为操作液;缓冲溶液:将0.20 mol/L Tris(三羟甲基氨基甲烷)溶液与0.10 mol/L盐酸混合,搅拌,用酸度计测定,配成pH 3.5~9.5 的溶液;HNO3溶液(V(HNO3)∶V(水)=1∶1,简称1∶1硝酸);三乙醇胺溶液(三乙醇胺与水的体积比为1∶2);水为超纯水。
1.2 仪器与设备
U-4100型紫外-可见-近红外分光光度计,日本日立公司;pHS-3C精密酸度计,上海虹益仪器仪表有限公司;EL104型电子天平,上海精密仪器仪表有限公司。SX-4-10高温炉,苏州江东精密仪器有限公司。
1.3 样品处理
用固定质量称量法在电子天平上快速、准确称取已捣碎、混匀、并按四分法缩分的样品(1 #~4 #)各10.000 0 g(允许误差±0.000 1 g),置于各瓷坩埚中,在电炉上低温加热至样品完全炭化,再调温至500~550 ℃,灼烧灰化约5 h,待冷却后取出坩埚,加2.0 mL HNO3溶液润湿灰分,再低温加热蒸干后,调温至500~550 ℃,继续灼烧约2 h,待冷却后取出坩埚,再加2.0 mL HNO3溶液,加水8 mL,搅拌,低温加热,待灰分完全溶解后,冷却,过滤,滤液收集于100 mL 容量瓶中,加三乙醇胺溶液(V(三乙醇胺)∶V(水)=1∶2)3.0 mL,用超纯水稀至刻度,即为待测液。
1.4 实验方法
用移液管准确移取3.50 mL 1.00×10-3mol/L 丽春红S溶液于10 mL 具塞比色管中,再加入1.00 mL pH 6.86 Tris-盐酸缓冲溶液和适量的6.355 mg/L Cu(Ⅱ) 标准溶液(或样液),用水稀至10 mL 刻度,摇匀,15 min 后,在U-4100型紫外-可见-近红外分光光度计上,以试剂空白作参比,扫描吸收光谱,以510 nm作参比波长,445 nm作测定波长,采用双波长法测定体系的吸光度值A。
2 结果与讨论
2.1 丽春红S-Cu(Ⅱ) 的吸收光谱特征
图1是可见光区Cu(Ⅱ)和丽春红S的吸收光谱图。曲线1表明,Cu(Ⅱ)在可见光区几乎无吸收;曲线2则表明丽春红S溶液在可见光区有强吸收,最大吸收波长位于500 nm;当在丽春红S 的弱酸性溶液中加入适量Cu(Ⅱ)溶液后,光谱曲线上出现了1个明显的正吸收峰和1个明显的负吸收峰,最大正吸收波长位于445 nm,紫移55 nm,最大负吸收波长位于510 nm,红移10 nm,在此二波长处,随着Cu(Ⅱ)溶液浓度的增加,正、负吸光度的绝对值不断增大。由于丽春红S在溶液中,其分子结构上的4个Na+可离解,离解后变成含4个磺酸根的阴离子,于是便与Cu(Ⅱ)以静电引力结合生成二元离子缔合物。从波移现象和反应机理可知,丽春红S和Cu(Ⅱ)在弱酸性的Tris-盐酸介质中确实生成了新物质,且Cu(Ⅱ)在一定质量浓度范围内与正吸收和负吸收的吸光度绝对值呈线性关系,服从朗伯-比尔定律。当用双波长法测定时(以510 nm为参比波长,445 nm为测定波长),由于吸光度的加和性,用双波法测定的吸光度与Cu(Ⅱ)的浓度间仍存在线性关系,服从朗伯-比尔定律,且双波长的灵敏度约为单波长的1.4~3.4倍。故单波长正吸收法、负吸收法及双波长法均可用于Cu(Ⅱ)的定量分析。
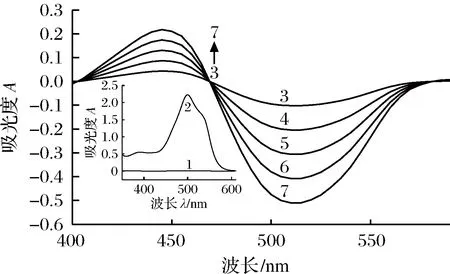
1.0.636 mg/L Cu(Ⅱ), 水作参比; 2. 2.00×10-5 mol/L丽春红S,水作参比; 3~7. (0.318, 0.636, 0.953,1.27, 1.59 mg/L)Cu(Ⅱ)-3.50×10-4 mol/L丽春红S,试剂空白作参比; pH 6.86图1 吸收光谱Fig.1 The absorption spectra
2.2 反应的适宜条件
2.2.1 溶液pH的选择
室温下,考察了用单波长法(正吸收法和负吸收法)及双波长法测定时,在不同pH值的缓冲溶液中对丽春红S-Cu(Ⅱ)体系吸光度绝对值(│A│)的影响(图2)。
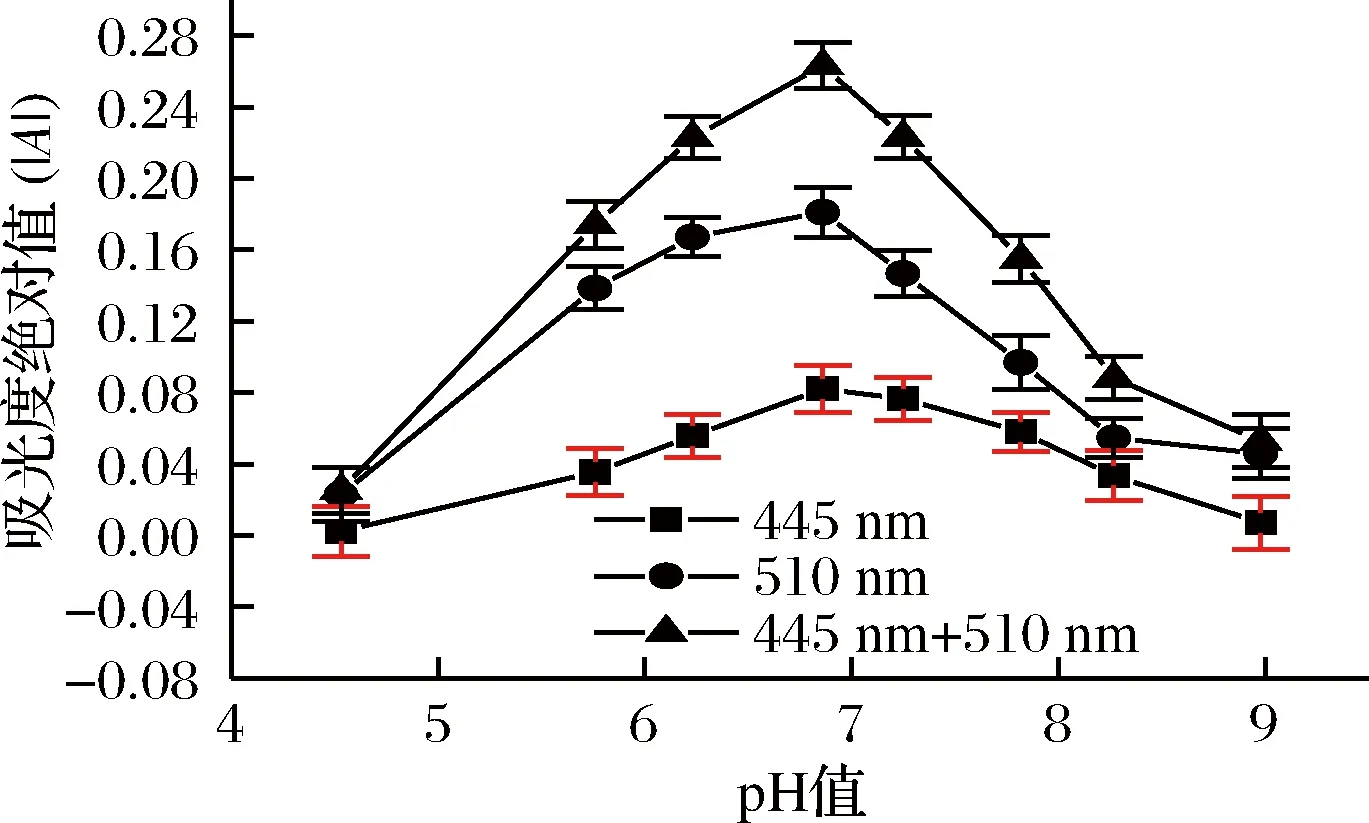
图2 pH值对│A│的影响Fig.2 Effect of buffer pH on │A│
图2表明,溶液的pH值为6.8时,无论用单波长法测定还是用双波长法测定,均有较高灵敏度,其│A│ 相对较大;而正吸收法、负吸收法及双波长法比较,又以双波长法的灵敏度为最高。故实验选用双波长法测定,用pH 6.86的Tris-盐酸溶液。继而考察了不同用量的pH 6.86溶液对丽春红S-Cu(Ⅱ)体系吸光度绝对值(│A│)的影响,结果表明,适宜用量为1.00 mL。
2.2.2 丽春红S溶液浓度的选择
室温下,考察了用单波长法(正吸收法和负吸收法)及双波长法测定时,在10 mL比色管中,丽春红浓度为(0.5、1.0、1.5、2.0、2.5、3.0、3.5、4.0、4.5、5.0)×10-4mol/L 时对丽春红S-Cu(Ⅱ) 体系吸光度绝对值(│A│)的影响(图3所示)。结果表明,丽春红S溶液的浓度为3.50×10-4mol/L 时,无论用单波长法还是用双波长法测定,其吸光度绝对值均最大,灵敏度最高;而单波长法和双波长法比较,又以双波长法的灵敏度为最高。故实验选用双波长法测定,用1.00×10-3mol/L 丽春红S溶液3.50 mL。
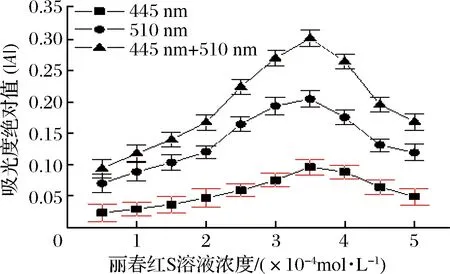
图3 丽春红S溶液浓度对│A│的影响Fig.3 Effect of ponceau S concentration on │A│
2.2.3 试剂加入顺序的选择
室温下,考察了用单波长法(正吸收法和负吸收法)及双波长法测定时,各物质不同加入顺序对丽春红S-Cu(Ⅱ) 体系吸光度绝对值(│A│)的影响。结果为:按丽春红S 溶液、缓冲溶液、Cu(Ⅱ) 溶液顺序加入时,│A│分别为0.085(正吸收法)、0.20(负吸收法)和0.29(双波长法);而按其他顺序加入各试剂时,无论是单波长法还时双波长法其│A│均较前者小;因此,按前述顺序加入各试剂溶液,其灵敏度相对较高,而单波长法和双波长法相比较,又以双波长法测定的灵敏度更大。故实验用双波长法测定,按最佳顺序加入各试剂。
2.2.4 反应时间及稳定性
室温下,考察了用单波长法(正吸收法和负吸收法)及双波长法测定时,反应时间对丽春红S-Cu(Ⅱ)体系吸光度绝对值(│A│)的影响,图4所示。结果表明,丽春红S与Cu(Ⅱ)的反应,在15 min内即可完全,之后其稳定时间约1.5 h。实验选在15 min后进行。

图4 时间对│A│的影响Fig.4 Effect of time on │A│
2.3 标准曲线及相关参数
按实验方法,在数支比色管中分别加入一定体积的Cu(Ⅱ)标准溶液,使其在10 mL比色管中的浓度分别为0.318、0.636、0.953、1.27、1.59 mg/L,再加入其他各试剂溶液,扫描Cu(Ⅱ)的标准系列溶液,作单波长正吸收法、负吸收法及双波长法的A-ρ标准曲线,如图5所示。根据检出限及标准曲线,即可求得线性范围。该方法的一元线性回归方程、回归系数、线性范围、表观摩尔吸光系数及定量限等列于表1。
图5 Cu(Ⅱ)的标准曲线Fig.5 Standard curve of copper(Ⅱ)
2.4 共存物质的影响


表1 标准曲线相关参数
2.5 样品分析
取1.3节中制得的待测样液1#~3#各3.00 mL,4# 2.00 mL,按实验方法分别配制溶液并用双波长法测定各样液中Cu(Ⅱ)的含量,最后推至原始样品中所含Cu的量,各平行测定5份。同时做加标回收试验(各水平分别平行测定5份),以判断该法的准确度。结果见表2。
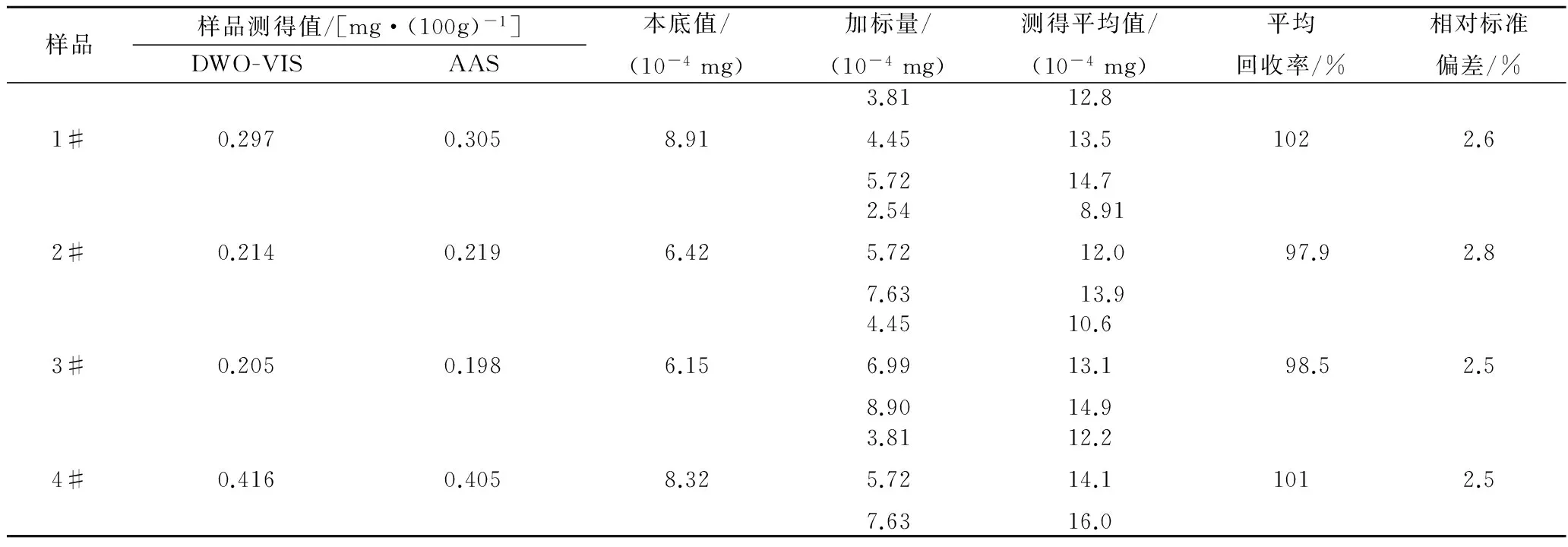
表2 样品分析结果及回收试验(n=5) Table 2 Analytical results and recovery tests of samples(n=5)
表2表明,本法测定结果与GB/T 5009.13—2003(AAS法)基本一致。从回收率(97.9%~102%)和相对标准偏差(2.5%~2.8%)看,本方法有较高的准确度和精密度。
3 结论
以丽春红S为探针,采用双波长可见吸收光谱法测定Cu的含量,方法简便,试剂用量少,有较高的准确度、精密度及较高的灵敏度,线性范围较宽,方法适于面制品和配方奶粉中Cu含量的快速测定。
[1] 孔祥瑞.必需微量元素的营养、生理及临床意义[M].合肥:安徽科学技术出版社,1982:155-201.
[2] 李加兴,傅伟昌,曾雪峰,等.螺旋藻预富集-FAAS 测定干制品浸出液中的痕量铜[J].食品与发酵工业,2008,34(9):146-149.
[3] CENNET K, DERYA K. Dispersive liquid-liquid microextraction based on solidification of floating organic drop for preconcentration and determination of trace amounts of copper by flame atomic absorption spectrometry [J]. Food Chemistry,2016,220:242-248.
[4] VANESSA C D P, JORGE L R. Ultrasound-assisted extraction for the determination of Cu, Mn, Ca, and Mg in alternative oilseed crops using flame atomic absorption spectrometry [J]. Food Chemistry,2016,196: 1 287-1 292.
[5] 梁艺馨,刘康书,蔡秋,等.连续光源火焰原子吸收法同时测定薏苡中铜、铁、钙和锰的不确定度评价[J].食品科学,2016,37(12):134-138.
[6] AYWENUR B,HILAL E,FATIH C,et al.Rapid determination of trace level copper in tea infusion samples by solid contact ion selective electrode[J].Journal of Food and Drug Analysis,2016,24(3):485-492.
[7] DOMINIKA J, PAWEL P, MAJA W. Determination of the total cadmium, copper, lead and zinc concentrations and their labile species fraction in apple beverages by flow-through anodic stripping chronopotentiometry [J]. Food Chemistry,2017,225:220-229.
[8] YASSER S, FARHAD A, FARNOOSH F. Voltammetric determination of Pb, Cd, Zn, Cu and Se in milk and dairy products collected from Iran:An emphasis on permissible limits and risk assessment of exposure to heavy metals [J].Food Chemistry,2016, 192:1 060-1 067.
[9] BHUSHAN G, PIA D, EVGENIA D, et al. Exploring amide linkage in a polyviologen derivative towards simultaneous voltammetric determination of Pb(II), Cu(II) and Hg(II) ions [J]. Electrochimica Acta,2016,192:482-488.
[10] 白延涛,高楼军,李环,等.Cu(Ⅱ)-桑色素-十六烷基三甲基溴化铵荧光体系测定微量Cu(Ⅱ)的研究[J].分析科学学报,2015,31(2):265-267.
[11] NAN Qian, RONG Pu, JIANG Yunbao, et al. New highly selective turn-on fluorescence receptor for the detection of copper(II) [J]. Spectrochimica Acta Part A: Molecular and Biomolecular Spectroscopy,2017,174:307-315.
[12] CHEN Linfeng, TIAN Xike, YANG Chao, et al. Highly selective and sensitive determination of copper ion based on a visual fluorescence method [J].Sensors and Actuators B:Chemical,2017,240:66-75.
[13] 黄子敬,陈孟君,邓华阳,等.微波消解—ICP-MS 混合模式测定动植物源食品中11 种金属元素[J].分析试验室,2017,36(1):24-28.
[14] 邢博,张霁,李杰庆,等.ICP-MS法测定云南省8种野生牛肝菌中矿质元素含量[J].食品科学,2016,37(12):89-94.
[15] 聂西度,符靓,唐莉娟,等.电感耦合等离子体质谱法测定黑小麦中多种元素[J].食品科学,2015,36(12):125-128.
[16] 赵丽杰,赵丽萍,常勇,等.邻菲啰啉活化催化褪色光度法测定食品中痕量Cu2+[J].食品科学,2009,30(10):169-172.
[17] 林瑜,韦小玲,唐明森.Cu2+-甲状腺素络合物的光谱特征及其分析应用[J].分析试验室,2016,35(1):17-20.
[18] ZOLAIKHA R, ZEINABE H, RAOUF G. Application of a new version of GA-RBF neural network for simultaneous spectrophotometric determination of Zn(II), Fe(II), Co(II) and Cu(II) in real samples: An exploratory study of their complexation abilities toward MTB [J].Talanta,2016,160:86-98.
[19] 黄运瑞,张廉奉,卢驰元,等.分散液相微萃取光度法测定水中痕量铜[J].冶金分析,2016,36(12):65-68.
