CVD法制备氮化硼陶瓷的化学反应热力学研究
2018-02-28任海涛
任海涛
(天津大学 材料科学与工程学院,天津 300072;先进陶瓷加工技术教育部重点实验室,天津 300072)
氮化硼(BN)是一种重要的非氧化物陶瓷材料,由等数量的B原子和N原子组成,与C2是等电子体,其晶体结构与碳元素单质非常相似,具有四种晶型结构,分别为六方氮化硼(h-BN)、立方氮化硼(c-BN)、纤锌矿氮化硼(w-BN)和菱面体氮化硼(r-BN)等。常见的氮化硼为六方氮化硼(h-BN)和立方氮化硼(c-BN)。h-BN与石墨具有类似的结构,每一层都是由B原子和N原子交替排列组成无限延伸的六边形网格,层面内原子以共价键相结合,层间则以弱的范德华力结合。h-BN这种独特的结构使其具有很多优异特性[1-3],比如高耐热性(可承受2 000℃高温,直到3 000℃才升华)、高导热性(是众多陶瓷材料中导热系数最大的材料之一)、优异的介电性能(高温绝缘性能好,是陶瓷材料中最好的高温绝缘材料,可以透微波和红外线)、良好的高温稳定性(在氧化环境下,使用温度可达900℃,在惰性气体环境中,使用温度可达2 800℃)、具有较低热膨胀系数(膨胀系数为10-6,仅次于石英玻璃,抗热震性能优异)、具有良好的润滑性(高温也具有良好的润滑性能,是优良的高温固体润滑剂)、化学性质稳定(具有良好的耐腐蚀性,与一般无机酸、碱、或氧化剂不发生反应,对几乎所有的溶融金属都呈现化学惰性),吸收中子(氮化硼还具有非常强的中子吸收能力,可用来做反应堆中子吸收控制棒,以及用来制作防中子福射的防护装置)。此外,由于h-BN具有与热解碳相似的层状晶体结构,比热解碳具有更好的抗氧化性能,氧化后形成的玻璃相B2O3能够弥合裂纹,是较好的界面相材料并得到成功应用[4]。立方氮化硼(c-BN)具有与金刚石类似的结构,属于面心立方晶系、闪锌矿型的正四面体结构,以硼和氮异类原子之间的共价键结合,4个键长相等。与金刚石一样,c-BN是集众多优异性能于一身的超硬材料,具有与金刚石相似的物理性质,比如高硬度、宽带隙、高电阻率、高热稳定性和化学稳定性等。c-BN的稳定性甚至优于金刚石,在大气1 300℃以下不发生氧化反应(金刚石600℃开始氧化),在真空1 550℃才开始向h-BN转变(金刚石1 300~1 400℃就开始向石墨转变),c-BN的耐高温性能使其被用于某些器件的耐高温涂层,也成为制备高速、高温器件和其他薄膜型材料衬底的首选化合物。另外,c-BN具有优异的耐化学腐蚀性和高化学稳定性,在1 150℃以下不与铁系金属反应(金刚石在700℃开始溶解于铁,因而不宜加工钢铁材料)。c-BN的这些优良性能使其大量应用于制备高效、经济、节能的磨削和切削工具,并在某些行业中替代了金刚石被广泛应用。除此之外,c-BN具有宽带隙和较高热导系数,在制造抗辐射材料、高温大功率半导体器件、紫外光电子器件方面都具有杰出应用价值和极大应用前景,c-BN在红外光和可见光范围内的透光性非常好,在精密光学仪器中被大量用做表面保护涂层[5-6]。
化学气相沉积(Chemical Vapor Deposition,简称“CVD”)是20世纪60年代发展的制备无机材料的新技术,它是在一定温度下,通过是一种或几种气体在一固体表面进行化学反应(包括分解反应、化合反应、化学输运反应等),在该固体表面生成固态沉积物的过程[7]。对于一个新的CVD体系,一般会先进行反应热力学分析,即根据化学平衡原理,计算在不同工艺参数(温度、压力及进气比)下一些重要产物,尤其是固相产物的平衡浓度分布,用来预测平衡条件下工艺参数对体系CVD产物类型与产量的影响。
本文针对BCl3-NH3-H2制备BN陶瓷体系,基于笔者之前工作[8]已建立的B-N体系热力学数据库,再结合体系相关重要固相产物,包括固相硼(B)和3种结构的氮化硼(h-BN,c-BN和w-BN)在JANAF[9]里的实验数据,得到典型工艺参数下的产物平衡浓度分布。通过分析和总结,从理论上说明不同固相产物沉积的最佳热力学条件,揭示反应规律,优化制备工艺参数,为实验研究提供理论指导。
1 相关产物平衡浓度计算方法
根据化学平衡原理,即体系总吉布斯自由能(化学势)最小的数学条件,由下式可获得所有物种的平衡浓度分布:

式(1)中:s为体系的总固相物种数;N为体系总物种数;p为总压;ni是气相第i个物种物质的量;为固相第i个物种的质量。
2 结果与讨论
本文参考BCl3-NH3-H2体系CVD法制备氮化硼的实验条件,选择接近实验的典型工艺参数,即总压为1 000 Pa,先驱体进气比为BCl3∶NH3∶H2=1∶3∶6进行计算。图1为计算得到的300~2 000 K体系总产物平衡浓度图,只绘出了最大浓度大于10-7mol的产物。
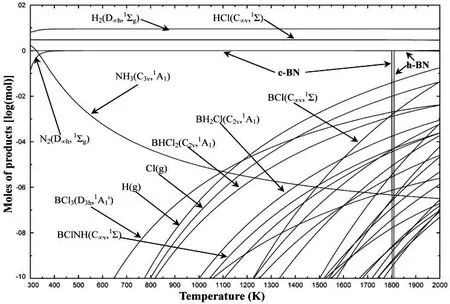
图1 BCl3-NH3-H2体系300~2 000 K的总产物平衡浓度图
由图1可以看出,从300 K开始,NH3的浓度迅速降低,同时H2浓度略有升高,但是却未发现BCl3,固相产物c-BN在300 K已经产生,HCl和N2的浓度从反应开始就迅速升高。由上述可推测,在300 K时,体系的化学反应已经开始,且大量消耗BCl3和NH3生成H2、N2、HCl和c-BN产物。可能发生的化学反应为:BCl3+NH3→H2+HCl+N2+c-BN.
由图1同样可以看出,约650 K时BCl3开始出现,其浓度随温度升高而逐渐升高,原因可能为固相产物c-BN的产出降低而减少BCl3的消耗。立方氮化硼(c-BN)只能在低于1 800 K时产生,高于1 800 K则生成六方氮化硼(h-BN),固相B单质在2 160 K以上才可能产生。
3 总结
本文对BCl3-NH3-H2体系进行了热力学产物平衡浓度分布研究,计算得到在典型CVD工艺参数下体系相关重要产物的平衡浓度分布,即在1 000 Pa总压,进气比BCl3∶NH3∶H2=1∶3∶6的CVD工艺参数下,BCl3和NH3在300 K即可发生反应,高于2 160 K可生成固相硼(B),1 800 K以下生成立方氮化硼(c-BN),1 800 K以上生成六方氮化硼(h-BN)。而纤锌矿氮化硼(w-BN)则无法稳定存在。
本文从理论上说明不同固相产物沉积的最佳热力学条件,为实验研究提供理论指导。需要说明的是,在体系CVD过程中,不可能达到理想状态的化学平衡,热力学分析只是一种分析方法,其假定反应时间无限长,不受动力学影响,该计算结果仅代表一种可能性,反应的实际情况还需结合动力学分析。
[1]袁颂东.氮化硼纳米材料的制备及性能研究[D].武汉:华中科技大学,2009.
[2]张雯,王红洁,金志浩.先驱体热解制备BN复合陶瓷材料研究进展[J].兵器材料科学与工程,2004(05):58-63.
[3]顾立德.氮化硼陶瓷[M].北京:中国建筑工业出版社,1987.
[4]R.R.Naslain,R.J.F.Pailler,J.L.Lamon.Single-and Multilayered Interphases in SiC/SiC Composites Exposed toSevereEnvironmentalConditions: An Overview.InternationalJournal ofApplied Ceramic Technology,2010,7(3):263-275.
[5]J.L.P.Castineira,J.R.Leite,J.L.F.da Silva,et al.Electronic Structure and Stability of B Impurities in Cubic Boron Nitride.physica status solidi(b),1998,210(2):401-405.
[6]谭华,韩钧万,贺红亮,等.冲击波合成氮化硼的形貌及热稳定性[J].高压物理学报,1995(01):53-58.
[7]孟广耀.化学汽相淀积与无机新材料[M].北京:科学出版社,1984.
[8]H.Ren,L.Zhang,K.Su,et al.Thermodynamic study on the chemical vapor deposition of boron nitride from the BCl3-NH3-H2system.Theor Chem Account,2014,133(11):1-13.
[9]M.W.Chase.NIST-JANAF Thermochemical Tables Forth Edition.Journal of Physical and Chemical Reference Data,1999(9).
