海藻酸钠模拟钙片和钙尔奇钙片缓释作用的实验探究
2018-02-27徐敏郑丽娟
徐敏 郑丽娟
摘要: 海藻酸钠以其独特的理化性能成为十分优质的缓释和控制制剂。运用手持技术探究负载不等量CaCO3的海藻酸钠微球和负载等量CaCO3的颗粒数不等的海藻酸钠微球分别与盐酸反应的速率以证明反应速率与固体反应物的质量和表面積的关系,并将实验结论运用于制作模拟钙片,以比较市售钙尔奇钙片对人体的缓释作用。
关键词: 海藻酸钠; 模拟钙片; 钙尔奇; 手持技术; 化学实验探究
文章编号: 10056629(2018)12008104中图分类号: G633.8文献标识码: B
1 引言
市售钙尔奇钙片的主要成分是碳酸钙,以一种每片含钙273.5mg的金装钙尔奇为例,其含钙量相当于每片含碳酸钙0.68g。实验表明一粒金装钙尔奇钙片与20mL3mol/L稀盐酸反应产生二氧化碳的速率较快(开始100s内气压约增大22kPa),能否找到缓释作用更好的补钙剂?有鉴于海藻酸钠在食品加工业中广泛用作缓释和控制制剂,将碳酸钙负载于海藻酸钠上与金装钙尔奇作对比,研究两者的缓释作用,以期为改进市售的各种补钙剂提供借鉴。
2 海藻酸钠和固化反应
海藻酸钠是从褐藻类的海带或马尾藻中提取碘和甘露醇之后的副产物,是一种天然高分子多糖,具有良好的生物兼容性,且无毒可食用,广泛应用于生物医药和食品加工业,用作缓释剂和控制剂。
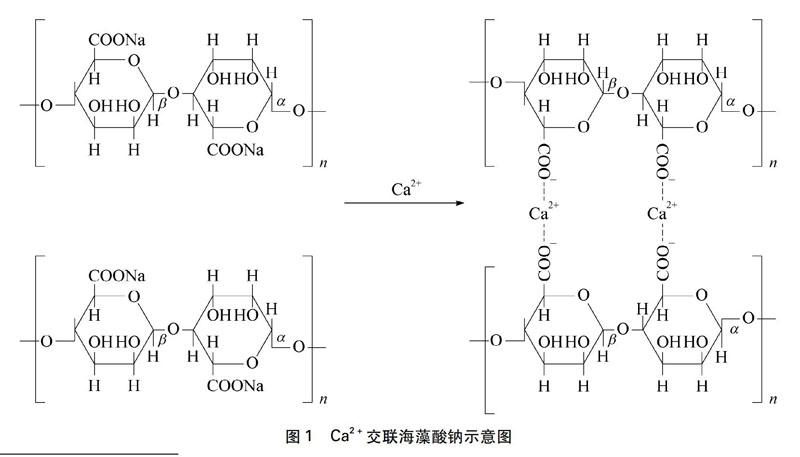
海藻酸钠是由和αL古罗糖醛酸和1,4聚βD甘露糖醛酸两种结构单元组成的线性聚合物,分子式为[C6H7O6Na]n,为阴离子型的高分子。当遇阳离子如Ca2+、 Zn2+,会交联固化(见图1)[1~4]。
3 负载碳酸钙粉的海藻酸钠微球的制备
(1) 配制3.8%的CaCl2溶液: 称取8g CaCl2加入200mL蒸馏水中搅拌得到3.8%的CaCl2溶液。
(2) 配制2.2%海藻酸钠溶胶: 称取15.5g海藻酸钠加入700mL沸水中搅拌30min,得到
2.2%的海藻酸钠溶胶。
(3) CaCO3微球的制备: 分别称取2g、 4g、 6g、 8g、 10g CaCO3加入到20.5g 2.2%的海藻酸钠溶胶中,得到含CaCO3 8.9%、 16.3%、 22.6%、 28.1%、 32.8%的悬浊液,再用20mL注射器将悬浊液逐滴滴入3.8%的CaCl2溶液进行固化,获得不同配比直径为2mm的负载CaCO3的海藻酸钠微球,漏勺过滤,蒸馏水清洗。
4 运用手持技术探究负载碳酸钙的海藻酸钠微球与盐酸的反应速率
4.1 手持技术
手持技术(Hand-held Technology),即数字化手持技术实验,又称为掌上实验室(Lab In Hand),是由计算机和微电子技术相结合的新型数字化实验手段,主要包括: 数据采集器、传感器、计算机及其配套软件三个部分。
(1) 数据采集器: 数字化实验的转换元件。它完成指令发送、接受从传感器传过来的电信号,收集、存储数据,再转化成数字信号传输给计算机,是连接传感器和计算机的桥梁。
(2) 传感器: 数字化实验的感知元件。传感器的作用是“感”与“传”,“感”是将感触到的物理量转换成数据采集器能够识别和分析的电信号,“传”是将电信号传递给数据采集器和计算机。它能感触到的相关信息包括气压、离子浓度和相对湿度等。
(3) 计算机及相应软件: 数字化实验的处理元件。专门的软件能够将实验数据进行记录与分析处理,并通过计算机完成对实验数据的显示、分析、存储以及传输,实现信息技术与学科教学的整合[5]。
4.2 运用手持技术探究负载不等量碳酸钙的海藻酸钠微球与盐酸的反应速率
实验仪器和药品: 威尼尔气体压强传感器、威尼尔数据采集器、台式电脑、500mL三颈烧瓶、橡皮塞、20mL注射器、负载不等量CaCO3的海藻酸钠微球、3mol/L盐酸
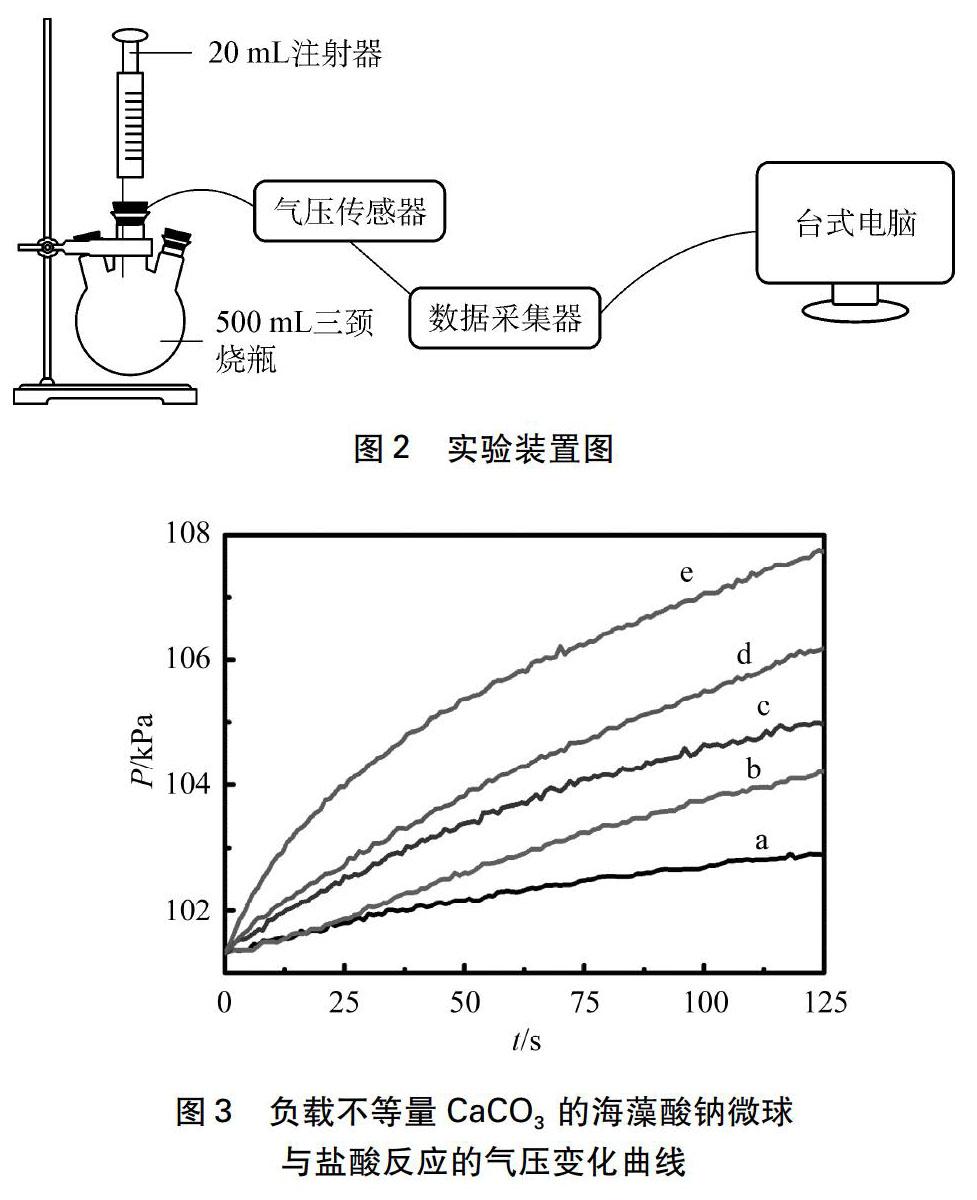
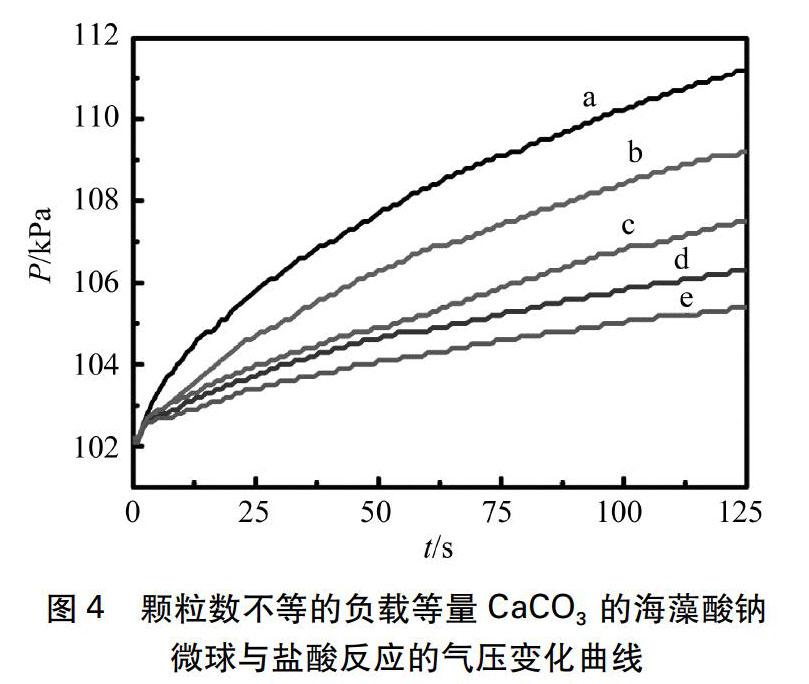
实验过程: 分别拣取80粒负载8.9%、 16.3%、 22.6%、 28.1%、 32.8%CaCO3的海藻酸钠微球于三颈烧瓶中,按图2方式连接仪器,分别用注射器向三颈烧瓶中注入浓度为3mol/L盐酸20mL,利用威尼尔气体压强传感器立即采集0~125s的气体压强数据作图(见图3)。
实验结论: 图3中a、 b、 c、 d、 e对应的是负载8.9%、 16.3%、 22.6%、 28.1%、 32.8%CaCO3的海藻酸钠微球分别与3mol/L盐酸反应产生CO2的压强变化曲线。图像显示随着海藻酸钠微球中CaCO3平均负载量的增加,单位时间内气压变化越明显,反应速率越快。
4.3 运用手持技术探究颗粒数不等的负载等量碳酸钙的海藻酸钠微球与盐酸的反应速率
实验仪器和药品: 威尼尔气体压强传感器、威尼尔数据采集器、台式电脑、 500mL三颈烧瓶、橡皮塞、 20mL注射器、负载等量CaCO3的海藻酸钠微球、 3mol/L盐酸
实验过程: 分别称取4.55g 8.9%、 2.32g 16.3%、 2.40g22.6%、 1.48g 28.1%、 1.25g 32.8%CaCO3的海藻酸钠微球(碳酸钙的含量都约为0.66g固化后的微胶囊的质量会小于之前的悬浊液,通过称取全部固化后微胶囊的质量,可得对应0.66g CaCO3的微胶囊的质量。)于三颈烧瓶中,按图2方式连接仪器,用注射器向三颈烧瓶中注入浓度为3mol/L盐酸20mL,利用威尼尔气体压强传感器立即采集0~125s的气体压强数据作图(见图4)。
实验结论: 图4中a、 b、 c、 d、 e对应的是含有0.66g CaCO3的负载8.9%、 16.3%、 22.6%、 28.1%、 32.8%CaCO3的海藻酸钠微球分别与3mol/L盐酸反应产生CO2的压强变化曲线。图像显示CaCO3平均含量小的微球与盐酸反应时单位时间内气压变化较大,反应速率较快。因为含有0.66g CaCO3的海藻酸钠微球数量关系为: N8.9%>N16.3%>N22.6%>N28.1%>N32.8%,因此,固体反应物的表面积大小关系为: S8.9%>S16.3%>S22.6%>S28.1%>S32.8%。上述实验数据也证实了固体反应物的表面积越大,反应速率越快。
5 运用手持技术探究负载碳酸钙的海藻酸钠模拟钙片与钙尔奇钙片的缓释作用
海藻酸钠所形成的水凝胶微球属于pH敏感型凝胶,当外界环境的pH偏酸性时,三维网络结构中的羧基结合氢离子形成羧酸,分子间的作用力减弱,微球处于收缩状态;当外界环境的pH偏中性或碱性时,羧基以阴离子形式存在,分子间的羧基因带负电荷而相互排斥,此时微球处于溶胀状态,可以释放所包封的活性成分或药物[6~10]。
基于上述实验结论和海藻酸钠的敏感性,利用海藻酸钠负载CaCO3制作的模拟钙片表面积不宜太大,负载的质量与每片钙尔奇钙片所含CaCO3质量相等(见表1)。
5.1 负载CaCO3的海藻酸钠模拟钙片的制备
称取负载10%CaCO3的海藻酸钠溶胶5g加入3.8%的CaCl2溶液中固化,过滤清洗后得到含0.5g的模拟钙片,干燥后称得质量为2.68g。
5.2 运用手持技术探究负载碳酸钙的海藻酸钠模拟钙片与钙尔奇钙片的缓释效果
实验仪器和药品: 威尼尔气体压强传感器、威尼尔数据采集器、台式电脑、500mL三颈烧瓶、橡皮塞、20mL注射器、负载0.5g CaCO3的海藻酸钠模拟钙片、3mol/L盐酸
实验过程: 用药匙分别取1片模拟钙片和1片钙尔奇钙片置于两个三颈烧瓶中,按图2方式连接仪器,用注射器向两个三颈烧瓶中分别注入浓度为3mol/L盐酸20mL,利用威尼尔气体压强传感器立即采集0~200s的气体压强数据作图(见图5)。
实验结论: 图5显示模拟钙片与3mol/L盐酸的反应在0~200s内产生二氧化碳气体的压强变化不大,比钙尔奇钙片的缓释作用好。
6 反思
实验探究了以海藻酸钠为载体负载不溶性固体CaCO3与盐酸反应的系列实验,探索了固体反应物的表面积和质量对反应速率的影响。以往的中学化学教学中大多通过改变液体反应物的浓度、环境温度来改变化学反应的速率,本实验探索了通过改变固体反应物的表面积来改变反应速率的可能性。
数字化实验仪器有效地监测了固液反应的进程,对气体压强变化曲线所做的斜率大小分析较好地诠释了固液反应的速率大小。
教学中教师引导学生从图像曲线中发现问题、分析并解决问题,培养了学生的宏观辨识与微观探析能力,发展了学生的核心素养。
参考文献:
[1]Mocanu G, Nichifor M. Cationic amphiphilic dextran hydrogels with potential biomedical applications [J].Carbohydrate Polymers, 2014,(99): 235~241.
[2]Anitha A, Rani V.V.D., Krishna R, et al. Synthesis, characterization, cytotoxicity and antibacterial studies of chitosan, O-carboxymethyl and N, O-carboxymethyl chitosan nanoparticles [J]. Carbohydrate Polymers, 2009, 78(4): 672~677.
[3]Lin H.R., Chen Y.C., Lin Y.J., et al. pH-sensitive hollow alginate-chitosan hydrogel beads for bitter gourd delivery [J].International Journal of Polymeric Materials and Polymeric Biomaterials, 2014, 63(1): 41~47.
[4]Yang F, Xia S.Q., Tan C., et al. Preparation and evaluation of chitosan-calcium-gellan gum beads for controlled release of protein [J]. European Food Research and Technology, 2013, 237(4): 467~479.
[5]馬宏佳.化学数字化实验的理论与实践[M].北京: 人民教育出版社, 2016.
[6]刘丽英.海藻酸钙凝胶微球的制备和pH敏感释放[J].中国组织工程研究与临床康复, 2009,13(42): 8303~8306.
[7]王秀娟等.海藻酸钠凝胶特性的研究[J].食品工业科技, 2008,(2): 259~262.
[8]吴秋惠等.海藻酸钠微球的制备及其在药物载体中的应用进展[J].中华中医药杂志, 2011,26(8): 1791~1794.
[9]王婷婷.海藻酸钠微球研究进展[C].第十届化妆品学术研讨会论文集: 156~164.
[10]樊华等.海藻酸钠在药剂应用中的研究进展[J].中国药房, 2006,17(6): 465~467.
