金柑叶片和果实总DNA提取方法比较
2018-01-30唐志鹏秦荣耀孙宁静徐石兰焦丁华
张 宇,唐志鹏,秦荣耀 ,孙宁静,徐石兰 ,焦丁华
(1. 广西大学 农学院,广西 南宁 530004;2. 广西壮族自治区亚热带作物研究所,广西 南宁 530001;3.遂川县果业局,江西 吉安 343900)
金柑Fortunella swingle又称金橘,属芸香科Rutaceae金柑属Fortunella药食兼用植物。金柑原产于中国,栽培历史近1 700 a,栽培地区遍布广西、江西、浙江、福建、湖南、广东等省(区),其中广西种植面积及产量居第1位,其次是江西、福建和湖南等地。主要产地为广西的融安和阳朔、江西的遂川、福建的尤溪和上杭、湖南的浏阳和蓝山、宁波北仑等地[1]。金柑清香味美、营养丰富,同时具有维护心血管功能、防治血管硬化和高血压等疾病的药用价值[2]。随着我国政府对果树品种资源的保护与开发越来越重视,许多金柑品种资源的调查采集工作取得了积极的研究成果。调查结果表明,金柑的种类较少,金柑品种主要来源于实生变异、无性变异种的芽变。同时,分子生物技术也被运用在金柑品种资源研究中,黄桂香等[3]和施维属等[4]利用ISSR技术分别得出了越南金柑可能是宽皮柑橘与金柑杂交的后代和该标记可以将金柑属和柑橘属区分开来的结论;张连峰等[5]利用SSR技术得出了宁波罗浮与宁波纹具有极其相近的亲缘关系。以上研究结果的获得均是以获取高质量的总DNA为基础,但较详尽获取金柑总DNA的方法报道较少。本文中研究了获取高质量金柑总DNA的方法,旨在为分子标记辅助选择在金柑育种中得到实际应用打下基础。
1 材料与方法
1.1 材 料
供试材料为融安金柑、滑皮金柑、脆密金柑。2016年7月6日,在广西融安县雅瑶乡分别采取3个金柑品种的嫩叶和果实,各收集叶片15张,果实6枚,放进冰壶,迅速运回广西大学农学院实验室,用双蒸水清洗叶片和果实并滤干水分,置于-30 ℃冰箱内保存备用[6-9]。
1.2 方 法
1.2.1 DNA提取试剂
① CTAB抽 提 液:115 mmol/L Tris-HCl,1.5 mol/L NaCl,20 g/L CTAB,20 mmol/L EDTA,4% β-巯基乙醇,20 g/L PVP-40(聚乙烯吡咯烷酮)(pH8.0);②饱和酚、氯仿、异戊醇提取液,各溶液体积比25∶24∶1;③SDS抽提液:115 mmol/L Tris-HCl,0.8 mol/L NaCl,质量浓度5%的SDS,55 mmol/L EDTA,2% β-巯基乙醇,20 g/L PVP-40(pH8.0)。
1.2.2 DNA提取流程
CTAB提取法:参考张宇等[10]的方法并进行适当的修改。取0.5 g鲜样,液氮中研磨成粉末(金柑果实用经75%酒精消毒过的刀片切割成1 cm3大小后研磨成粉末),放入10 mL离心管中;加入65 ℃预热的6 mL提取试剂①,上下颠倒混匀,65 ℃温浴1 h,期间不时晃动离心管几次,常温下11 500 r/min离心11 min,留清液;加入等体积提取试剂②,震荡混匀,静置5 min,4 ℃下11 500 r/min离心11 min;取上清液,加1/10体积3 mol/L NaAc和上清液等体积预冷的异丙醇,混匀,-30 ℃静置1 h,4 ℃下11 500 r/min离心18~20 min;弃上清,75%乙醇洗涤沉淀2~3次,超净台上风干,用100 μL ddH2O溶解,-25 ℃保存备用。
SDS提取法:参考井赵斌等[11]方法。选0.5 g鲜样,液氮中研磨成粉末(鲜样研磨前处理同CTAB提取法),放入10 mL离心管;加入65 ℃预热的6 mL提取试剂③,上下颠倒混匀,65 ℃温浴0.5 h,期间不时晃动离心管3~5次,常温下11 800 r/min离心10 min,留上清液;加入与上清液同体积提取试剂②,震荡混匀,静置5 min,4 ℃下11 800 r/min离心10 min,取上清液,加1/10体积3 mol/L NaAc和1/3体积LiCl,混匀,-25 ℃静置0.5 h,4℃下11 800 r/min离心18~20 min;弃上清,80%酒精洗沉淀2~3次,超净台上风干,用100 μL ddH2O溶解,-25 ℃保存备用。
试剂盒提取法:选0.2 g鲜嫩样品,液氮中研磨成粉末(鲜样研磨前处理同CTAB提取法),选用天根生化科技(北京)有限公司生产的DNA secure plant Kit(DP320)新型植物基因组DNA提取试剂盒(离心柱型)进行提取,提取流程严格遵照产品说明书操作。
1.2.3 所提取DNA质量检验及浓度计算
取DNA样品10 µL,用ddH2O缓冲液稀释至20倍,用紫外分光光度计测定230、260及280 nm波长的吸光度值(A),依据A260计算金柑总DNA的浓度,1个单位的吸光度值相当于50 μg/mL双链DNA,对照为ddH2O,依据260 nm的吸光值分别与230 nm和280 nm的吸光值的比值A260/230和A260/280计算DNA纯度。取5 μL稀释20倍的DNA样品,加入1 μL溴酚蓝指示剂,用1%琼脂糖凝胶,110 V恒压电泳,20 min后,EB染色后拍照,分析基因组DNA的质量。
1.2.4 SCoT分子标记验证提取效果
以3种提取方法所获得的DNA为模板,采用SCoT引物SCoT22进行PCR扩增,以检测3种DNA提取方法的效果。SCoT22序列信息来自LUO C等[12]的文献,金柑的SCoT-PCR扩增反应体系参照LUO C等[13]的方法。扩增反应结束后,取10 µL扩增产物,经2%琼脂糖凝胶电泳、染色、拍照分析。
2 结果与分析
2.1 紫外分光光度计检测结果
用3种方法提取金柑叶片和果实总DNA的结果表明(见表1),3种方法均可有效获取金柑叶片和果实总DNA,但在纯度和产率上有差异。采用CTAB法和试剂盒法提取的金柑叶片和果实总DNA其A260/280比值分别在1.87~1.90和1.82~1.84区间内,表明RNA和蛋白质等大分子物质的干扰极少,2种方法均可以较好地去除大分子物质,DNA纯度较高;采用SDS提取法所提取DNA的A260/280比值在1.85~1.94区间内,部分比值大于1.9,且金柑果实DNA的A260/280比值在1.87~1.94区间内,说明仍有RNA等大分子残留,且金柑果实DNA中残留的RNA等大分子物质多于金柑叶片DNA。采用CTAB法和试剂盒法提取的金柑叶片和果实总DNA,其A260/230比值在1.99~2.03和2.01~2.04区间内,表明试剂盒提取法和CTAB提取法除去小分子、盐和酚类物质等杂质的能力较理想,且试剂盒提取法提取效果更好;采用SDS提取法其A260/230比值在1.89~2.03区间内,采用SDS提取法所提取金柑叶片DNA的A260/230比值在2.00~2.03区间内,而提取金柑果实DNA的A260/230比值在1.89~1.95区间内。整体而言,SDS提取法除去小分子、盐和酚类物质等杂质的能力比CTAB提取法和试剂盒提取法弱,SDS提取法除去金柑叶片DNA中小分子、盐和酚类物质干扰的能力比除去金柑果实DNA中小分子、盐和酚类物质干扰的能力强;就总DNA的得率而言,SDS提取法提取总DNA得率最高,试剂盒提取法提取总DNA得率最低。尽管CTAB提取法提取DNA得率不是最高,却是能够从金柑叶片和果实中提取到符合纯度标准总DNA的较好方法。

表1 不同方法提取不同金柑品种叶片及果实DNA的结果比较†Table1 Comparison of extracted DNA in different cultivars of F. swingle leaves and fruits by different methods
2.2 琼脂糖凝胶电泳检测结果
DNA的完整性、纯度和DNA产率是判断DNA质量的主要标准。将提取液稀释20倍,取8 μL DNA稀释液,进行琼脂糖凝胶电泳(见图1)。3种DNA提取方法均可以获得完整性较好的DNA,SDS提取法和CTAB提取法所提取的DNA条带亮度远大于试剂盒提取法所获得DNA条带亮度,这与表1中产率结果相一致(产率越高,亮度越大),说明SDS提取法和CTAB提取法提取金柑叶片和果实总DNA可以获得较高的DNA产率;SDS提取法提取的金柑果实总DNA点样孔存留少量杂质,说明有蛋白质存留,还存在少量RNA;3种方法提取的金柑叶片和果实DNA,带型清晰整齐,表明其质量较高,可用于开展后续的试验,但哪种方法更理想,还须采用SCoT-PCR进一步检验。
2.3 SCoT扩增反应检测结果
分别用SDS提取法、CTAB提取法和试剂盒提取法提取的金柑叶片和果实总DNA为模板,用SCoT22进行SCoT-PCR扩增(见图2)。采用3种方法所提取的金柑叶片和果实总DNA均可以扩增出多态性丰富、层次感分明的多态性条带,但以试剂盒提取法提取的总DNA模板进行SCoTPCR扩增所得琼脂糖电泳图谱多态性条带亮度偏低,背景色浅,SDS提取法和CTAB提取法提取的总DNA进行SCoT-PCR扩增效果比较理想,多态性高,凝胶电泳图谱清晰,多态性强,易于统计分析。对3种提取总DNA方法进行比较分析可知,SDS提取法和CTAB提取法提取总DNA效果较好。
3 结 论
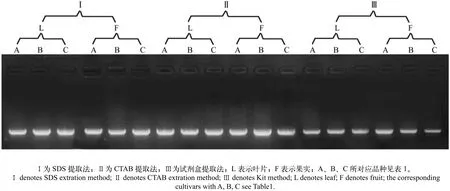
图1 3种方法提取金柑叶片和果实DNA的电泳结果比较Fig.1 Comparison of electrophoretic results of extracted DNA in F. swingle leaves and fruits by different methods

图2 3种方法提取的DNA为模板的SCoT-PCR电泳结果比较Fig.2 Comparison of electrophoretic results of SCoT-PCR with the extracted DNA by three methods as templates
由A值和DNA得率可知:3种提取方法中,试剂盒提取法除去杂质的能力最强;就总DNA的得率而言,SDS提取法提取总DNA得率最高;3种提取方法的综合比较结果表明,尽管CTAB提取法提取DNA得率不是最高,却是能够从金柑叶片和果实中提取到符合纯度标准总DNA的较好方法。SCoT扩增效果显示:SDS提取法和CTAB提取法提取总DNA的SCoT-PCR扩增效果较好。分析比较3种检测方法可以得出,CTAB提取法是提取金柑叶片和果实组织总DNA的最优选择。
4 讨 论
金柑叶片和果实富含蛋白质、糖类、酚类、单宁及色素等次生代谢物质,这些物质是影响提取高质量总DNA的关键因素。因此,采用普通的SDS法和CTAB法提取金柑叶片和果实总DNA效果有可能不理想。笔者在SDS提取液和CTAB提取液中加入了PVP-40和β-巯基乙醇,在液氮中研磨样品时,样品经过机械破坏,大量的植物细胞破碎,提取液中的PVP可以充分络合干扰DNA提取纯度的酚类物质,阻止酚类物质进行电位氧化还原反应生成醌类物质,醌类物质极易与氢键络合,引起总DNA氧化褐变;β-巯基乙醇可以破坏蛋白质的肽链,使得肽链断裂,从而降解蛋白质,同时抑制多种氧化酶的活性;多糖物质常与总DNA同时沉淀形成白色胶粉,影响总DNA纯度与后续试验的进行,在CTAB提取法和SDS提取法操作流程中均使用了提取试剂②(饱和酚、氯仿、异戊醇体积比25∶24∶1),该提取试剂可有效去除多糖的干扰[14-16]。观察图1可知,SDS提取法点样孔残留微量蛋白质,CTAB提取法和试剂盒提取法肉眼未观察到蛋白质残留,这有可能是因为在进行65 ℃水浴时CTAB提取液与蛋白质充分结合,不论从CTAB的浓度还是水浴时间来说,均满足CTAB提取液与蛋白质充分结合的条件,从而更大程度上抑制了PPO的活性,也有可能是因为提取试剂①(CTAB抽提液)较提取试剂③(SDS抽提液)能更彻底地去除蛋白质。由表2可知,尽管理论计算中SDS提取法提取的总DNA得率较高,但是从A260/230、A260/280可以看出,SDS法提取金柑叶片和果实总DNA还是有少量蛋白质残留,图1点样孔上有少量蛋白质残留痕迹,也印证了这点。金柑果实总DNA有少量RNA和其他盐类物质残留,但金柑叶片总DNA无残留,很有可能是因为金柑叶片和果实中多糖、多酚、蛋白质、单宁及色素含量以及比例组合不同而引起,因此推断SDS提取法更适合金柑叶片组织总DNA的提取。将3种提取方法提取的总DNA通过SCoT扩增均可以得到适合后续PCR试验要求的金柑叶片和果实总DNA,但SDS提取法和CTAB提取法所提取的总DNA的扩增效果图谱清晰、多态性高;而试剂盒提取法所提取的金柑叶片和果实总DNA的扩增效果图谱背景偏浅、条带较模糊,这很可能是因为试剂盒提取法在较彻底除去杂质干扰的同时也损失掉了较多的总DNA,由于总DNA浓度相对偏低,使得PCR扩增条带不如其他2种提取方法所提取的总DNA扩增条带明亮。笔者选用的3种方法均能够提取出金柑叶片和果实总DNA,但3种方法所提取的总DNA产率和纯度存在差异。其中CTAB法能够较好地除去多糖、多酚、单宁、色素以及蛋白质等杂质,提取的DNA纯度最高,产量也较理想,可以获得高质量的金柑叶片和果实总DNA,可用于开展分子标记、品种鉴定、遗传图谱构建等分子生物学相关工作的研究[17-20]。但是本研究也存在一定的局限性,如:高产率和高质量总DNA的提取不能集中在同一种方法上,效果较理想的方法却存在需要消耗更多的时间成本等问题。要克服上述研究的局限性,需更精致的实验设计、更多的研究工作量以及较大量的实验数据支撑来解决。
[1] 黄桂香,何 静.金柑优质高效栽培[M].北京:金盾出版社, 2006.
[2] 卓春宣.2006年福建金柑鉴评结果分析及其对策[J].福建果树,2007(3):19-20.
[3] 黄桂香,郭丽英,张树伟,等.中越金柑种质资源的ISSR分析[J].果树学报,2011,28(4):563-567.
[4] 施维属,钟凤林,李开拓,等.福建柑橘类种质资源ISSR分子评价[C]//中国园艺学会果树专业委员会.第二届全国果树分子生物学学术研讨会.南京: 中国园艺学会果树专业委员会,2009.
[5] 张连峰,何 建,冯 炎,等.金柑属及其近缘属植物亲缘关系的SSR分析[J].果树学报,2006,23(3):335-338.
[6] 张 宇,唐志鹏,邓海燕,等.富含多糖多酚芒果果肉组织总RNA的提取[J].湖南农业大学学报(自然科学版),2009,35(6): 637-639.
[7] 张丽杰,王玉霞,郜亚婷,等.平邑甜茶基因组DNA提取方法的比较[J].经济林研究,2012,30(1):114-117.
[8] 原勤勤,文亚峰,刘 儒,等.枣优良品种亲缘关系的ISSR分析[J].经济林研究,2012,30(1):56-61.
[9] 彭继庆,曹福祥,范海燕.博白大果油茶遗传多样性的ISSR研究[J].中南林业科技大学学报,2013,33(7):62-66.
[10] 张 宇,黄国弟,唐志鹏,等.芒果总DNA提取方法比较分析[J].经济林研究,2014,32(2):62-65.
[11] 井赵斌,徐 明,雷玉山.猕猴桃SRAP-PCR体系的建立及品种资源亲缘关系研究[J].园艺学报,2016,43(2):337-346.
[12] LUO C, HE X H, CHEN H, et al. Analyis of diversity and relationships among mango cultivars using Start Codon Targeted(SCoT) markers[J]. Biochem Syst Ecol, 2010, 38:1176-1184.
[13] LUO C, HE X H, CHEN H, et al. Genetic diversity of mango cultivars estimated using SCoT and ISSR markers[J]. Biochem Syst Ecol, 2011, 39:676-684.
[14] Dreher M L, Davenport A J. Hass avocado composition and potential health effects[J]. Critical Reviews in Food Science and Nutrition, 2013, 53(7):738-750.
[15] Kilaru A, Cao X, Dabbs P B, et al. Oil biosynthesis in a basal angiosperm: transcriptome analysis of Persea americana mesocarp[J]. BMC Plant Biology, 2015, 15(1):203.
[16] 赵志常,陈业渊,高爱平,等.改良CTAB法提取番石榴总DNA的初步研究[J].北方园艺, 2013, 9(1):123-125.
[17] 杨合宇,李发根,翁启杰,等.KingFisher Flex核酸纯化系统上树木叶片DNA的提取方法[J].分子植物育种,2017,15(5):1854-1861.
[18] 周海兰,李绍鹏,李卫亮,等.油梨基因组DNA提取、SSRPCR反应体系优化及引物筛选[J].生物技术通报, 2016,32(4): 143-150.
[19] 崔 波,王若斓,张 燕,等.牡丹种子总RNA提取方法比较[J].分子植物育种,2017,15(5):1800-1805.
[20] 毛积鹏,祝文娟,王 博,等.火炬松总RNA提取方法的比较[J].分子植物育种,2016,14(8):2031-2035.
