不同分子量丝素肽的开发
2018-01-26徐国文
钱 坤,刘 迪,徐国文
(1.湖州师范学院,浙江 湖州 313000; 2.浙江大学 动物科学学院,浙江 杭州 310058;3.湖州新天丝生物技术有限公司,浙江 湖州 313000)
蚕丝是人类最早利用的天然蛋白质纺织纤维材料之一,享有“纤维皇后”之美誉。具有良好的吸湿性和优雅的光泽,丝绸服装穿着舒适、优美、典雅,对人体有良好的保健功能,深受国内外消费者喜爱。随着对蚕丝结构研究的不断深入,其开发利用的研究领域也不断的拓宽,逐渐延伸到食品、发酵、生物制药、工业新材料、医用材料及化妆品等领域,并呈现出蓬勃发展的态势。蚕丝蛋白在食品、新型保健品的应用更是雨后春笋般的发展。丝素肽作为小分子肽更容易被人体吸收,更适合在保健食品上的开发与应用[1~3]。丝素是一种天然的大分子纤维蛋白质,分子量在30万±0.5万道尔顿。用生物化学工程法精加工成分子量500~5000(d)的可溶性丝素肽,可作为食品工业、医药工业、化妆品工业的特殊营养添加剂[4]。制取丝素肽的原料可用缫丝、织绸中的下脚料,经脱胶净化等加工成纯丝素。蚕丝纤维的主要成分是丝胶和丝素,另外还有少量的蜡质层,碳水化合物,色素,无机成分,一般蚕丝含丝素70%~80%,丝胶25%左右,其它物质2.5%左右。(茧衣中丝胶含量有40%~42%丝素含量相对较低),丝素蛋白属于硬蛋白,与皮肤表层,毛发角蛋白属同一大类,丝素蛋白的分子量最大达30万±0.5万道尔顿。丝素为纤维状结构,每根茧丝由两种平行单丝黏合而成,每根单丝中间为丝素纤维,外为丝胶,丝素纤维的断面积平均为80μ2,每根丝素纤维由50~100根细纤维经丝胶黏合而成。细纤维又由径为10μ的微纤维组成,而微纤维由蛋白质分子构成[5]。
丝素蛋白中的各种氨基酸由肽键(-CONH-)联结成肽链,再通过肽键、氢键、酯键、盐键、二硫键等构成蛋白质。丝素纤维的蛋白质结构分为结晶区、非结晶区,每个结晶区和非结晶区都会有若干条肽链的链段,而每条肽链都要通过若干个结晶区和非结晶区,结晶区主要由甘氨酸、丙氨酸和丝氨酸组成,比例大致为3∶2∶1,甘氨酸和丙氨酸总量占70以上,而非结晶区主要由酸性氨基酸、碱性氨基酸、脯氨酸、酪氨酸等组成[6]。根据丝素纤维蛋白的结构特点,可以采用不同的方法,使高分子量的丝素,转变成分子量较低可溶于水的多肽。在酸碱溶液、氯化钙中性溶液中,由于H+、OH-、Ca2+、Cl-等极性离子的作用,水分子不仅进入丝素的非结晶区,而且进入结晶区,削弱了分子链间的范德华力,使丝素分子从紧密状态变成疏松无序状态,无限膨润分解。分子量下降到10×102~10×102的多缩氨酸。丝素肽的分子构象为无规卷曲结构为主,这使具有优良的水溶性,可以在不添加任何乳化剂、分散剂情况下,按任意比例与其它水溶性原料掺和,同时又保持了平衡状况下各类氨基酸。
现介绍将分子量在30万±0.5万、结构比较复杂,一般情况下人体难于消化吸收的丝素转变成由平均分子量为90的氨基酸及由5个至6个直至100个左右构成的多肽类物质,以及单一氨基酸的复合物,可以采用强酸、强碱、中性盐和酶等降解剂予以消化。
1 中性盐法制备丝素肽
按照氯化钙∶水∶丝素=1∶2∶5,即100 g丝素(干)200 g CaCl2(试剂级),500 m l水(纯水)配方,先将CaCl2溶于水成溶液,加温至沸110℃±2℃时,投丝素(105℃可投),100 min内,在搅动情况下就会全部溶解,加入少量(1左右)纯水,冷却后,装入透析袋透析。由于半透膜的盐渗析作用,72 h内,可将绝大部分Ca2+、Cl-带走,而剩下丝肽蛋白此时的平均分子量一般为10000 D左右,此方法所得产品平均分子量较大,水溶性很好,色泽为纯白色,可在塑袋真空装下。
上述获得的丝肽,再经碱或酶降解,就可得平均分子量较低的丝肽,如表1、表2所示。
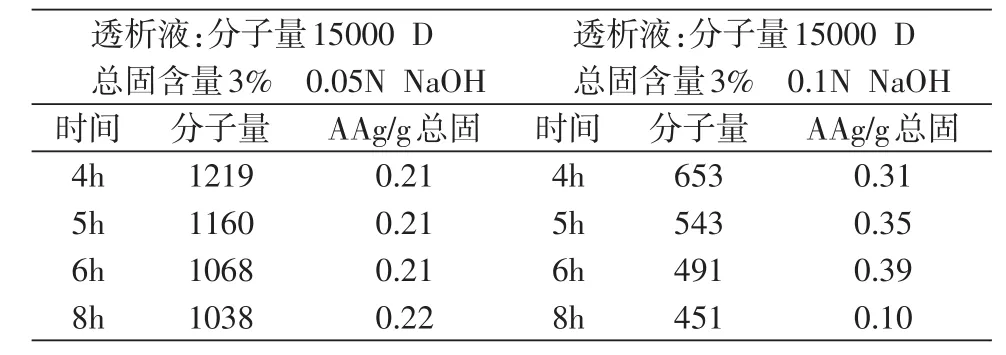
表1 不同浓度氢氧化钠(0.05 N~0.1N)的碱解结果
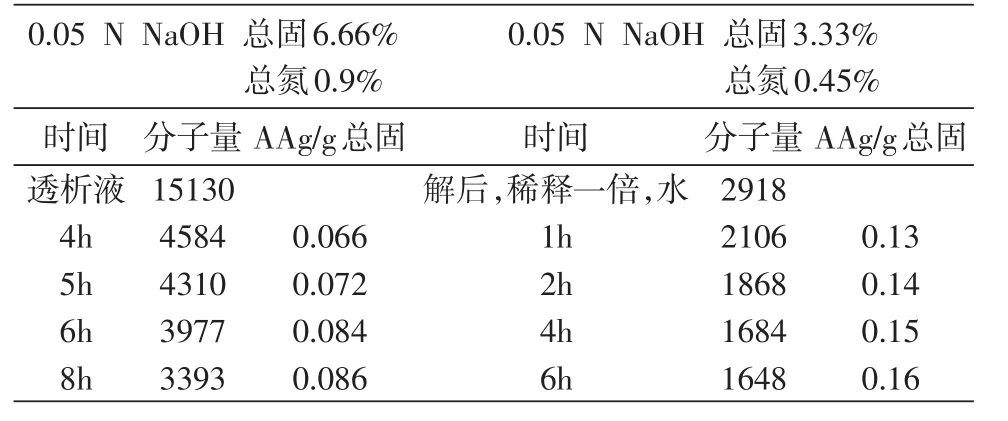
表2 不同浓度氢氧化钠(0.05N)的碱解结果
经透析水解液用胰酶进一步降解,那么丝肽的质量更好。因为采用NaOH,必须用中和法除去,加了丝肽中盐分的含量,往往使灰分达不到规定指标。
胰酶的降解需掌握以下条件,当丝素的中性盐水解液,经半透膜渗析除盐72 h~90 h后,一般Ca2+Mg2+的含量在<80 mgN/升氯根<80 mgN/升,(2 mg~3 mg当量)。灰分能达规定指标要求。此时将透析液煮沸后,测总固含量,再按总固量加0.1%~0.5%的胰酶(先用氨水调水解液pH 7.5~8)。40℃±2℃下恒温2 h~4 h不等。再升温失活,加活性炭脱色(活性炭量视液体色泽而定,色浅也可不加活性炭)然后浓缩,喷粉,可得成品。
蚕丝蛋白在分解反应过程中,由于酶的作用,微量氨基酸分子结构发生断裂,即蚕丝蛋白中的微量丙氨酸(ɑNH丙酸)、丝氨酸(ɑOH丙酸)、胱氨酸(ɑNHßSH丙酸)的COOH等基团产生了裂解转位,从而会形成微量丙酸基团。当然,酶解浓度、时间的变化都会对裂解的效果产生影响。所产生的丙酸含量大约在10 mg/kg~100 mg/kg左右。
2 中性盐-乙醇法制备丝素肽
有文献[7~9]介绍采用CaCl2-C2H5OH溶液溶解丝素的方法,其比例为氯化钙∶乙醇∶水=1∶2∶8(M比,即摩尔比),而丝素与以上三元溶液的浴比为1∶50和1∶25。我们根据自己的经验,列出如下表(表3),再行选择。
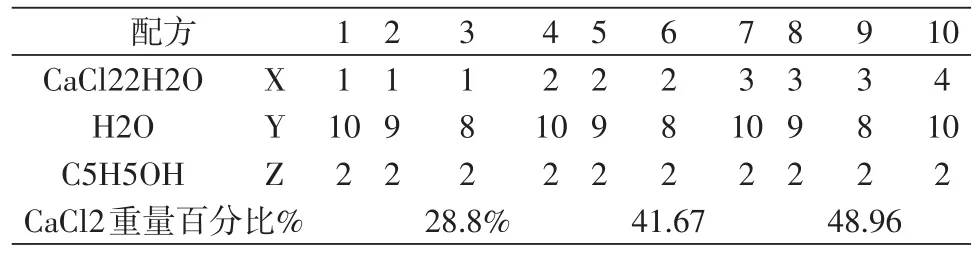
表3 采用三元溶液配方表(丝素浴比为1:8)
1 mol CaCl2为 146 g,1mol H2O 为 18 g,1 mol C2H5OH为46 g。取3号配方及1∶8浴比进行实验室试验:取净化毛丝丝素160g。氯化钙=水∶乙醇=146∶144∶92=38.2%:37.7%∶24.1%。故此,需CaCl22H2O 160×8×38.2%=489 g,需H2O483g和乙醇308 g。由于乙醇为95%浓度,已含水23 g,所以实际需水460 g和乙醇331 g(95%含量)。以上配成三元溶液计1280 g,水浴加热至70℃投入丝素,在70℃±2℃的条件下进行水解,1.5 h左右溶解,再经2h水解。水解时要装乙醇回流装置,防止乙醇浓度降低。然后扎带用透析包透析,除盐后过滤测总固,经中科院上海昆虫所采用凝胶电泳法检测,其分子量峰值集中在48000 D~67000 D,以后再采用此法连续投料,得透析液,采用喷雾干燥,得白色丝肽粉。所以,采用以上工艺可以生产50000 D~70000 D高分子丝肽。
3 酸、碱水解法制备丝素肽
我们重点选用硫酸和氢氧化钡、氢氧化钙,因为硫酸钡的溶解度极低,并且可以用离子交换732树脂除去部分钙、镁离子,使成品的灰分降到标准以下。BaSO4在纯水中,25℃时溶解度为1.04×10-5M(摩尔/升),或为2.8 mg/L,CaSO4在25 ℃时在纯水中溶解度为7.8×10-3摩尔/L(1摩尔BaSO4171 g,1摩尔CaSO4136 g,171×1.04×10-5=0.0017784 g/L,136×7.810-3=1.0608 g/L)。如果在常温下用硫酸或用氢氧化钡相互中和后,在溶液中所含BaSO4的量为0.0018 mg/L,而含量为10%丝肽液1000 L,可喷100 kg粉,内可能含BaSO4为0.0018×1000=1.8 g,只占1.8 g/100 kg,即十万分之一点八克。而同样用Ca(OH)2中和H2SO4,在常温下溶液所含硫酸钙的浓度为1.0608×1000=1061 g,即1.061 kg/100 kg。
这只是理论计算,在实际操作中,由于中和过滤温度较高含量还会增加。
用盐酸酸水解制备丝素肽的方法,例如,采用3 N~4 N盐酸,按1∶3浴比对丝素进行16 h~18 h水解,然后用减压去酸办法,除去部分盐酸,再用碱中和至pH 5~7。但内含氯化钠量较多,虽用活性炭脱色,可得淡黄丝肽液,但含量较低,质量较差,无法制成固体粉末。改用硫酸代替盐酸用15%~22%硫酸,不完全水解丝素。经过15 h~18 h,再用氢氧化钡或氢氧化钙中和除去硫酸,可得丝素肽液体,经脱色过滤离子交换发脱灰生产液态丝素肽,或喷粉成固体。如将以上水解液测总固后,再用胰酶水解成分子量较低的丝素肽。
22%H2SO4回流水解22 h,然后用Ba(OH)28H2O中和至终点(pH 5.33~5.5)搅0.5 h,板框压滤,滤液得淡黄色滤液,测含固(投111 kg净干,得860 L脱色液,含固0.06033 g/ml,共得51.63 kg,Mn132)。采用732~717树脂纯化,去除重金属,各0.5 h,即可得低分子量的丝肽。
总之,利用蚕丝丝素,经生物化学法,精加工生产分子量为500 D~10000 D的系列丝素肽,作为食品、化妆品、医药材料的重要原料,从而可将废蚕茧丝低值原料加工为高附加值产品。
