氨茶碱药物代谢动力学实验研究
2018-01-24霁阳
李 霁阳 剑*张 源
(1 昆明医科大学药学院暨云南省天然药物药理重点实验室,云南 昆明 650021;2 昆明医科大学第一附属医院骨科,云南 昆明 650032)
药代动力学是药学、药物制剂、临床药学等专业的主干专业课程之一,广泛应用于新药筛选、制剂研究和药物质量评价、临床合理用药等方面,是一门实践性很强的课程[1-2]。药物代谢动力学实验是教学的重要组成部分,是理论与实践结合的主要方式之一,我校主要是临床药学专业开设了药代动力学实验课。其中“氨茶碱在兔子体内药代动力学研究”中药动参数的测定是主要的实验内容之一,对于学生理解并掌握通过血药浓度的测定来获取药物的药动参数具有重要的指导意义,实验内容包括血样的采集、样品前处理、血药浓度的测定及实验数据处理。在实验带教过程中,笔者认为在检测过程中,当选择274 nm作为检测波长时,血中的内源性成分在该波长处有吸收,对测定有干扰,有必要选择更为合理的测定方法,使测定结果更为准确合理;此外实验中使用5%异丙醇-氯仿作为提取溶剂,对人体毒性大且污染环境,需要寻找一种能够满足氨茶碱药代动力学研究要求,替代氯仿,安全的提取溶剂。因此经过分析、查阅资料、预实验,对实验方法进行了改革,改革后的实验方法结果重现性好、准确度高,提取回收率较高,能够满足氨茶碱药代动力学实验要求,且无毒无害,适合学生教学实验。现报告如下。
1 氨茶碱药代动力学研究的实验现况
我校采用的药代动力学实验讲义中,氨茶碱在兔体内药代动力学研究是通过给家兔耳静脉给药注射用氨茶碱后耳静脉取血,使用5%异丙醇-氯仿对血样进行液液萃取前处理后采用紫外分光光度法在274 nm处测定血药浓度,然后进行数据处理:绘制药时曲线、将测得的血药浓度代入药动公式求算消除速率常数K、半衰期t等药动参数。实验内容包括血样的采集、血样的前处理、血药浓度的测定及实验数据处理。其中生物样品前处理和血药浓度测定是本实验的重要内容,涉及到后续测定是否准确合理。
目前氨茶碱的含量测定方法主要有紫外分光光度法[3-4]HPLC法[5-6],因紫外分光光度法操作简捷、结果准确、专属性强、仪器价格便宜而被广泛用于学生实验中。在以前设计的实验中,选择紫外光274 nm下测定氨茶碱血药浓度,使用5%异丙醇-氯仿进行液液萃取,实验得率高,现性好,但最主要的问题血中内源性成分在274 nm下有吸收,容易产生干扰,使结果不够准确;此外提取溶剂氯仿毒性大,对心、肝、肾有损害,吸入后容易中毒,在学生实验中使用不合适,为此需要改进检测方法,提高方法的准确性,并且寻找到提取率能够满足氨茶碱药代动力学研究的、合适的提取溶剂,从而替代氯仿。
2 改革后的实验方法
2.1 家兔空白血的采集 取体重3 kg左右家兔1只,耳缘动脉取血或心脏取血20~80 mL,置于加有肝素的10 mL具塞离心管中,离心 (3000 rpm/min)10 min,取血清供标准曲线制备用。
2.2 标准曲线的制备 取氨茶碱标准品,精密称量以0.1 mol/L NaOH溶液配成500 mg/L的贮备液。另取试管5支,各加入0.5 ml空白血清,然后依次加入上述贮备液4.0 μL、8.0 μL、12.0 μL、16.0 μL、20.0 μL,各加入0.1 mol/L NaOH溶液至4.0 mL,其浓度分别为0.5 μg/mL、1.0 μg/mL、1.5 μg/mL、2.0 μg/mL、2.5 μg/mL的标准液。按生物样品前处理,用紫外分光光度计在波长274 nm及波长298nm处测定吸收度A274、A298(以空白血清按生物样品前处理后作空白对照)以吸收度差△A(A274-A298)对含药量C进行线性回归,结果见图1。
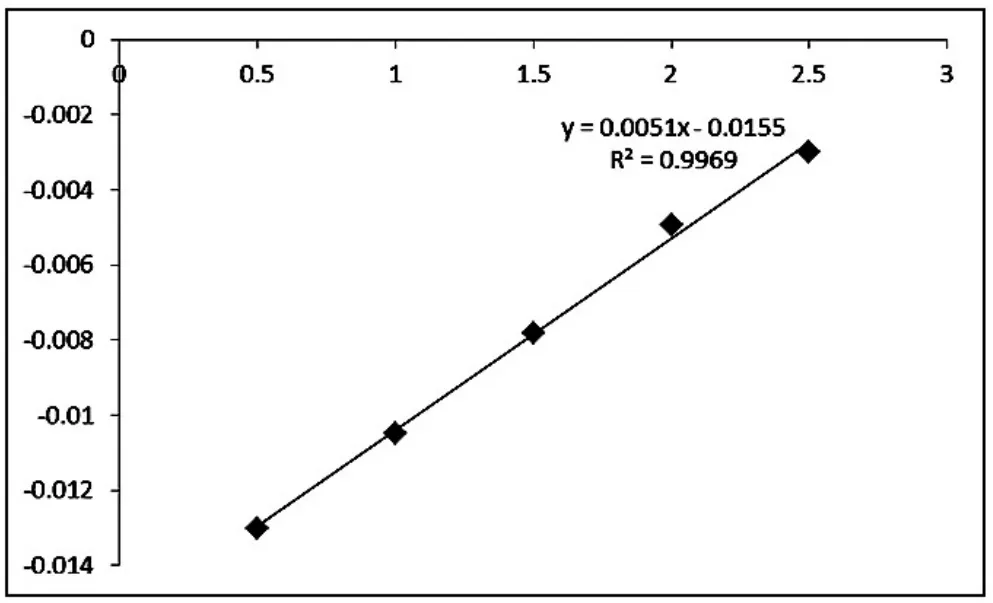
图1 氨茶碱标准曲线
2.3 生物样品前处理 取血清样品0.5 mL置试管中,加0.1 mol/L盐酸溶液0.2 mL,乙酸乙酯液5 mL,振摇混合,离心(3000 r/min) 10 min。吸取乙酸乙酯4.0 mL置于另一试管中,加入0.1 mol/L NaOH溶液4.0 mL,混匀,离心10 min,吸取碱液(上层)3~3.5 mL,用紫外分光光度计,测定碱液在波长274 nm和波长298 nm处的吸收度A274、A298。
2.4 稀释效应 考虑到氨茶碱静注给药血清样品浓度高,需用兔空白血清稀释,以满足氨茶碱的血清标准曲线线性范围。由预试验结果可知,部分兔血清样品需要稀释,稀释倍数为5、25倍。因此,需要考察氨茶碱血清样品的稀释效应。由于将血清样品直接稀释25倍会引入较大的操作误差,因此本实验操作将高浓度血清样品先稀释5倍,再将稀释5倍后的血清样品稀释5倍,由此得到稀释25倍的血清样品。
为此,血清样品的稀释效应考察方法如下:配制成浓度为10.0 μg/mL的氨茶碱标准血清样品,分析前样品保存于20℃,分析时将其稀释5倍,得到浓度为2.0 μg/mL样品,按上述氨茶碱血清样品预处理步骤操作并进样分析,所得氨茶碱吸光度差值△A代入随行标准曲线,计算相应浓度,乘以相应的稀释倍数即获得高浓度血清样品的实际测定浓度,通过与标准添加浓度相比较,计算其百分回收率与RE值,结果见表1。
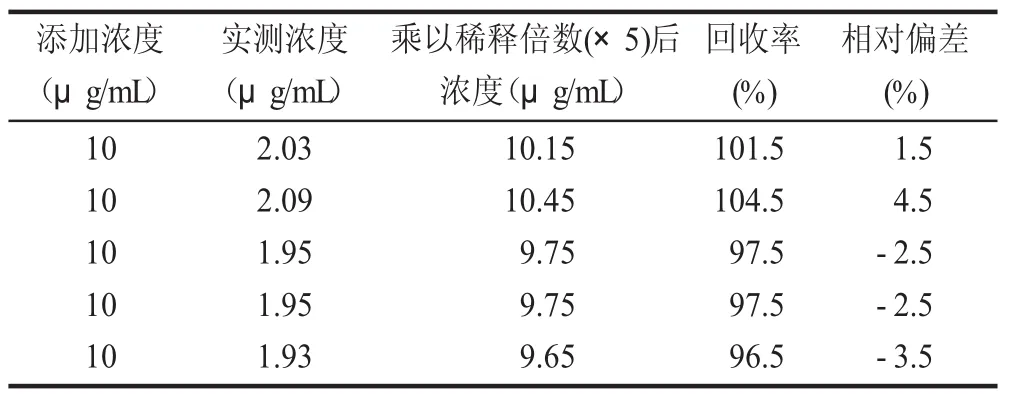
表1 氨茶碱稀释效应考察 (n=5)
2.5 家兔体内血药浓度的测定
2.5.1 血样的采集 选用雄性家兔称重,按10 mg/kg剂量给药,以5%葡萄糖溶液稀释氨茶碱注射剂10倍,由耳静脉给药(2 min内注完)。然后分别于0.167 h、0.25 h、0.5 h、1 h、2 h、3 h、4 h、6 h、8 h、10 h、12 h、24 h取血约2 mL(另一耳静脉取血)。分离血清(试管不涂肝素,静置,离心2000 rpm),备用。按生物样品前处理,用紫外分光光度计在波长274 nm及波长298 nm处测定吸收度A274、A298,计算吸收度差△A后,代入标准曲线方程得到氨茶碱血药浓度。
2.6 实验数据处理 绘制药时曲线,将测得的血药浓度代人药动公式求算消除速率常数K、半衰期t等药动参数。
3 结果
用改进后的实验方法进行实验,测得血药浓度数据见表2,绘制的药时曲线见图2。由实验结果可知,测得的血药浓度数据符合对氨茶碱在家兔体内的代谢情况,与静脉给药药-时曲线的规律一致,且在实验过程中发现改进后的方法对血样进行处理后所得的样品澄明,血药浓度测定结果稳定,重现性好。

表2 血药浓度测定结果
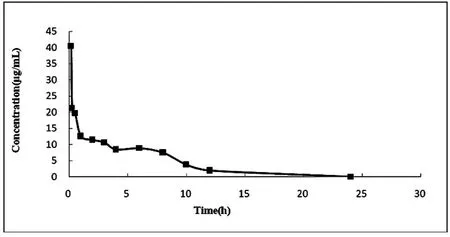
图2 血药浓度-时间曲线
4 讨论
4.1 实验特点 本实验在生物样品前处理过程中使用乙酸乙酯作为萃取溶剂来替代原先使用的萃取溶剂5%异丙醇-氯仿,提取回收率较高,满足药动学实验需要。此外使用两点校正法测定并计算血药浓度,较之前在274 nm测定血药浓度,该方法更加准确,能够扣除血样中其他内源性杂质的干扰,血药浓度测定结果稳定,重现性好。实验无毒无害,适合学生操作。

表2 改革前后实验比较
4.2 实验收获 本次实验各项工作包括文献查阅、实验方案设计到实际操作、仪器使用、数据处理等多项工作都是笔者带领学生完成,学生在参与本次实验改革中,熟练掌握了查阅国内外文献的方法,了解了科学研究的基本思路与流程,加深了对药物动力学基本理论知识的理解,掌握了相关仪器的使用以及获得较强的数据处理能力。实验过程中,学生充分利用数据库资源,在实验中遇到的相关问题能够通过查阅文献,设计、改进实验,有效激发了独立思考,对于培养学生独立分析、解决实际工作中出现的问题及动手能力有很大的帮助。实践证明,本次实验改革,相对于以前的实验课程,增加实验的科学性和合理性,让学生更深层地理解了药代动力学实验的过程、意义,实验结果更为准确合理,试剂对环境和人体无害,适合学生教学实验。
[1]缪明星,刘晓东,刘李,等.基于创新能力提升的药代动力学实验教学平台[J].药学教育,2015,31(6):51-54.
[2]桂卉,李美云,周江,等.血药浓度法测定乙酰氨基酚片生物利用度的实验教学改革[J].中国中医药现代远程教育,2015,13(7):95-96.
[3]黄先菊,高林,马玲.紫外分光光度法检测氨茶碱在家兔中的血药浓度[J].湖北省卫生职工医学院学报,2004,17(3):80-83.
[4]张国宏,潘丽春,赵婧岚.磺胺甲口恶唑对紫外分光光度法测定氨茶碱血药浓度的影响[J].广西医学,2005,27(12):1924-1926.
[5]周明神,陈秋展,付婴子,等.氨茶碱在大鼠体内的药代动力学研究[J].化学与生物工程,2011,28-(10):72-74.
[6]田淑艳,艾德华,焦旭阳,等.氨茶碱在家兔体内的药代动力学研究[J].求医问药,2012,10(7):188-189.
