黑曲霉所产α-L-鼠李糖苷酶酶学性质及其在异槲皮素制备上应用
2018-01-22,,,,,*
,,, , ,*
(1.南昌大学资源环境与化工学院,江西南昌 330031;2.南昌大学化学学院,江西南昌 330031;3.中德联合研究院,江西南昌 330047)
黄酮类化合物广泛存在于自然界,是大多药用植物的有效成分,普遍具有抗炎抑菌、抗病毒、抗氧化、抗肿瘤、抗辐射和免疫调节等多种活性,是国内外天然药物开发利用的研究热点[1-2],但是多数黄酮苷元或黄酮苷类在水相中溶解度低,大大限制了其药物制剂的开发,目前国内外主要通过去糖基化,对黄酮类化合物进行分子修饰以提高其在水相中的溶解性。对于复杂结构的天然活性成分,利用化学合成来进行结构修饰存在着得率低、反应专一性差、副产物多等缺点,特别是有些反应目前利用化学手段较难实现。而生物转化技术却可弥补化学合成的不足,已经报道许多研究人员筛选出来产α-L-鼠李糖苷酶的菌株[3-5],这种酶可以将一些黄酮类化合物的末端糖基去掉以增加黄酮类化合物的水溶性和稳定性,降低其细胞毒性[6]。
α-L-鼠李糖苷酶是一种水解末端鼠李糖糖苷的水解酶类,能高效、专一水解α-1,2、α-1,3、α-1,4、α-1,6位连接的糖苷键,可应用于水解部分黄酮类化合物。α-L-鼠李糖苷酶来源广泛,分布于动物组织[7]、植物[8]、微生物[9-10]中。目前国内对微生物产α-L-鼠李糖苷酶的研究,主要集中在黑曲霉[11-13]上;国外研究主要涉及的菌种有黑曲霉、棘孢曲霉、白曲霉、青霉菌、土曲霉、构巢曲霉、热微菌门和拟杆菌属等[14-16]。
作者采用实验室前期筛选的1株黑曲霉[17]进行液态发酵生产α-L-鼠李糖苷酶,通过简单的硫酸铵盐析,膜透析即可获得α-L-鼠李糖苷酶的粗酶液,同时对该粗酶液的酶学性质进行深入探讨。后期该粗酶液对芦丁进行去糖基化得到异槲皮素(Isoquercitrin),同时对产物进行了结构分析。
1 材料与方法
1.1材料与仪器
黑曲霉 实验室筛选菌株;芦丁标准品、异槲皮素标准品 HPLC≥98%,上海源叶生物有限公司;酵母提取物、蛋白胨 美国OXOID公司;琼脂粉、三羟甲基氨基甲烷(Tris)、十二烷基硫酸钠(SDS) solarbio公司;甘氨酸、透析袋 Acros公司;考马斯亮蓝R-250、SDS上样缓冲液、蛋白质marker(200 kDa) Takara公司,其他常规试剂均为国产分析纯。
SPD-15C型高效液相色谱仪 日本岛津有限公司;TGL-16C型离心机 上海安亭科学仪器厂;M3型电热循环水浴锅 德国LAUDA公司;mLS-3750型灭菌锅 日本SANYO公司;HWY-200型全温摇床 常州诺基仪器有限公司;SW-CT-1D型超净工作台 苏州净化设备有限公司;2720型PCR仪 美国ABI有限公司;DYY-10C型垂直电泳仪 北京六一仪器厂;Gel Doe XR型胶扫描系统 美国BIO-RAD公司。
1.2实验方法
1.2.1 培养基的配制 斜面培养基(g/L):KNO31.5,MgSO4·7H2O 1.0,KH2PO41.0,(NH4)2SO41.5,KCl 0.5,无水CaCl20.1,酵母膏2.0,芦丁2.5,琼脂15。初始pH6.0,121 ℃灭菌20 min,倒平板。
液体发酵培养基(g/L):KNO31.5,MgSO4·7H2O 1.0,KH2PO41.0,(NH4)2SO41.5,KCl 0.5,无水CaCl20.1,酵母膏2.0,芦丁2.5。初始pH6.0,121 ℃灭菌20 min。
1.2.2 菌株的培养 将黑曲霉接种斜面培养基上,于恒温培养箱中30 ℃培养5 d,待斜面上长满黑褐色孢子,用接种针挑取孢子,用0.9%的生理盐水洗涤数次,然后30 ℃振荡培养2 h,配成悬浊液,按体积分数10%的接种量接种于液体培养基中,30 ℃,200 r/min振荡培养5 d。
1.2.3 粗酶液的制备 取发酵液于4 ℃、3000×g离心10 min后,取上清液。缓慢取50 mL的上清液加入(NH4)2SO4粉末至其饱和度70%,边添加边搅拌,4 ℃静置过夜,然后4 ℃、8000×g冷冻离心20 min,得到的沉淀用一定体积HAc-NaAc缓冲液(10 mmol/L,pH5.5)溶解。置于透析袋中,4 ℃透析2 d,每隔4 h换一次透析液。透析完毕,取出透析液,所得到的袋内的透析液即为粗酶液。
1.2.4 酶蛋白分子量测定 采用SDS-PAGE法测定酶蛋白分子量。分离胶和浓缩胶浓度分别为10%和5%,上样量为20 μL。先用80 V电泳30 min,再用120 V电泳90 min。电泳结束后用考马斯亮蓝染色45 min,过夜脱色。
1.2.5 酶活的测定 分别配制0.2、0.4、0.6、0.8、1.0、1.2、1.4 mg/mL的异槲皮素标准液,用HPLC检测,记录峰面积,做异槲皮素的标准曲线。HPLC条件:分离柱为4.6 mm×250 mm Hypersil ODS 5 μm,流动相为 甲醇:0.1%三氟乙酸水溶液=40∶60,流速为0.5 mL/min,进样量10 μL,检测波长360 nm,柱温30 ℃。取pH5.5的HAC-NaAC缓冲液溶液2.0 mL于试管中,加入1 mL粗酶液,在40 ℃下水浴保温5 min,再加入2.0 mL 300 μg/mL的芦丁标准溶液,在55 ℃下水浴反应45 min后于沸水中灭活20 min,取出后迅速冷却至室温,用HPLC测定异槲皮素的峰面积,计算生成物含量。酶活定义,在上述条件,每分钟生成1 μg异槲皮素所需要的酶量定义为一个酶活(U/mL)。
1.3α-L-鼠李糖苷酶酶学性质研究
1.3.1 粗酶液的最适温度 取2 mL 10 mg/mL芦丁悬浊液,加入2 mL HAc-NaAc缓冲液(10 mmol/L,pH5.5)分别与1 mL粗酶液在30、35、40、45、50、55、60、65、70、75、80 ℃的温度条件下进行反应,反应45 min后,测定异槲皮素的含量,计算相对酶活,相对酶活=实际测得酶活/实验中最大酶活。根据相对酶活的大小,确定酶的最适反应温度。
1.3.2 粗酶液的热稳定性研究 分别取1 mL的α-L-鼠李糖苷酶分别置于20、30、40、50、60、70、80 ℃的条件下保温2 h后,取出与2 mL 10 mg/mL芦丁悬浊液和2 mL HAc-Nac缓冲液(10 mmol/L,pH5.5)进行反应,反应45 min后,测定异槲皮素的含量,比较酶经过不同温度处理后的相对酶活,确定其热稳定性。
1.3.3 粗酶液的最适pH 取2 mL 10 mg/mL芦丁悬浊液,加入2 mL HAc-NaAc缓冲液(10 mmol/L,pH5.5)分别与1 mL酶液在pH4.0、4.5、5.0、5.5、6.0、7.0、8.0的条件下进行反应,反应45 min后,测定异槲皮素的含量,计算相对酶活,确定酶的最适pH。
1.3.4 粗酶液的pH稳定性研究 分别取1 mL的α-L-鼠李糖苷酶分别置于pH2.0、3.0、4.0、5.0、6.0、7.0、8.0、9.0、10.0的条件下,静置2 h后,取出与2 mL 10 mg/mL芦丁悬浊液和2 mL HAc-NaAc缓冲液(10 mmol/L,pH5.5)进行反应,反应45 min后,测定异槲皮素的含量,计算相对酶活,比较酶经过不同pH缓冲液处理后的相对酶活,确定其pH稳定性。
1.4芦丁的酶转化反应及反应产物的分离纯化
1.4.1 芦丁的酶转化反应 称取0.50 g 芦丁制成40 mL的悬浊液,加入40 mL HAc-NaAc缓冲液(10 mmol/L,pH5.5)分别与10 mL的酶液混合,于55 ℃反应45 min后,用沸水终止反应。取反应液进行薄层色谱分析,并与芦丁标准品进行对照,展开剂比例为乙酸乙酯∶丙酮∶乙酸∶甲醇=5∶3∶1∶1。并用HPLC分别测定反应液中芦丁和异槲皮素的峰面积,计算芦丁的转化率。
1.4.2 产物的分离纯化 将反应液蒸干,于真空干燥箱过夜。硅胶经烘干预处理后干法装入层析柱(2.0 cm×50 cm)中,压紧。准确称取一定量的反应物粗提物溶解于少量的洗脱剂(洗脱剂比例为乙酸乙酯∶甲醇=8∶1)中,加到柱上方,再泵入洗脱剂进行柱层析。并开始计时、取样。TLC跟踪检测,进行分段收集。含有异槲皮素的洗脱液合并蒸干,测定含量,计算芦丁的转化率,转化率=转化的芦丁/总芦丁。
1.5产物的结构分析
取大约10 μg样品溶于1 mL色谱级甲醇中,振荡摇匀,交给南昌大学分析测试中心进行质谱分析(LC-MS,一级质谱);同时取10 mg样品(粉末状态)放在核磁管中,交给南昌大学分析测试中心进行1HNMR分析。2 d后返回质谱和氢谱结果,并结合谱图进行分析确认。
1.6统计分析
所有实验至少设3次重复,采用SPSS V21.0软件分析数据。数据表示为均值±标准偏差。
2 结果与分析
2.1酶蛋白分子量与酶活测定
2.1.1 酶蛋白分子量测定 根据文献报道α-L-鼠李糖苷酶的分子量在40~170 kDa之间[18-21],本实验采用SDS-PAGE方法测定粗酶液的分子量,如图1所示,泳道1为蛋白marker,泳道2为粗酶液,通过SDS-PAGE蛋白质迁移率实验计算得蛋白质分子量为58.1 kDa。
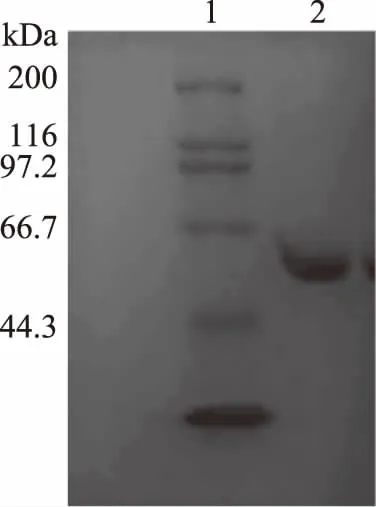
图1 粗酶的SDS-PAGE电泳图谱Fig.1 SDS-PAGE electrophoresis of crude enzyme.注:泳道1.蛋白marker;2.粗酶液。
2.1.2 酶活的测定 分别配制不同浓度的异槲皮素,利用HPLC测定各浓度异槲皮素的峰面积,根据峰面积与异槲皮素的浓度关系,做异槲皮素的标准曲线,如图2所示。反应结束后,用HPLC测定异槲皮素的峰面积,其峰面积为9.85×106,所以反应液中异槲皮素的浓度为0.798 mg/mL。通过计算得到粗酶液酶活为798 U/mL。
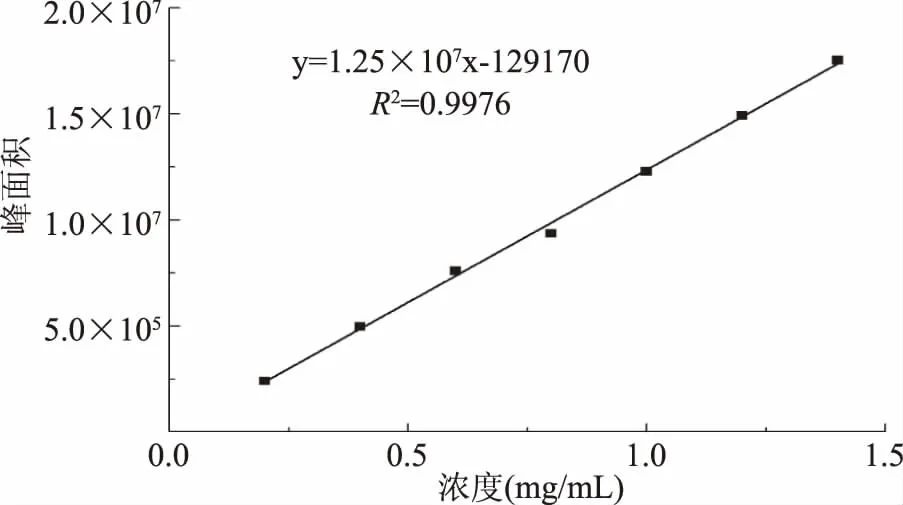
图2 异槲皮素的标准曲线Fig.2 Curve of isoquercetin
2.2α-L-鼠李糖苷酶酶学性质研究
2.2.1 温度对酶活的影响 酶催化的反应速率与温度密切相关,因此温度是α-L-鼠李糖苷酶酶学性质研究的重要因素。文献报道,不同来源的α-L-鼠李糖苷酶,其最适反应温度也各不相同,但多在30~60 ℃[19-23]。将纯化后得到的α-L-鼠李糖苷酶在不同温度(30~80 ℃)下进行酶活性测定,结果如图3所示:当温度由30~55 ℃逐步上升时,酶的活力随着温度的升高逐渐增强,到55 ℃时,酶活力最高,而55 ℃之后,随着温度的升高,酶的活力逐渐降低,当温度增加到80 ℃以上时,酶全部失活。因此,根据以上数据,可以确定酶的最适反应温度为55 ℃。

图3 α-L-鼠李糖苷酶的最适反应温度Fig.3 The optimal reaction temperature of alpha-L-rhamnosidase
2.2.2 酶的热稳定性研究 为了进一步研究温度对α-L-鼠李糖苷酶稳定性的影响,将酶液于20~80 ℃条件下保温2 h后,进行酶活力的测定,结果如图4所示:α-L-鼠李糖苷酶在20~40 ℃条件下保温,酶活力下降不明显,能保持在原酶活的85%以上;而当温度超过50 ℃时,酶活力迅速下降迅速下降;在80 ℃时,粗酶液几乎全部失活。
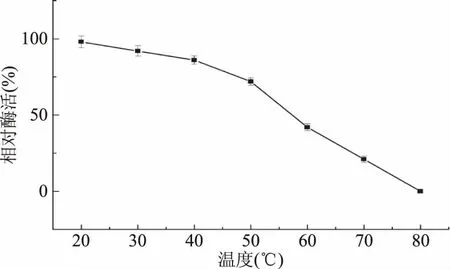
图4 α-L-鼠李糖苷酶的热稳定性Fig.4 The temperature stability of alpha-L-rhamnosidase

图5 α-L-鼠李糖苷酶的最适反应pHFig.5 The optimal reaction pH of alpha-L-rhamnosidase
2.2.3 pH对酶活的影响 据文献报道,α-L-鼠李糖苷酶的最适pH大部分在4.5~6.0之间[19-23],用pH4.0~8.0的缓冲溶液(10 mmol/L)配制底物和稀释酶液,检测pH对α-L-鼠李糖苷酶活性的影响,得到如图5所示:α-L-鼠李糖苷酶属于酸性酶,其中pH在4.0~5.5时,酶活快速增大,pH为5.5时,酶活达到最大,pH大于5.5时,酶活迅速降低。因此,可以确定,酶反应的最适pH为5.5。
2.2.4 酶的酸碱稳定性研究 酶液置于pH2.0~9.0 的缓冲液(10 mmol/L)中24 h后,测定pH对α-L-鼠李糖苷酶稳定性的影响。如图6所示,在pH小于5.0 和pH大于6.5时,可能由于α-L-鼠李糖苷酶发生了失活现象,因此酶活性急剧降低。

图6 α-L-鼠李糖苷酶的酸碱稳定性Fig.6 The pH stability of alpha-L-rhamnosidase
2.3芦丁的酶转化反应及产物分离纯化
2.3.1 芦丁的酶转化反应 通过酶解产物与异槲皮素、芦丁标准品的薄层层析图谱,如图7所示,芦丁在实验所得高纯度α-L-鼠李糖苷酶的作用下,几乎全部转化生成了唯一产物[24-26],其中芦丁的迁移率Rf为0.29,异槲皮素的迁移率Rf为0.72,产物的迁移率Rf为0.72,Rf=点样基线至展开斑点中心的距离/从基线到展开前沿的距离。因此可初步确定其反应产物应为异槲皮素。

图7 反应产物TLC分析Fig.7 The reaction products of TLC注:1.芦丁标准品;2.异槲皮素标准品;3.产物。
为了进一步检测异槲皮素的产率,进行HPLC检测,检测反应产物中的芦丁与异槲皮素的情况。图谱如图8所示,芦丁标准品的出峰时间是7.824 min,异槲皮素标准品的出峰时间是8.633 min,如图9所示,反应产物出峰时间是8.537 min。根据HPLC图谱的峰面积,异槲皮素的含量高达95%。因此,可以判断酶解生成的产物应为异槲皮素,也进一步证明本实验纯化获得的α-L-鼠李糖苷酶具有良好的酶解效果,专一性好且转化率高。

图8 标准品的HPLC图谱Fig.8 HPLC of standard map

图9 反应产物的HPLC图谱Fig.9 HPLC of reaction products
2.3.2 产物的分离纯化 将柱层析得到的产物进行质谱分析,如图10所示:一共出现3个峰型,ESI-MS m/z(%):464.09[M]+,927.19、435.13。其中464.09可以确定是异槲皮素的相对分子质量,其核磁氢谱如图11所示。

图10 产物的质谱分析Fig.10 MS of the products

图11 产物的核磁氢谱分析Fig.11 NMR of the products
1H-NMR(CH3DO,600 MHz)δ:7.709(d,1H),7.589(1H,dd),6.873(1H,d),6.873(1H,d),6.392(1H,d),6.200(1H,d),5.257(1H,d),4.848(1H,s),3.723(1H,dd),3.587(1H,m),3.494(1H,t),3.331(1H,t),3.209(1H,m)。
3 结论
由实验结果可以得出,利用黑曲霉发酵产α-L-鼠李糖苷酶,该粗酶液的酶活达到了798 U/mL;利用α-L-鼠李糖苷酶将芦丁转化为异槲皮素,传统方法制备异槲皮素需要高温高压,对设备要求高,该方法比传统的化学法有更多优势,反应条件温和,反应时间短,对底物的选择性强,并且反应过程容易控制,转化率高达95%。同时对酶学性质进行探究,酶蛋白的分子量为55 kDa,酶反应的最适温度是55 ℃,最适pH是5.5。通过酶法水解芦丁,为实现异槲皮素的工业化生产提供了理论依据。
[1]Wolfe K L,Liu R H. Structure-Activity Relationships of Flavonoids in the Cellular Antioxidant Activity Assay[J]. Agric Food Chem,2008,56(18):8404-8411.
[2]Suzuki Y,Suzuki K. Enzymatic formation of 4G-alpha-D-glucopyranosyl-rutin[J]. Agric Biol Chem,1991,55(1):181-187.
[3]Manzanares P,Hc V D B,de Graaff L H,et al. Purification and characterization of two different alpha-L-rhamnosidases,RhaA and RhaB,fromAspergillusaculeatus[J]. Applied & Environmental Microbiology,2001,67(5):22-30.
[4]Manzanares P,de Graaff L H,Visser J. Purification and characterization of an alpha-L-rhamnosidase fromAspergillusniger[J]. Fems Microbiology Letters,1997,157(2):279-283.
[5]Xiao J,Cao H,Chen T,et al. Molecular property-binding affinity relationship of flavonoids for common rat plasma proteinsinvitro[J]. Biochimie,2011,93(2):134-140.
[6]Amado N G,Fonseca B F,Cerqueira D M,et al. Effects of natural compounds on Xenopus embryogenesis:a potential read out for functional drug discovery targeting Wnt/β-catenin signaling[J]. Current Topics in Medicinal Chemistry,2012,12(19):2103-2109.
[7]Qian S,Yu H,Zhang C,et al. Purification and characterization of dioscin-alpha-L-rhamnosidase from pig liver[J]. Journal of General & Applied Microbiology,2009,55(3):191-199.
[8]Bourbouze R,Percheron F,Courtois J. alpha-L-Rhamnosidase from Fagopyrum esculentum:purification and some properties[J]. European Journal of Biochemistry,1976,63(2):331-337.
[9]Manzanares P,Graaff L H,Visser J. Purification and characterization of an alpha-L-rhamnosidase from Aspergillus niger[J]. Fems Microbiology Letters,1997,157(2):279-283.
[10]Romero C,Manjon A,Bastida J,et al. A method for assaying the rhamnosidase activity of naringinase[J]. Analytical Biochemistry,1985,149(2):566-571.
[11]王侃,鱼红闪,金凤燮. 芦丁-α-鼠李糖苷酶分离提纯及其酶性质[J]. 大连轻工业学院学报,2004,23(1):30-33.
[12]金赞敏,鱼红闪,金凤燮. 人参皂甙-α-鼠李糖苷酶分离提纯及其酶性质[J]. 大连工业大学学报,2003,22(2):103-106.
[13]韩冰,付绍平,金凤燮,等. 两种菌产两种不同天然苷类α-鼠李糖苷酶的研究[J]. 大连工业大学学报,2008,27(2):105-109.
[14]Hashimoto W,Nankai H,Sato N,et al. Characterization ofα-l-Rhamnosidase of Bacillus,sp. GL1 Responsible for the Complete Depolymerization of Gellan[J]. Archives of Biochemistry & Biophysics,1999,368(1):56-60.
[15]Stuart M. Pitson,Margien Mutter,Lambertus A.M. van den Broek. Stereochemical Course of Hydrolysis Catalysed byα-L-Rhamnosyl andα-D-Galacturonosyl Hydrolases from Aspergillus aculeatus,[J]. Biochemical & Biophysical Research Communications,1998,242(3):552-558.
[16]Koseki T,Mese Y,Nishibori N,et al. Characterization of anα-l-rhamnosidase from Aspergillus kawachii,and its gene[J]. Applied Microbiology & Biotechnology,2008,80(6):1007-1013.
[17]邬子彬,李大伟,陆豫.一株产α-L-鼠李糖苷酶菌株的分析与鉴定[J].南昌大学学报(理科版),2016,40(4):346-350.
[18]Yadav S,Yadav V,Yadav S,et al. Purification,characterisation and application ofα-l-rhamnosidase from Penicillium citrinum,MTCC-8897[J]. International Journal of Food Science & Technology,2012,47(2):290-298.
[19]Federica De Lise,Francesca Mensitieri,Vincenzo Tarallo. RHA-P:Isolation,expression and characterization of a bacterialα-L-rhamnosidase from Novosphingobium,sp. PP1Y[J].Journal of Molecular Catalysis B Enzymatic,2016,134(3):136-147.
[20]Sarita Yadav,Sudha Yadava,Kapil D.S. Yadav.α-L-Rhamnosidase selective for rutin to isoquercitrin transformation from Penicillium griseoroseum,MTCC-9224[J]. Bioorganic Chemistry,2017,14(3):196-202.
[21]Taehwan,Lim,Hana,Jung,Keum Taek,Hwang. Bioconversion of Cyanidin-3-Rutinoside to Cyanidin-3-Glucoside in Black Raspberry by Crudeα-L-Rhamnosidase from Aspergillus Species[J]. Journal of Microbiology sbiotechnology,2015,25(11):1842-1848.
[22]Vinita Yadav,Saroj Yadav,Sarita Yadav,et al.α-L-rhamnosidase from Aspergillus clavato-nanicus MTCC-9611 active at alkaline pH[J]. Applied Biochemistry & Microbiology,2012,48(3):295-301.
[23]Ge L,Chen A,Pei J,et al. Enhancing the thermostability ofα-L-rhamnosidase from Aspergillus terreus and the enzymatic conversion of rutin to isoquercitrin by adding sorbitol[J].Bmc Biotechnology,2017,17(1):21-28.
[24]You H J,Ahn H J,Ji G E. Transformation of rutin to antiproliferative quercetin-3-glucoside by Aspergillus niger.[J]. Journal of Agricultural & Food Chemistry,2010,58(20):10886-10892.
[25]Guan C J,Ji Y J,Hu J L,et al. Biotransformation of Rutin Using Crude Enzyme from Rhodopseudomonas palustris[J]. Current Microbiology,2017,74(4):431-436.
[26]Kim D Y,Yeom S J,Park C S,et al. Effect of high hydrostatic pressure treatment on isoquercetin production from rutin by commercialα-L-rhamnosidase.[J]. Biotechnology Letters,2016,38(10):1-6.
