基于木质素部分脱除及其含量对生物质热解特性的影响
2018-01-18吴丹焱辛善志陈应泉杨海平王贤华陈汉平
吴丹焱,辛善志,刘 标,陈应泉,杨海平※,王贤华,陈汉平
(1. 华中科技大学能源与动力工程学院煤燃烧国家重点试验室,武汉 430074;2. 江汉大学工业烟尘污染控制湖北省重点试验室,武汉 430056)
0 引 言
木质素是生物质中的一种主要组分,其相对含量介于15%~35%,是生物质组分中比能量最高的组分[1]。相比纤维素与半纤维素,木质素热稳定性高,其分解温度范围为 200~900℃[2]。生物质裂解过程中,木质素是形成焦炭的主要来源组分,而综纤维素(纤维素和半纤维素)通常较易裂解形成气、液态产物,两者之间相互影响,最终决定气、液、固相产物的分布、组成[3-7]。Wang Shurong等[8]采用干式混合法研究生物质热解过程中不同组分的交互影响。研究发现木质素的存在加宽了左旋葡聚糖的分解区间;同时,综纤维素在木质素热解过程中能够促进酚类物质的生成,如 2,6-二甲氧基苯酚。Burhenne等[6]采用模型混合物直混模拟实际生物质的组分构成,并与天然生物质麦秆、油菜秆、云杉对比,研究发现,随着样品中木质素含量的增加,生物质样品的热解速度变慢,气体产物含量降低。李小华等[9]在生物质真空热解液化系统上考察三组分含量对热解液化产物分布的影响,结果发现,较高的纤维素含量有助于产生更多的液体产物,并且适量的木质素有利于促进纤维素的分解。辛善志[10]在研究纤维素、半纤维素、木质素组分之间气相交互过程中,发现木质素、半纤维素与纤维素之间的气相交互能够促进糖类化合物的生成,而纤维素与木质素的气相交互抑制了愈创木基的脱甲氧基作用。
由上可知,在生物质热解过程中,组分之间确实存在交互作用,对最终热解产物特性、分布均具有较大影响。但在前期的文献调研中,发现大部分研究者的组分交互研究原料都集中于模型化合物[11-14],而对于生物质原始交联结构下,组分之间的交互影响、产物特性研究非常少。然而模型化合物与天然生物质之间存在不可忽略的差异,原始交联结构下,天然组分之间具有化学连接键,比如半纤维素与纤维素之间的氢键、半纤维素中4-O-甲基葡萄糖醛酸与木质素的酯、醚键形成不同化学键等[15]。因此,研究天然组分之间的交互作用,对于产物分布和特性评估预测具有更加深刻、实际的意义。
基于此,本文采用亚氯酸钠-乙酸法对生物质原料进行处理,极大程度保留了生物质组分之间的原始交联结构。花生壳与核桃壳经过不同时间的亚氯酸钠-乙酸处理后,得到含有不同木质素含量的生物质样品,经固定床热解,探索不同热解温度下,不同木质素含量对生物质热解的影响,以及这种影响在气、液体产物中的具体影响。本研究对于生物质组分间交互和产物形成特性研究具有积极意义,为全面理解生物质三组分在热解过程中的交互影响以及产物的高值化利用打下了基础。
1 材料与方法
1.1 试验原料
本文选取花生壳与核桃壳作为生物质原料,经粉粹过筛后,所得样品粒径为40~60目。根据范式洗涤法测得花生壳和核桃壳的木质素质量分数分别为 31.08%、33.82%。采用亚氯酸钠-乙酸法对花生壳与核桃壳进行木质素部分脱除,该方法广泛用于综纤维素的制备,不损伤纤维素结构,对半纤维素的结构影响较小[16-18]。花生壳和核桃壳经不同时间的(1、2.5、4 h)亚氯酸钠-乙酸处理后,对应花生壳的木质素质量分数分别为25.02%、15.13%和 4.28%,核桃壳的木质素质量分数分别为26.01%、15.37%、5.42%。不同木质素含量的花生壳样品和核桃壳样品的工业分析与元素分析如表1所示。

表1 不同木质素含量花生壳和核桃壳样品的工业分析与元素分析Table 1 Ultimate and proximate analysis of different lignin content peanut shell and walnut shell
1.2 试验设备与方法
本试验采用的是小型立式管式炉热解装置[10],系统包括石英管反应器(内径30 mm,总长700 mm)、电炉、温度控制器、冷凝系统、过滤器、干燥器、气体分析仪以及供气系统等。试验过程中,先将炉体加热到设定温度,分别为300、500、700 ℃。并通入1 000 mL/min的高纯氮气对石英管内部进行吹扫10 min,以确保排净管内空气,之后调整N2流量至400 mL/min。称取1 g的样品放入样品盘中,将样品盘推入中心反应区。试验过程中产生的挥发分经过冰水混合物冷凝后收集。热解15 min后,取出石英管反应器并在持续的氮气吹扫下冷却至室温,取出样品盘并称量,并用3 mL丙酮收集冷凝管中的生物油。液体生物油采用GC/MS进行分析,具体分析方法参考文献[19],气体产物经气袋收集后,利用 micro GC3000进行成分分析。每组试验重复3次,取3次的平均值作为结果。
2 结果与分析
2.1 热解产物分布特性
图 1为不同热解温度下,不同木质素含量的花生壳样品和核桃壳样品的热解产物分布图。表明由图2可知,当热解温度为 300 ℃时,花生壳和核桃壳样品热解产物中,固体产率均随样品中木质素含量的增加而明显增加,而液体产物和气体产物生成量均出现了下降,且气体产物产率较低。原因是300 ℃热解条件下,生物质中的木质素降解量非常少,主要是半纤维素和纤维素的分解[20-21]。因此,随着木质素含量的升高,焦炭产率会明显增加,气、液体产物产率会随之下降。
当热解温度进一步升高(500、700 ℃),固体产率相比 300 ℃有明显的下降;但随着样品中木质素含量增多,固体产率并无明显变化,这与常规的组分混合模拟法结果不同,表明在生物质原始交联结构下,木质素与综纤维素在裂解过程中存在相互影响,导致在高综纤维素含量、高木质素含量条件下出现了均等的焦炭产率。相比 300 ℃的裂解产物分布,由于温度升高,生物质裂解更充分,气体产物生成量增大,但随木质素含量的增加而不断下降;液体产率变化趋势与 300 ℃时呈现相反趋势,随木质素含量的增加出现小幅上涨。当热解温度达到500、700 ℃时,综纤维素完全分解,液体生物油产率随木质素含量的增加并没有明显的降低,反而有轻微的增加,进一步说明生物质原始交联结构下,木质素与综纤维素之间存在强烈的交互反应,促使高综纤维素含量下的成炭作用,和高木质素含量下的成油特性。
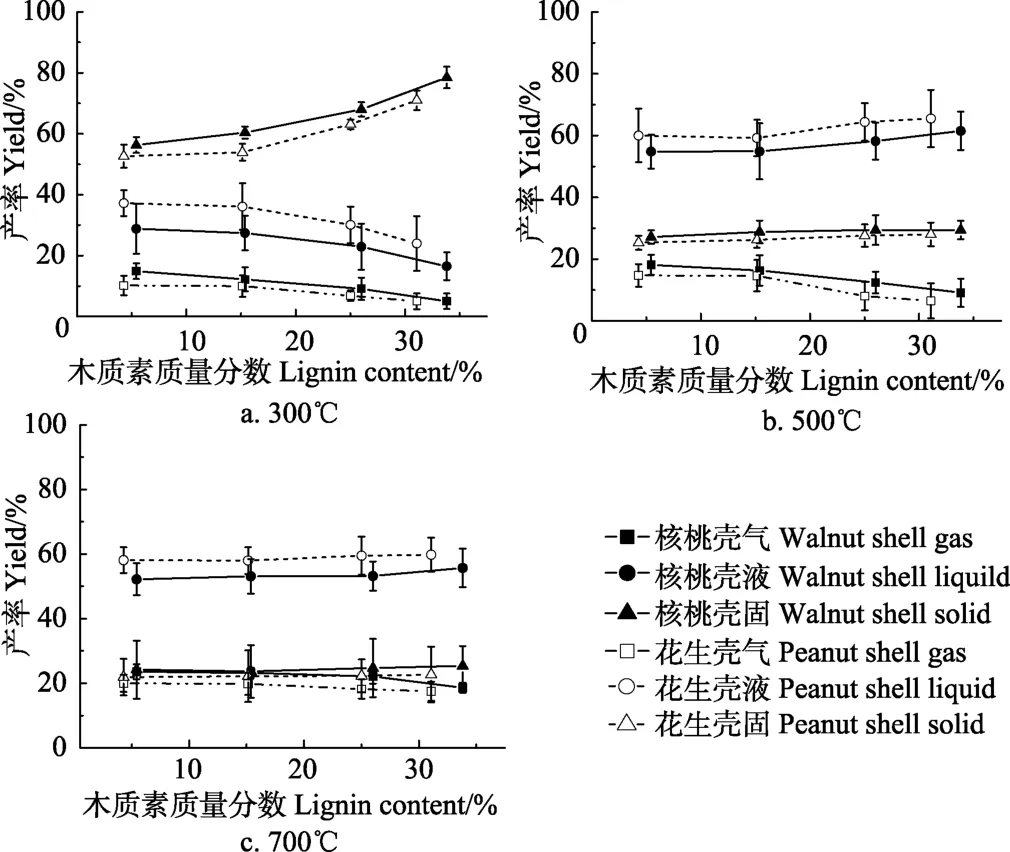
图1 花生壳和核桃壳在不同温度下的热解产物分布图Fig.1 Prolysis product distribution of peanut shell and walnut shell at different temperatures
2.2 气体产物释放特性
不同木质素含量的花生壳和核桃壳热解后的气体产物主要组分变化如图2所示。由图2可知,气体产物的主要成分包括H2、CH4、CO及CO2,除此以外,气体产物中还含有极少量的C2+轻质烃,由于含量极少,未列入图中。此外,300 ℃热解条件下,木质素降解量小,木质素与综纤维素之间的交互作用弱,气体产率较低,且主要组成成分为CO和CO2,因此未列出。
由图2可知,当热解温度为500 ℃时,花生壳与核桃壳样品热解气体产物主要组分为 CO2、CH4、CO,H2含量相对较低。随着样品中木质素含量增加,花生壳与核桃壳气体产物中的CH4含量均出现了快速增加,而CO2相对含量快速下降。根据前人研究[22]可知,CH4主要来源于木质素中苯丙烷基的甲氧基断裂,而 CO2来源于综纤维素羟基氧化和脱羧基反应,因此随着样品中木质素含量增加、综纤维素含量减少,气体产物中的 CH4含量会明显增加,CO2含量会快速下降。相对CH4、CO2,随着样品中木质素含量增加,花生壳气体产物中CO的相对含量变化快速增加,而核桃壳气体产物中CO的相对含量变化较为平稳,这与 2种原料的自身特性有关。在众多的生物质热解机理研究中,CO生成来源被归类于脱羰基、气相交互、气固相交互反应,是一种比较好的二次反应表征物[23-27]。因此,CO含量增加可能来源于木质素和综纤维素在裂解过程中的气相交互、气固相交互反应。

图2 花生壳和核桃壳样品热解的气体产物分布Fig.2 Peanut shell or walnut shell pyrolysis gas products distribution
当热解温度升至 700 ℃,花生壳与核桃壳的热解气体产物中均出现了较高的 H2含量,且随样品中木质素含量增加而明显下降,CO2、CO、CH4变化趋势与500 ℃热解条件一致。气体产物中的 H2主要来源于芳香烃的脱氢缩聚反应,随着热解温度升高,木质素进一步分解,脱氢缩聚反应加剧,H2产量大幅提高。但根据图2中700 ℃热解产物分布图,随着样品中木质素含量增加,芳烃类化合物相应增加,而H2含量不升反降,这与常规的模型化合物干混热解研究结果不一致,可能与天然生物质内部组分间的原生态结构连接相关,导致高综纤维素条件下的交互反应,脱氢、脱羟基、缩环类反应增加,生成大量的H2;而在高木质素含量条件下,综纤维素与木质素的交互裂解反应抑制了脱氢缩聚反应,从而导致H2产量减少。
根据花生壳样品与核桃壳样品热解气体产物变化趋势可知,随着木质素含量增加,2种样品气体产物的变化趋势基本一致,但其升降幅度存在差异(比如 500 ℃热解条件下,核桃壳气体产物中CO2、CO的升降幅度明显高于花生壳样品),这与2种生物质的组分构成及连接键相关,组分之间相互连接,热解过程中发生交互作用,对热解产物特性、分布存在较大影响。
2.3 液体产物的组成
表2为花生壳、核桃壳样品在500 ℃热解条件下制备的生物油GC-MS成分图,表中左旋葡聚糖、脱水糖对应于生物质中纤维素的热解产物,乙酸、糠醛等小分子含氧化合物为半纤维的典型热解产物,而愈创木酚等酚类以及环酮等物质主要为木质素的典型产物[28]。

表2 花生壳和核桃壳不同木质素含量的样品在500 ℃热解时的液体产物组成Table 2 Liquid composition of different lignin content peanut shell or walnut shell at 500 ℃ pyrolysis %
由表 2可知,随着生物质样品中木质素含量增加,纤维素热解产物左旋葡聚糖的相对含量不断增加,这与样品中纤维素含量成反比例关系,说明热解过程中,木质素的存在有利于热解产物中左旋葡聚糖的生成,具体原因可能是由于综纤维素熔融相中的左旋葡聚糖与木质素分解后生成的愈创木酚等芳香族化合物之间形成CH-π的电子结构从而增强了左旋葡聚糖的热稳定性[29]。随着样品中木质素含量增加,芳香族化合物含量相应增加,导致CH-π电子结构增加,左旋葡聚糖含量相应增加。相比左旋葡聚糖,纤维素的另外一种典型产物,1,4:3,6-脱水-α-D-吡喃葡萄糖随木质素含量增加小幅下降,这可能是由于纤维素与半纤维之间的交互影响促进了低聚糖的脱水反应,随着木质素含量增加,含量相对减少,脱水反应减弱。
羟基丙酮、乙酸等小分子化合物是半纤维素热解后的典型产物,其含量随木质素增加而逐渐减少。在辛善志等[10]对生物质三组分热解的研究过程中发现CO2、乙酸、羟基丙酮主要来自于半纤维素降解,本研究中这 3种物质的相对含量随木质素增加而减少,对应于样品中的半纤维素含量变化规律。
酚类是热解产物中一种重要的产物,其含量的变化反应了综纤维素对木质素热解特性的影响。由表 2中可知,木质素热解的典型产物酚类包括愈创木酚、愈创木酚取代衍生物(4-羟基-3-甲氧基苯乙酮,4-乙基-2-甲氧基苯酚及香兰素等)以及苯酚和烷基苯酚等。随着木质素含量增加,木质素中脂肪醚和芳基烷基醚键断裂生成的愈创木基取代衍生物增加,而木质素的初级热解产物,愈创木酚的含量却出现了下降趋势。这可能是因为综纤维素含量增加促进了木质素脂肪烃取代基的脱除反应,抑制了愈创木酚的脱甲氧基反应,气体产物中的 CH4含量上升可能来源于愈创木基的脱烷基反应,导致液体产物中愈创木酚含量减少,4-乙基-2-甲氧基苯酚、4-甲基-2-甲氧基苯酚等含量增加。Hosoya等[30]在研究木材及其组分的气化研究过程中,也发现了纤维素能够促进愈创木酚类衍生物的生成。
3 结 论
本文采用花生壳和核桃壳作为原料,利用亚氯酸钠-乙酸法对原料中的木质素进行脱除,该方法较好的保留了生物质中综纤维素与木质素的原始交联结构,能更加准确地研究原始交联结构下,天然组分之间交互影响,具体研究结果如下:
1)300 ℃热解条件下,木质素还未大量裂解,木质素与综纤维素之间的交互作用不明显。500、700 ℃热解条件下,随着样品中木质素含量增加,其焦炭产率保持稳定,与模型化合物混合研究结果不一致,表明生物质原始交联结构下,木质素与综纤维素之间发生了强烈的交互反应,促使高综纤维素含量下生成更多焦炭,而高木质素含量下生成更多挥发分。
2)500、700 ℃热解条件下,木质素与综纤维素的交互作用促进了 CO生成,抑制了 CO2生成。700 ℃热解条件下,气体产物中H2含量随着木质素增加而减少,这可能是综纤维素与木质素的交互作用抑制了芳环的脱氢缩聚反应,从而导致氢气产量减少。
3)木质素能够促进纤维素分解,生成大量左旋葡聚糖,并抑制左旋葡聚糖分解;而综纤维素抑制木质素单体愈创木基的脱甲氧基反应,促进苯丙烷基的脱烷基反应,形成更多的酚类化合物。
[1] Pandey M P, Kim C S. Lignin depolymerization and conversion: A review of thermochemical methods[J].Chemical Engineering & Technology, 2011, 34(1): 29-41.
[2] Mu Wei, Haoxi Ben, Art Ragauskas, et al. Lignin pyrolysis components and upgrading-technology review[J]. Bioenergy Research, 2013, 6(4): 1183-1204.
[3] Cao Xuefei, Lin Xinzhong, Peng Xinwen, et al. Comparative study of the pyrolysis of lignocellulose and its major components:Characterization and overall distribution of their biochars and volatiles[J]. Bioresource Technology, 2014, 155: 21-27.
[4] Zhao Chenxi, Jiang Enchen,Chen Aihui. Volatile production from pyrolysis of cellulose, hemicellulose and lignin[J].Journal of the Energy Institute, 2017, 90(6): 902-913.
[5] Xin Shanzhi, Yang Haiping, Chen Yingquan, et al. Assessment of pyrolysis polygeneration of biomass based on major components: Product characterization and elucidation of degradation pathways[J]. Fuel, 2013, 113: 266-273.
[6] Burhenne Luisa, Messmer Jonas, Aicher Thomas, et al. The effect of the biomass components lignin, cellulose and hemicellulose on TGA and fixed bed pyrolysis[J]. Journal of Analytical and Applied Pyrolysis, 2013, 101: 177-184.
[7] Ye X N, Q Lu, Jiang X Y, et al. Interaction characteristics and mechanism in the fast co-pyrolysis of cellulose and lignin model compounds[J]. Journal of Thermal Analysis and Calorimetry, 2017, 130(2): 975-984.
[8] Wang Shurong, Guo Xiujuan, Wang Kaige, et al. Influence of the interaction of components on the pyrolysis behavior of biomass[J]. Journal of Analytical and Applied Pyrolysis,2011, 91(1): 183-189.
[9] 李小华,焦丽华,樊永胜,等. 纤维素木聚糖和木质素含量对生物质热解特性及产物的影响[J]. 农业工程学报,2015,31(13):236-243.Li Xiaohua, Jiao Lihua, Fan Yongsheng, et al. Effects of cellulose, xylan and lignin content on biomass pyrolysis characteristic and product distribution[J]. Transactions of the Chinese Society of Agricultural Engineering (Transactions of the CSAE), 2015, 31(13): 236-243. (in Chinese with English abstract)
[10] 辛善志. 基于组分的生物质热分解及交互作用机制研究[D]. 武汉:华中科技大学,2014.Xin Shanzhi. Study on Tje Mechanism of Biomass Pyrolysis and the Interaction based on its Components[D]. Wuhan:Guazhong University of Science and Thechnology, 2010
[11] Giudicianni Paola, Giuseppe Cardone, Giancarlo Sorrentino,et al. Hemicellulose, cellulose and lignin interactions on Arundo donax steam assisted pyrolysis[J]. Journal of Analytical and Applied Pyrolysis, 2014, 110: 138-146.
[12] Liu Qian, Zhong Zhaoping, Wang Shurong, et al. Interactions of biomass components during pyrolysis: A TG-FTIR study[J]. Journal of Analytical and Applied Pyrolysis, 2011,90(2): 213-218.
[13] Hosoya T, Kawamoto H, Saka S. Cellulose–hemicellulose and cellulose–lignin interactions in wood pyrolysis at gasification temperature[J]. Journal of Analytical and Applied Pyrolysis, 2007, 80(1): 118-125.
[14] Smith Matthew W, Brennan Pecha, Greg Helms, et al.Chemical and morphological evaluation of chars produced from primary biomass constituents: Cellulose, xylan, and lignin[J]. Biomass & Bioenergy, 2017, 104: 17-35.
[15] 杨淑蕙. 植物纤维化学[M]. 北京:中国轻工业出版社,2006.
[16] Ding Shiyou, Liu Yusan, Zeng Yining, et al. How does plant cell wall nanoscale architecture correlate with enzymatic digestibility?[J]. Science, 2012, 338(6110): 1055-1060.
[17] Saar B G, Zeng Yining, Christian W Freudiger, et al.Label-free, real-time monitoring of biomass processing with stimulated raman scattering microscopy[J]. Angewandte Chemie International Edition, 2010, 49(32): 5476-5479.
[18] Ishizawa, Claudia I, Tina Jeoh, William S Adney, et al. Can delignification decrease cellulose digestibility in acid pretreated corn stover?[J]. Cellulose, 2009, 16(4): 677-686.
[19] Zhe Tang, Lu Qiang, Zhang Ying, et al. One step bio-oil upgrading through hydrotreatment, esterification, and cracking[J]. Industrial & Engineering Chemistry Research,2009, 48(15): 6923-6929.
[20] 杨海平,陈汉平,晏蓉,等. 油棕废弃物及生物质三组分的热解动力学研究[J]. 太阳能学报,2007,28(6):626-631.Yang Haiping, Chen Hanping, Yan Rong, et al.Themodynamic analysis of pyrolysis of oil palm waste and biomass components[J]. Acta Energiae Solaris Sinica, 2007,28(6): 626-631. (in Chinese with English abstract)
[21] 吴逸民,赵增立,李海滨,等. 生物质主要组分低温热解研究[J]. 燃料化学学报,2009,37(4):427-432.Wu Yimin, Zhao Zengli, Li Haibin, et al. Low temperature pyrolysis characteristics of major components of biomass[J].Journal of Fuel Chemistry and Technology, 2009, 37(4): 427-432. (in Chinese with English abstract)
[22] Collard F X, Blin J. A review on pyrolysis of biomass constituents: Mechanisms and composition of the products obtained from the conversion of cellulose, hemicelluloses and lignin[J]. Renewable & Sustainable Energy Reviews, 2014,38: 594-608.
[23] Tripathi Manoj, Sahu J N, Ganesan P. Effect of process parameters on production of biochar from biomass waste through pyrolysis: A review[J]. Renewable and Sustainable Energy Reviews, 2016, 55: 467-481.
[24] Luo Guanqun, Resende F L P. In-situ and ex-situ upgrading of pyrolysis vapors from beetle-killed trees[J]. Fuel, 2016,166: 367-375.
[25] Collard F X, Blin J. A review on pyrolysis of biomass constituents: Mechanisms and composition of the products obtained from the conversion of cellulose, hemicelluloses and lignin[J]. Renewable and Sustainable Energy Reviews, 2014,38: 594-608.
[26] Peng Fu, Hu Song, Xiang Jun, et al. Study on the gas evolution and char structural change during pyrolysis of cotton stalk[J]. Journal of Analytical and Applied Pyrolysis,2012, 97: 130-136.
[27] Yang, H P, Yan R, Chen H P, et al. Characteristics of hemicellulose, cellulose and lignin pyrolysis[J]. Fuel, 2007,86(12/13): 1781-1788.
[28] 朱玲莉,仲兆平,王佳,等. 基于PY-GC/MS的生物质组分间相互作用的热解实验[J]. 化工进展,2016,35(12):3879-3883.Zhu Lingli, Zhong Zhaoping, Wang Jia, et al. The interactions among the pyrolysis of biomass components based on the PY-GC/MS[J] Chemical Industry and Engineering Progress, 2016, 35(12): 3879-3883. (in Chinese with English abstract)
[29] Hosoya, Takashi, Haruo Kawamoto,Shiro Saka. Thermal stabilization of levoglucosan in aromatic substances[J].Carbohydrate Research, 2006, 341(13): 2293-2297.
[30] Hosoya T, Kawamoto H, Saka S. Pyrolysis behaviors of wood and its constituent polymers at gasification temperature[J].Journal of Analytical and Applied Pyrolysis, 2007, 78(2): 328-336.
