Pt@rGO-Bi2WO6/FTO复合材料的制备及其光电催化甲醇氧化性能
2018-01-17,,,
, ,,
(浙江工业大学 绿色化学合成技术国家重点实验室培育基地,浙江 杭州 310014)
经过几十年的发展和改进,直接甲醇燃料电池(Direct methanol fuel cells, DMFC)已经在相关领域得到应用[1-4].Pt,Au和Ru等贵金属常作为DMFC的电极材料[5-7],而这些贵金属材料价格昂贵,在工作过程中易吸附CO中毒,因此目前解决方法之一是开发新型的光电催化剂,即将极少量的贵金属颗粒负载在半导体光催化材料上.这样一方面可以减少贵金属的用量,另一方面可以利用半导体来光催化氧化甲醇,同时半导体光催化与贵金属颗粒电催化之间存在协同效应,可以进一步氧化甲醇[8-10].半导体Bi2WO6有特殊的层状结构,光谱响应范围可达450 nm,且因其价带电位为3.2 eV(vs. NHE)而具强氧化能力[11-15],故可作为一种较为理想的基体材料.然而Bi2WO6自身存在光生载流子转移速率慢,易在体相内复合等问题,导致其光催化效率低.因此,需要在复合材料内部建立光生载流子快速转移的通道[16].石墨烯因具备独特的物理化学性质,如较大的比表面积,高速多向的电子转移速度等,使其作为支撑材料在催化领域中得到广泛应用[17].为此,笔者拟先将还原氧化石墨烯修饰到Bi2WO6表面上,然后将Pt颗粒均匀地负载到还原氧化石墨烯rGO上,制备得到新型的Pt@rGO-Bi2WO6/FTO光电催化剂.rGO一方面可以有效地加快Bi2WO6光生载流子的转移速率,提高Bi2WO6的光催化氧化能力;另一方面,rGO巨大的表面积可使Pt颗粒更加均匀地分散在材料表面,提高材料电催化氧化甲醇的能力.另外,rGO表面的羟基自由基能吸附甲醇氧化过程中产生的中间体CO,利用Bi2WO6的光催化作用,将CO进一步氧化,以提高复合材料的抗中毒性能.
1 实验部分
1.1 复合材料Pt@rGO-Bi2WO6/FTO的制备
复合材料的制备流程图如图1所示.首先在FTO基体上制备得到垂直于基体表面的WO3纳米片,相关的合成方法和过程已有详细的报道[18-20].然后称取4 mmol Bi(NO3)3·5H2O,溶于50 mL 5%的稀硝酸,搅拌至澄清.将澄清液转至80 mL聚四氟乙烯内衬中,将事先制备好的WO3/FTO样品斜放入溶液中,反应釜在160 ℃下保温24 h后,自然冷却.取出样品,洗涤干燥,并在空气气氛下,400 ℃锻烧2 h,升温速率2 ℃/min,冷却至室温后取出样品,得到Bi2WO6/FTO.
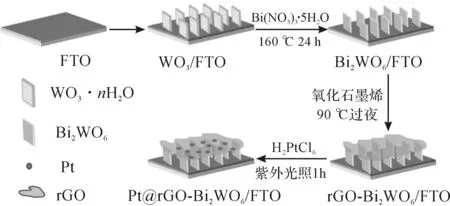
图1 Pt@rGO-Bi2WO6/FTO的制备流程图Fig.1 The schematic diagram for preparation of Pt@rGO-Bi2WO6/FTO
采用Hummers法制备氧化石墨烯[21].将上述制备好的Bi2WO6/FTO样品浸泡在20 mL 1.25 g/L氧化石墨烯水溶液中,90 ℃油浴下过夜,待自然冷却后,取出样品,洗涤,用氮气吹干,得到rGO-Bi2WO6/FTO样品.然后将rGO-Bi2WO6/FTO样品平放入到10 mL 0.5 mM H2PtCl6的水溶液中,紫外光下照射1 h后,取出样品,洗涤,干燥,得到Pt@rGO-Bi2WO6/FTO.
1.2 材料的形貌观察与结构表征
分别采用Hitachi S-4800型扫描电子显微镜(SEM,操作电压15 kV)以及JEM-2010型高分辨透射电子显微镜(HRTEM,操作电压为200 kV)观察样品的表面形貌.采用X’Pert PRO型X射线衍射仪(XRD,Cu Kα为X射线源)表征样品的物相结构.采用岛津UV 2700型紫外可见分光光度计测试材料的光学性能.
1.3 光电催化性能测试
复合材料的光电催化性能是采用循环伏安法,在CHI 760D型电化学工作站上进行测试的.采用三电极体系,制备所得到的复合材料电极、Pt(1 cm×1 cm)片、饱和甘汞电极(SCE)分别用作工作电极、辅助电极和参比电极,循环伏安的扫描速度为50 mV/s.电解液为1 mol/L KOH和0.5 mol/L CH3OH的混合溶液.每一次测试前,往电解液通30 min氮气以驱走溶液中的游离氧.光催化的光源采用150 W氙灯(Perfect Labsolar 300),光强度控制在100 mW/cm2.计时光电流曲线在无外加偏压的情况下进行测试,时间间隔为20 s.
2 结果与讨论
2.1 样品的形貌分析
图2为3种材料Bi2WO6/FTO,rGO-Bi2WO6/FTO和Pt@rGO-Bi2WO6/FTO的SEM图.图2(a)为Bi2WO6/FTO的微观形貌.图2(a)中,Bi2WO6纳米片比较均匀地直立生长在FTO表面,片与片有交错,纳米片的厚度约为20~30 nm,长度约1~3 μm;图2(b)为rGO-Bi2WO6/FTO的微观形貌.图2(b)中,Bi2WO6纳米片层表面已均匀覆盖了光滑顺溜的rGO层.图中虽然覆盖了rGO层,但Bi2WO6纳米片层依然保持了直立不折的状态;图2(c)为Pt@rGO-Bi2WO6/FTO复合材料的微观形貌.图2(c)中,其微观结构形貌与rGO-Bi2WO6/FTO基本一致,直立生长的Bi2WO6纳米片有不完全覆盖的rGO层,但光沉积Pt颗粒后,rGO表层颜色加深,表面有皱痕而不光滑,表明rGO表面有贵金属颗粒沉积.为此,对Pt@rGO-Bi2WO6/FTO做进一步的元素分布Mapping图和能谱EDX测定,结果见图3所示.从图3可以看到:复合材料表面测到Bi,W,O,C和Pt等5种元素,且每种元素均匀分布.这进一步说明Pt颗粒已经均匀地负载到rGO-Bi2WO6/FTO的表面上.

图2 3种复合材料的SEM图Fig.2 SEM images of samples
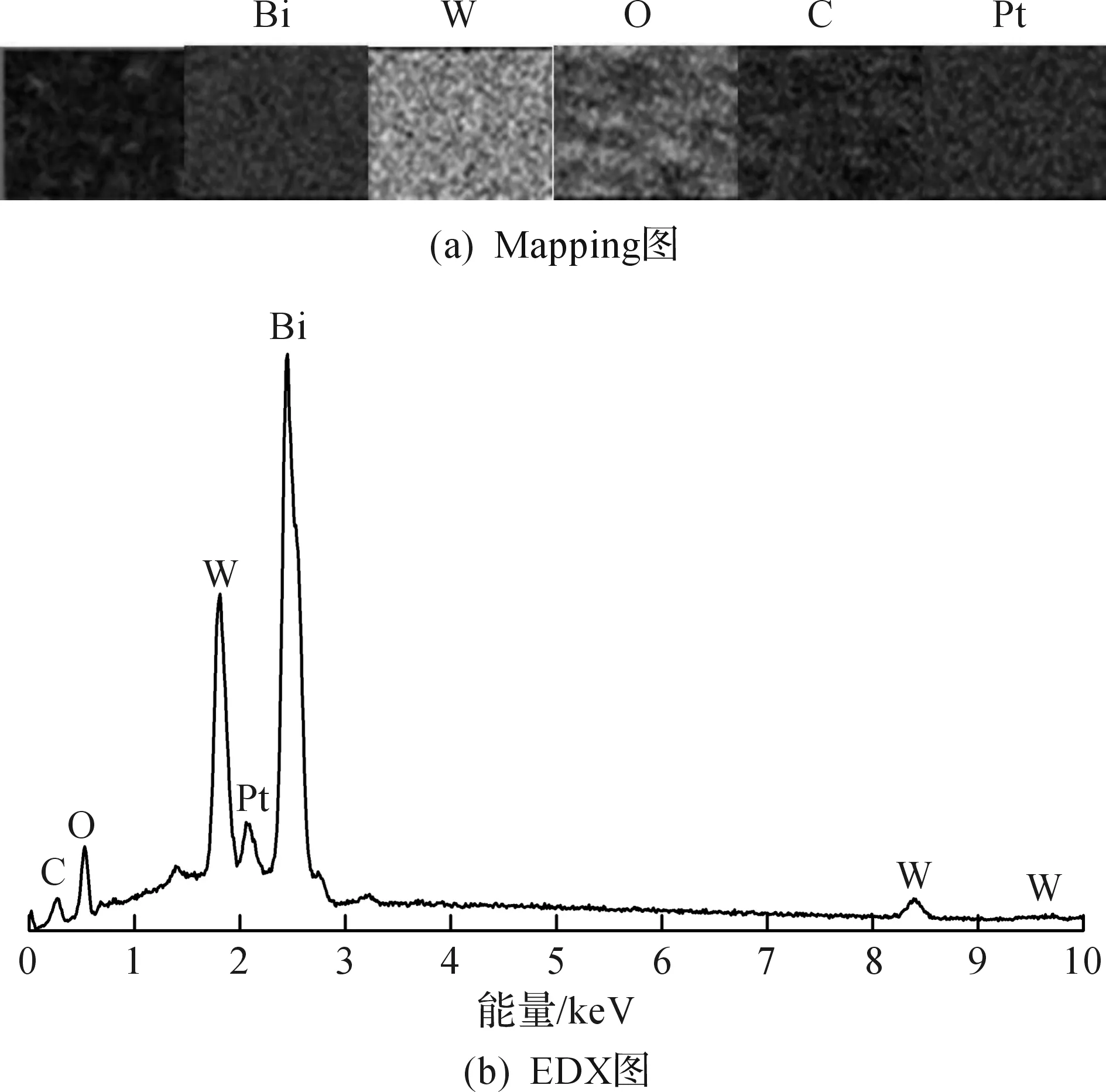
图3 Pt@rGO-Bi2WO6/FTO的(a)Mapping图和(a)EDX图Fig.3 Mapping images(a) and EDX(b) of Pt@rGO-Bi2WO6/FTO
图4为复合材料Pt@rGO-Bi2WO6/FTO的TEM图.由图4(a,b)可以看出,颜色较深的部分为Bi2WO6纳米片,浅色近透明的部分为rGO层,Bi2WO6纳米片与rGO层贴合紧密.图4(c)为图4(b)的局部放大图.从图4(c)可以发现rGO层上的铂颗粒,其均匀负载在rGO的表面上.为了进一步观察铂颗粒的负载情况,我们选取了局部进行高倍透视电镜观察见图4(d),从图4(d)观察到的结构形貌,并结合元素分布图(图3),可以判断铂纳米颗粒比较密集均匀生长在rGO表面上,纳米颗粒直径大约为2~3 nm.

图4 材料Pt@rGO-Bi2WO6/FTO的TEM图Fig.4 TEM images of Pt@rGO-Bi2WO6/FTO
2.2 材料的晶体结构
图5为材料Bi2WO6/FTO,Pt-Bi2WO6/FTO和Pt@rGO-Bi2WO6/FTO的XRD图.对于Bi2WO6/FTO材料,从图5中可以看到:分别在28.3°,32.9°,47.2°,55.8°,76.0°和78.5°等衍射角处出现衍射峰,可以分别对应于Bi2WO6的(131),(002),(202),(331),(210)和(204)晶面,与标准卡片JCPDS:39-0256相吻合,而其余的衍射峰(26.6°,33.8°,51.8°,61.7°,65.7°)均属于FTO基体上(JCPDS:46-1088)的SnO2,结果说明长在FTO基体上的Bi2WO6属于正交晶系.而对于Pt-Bi2WO6/FTO材料,Pt-Bi2WO6/FTO衍射峰的位置与Bi2WO6/FTO基本保持一致,可能是负载的Pt颗粒含量比较少的原因.而与复合材料Pt-Bi2WO6/FTO相比,Pt@rGO-Bi2WO6/FTO峰强度大大减弱,这是由于Bi2WO6/FTO纳米片表面均匀覆盖有rGO层而引起的.
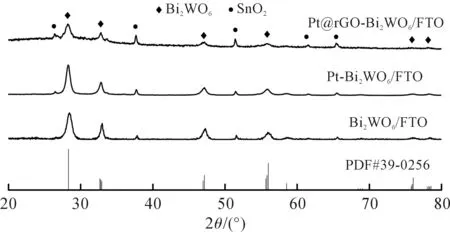
图5 3种材料的XRD图Fig.5 XRD patterns of samples of samples
2.3 复合材料的紫外-可见漫反射光谱
UV-vis漫反射谱能反映半导体材料的光学吸收性能.图6(a)为Bi2WO6/FTO,rGO-Bi2WO6/FTO,Pt-Bi2WO6/FTO和Pt@rGO-Bi2WO6/FTO四种材料的UV-vis漫反射谱图.由图6(a)可知:Bi2WO6/FTO的吸收波长为450 nm;当表面覆盖rGO层后,rGO-Bi2WO6/FTO的吸收范围明显红移,达到460 nm.而Pt颗粒负载到Bi2WO6/FTO和rGO-Bi2WO6/FTO表面上后,光吸收范围发生红移的现象更为明显,Pt-Bi2WO6/FTO材料的吸收范围达到了485 nm,而Pt@rGO-Bi2WO6/FTO复合材料的吸收边可以达到540 nm.这可能是Pt纳米颗粒存在等离子共振现象,拓宽了Bi2WO6/FTO和rGO-Bi2WO6/FTO对太阳光的吸收范围.根据Tauc公式,可以计算出半导体材料的禁带宽度,有
αhν=A(hν-Eg)n
式中:h为普朗克常数;ν为振动频率;α为吸收因子;Eg为半导体材料的禁带宽度.根据文献[15],Bi2WO6的n取值为1/2.通过计算得到Bi2WO6/FTO,rGO-Bi2WO6/FTO,Pt-Bi2WO6/FTO和Pt@rGO-Bi2WO6/FTO材料对应的Tauc曲线,如图6(b)所示.由图6(b)可得:4种材料的禁带宽度分别为2.96,2.93,2.88,2.73 eV,说明贵金属Pt颗粒负载和石墨烯层的覆盖,均有助于减小半导体材料Bi2WO6的禁带宽度.
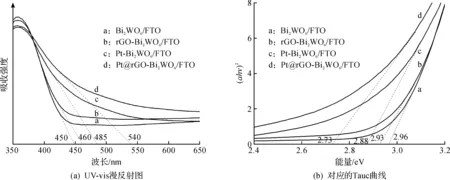
图6 4种复合材料的漫反射图和Tauc曲线Fig.6 Absorption spectra and Tauc curves of samples
2.4 电极材料的计时光电流
计时光电流曲线,可以衡量半导体材料对光的响应能力.图7为Pt-Bi2WO6/FTO和Pt@rGO-Bi2WO6/FTO电极材料在0 V(vs. SCE)偏压下的计时光电流曲线.为了考察电极材料对甲醇光催化氧化的能力,计时光电流曲线分别在1 mol/L KOH电解液和1 mol/L KOH +0.5 mol/L CH3OH电解液中测定.图7(a)为Pt-Bi2WO6/FTO和Pt@rGO-Bi2WO6/FTO材料在1 M KOH电解液中的光电流响应.由图7(a)可知:2种复合材料电极受光辐照后,反应体系都迅速产生光电流,说明2种半导体材料内部电子快速被激发并跃迁;Pt@rGO-Bi2WO6/FTO材料电极的光电流比Pt-Bi2WO6/FTO材料电极的高一些,这一现象与材料的光谱吸收相一致.2种材料的光电流随着时间的推进而逐步降低,并到一定程度光电流衰退的现象趋于平稳,这是由于材料体相内存在着光生电子和空穴复合的现象.可以看到Pt-Bi2WO6/FTO的光电流密度在360 s后降至1.5 μA/cm2,而Pt@rGO-Bi2WO6/FTO的光电流密度为3.5 μA/cm2,比Pt-Bi2WO6/FTO高出2倍多,这说明rGO层为光生载流子提供了快速迁移的通道,有助于减少光生载流子的复合.图7(b)为Pt-Bi2WO6/FTO和Pt@rGO-Bi2WO6/FTO材料在1 mol/L KOH+0.5 mol/L CH3OH电解液中的光电流响应结果.从图7(b)可以看到:2种光催化材料的光电流密度分别达到10 μA/cm2和16 μA/cm2,都比在没有甲醇的电解液中高很多;而且随着时间的推移,Pt-Bi2WO6/FTO和Pt@rGO-Bi2WO6/FTO电极的光电流密度保持稳定,没有出现衰退现象,这说明2种光催化材料都具有光催化氧化甲醇的能力.Pt@rGO-Bi2WO6/FTO在光源打开的瞬间,光电流密度有比较明显增加的现象,而在Pt-Bi2WO6/FTO复合材料电极上没有看到这种现象,这是rGO为光生载流子提供迁移到氧化石墨烯表面,参与甲醇氧化过程的证据.同样地,Pt@rGO-Bi2WO6/FTO的光电流密度为16 μA/cm2,是Pt-Bi2WO6/FTO电极的1.6倍,说明Pt@rGO-Bi2WO6/FTO复合材料电极比Pt-Bi2WO6/FTO具有更好的光催化氧化甲醇能力.
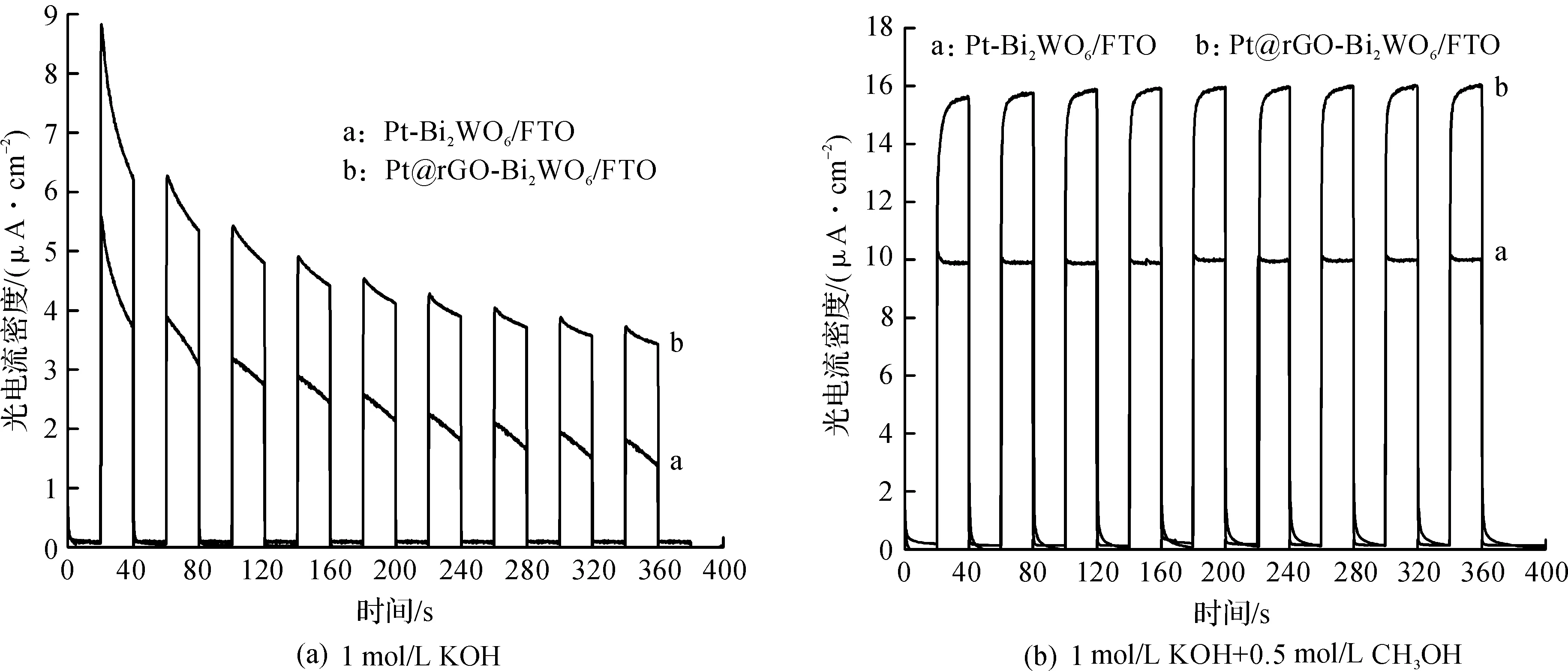
图7 不同电解液下2种电极的计时光电流图Fig.7 I-t curves of electrodes in different electrolyte
2.5 电极的光电催化氧化甲醇的性能
图8为Pt-Bi2WO6/FTO和Pt@rGO-Bi2WO6/FTO电极在1 mol/L KOH+0.5 mol/L CH3OH电解液中的循环伏安曲线,曲线a和b分别表示Pt-Bi2WO6/FTO和Pt@rGO-Bi2WO6/FTO电极在没有受光辐射时的循环伏安曲线,曲线a′和b′分别表示Pt-Bi2WO6/FTO和Pt@rGO-Bi2WO6/FTO电极在光辐射时的循环伏安曲线.可以看到,无论光辐射与否,这两种电极在碱性甲醇溶液中以50 mV/s扫描速度进行循环扫描时,都出现典型的双氧化峰,即当正向扫描时,在电位在-0.16~0.21 V左右出现氧化峰,此氧化峰为甲醇的直接氧化,此时峰电流密度记为If,峰电流对应的电势记为Uf.当反向扫描时,在-0.25~0.27 V左右出现第二个氧化峰,这是甲醇氧化后所得中间产物的再氧化过程,此时峰电流密度记为Ib,峰电流对应的电势记为Ub.循环伏安测试的结果分别汇总见表1,2.
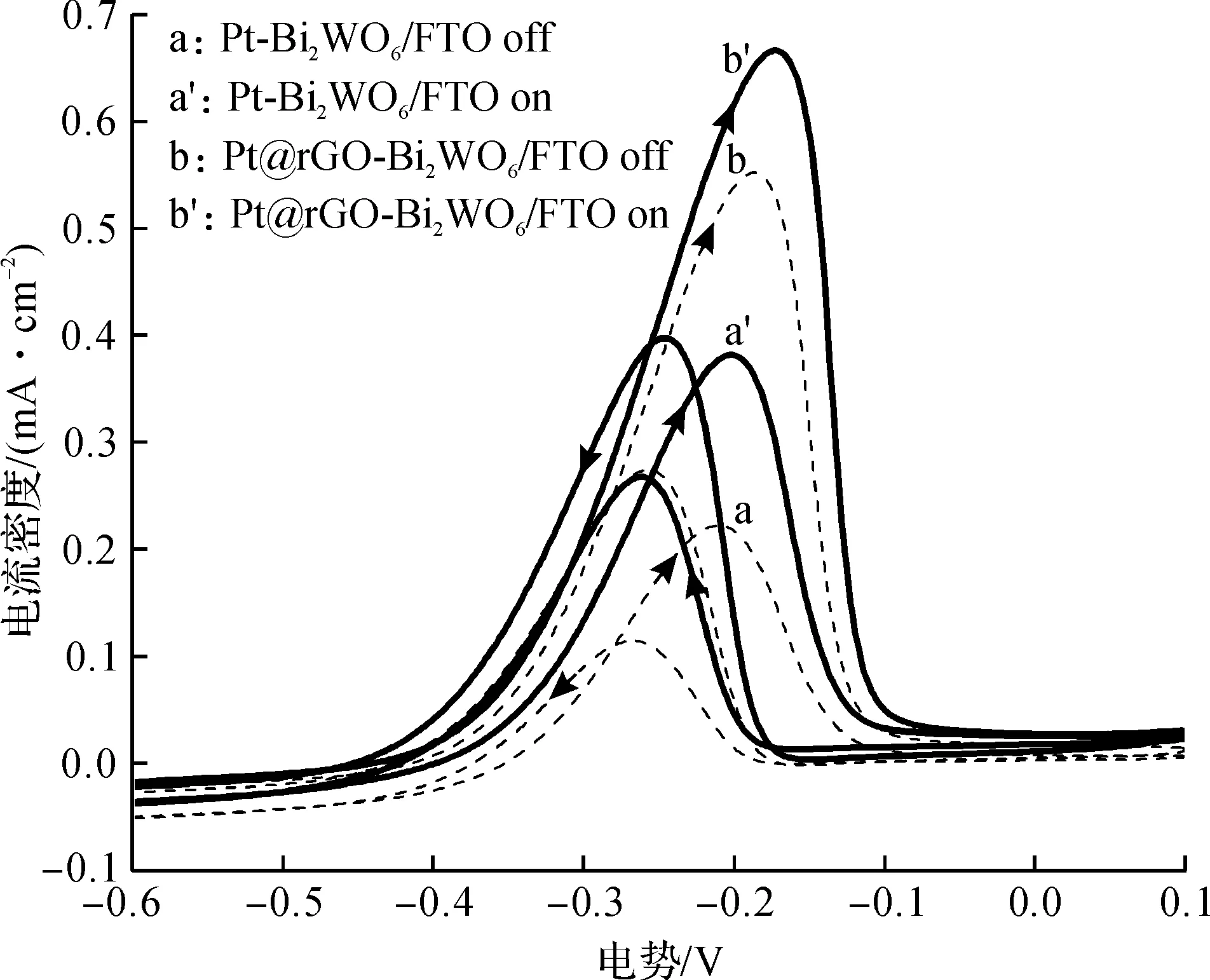
图8 2种电极的CV曲线Fig.8 Cycle voltammentry curves of electrodes
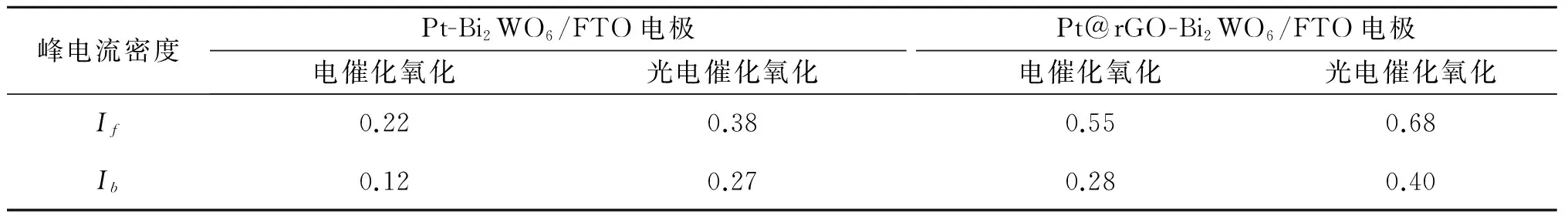
峰电流密度Pt-Bi2WO6/FTO电极电催化氧化光电催化氧化Pt@rGO-Bi2WO6/FTO电极电催化氧化光电催化氧化If0.220.380.550.68Ib0.120.270.280.40
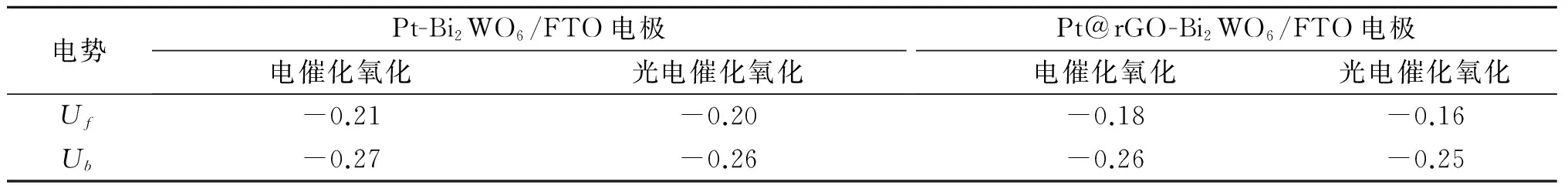
表2 不同电极材料的电催化和光电催化的电势参数Table 2 Electrocatalytic and photoelectrocatalytic potential parameters of different electrodes V
对于Pt-Bi2WO6/FTO电极,在没有光辐射下,If和Ib分别为0.22 mA/cm2和0.12 mA/cm2,对应Uf和Ub为-0.21 V和-0.27 V (vs. SCE).而在有光辐射下,If和Ib均有所提高,达到0.38 mA/cm2和0.27 mA/cm2,对应Uf和Ub为-0.20 V和-0.26 V(vs. SCE).电流密度的提高和电势的正移都归因于Bi2WO6材料的光催化作用.而Pt@rGO-Bi2WO6/FTO电极,无论光辐射与否,相比于Pt-Bi2WO6/FTO电极,其电流密度增加明显,且对应电势也有较大程度的正移.在没有光辐射时,If和Ib分别达到0.55 mA/cm2和0.28 mA/cm2,比Pt-Bi2WO6/FTO电极高了0.33 mA/cm2和0.16 mA/cm2,对应Uf和Ub也分别正移了0.03 V和0.01 V.当受光辐照时,If和Ib分别达到0.68 mA/cm2和0.40 mA/cm2,比Pt-Bi2WO6/FTO电极受光辐射时也高出0.30 mA/cm2和0.13 mA/cm2,对应Uf和Ub也分别正移了0.04 V和0.01 V.这主要归因于rGO的高导电性,使得复合材料自身电子传输能力增强,抑制了光生载流子的复合.
利用计时安培法可以测定电极材料的稳定性.图9为Pt-Bi2WO6/FTO和Pt@rGO-Bi2WO6/FTO电极在1 M KOH+0.5 M CH3OH的电解液中,外加偏压-0.20 V下测得的结果.可以看到,在初始200 s内,2种电极的光电流密度迅速降低,这是由于在甲醇氧化过程的初期,生成的碳质中间体(主要为CO)会吸附在电极的活性位点上.随着氧化反应的进行,光电流降低的趋势有所减缓,Pt@rGO-Bi2WO6/FTO的光电流始终高于Pt-Bi2WO6/FTO.受光辐射1 200 s后,Pt@rGO-Bi2WO6/FTO的电流密度是Pt-Bi2WO6/FTO的2倍.这一现象说明,在复合材料中引入rGO,能极大地提高电极的抗CO中毒性能.这可能是rGO表面具有含氧基团,比较多地吸附了CO等氧化中间产物;有利于Bi2WO6受光激发的光生载流子和空穴将这些氧化中间体进一步氧化,使得Pt@rGO-Bi2WO6/FTO具有比Pt-Bi2WO6/FTO更好的稳定性.

图9 光照下2种电极的稳定性图Fig.9 Stability curves of electrodes under solar light
2.6 Pt@rGO-Bi2WO6/FTO光电催化甲醇氧化机理
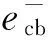
光照后,阳极上的反应方程式分别为
(1)
(2)
Pt+CH3OH+6OH-→Pt+CO2+5H2O+6e-
(3)
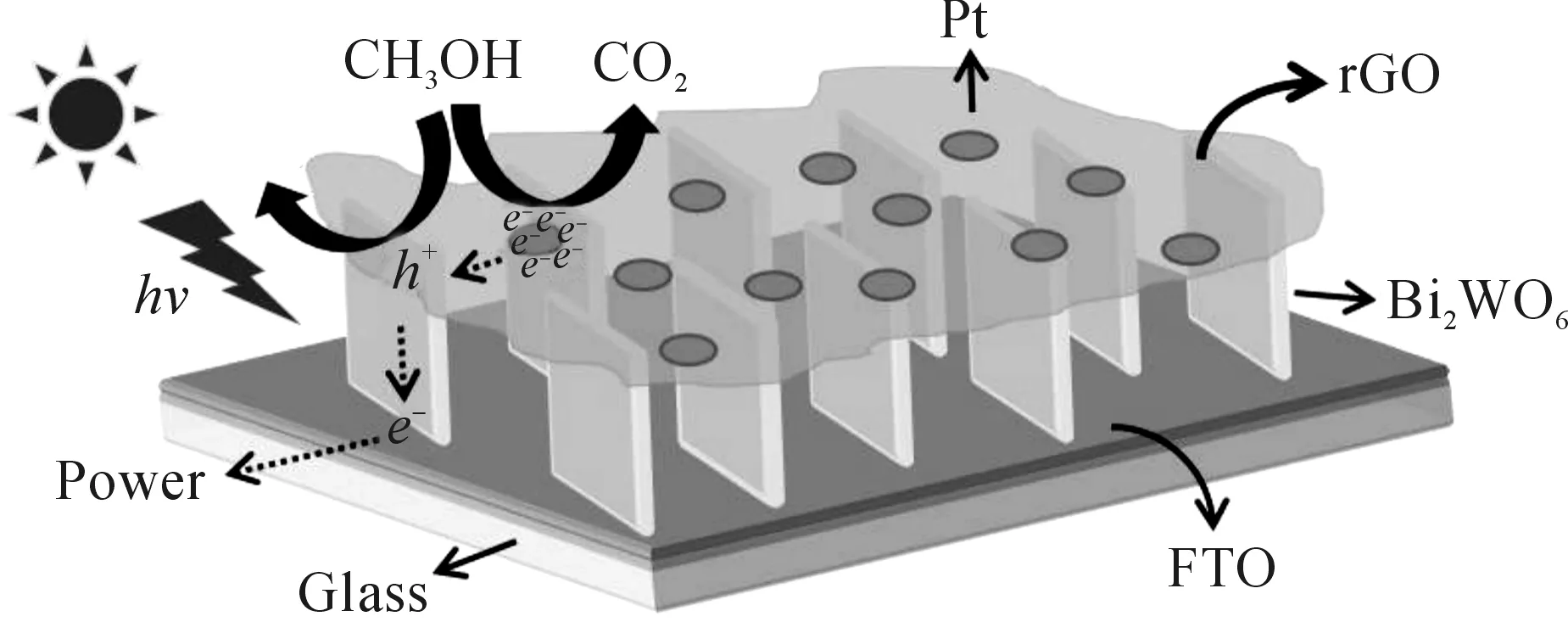
图10 Pt@rGO-Bi2WO6/FTO光电催化甲醇氧化机理示意图Fig.10 Schematic diagram of photoelectrocatalytic oxidation of methanol of Pt@rGO-Bi2WO6/FTO electrode under solar light
3 结 论
采用水热法、热还原法和光沉积法,将还原氧化石墨烯(rGO)和铂纳米颗粒负载到钨酸铋垂直纳米片,分别制得rGO-Bi2WO6/FTO,Pt-Bi2WO6/FTO和Pt@rGO-Bi2WO6/FTO等复合材料.Bi2WO6的存在减少了贵金属Pt的用量,同时起到光电催化协同作用.与Pt-Bi2WO6/FTO相比较,Pt@rGO-Bi2WO6/FTO呈现出更好的光电催化甲醇氧化能力.当受光辐照时,Pt@rGO-Bi2WO6/FTO峰电流密度分别达到0.68 mA/cm2和0.40 mA/cm2,比Pt-Bi2WO6/FTO电极高出0.30 mA/cm2和0.13 mA/cm2,峰电流对应的电位正移0.04 V和0.01 V.Pt@rGO-Bi2WO6/FTO具有更强的抗CO中毒性.在经历1 200 s光电催化后,Pt@rGO-Bi2WO6/FTO的光电流密度是Pt-Bi2WO6/FTO的2倍.总之,rGO的引入有效提高了Pt-Bi2WO6/FTO电极的光电催化性能和稳定性能,对后续电极应用于DMFC具有较大意义.
[1] ZHANG Z H, YUAN Y, FANG Y J, et al. Photoelectrochemical oxidation behavior of methanol on highly ordered TiO2nanotube array electrodes[J]. Journal of electroanalytical chemistry,2007,610(2):179-185.
[2] WANG L, LIU Y N, YANG X D, et al. A high-performance direct methanol fuel cell with a polymer fiber membrane and RuO2/CNTs as a cathode catalyst[J]. Journal of materials chemistry A,2013,1(5):1834-1839.
[3] ROKESH K, PANDIKUMAR A, MOHAN S C. K, et al. Aminosilicate sol-gel supported zinc oxide-silver nanocomposite material for photoelectrocatalytic oxidation of methanol[J]. Journal of alloys and compounds,2016,680: 633-641.
[4] 滕文娟,毛信表,马淳安.碳纳米管载碳化钨的制备及其对甲醇氧化的电催化性能[J].浙江工业大学学报,2011,39(4):364-368.
[5] WANG X, LI X, LIU D, et al. Green synthesis of Pt/CeO2/graphene hybrid nanomaterials with remarkably enhanced electrocatalytic properties[J]. Chemical communication,2012,48(23):2885-2887.
[6] CHOI Y, GU M, PARK J, et al. Graphene multilayer supported gold nanoparticles for efficient electrocatalysts toward methanol oxidation[J]. Advanced energy materials,2012,2(12):1510-1518.
[7] ZHAO S, YIN H, DU L, et al. Three dimensional N-doped graphene/PtRu nanoparticle hybrids as high performance anode for direct methanol fuel cells[J]. Journal of materials chemistry A,2014,2(11):3719-3724.
[8] DREW K, GIRISHKUMAR G, VINODAGOPAL K, et al. Boosting fuel cell performance with a semiconductor photocatalyst: TiO2/Pt-Ru hybrid catalyst for methanol oxidation[J]. Journal of physical chemistry B,2005,109(24):11851-11857.
[9] PANDIKUMAR A, MURUGESAN S, RAMRAJ R. Functionalized silicate sol-gel-supported TiO2-Au core-shell nanomaterials and their photoelectrocatalytic activity[J]. ACS applied materials & interfaces,2010,2(7):1912-1917.
[10] WANG C Q, YUE R R, WANG H W, et al. Dendritic Ag@Pt coreeshell catalyst modified with Reduced graphene oxide and titanium dioxide: fabrication, characterization, and its photo-electrocatalytic performance[J]. International journal of hydrogen energy,2014,39:5764-5771.
[11] YUE L F, WANG S F, SHAN G Q, et al. Novel MWNTs-Bi2WO6composites with enhanced simulated solar photoactivity toward adsorbed and free tetracycline in water[J]. Applied catalysis B: environmental, 2015,176/177:11-19.
[12] DI J, XIA J X, GE Y P, et al. Novel visible-light-driven CQDs/Bi2WO6hybrid materials with enhanced photocatalytic activity toward organic pollutants degradation and mechanism insight[J]. Applied catalysis B: environmentral,2015,168/169:51-61.
[13] NG C, IWASE A, NG Y H, et al. Transforming anodized WO3films into visible-light-active Bi2WO6photoelectrodes by hydrothermal treatment[J]. Journal of physical chemistry letters,2012,3(7):913-918.
[14] ZHOU Y, ZHANG X J, ZHANG Q, et al. Role of graphene on the band structure and interfacial interaction of Bi2WO6/grapheme composites with enhanced photocatalytic oxidation of NO[J]. Journal of materials chemistry A,2014,2(39):16623-1663.
[15] TANG R F, SU H F, DUAN S X, et al. Enhanced visible-light-driven photocatalytic performances using Bi2WO6/MS (M=Cd, Zn) heterostructures: facile synthesis and photocatalytic mechanisms[J]. RSC advances,2015,5(52):41949-41960.
[16] 朱英红,李艳芳,朱颍,等. MnO2/CNTs电催化剂及其对C—H键的选择性催化活性[J].浙江工业大学学报,2015,43(2):128-132.
[17] ZHENG J N, LV J J, LI S S, et al. One-pot synthesis of reduced graphene oxide supported hollow Ag@Pt core-shell nanospheres with enhanced electrocatalytic activity for ethylene glycol oxidation[J]. Journal of materials chemistry A,2014,2(10):3445-3451.
[18] 郑华均,赵浙菲,李世雄,等.三氧化钨纳米线的制备及对染料的选择性吸附[J].浙江工业大学学报,2015, 43(2):119-123.
[19] ZHAO Z F, BUTBUREE T, PEERAKIATHAJOHN P, et al. Carbon quantum dots sensitized vertical WO3nanoplates with enhanced photoelectrochemical properties[J]. Chemistryselect,2016,1(11):2772-2777.
[20] ZHAO Z F, BUTBUREE T, LYV M Q,et al. Etching treatment of vertical WO3nanoplates as a photoanode for enhanced photoelectrochemical performance[J]. RSC advances,2016,6(72):68204-68210.
[21] HUMMERS W S, OFFEMAN R E. Preparation of graphitic oxide[J]. Journal of the american chemical society,1958,80:1339.
