Ti-Nb合金在冷变形中的微观组织和力学性能研究
2018-01-13马凤仓刘新宽何代华
郑 博, 马凤仓, 刘新宽, 李 伟, 何代华
(上海理工大学 材料科学与工程学院, 上海 200093)
钛合金作为一种具有良好生物相容性、抗腐蚀性和力学性能的生物医用金属材料,已经得到了实际应用[1].早在20世纪60年代[2],纯钛作为人体植入物就开始应用于临床.发展至今,医用钛合金的开发和应用先后经历了三个阶段[3]:第一阶段以纯钛和TC4为代表的传统α型钛合金,由于强度低,耐磨性差,仅用于承载较小部位的骨替代及口腔修复[4].第二阶段是以Ti-5Al-2.5Fe和Ti-6Al-7Nb合金为代表的新型α+β型钛合金,其中Ti-Ni基形状记忆合金,因其具有优异的形状记忆特性和超弹性以及耐腐蚀性,已成为继Fe-Cr-Ni,Co-Cr,Ti-6Al-4V合金后在生物医学领域广泛使用的金属材料[5-6].但由于Ni是潜在的毒性元素,以及Ni表面逸出问题令人担忧,因此用于替代Ti-Ni合金的无Ni生物医用形状记忆合金得到了发展[7].与其他金属相比,这两代材料的弹性模量较低,约110 GPa,但远远高于骨头的弹性模量(10~30 GPa),这就会造成植入物与人体骨头界面上力学性能不匹配,容易引起“应力屏蔽”效应[8-9],从而导致种植失败.因此,近年来各国学者相继研发具有更好生物相容性和更低弹性模量的第三代钛合金,即生物医用β钛合金.相较于其他常用的钛合金,这类新型钛合金具有更低的弹性模量和更高的强度.其含有稳定β相和降低弹性模量的元素,不含对人体有害的V,Al,Ni等元素.目前国内外研究最多的是Ti-Nb[10]系超弹性β钛合金,其抗腐蚀性能高,生物相容性好,且具有最低的弹性模量和较好的形状记忆效应,是最有开发潜力和发展前景的医用钛合金,也是目前医用钛合金的研究热点和重点,具有重要的学术研究和实际临床应用价值.
本论文将对Ti-35Nb-2Ta-3Zr β钛合金在冷变形组织和性能进行研究,主要探讨冷变形对合金中马氏体转变和力学性能的影响.
1 试验方案
本试验采用钨极电弧炉熔炼Ti-35Nb-2Ta-3Zr(质量分数,%,下同)合金.试验用原料有:高纯Ti颗粒(纯度>99.995%)、高纯Nb颗粒(纯度>99.95%)、高纯Ta颗粒(纯度>99.95%)、高纯Zr颗粒(纯度>99.5%).按照设计的成分用电子天平精确称量每种原料.混合后在去离子水中超声清洗30 min,以去除表面杂质.采用钨极电弧炉熔炼合金,合金在炉腔内反复翻转熔炼四次,使其成分均匀,最后将铸锭在长条形的模腔内熔铸成型.将合金在780 ℃固溶处理0.5 h,然后打磨除去表面氧化皮和缺陷.通过双辊轧机对合金进行轧制处理,轧制到厚度为1 mm左右,轧制完成后对轧制薄片按照轧制方向取纵向拉伸试样.拉伸后的样品通过切割、镶样、粗磨、细磨、常规抛光等处理,金相腐蚀液采用HF∶HNO3∶H2O=1∶3∶6(体积比)的混合液,进行显微组织观察分析.
利用XRD分析不同拉伸变形率下合金的物相变化规律,利用偏光显微镜和透射电子显微镜观察不同拉伸变形量下的微观组织.采用纳米压痕试验测试合金的弹性模量及硬度.拉伸试验在2.5 kN的万能拉伸试验机上进行,拉伸速度为0.5 mm/min.
2 结果和分析
2.1 拉伸过程中马氏体相变
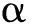
2.2 显微组织分析
图2为固溶样品和拉伸变形率分别为5%,15%,25%及拉断的样品的光学显微组织.
图1 固溶和不同伸长率试样的XRD图谱Fig.1 XRD patterns of solid solution and different elongation

图2 780 ℃,0.5 h固溶样品的微观组织,拉伸形变组织和拉断组织Fig.2 Microstructure of solution-treated specimen at 780 ℃ for 0.5 h and tensile deformation specimens with the different reductions,and snap

图3 应力诱发马氏体TEM明场像、暗场像、选区电子衍射图和位错Fig.3 TEM bright and dark field images of stress-induced ″ martensite,respectively,electron diffraction diagram for the constituency and the image of dislocation structure
2.3 力学性能
表1 为纳米压痕试验测得的固溶和不同轧制状态下样品的硬度及弹性模量,分析表1中数据不难得出,轧制对合金弹性模量影响不大,合金的弹性模量在74 GPa左右,相比其他合金,该合金的弹性模量较小;固溶态的合金硬度较轧制态的合金小,当合金轧制变形量为20%时,合金硬度较固溶时有大幅度增大,当轧制变形量为40%~90%时,合金硬度的增加较为缓慢,这与合金在冷变形中残余应力的累积、位错塞积以及马氏体的转变有关.

表1 样品在固溶和不同轧制状态下的硬度和弹性模量Tab.1 Hardness and elastic modulus under different rolling state and solid solution
图4为合金样品在固溶处理和冷轧后的应力-应变曲线(a)和断裂伸长率(b).如图4所示,固溶处理的合金试样抗拉强度大约为500 MPa,它的断裂伸长率将近27%,表现出良好的塑性.随着轧制变形率的增加,合金的抗拉强度逐渐增加,除了变形中产生的位错,应力诱发马氏体组织也对合金的强度做出了较大的贡献[12],但是合金的断裂伸长率随轧制变形量的增加而逐渐降低,马氏体的可塑性很大程度上取决于二级马氏体的微观结构[13].和固溶样品相比,当合金轧制变形量为20%时,合金的伸长率迅速下降,然而,当合金轧制变形量为40%~60%时,伸长率下降变得缓慢.当轧制变形量达到90%时,合金的抗拉强度增加到800 MPa,断裂伸长率却不到5%,而且几乎没有塑性变形阶段,发生屈服后就断裂,这在很大程度上取决于次生马氏体的微观结构.纵观整个过程,冷变形后的合金抗拉强度高于固溶态合金的抗拉强度,但是固溶态合金的塑性远高于轧制态的合金,这是由于在轧制过程中合金中的马氏体的形态发生转变,马氏体之间相互交叉变异,以及位错的缠结和塞积使合金塑性变差.相比其他金属而言,即使TiNb β钛合金在轧制变形量为达90%的状态下,断裂伸长率仍能达到5%,表现出良好的冷加工性能.
图5显示了轧制变形量为20%和80%样品拉伸断面的SEM图像.两组样品的断裂形态都表现为韧性断裂.由图4(b)可以看出,两组合金样品在断裂之前都经过较大的伸长量,但是两组样品断面的韧窝有所不同.如图5所示,轧制变形量为20%的合金样品塑性较好,断面韧窝较密,且较大韧窝中还会出现小韧窝,韧窝大致呈卵形;轧制变形量为80%的合金样品韧窝较少,且韧窝大小不一,韧窝形状较为复杂多样.

图4 合金样品在固溶处理和冷轧后的应力-应变曲线Fig.4 Alloy samples after solid solution treatment and cold rolling stress strain curveand elongation at break

图5 拉伸试样的断裂表面SEM照片Fig.5 SEM images of the fracture surface of tensile tested specimens
3 结 论
从上述试验结果及讨论中,我们观察到了拉伸过程中应力诱发马氏体的生成现象,综合合金在冷变形前后的力学性能特点,主要结论如下:
(2) 从力学试验结果看出,合金的弹性模量较低,在74 GPa左右,合金硬度随冷变形程度的增加而增大.分析应力-应变曲线可以看出,固溶态的合金具有很高的断裂伸长率,能达到27%,屈服强度达到430 MPa,抗拉强度达到500 MPa,当合金轧制变形量为90%时,抗拉强度增大到800 MPa,断裂伸长率将近5%,表现出了良好的可塑性和高强度性能.
[1]茹志芳,李岩,罗坤,等.低弹性模量钛合金的研究进展[J].材料导报,2011,25(S1):250-253,263.
[2]王运锋,何蕾,郭薇.医用钛合金的研究及应用现状[J].钛工业进展,2015,32(1):1-6.
[3]许标,姜云海,朱渊.医用钛合金的研究现状及发展[J].科技创新导报,2015(6):201-202,204.
[4]VAN NOORT R.Titanium:the implant material of today[J].Journal of Materials Science,1987,22(11):3801-3811.
[5]袁志山,白鸽玲,冯昭伟,等.生物医用无Ni超弹性β钛形状记忆合金研究进展[J].材料导报,2009,23(7):86-89,100.
[6]蔡伟,孟祥龙,赵新青,等.TiNi基高温形状记忆合金的马氏体相变与形状记忆效应[J].中国材料进展,2012,31(12):40-47.
[7]LAING P G,FERGUSON A B JR,HODGE E S.Tissue reaction in rabbit muscle exposed to metallic implants[J].Journal of Biomedical Materials Research,1967,1(1):135-149.
[8]HUISKES R,WEINANS H,VAN RIETBERGEN B.The relationship between stress shielding and bone resorption around total hip stems and the effects of flexible materials[J].Clinical Orthopaedics and Related Research,1992(274):124-134.
[9]SUMNER D R,GALANTE J O.Determinants of stress shielding:design versus materials versus interface[J].Clinical Orthopaedics and Related Research,1992(274):202-212.
[10]刘福,吴树建,王立强.新型医用钛合金的特点及发展现状[J].热加工工艺,2008,37(12):100-103.
[11]WANG L Q,LU W J,QIN J N,et al.Tensile properties of in situ synthesized (TiB+La2O3)/β-Ti composite[J].Materials Science and Engineering:C,2009,29(6):1897-1900.
[12]WANG L Q,LU W J,QIN J N,et al.Influence of cold deformation on martensite transformation and mechanical properties of Ti-Nb-Ta-Zr alloy[J].Journal of Alloys and Compounds,2009,469(1/2):512-518.
[13]WANG L Q,LU W J,QIN J N,et al.Microstructure and mechanical properties of cold-rolled TiNbTaZr biomedical β titanium alloy[J].Materials Science and Engineering:A,490(1/2):421-426.
