微波辐射下丙烯海松酸烯丙酯的合成、表征及UV固化反应
2018-01-09卢言菊赵振东徐士超
卢言菊, 赵振东*, 古 研, 王 婧, 徐士超
(1.中国林业科学研究院 林产化学工业研究所;生物质化学利用国家工程实验室;国家林业局 林产化学工程重点开放性实验室;江苏省 生物质能源与材料重点实验室,江苏 南京 210042;2.中国林业科学研究院 林业新技术研究所,北京 100091)
微波辐射下丙烯海松酸烯丙酯的合成、表征及UV固化反应
卢言菊1,2, 赵振东1,2*, 古 研1, 王 婧1, 徐士超1,2
(1.中国林业科学研究院 林产化学工业研究所;生物质化学利用国家工程实验室;国家林业局 林产化学工程重点开放性实验室;江苏省 生物质能源与材料重点实验室,江苏 南京 210042;2.中国林业科学研究院 林业新技术研究所,北京 100091)

微波辐射;丙烯海松酸;丙烯海松酸烯丙酯;UV固化反应;表干时间
松香是天然可再生资源,主要来源于松树的采脂。松香树脂酸为多种组分的同分异构体,主要成分为枞酸型树脂酸,此类型的树脂酸在加热的条件下可以发生构型转化生成具有共轭双键的左旋海松酸,而左旋海松酸可以与丙烯酸发生双烯加成(Diels-Alder)反应,生成二元的丙烯海松酸,对松香自身及改性加上去的羧基进行改性可以合成多种新型松香基功能性衍生物[1-5]。丙烯海松酸酯类产品是松香的重要改性产品,且无毒环保。毛英利等[6]合成了端羟基丙烯海松酸新戊二醇酯(ANGE),并以其为主要原料,通过预聚体法制备了固含量为33%~35%的ANGE改性水性聚氨酯乳液,乳液的综合性能良好。Yu等[7]以丙烯海松酸和2-羟基甲基丙烯酸酯为原料,制备得到松香的丙烯酸酯,并研究了其聚合反应,结果表明其在聚合反应中可代替二乙烯基苯单体。目前还未见丙烯海松酸烯丙酯(AA)的制备及性能研究的文献报道。AA是一类含有活泼环外双键的高分子单体,可作为涂料、胶黏剂、环氧树脂等生物质基高分子材料的单体[8-10]。对于以松香衍生物为单体进行的UV固化近年来也有诸多文献报道,但均是将松香的结构作为附属结构引入到聚合物,而并不是松香的主体结构直接参与聚合反应[11-13]。因此,本研究尝试将松香的主体结构直接作为聚合反应的单体,以松香为原料,经改性制备丙烯海松酸,进一步与氯丙烯反应得到AA,然后将AA进行UV固化反应,研究其固化性能。
1 实 验
1.1原料、试剂与仪器
湿地松松香(含树脂酸92%),购于江西飞尚林产有限公司;丙烯酸为化学纯,氢氧化钠、十六烷基三甲基溴化铵、氯丙烯、对苯二酚、 N,N-二甲基甲酰胺(DMF)、正己烷,均为分析纯。
单模微波有机合成仪,上海新仪微波化学科技有限公司;MAGNA-IR 550红外光谱议,美国尼高力公司;岛津GC2014气相色谱仪,上海精密科学仪器有限公司;Agilent 6890N/5973N质谱仪,美国安捷伦公司;Diamond DSC差示扫描量热仪,美国Perkin-Elmer公司。
1.2丙烯海松酸烯丙酯(AA)的制备
1.2.1丙烯酸改性松香 以松香为原料,经乙醇洗涤除去中性物后制备得到树脂酸,在三口烧瓶中加入树脂酸和丙烯酸,n(树脂酸)∶n(丙烯酸)=2∶1,在反应温度230 ℃、微波功率400 W和反应时间 90 min 条件下,通过Diles-Alder反应,制备得到丙烯酸改性松香。
1.2.2丙烯海松酸钠 将丙烯酸改性松香用过量的NaOH水溶液溶解后,用5%的HCl滴定至pH值6.0,过滤除去生成的沉淀,将滤液滴定至过酸后过滤得丙烯海松酸。将一定量的氢氧化钠用乙醇溶解,随后以滴加的方式边搅拌边加入到丙烯海松酸的乙醇溶液中,滴加完毕后继续搅拌1 h,再减压过滤,取滤饼干燥后得到丙烯海松酸钠。
1.2.3丙烯海松酸烯丙酯(AA) 在100 mL微波专用三口烧瓶中加入丙烯海松酸钠和氯丙烯,n(丙烯海松酸钠)∶n(氯丙烯)=1∶2,氯丙烯逐滴加入,以N,N-二甲基甲酰胺(DMF)为溶剂,同时在反应瓶中加入5%的十六烷基三甲基溴化铵为催化剂,0.2%的对苯二酚为阻聚剂,在微波辅助的条件下发生反应,设定反应条件为:微波功率400 W、反应时间2.5 h、反应温度50 ℃。在本实验条件下制备的AA为黄色黏状液体,产物收率为72.9%,经纯化后GC含量为98.6%。
AA的合成反应如下:

1.3AA的UV固化反应
采用丙烯海松酸烯丙酯为单体, 2-羟基-2-甲基-1-苯基-1-丙酮(1173)为引发剂,引发剂添加量为单体质量的5%,在四氢呋喃中搅拌均匀,将配制好的溶液均匀涂布于马口铁片上,制成均匀的液膜,在紫外光固化仪光照强度100%,光照距离13.5 cm条件下固化并按照标准GB/T 1728—1979(1989)测定固化表干时间;固化完全后溶解固化后的产物,除去溶剂后做FT-IR、TG、DSC等表征。
1.4分析方法
GC分析条件:采用色谱柱为RTX-5(30 m×0.25 mm×0.25 μm)的岛津GC 2014气相色谱仪,进样量2 μL,升温程序:以5 ℃/min的升温速率从200 ℃升温至270 ℃,保留 40 min。
在气相色谱条件下采用Agilent 6890N/5973N质谱仪分析其碎片离子。采用扫描范围为4000~600 cm-1的红外光谱仪进行红外光谱分析,采用压片法表征丙烯海松酸,采用涂膜法表征AA。
采用综合热分析仪分析产物的热重曲线,升温速率为10 ℃/min,测定范围0~800 ℃,气氛为流速20 mL/min的高纯氮;差示扫描量热分析(DSC)扫描温度范围为-100~180 ℃,升温速率为20 ℃/min,气氛为流速20 mL/min的高纯氮。
2 结果与讨论
2.1丙烯海松酸烯丙酯(AA)的表征

2.1.2AA制备过程的气相色谱分析 AA反应过程的气相色谱图如图2所示,其中图2中曲线a为丙烯酸改性松香的GC谱图,从图中可以看出,丙烯酸改性松香除了含有丙烯海松酸的两种同分异构体外[14],还含有少量的海松酸型树脂酸,如8,15-异海松酸、8,15-海松酸、海松酸、山达海松酸、异海松酸,其出峰时间分别为:8.8、 9.1、 9.3、 9.5和10.1 min,GC含量分别为2.4%、 0.3%、 0.8%、 1.2%和7.3%,此外还含有少量的去氢枞酸、枞酸及少量未鉴定的脂肪酸,出峰时间分别为10.6、 11.2及 12.7 min,GC含量分别为7.8%、 1.0%和0.3%。

图1原料及产物的红外光谱图
Fig.1FT-IRspectraofacrylpimaricacidandallylacrylpimarate

图2原料及产物的气相色谱图
Fig.2Gaschromatographyspectraofmaterialandallylacrylpimarate
图2中曲线b为丙烯海松酸的GC谱图,从图中可以看出,丙烯酸改性松香经过提纯后除去了树脂酸部分,制备得到含有两种同分异构体的丙烯海松酸,两个同分异构体产物的主要峰出峰时间分别为15.1和16.6 min,对应的GC含量分别为16.0%和72.3%,此外还含有少量骨架异构的丙烯海松酸。图2中曲线c为制备得到两种同分异构体AA的GC谱图,与曲线b相比,AA的峰形与丙烯海松酸基本相近,但是出峰时间推迟,AA的GC含量总和为98.6%。
2.1.3GC-MS分析 AA的质谱解析中主要碎片离子如图3所示,主要的碎片离子峰中455为M+1峰,分子离子峰为454,AA失去丙烯酸烯丙酯生成了稳定的树脂酸烯丙酯为基峰342,其他碎片离子见文献[15]。
2.1.41H NMR分析 AA的核磁氢谱图如图4(a)所示。δ1.46(m, 1H, C2—H),1.39(m, 1H, C2—H),1.78(t, 2H, C3—H,C22—H),5.36(m,1H,C25—H),5.35(m, 1H,C28—H),5.31(d, 2H,C29—H,C26—H),5.27(s, 1H,C14—H),5.26(d, 2H,C29—H,C26—H),4.59(d, 2H, C24—H),4.58(d, 2H, C27—H),1.79(m, 2H,C12—H,C15—H),1.75(d, H,C21—H),1.73(t, H,C5—H),1.58(t, 3H,C3—H,C21—H,C22—H),1.55(t, H,C11—H),1.54(m, 2H,C6—H,C7—H),1.52(m, 3H,C20—H),1.47(t, 2H,C1—H,C9—H),1.44(m, 2H,C6—H,C7—H),1.28(s, 3H,C19—H),1.17(t, 2H,C1—H,C11—H),1.13(d, 6H,C16—H,C17—H)。

图4 丙烯海松酸烯丙酯的NMR谱图Fig.4 NMR spectrum of allyl acrylpimarate
2.1.513C NMR分析 AA的13C NMR如图4(b)所示,由于AA存在同分异构体,因此,13C NMR解析时发现所得核磁峰均为双重峰,谱图中溶剂氘代氯仿的三重峰分别为δ77.25、77.00和76.75,其他特征化学位移为:松香自身所带羰基及两个同分异构体加成上去的酯键羰基的δ分别为178.14、175.10和174.65,两个同分异构体AA三环菲骨架上双键C原子的δ为149.18和126.55及148.24和123.05,两个同分异构体AA烯丙基双键C原子δ分别为132.41和132.39及118.20和117.81,其他峰的归属见表1所示(150 MHz, CDCl3)。
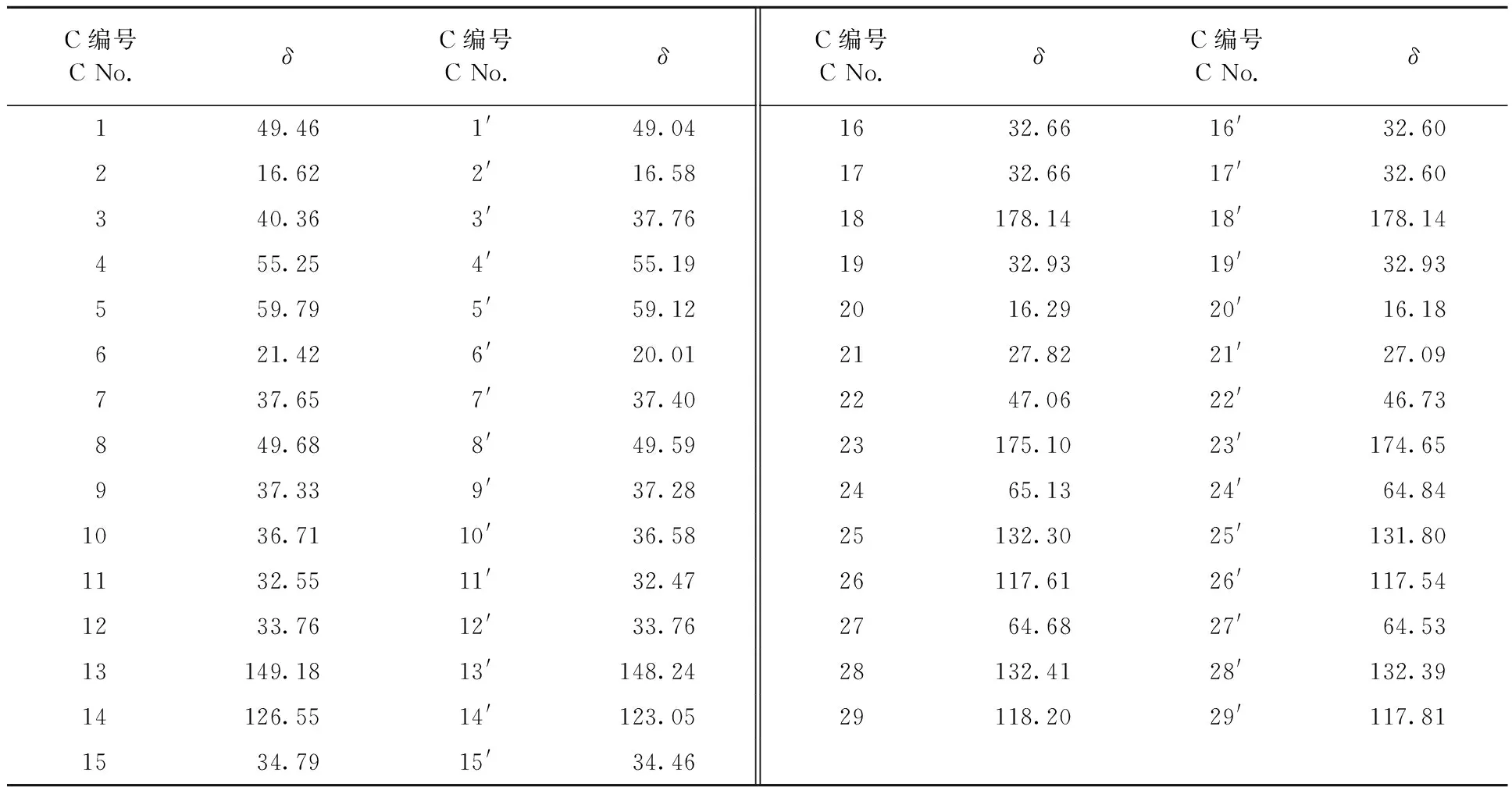
表1 13C NMR中丙烯海松酸烯丙酯各碳原子归属
对制备得到的AA物理性能进行了测试,所得产物为黄色黏状液体,黏度(25 ℃)为980 mPa·s,密度(25 ℃)为1.033 0×103kg/m3,酸值为0.20 mg/g。
2.2AA的UV固化反应

图5 丙烯海松酸烯丙酯UV固化反应的红外谱图Fig.5 FT-IR spectra of allyl acrylpimarate at different curing time

2.2.2不同条件对表干时间的影响 表干时间越短,相对固化速率越快,说明固化反应进行的越快。图6是AA在不同条件下固化的表干时间趋势图,从图6(a)可以看出,当引发剂添加量不大于6%时,表干时间随引发剂添加量的增加快速缩短,当引发剂添加量大于5%时,单体UV固化反应的表干时间随着引发剂添加量的增加下降缓慢并逐渐趋于稳定。这是因为在光照距离和光照强度不变的情况下,初级自由基的数目随着引发剂添加量的增加而增多,固化反应加快,故表干时间缩短;当初级自由基的数目达到一定的程度时使得链增长反应和链终止反应正好处于平衡阶段,引发剂添加量的增加并不能使表干时间缩短。从图6(b)可以看出,表干时间随着光照距离的增大而延长,这是因为光照距离越大,固化组分离光源的距离就越远,能接收到的紫外光强度减弱,从而使得引发的初级自由基数目减少,相对固化速率变慢。从图6(c)可以看出,表干时间随光照强度的增大而缩短,这是因为在其他条件不变的情况下,光照强度增大使得相同表面积上接收到的光子数增加,从而能引发的自由基数目增多。

图6 不同条件对丙烯海松酸烯丙酯UV固化反应表干时间的影响
2.2.3AA的UV固化产物的热分析 图7为AA固化产物的TGDTG谱图,可以看出AA的固化产物热稳定性比较好,具有两段热分解,第一阶段的初始热分解温度为292.9 ℃,终止热分解温度为 348.9 ℃,最大失重温度在335 ℃,此段热失重是AA交联聚合固化产物外层的热分解(如脱羧基等)造成的,失重率为36.84%;第二阶段的初始热分解温度为397.6 ℃,终止热分解温度为430.6 ℃,最大失重温度在421.6 ℃,此段热失重主要是AA聚合物内层的热分解,即树脂的主体结构的分解,失重率为61.4%。
图8为丙烯海松酸烯丙酯UV固化产物DSC图。从图8可以看出,AA的玻璃化转变起始温度为 49.6 ℃,终止温度为55.8 ℃,发生玻璃化转变时的比热变化ΔCp=0.195 J/(g·℃)。

图7丙烯海松酸烯丙酯UV固化产物TG/DTG图
Fig.7TG/DTGcurvesofUVcuredproductfromallylacrylpimarate

图8丙烯海松酸烯丙酯UV固化产物DSC图
Fig.8DSCcurveofUVcuredproductfromallylacrylpimarate
3 结 论
3.1以丙烯海松酸钠和氯丙烯为原料(物质的量之比为1∶2),氯丙烯逐滴加入,以N,N-二甲基甲酰胺(DMF)为溶剂,同时在反应瓶中加入5%的十六烷基三甲基溴化铵为催化剂,0.2%的对苯二酚为阻聚剂,在微波功率400 W、反应温度50 ℃和反应时间2.5 h的条件下,制备得到丙烯海松酸烯丙酯(AA),产品为黄色黏状液体,产物收率为72.9%,经纯化后GC含量为98.6%。
3.2采用气相色谱法、气质联用、红外光谱法、核磁共振等现代分析方法表征了中间产物及目标产物的结构,AA结构中含有2个端基不饱和双键,可作为新型的UV聚合物单体,具有较好的应用前景。

[1]李宇彬,段文贵,陈秋菊,等. 丙烯海松酸基双酰胺类化合物的合成及生物活性研究[J]. 化学试剂,2012,34(1):9-15,54.
LI Y B,DUAN W G,CHEN Q J,et al. Synthesis and study on biological activities of diamide compounds containing acrylpimaric acid moiety[J]. Chemical Reagents,2012,34(1):9-15,54.
[2]SERREQI A N,GAMBOA H,STARK K,et al. Resin acid markers for total resin acid content of in-mill process lines of a TMP/CTMP pulp mill[J]. Water Research,2000,34(5):1727-1733.
[3]WANG H H,LIU B,LIU X Q,et al. Synthesis of biobased epoxy and curing agents using rosin and the study of cure reactions[J]. Green Chemistry,2008,10(11):1190-1196.
[4]赖刚,何熙璞,李芳耀,等. 丙烯海松酸基双硫脲类化合物的合成与表征[J]. 广西大学学报:自然科学版,2012,37(3):489-494.
LAN G,HE X P,LI F Y,et al. Synthesis and characterization of acrylpimaric acid-based dithioureas[J]. Journal of Guangxi University:Natural Science Edition,2012,37(3):489-494.
[5]LOAN B. Polymers from a levopimaric acid-acrylic acid Diels-Alder adduct[J]. Journal of Polymer Science Part A:Polymer Chemistry,2007,45(24):5979-5990.
[6]毛英利,梁鉴泉,李会宁,等. 丙烯海松酸酯改性水性聚氨酯乳液及性能的研究[J]. 现代涂料与涂装,2009,12(11):20-23.
MAO Y L,LIANG J Q,LI H N,et al. Synthesis and performance of new waterborne polyurethane modified by acrylpimaric acid neopentyl glycol ester[J]. Modern Paint & Finishing,2009,12(11):20-23.
[7]YU C L,WANG X L,CHEN C W,et al. Preparation of polystyrene microspheres using rosin-acrylic acid diester as a cross-linking agent[J]. Industrial & Engineering Chemistry Research,2014,53(6):2244-2250.
[8]林桂汕,阮战辉,段文贵,等. 新型丙烯海松酸基双酰胺-噻二唑化合物的合成及生物活性研究[J]. 林业工程学报,2017,2(3):45-51.
LIN G S,RUAN Z H,DUAN W G,et al. Synthesis and biological activity of novel acrylpimaric acid-based diamide-thiadiazole compounds[J]. Journal of Forestry Engineering,2017,2(3):45-51.
[9]李健,饶小平,宋湛谦,等. 丙烯海松酸及其噻二唑衍生物的制备及抑菌活性[J]. 林产化学与工业,2014,34(4):55-59.
LI J,RAO X P,SONG Z Q,et al. Synthesis and antibacterial activity of acrylpimaric acid and its thiadiazole derivatives[J]. Chemistry and Industry of Forest Products,2014,34(4):55-59.
[10]FUKUDA W,MARVEL C S. Polymers from the vinyl esters of different samples of hydrogenated rosins[J]. Journal of Polymer Science Part A:Polymer Chemistry,1968,6(4):1050-1054.
[11]EL-GHAZAWY R A,EL-SHAFEY H I,ELSAEED A M,et al. Liquid crystal bio-based epoxy coating with enhanced performance[J]. Journal of Engineering Research and Applications,2014,4(11):90-96.
[12]ATTA A M,EL-MAHDY G A,AL-LOHEDA H A N,et al. Application of eco-friendly magnetite nanoparticles coated with rosin amidoxime as corrosion inhibitor for mild Steel in 1 M hydrochloric acid solution[J]. International Journal of Electrochemical Science,2015,10:2621-2633.
[13]WILBON P A,CHU F X,TANG C B. Progress in renewable polymers from natural terpenes,terpenoids,and rosin[J]. Macromolecular Rapid Communications,2013,34(1):8-37.
[14]林明涛,王基夫,刘玉鹏,等.丙烯海松酸的合成研究[J]. 应用化工,2014,41(5):802-806.
LIN M T,WANG J F,LIU Y P,et al. Study on the synthesis of acrylpimaric acid[J]. Applied Chemical Industry,2014,41(5):802-806.
[15]卢言菊,王迷霞,古研,等. 二元端乙烯基型松香衍生物的微波辅助制备及表征[J]. 林产化学与工业,2015,35(6):63-68.
LU Y J,WANG M X,GU Y,et al. Synthesis and characterization of di-vinyl-terminated rosin derivatives under microwave irradiation[J]. Chemistry and Industry of Forest Products,2015,35(6):63-68.
Microwave Irradiation Synthesis, Characterization and UV-curing Reaction of Allyl Acrylpimarate
LU Yanju1,2, ZHAO Zhendong1,2, GU Yan1, WANG Jing1, XU Shichao1,2
(1.Institute of Chemical Industry of Forest Products,CAF;National Engineering Lab. for Biomass Chemical Utilization; Key and Open Lab. of Forest Chemical Engineering,SFA;Key Lab. of Biomass Energy and Material,Jiangsu Province, Nanjing 210042, China; 2.Research Institute of Forestry New Technology,CAF, Beijing 100091, China)

microwave irradiation; acrylpimaric acid; allyl acrylpimarate; UV curing reaction; surface drying time
10.3969/j.issn.0253-2417.2017.06.007
2017- 05- 05
中国林科院中央级公益性科研院所基本科研业务费专项资金(CAFYBB2017QA018);国家自然科学基金资助项目(31370575)
卢言菊(1982— ),女,山东临沂人,助理研究员,博士,主要从事萜类化学加工与利用研究;E-mailluyanju-1982@163.com
*通讯作者:赵振东,研究员,博士生导师,主要从事萜类化学、松树病虫害化学、天然产物化学、应用化学等方面的研究与利用;E-mail: zdzhao@189.cn。

LU Yanju
TQ351
A
0253-2417(2017)06- 0049- 07
卢言菊,赵振东,古研,等.微波辐射下丙烯海松酸烯丙酯的合成、表征及UV固化反应[J].林产化学与工业,2017,37(6):49-55.
