2型糖尿病肾病患者血尿酸与肾素-血管紧张素-醛固酮系统的相关性研究*
2018-01-05何建秋王艳新
何建秋,王艳新
(承德医学院附属医院内分泌科,河北承德 067000)
·经验交流·
2型糖尿病肾病患者血尿酸与肾素-血管紧张素-醛固酮系统的相关性研究*
何建秋,王艳新△
(承德医学院附属医院内分泌科,河北承德 067000)
目的探讨2型糖尿病(T2DM)肾病患者血尿酸(UA)水平与肾素-血管紧张素-醛固酮系统(RAAS)的相关性。方法收集2015年3月至2016年3月在该院住院的T2DM患者107例,根据尿清蛋白/肌酐比值(ACR)将其分为3组:正常尿蛋白组(39例)、微量蛋白尿组(38例)和临床蛋白尿组(30例),收集3组受试者的一般临床资料并检测肾素及血管紧张素Ⅱ水平。结果3组患者UA、肾素及血管紧张素Ⅱ水平比较,差异均有统计学意义(P<0.05),且正常蛋白尿组、微量蛋白尿组、临床蛋白尿组UA、肾素及血管紧张素Ⅱ水平均逐渐升高,组间两两比较,差异均有统计学意义(P<0.05)。相关性分析显示,T2DM肾病患者UA水平与肾素及血管紧张素Ⅱ水平均呈正相关(r==0.961,0.961,P<0.05)。结论T2DM患者血UA可能通过激活RAAS参与糖尿病肾病的发病机制。
糖尿病肾病;尿酸;肾素-血管紧张素系统
糖尿病肾病是导致慢性肾衰竭的重要病因,但其发病机制目前尚不确切。近年来的研究提示,高尿酸血症是导致糖尿病肾病发生、发展的危险因素[1]。本研究检测2型糖尿病(T2DM)肾病患者血尿酸(UA)、肾素及血管紧张素Ⅱ水平,探讨患者血UA水平与肾素、血管紧张素水平的相关性,以进一步了解糖尿病肾病的发病机制,并为糖尿病肾病的防治提供理论依据。
1 资料与方法
1.1一般资料 1.1收集2015年3月至2016年3月在本院内分泌科住院的T2DM患者107例,男55例,女52例;年龄18~78岁,平均(53.9±13.7)岁。根据尿微量清蛋白/肌酐比值(ACR)将患者分为3组:正常尿蛋白组39例(ACR<30 μg/mg),微量蛋白尿组38例(ACR为30~<299 μg/mg),临床蛋白尿组30例(ACR>299 μg/mg)。排除标准:合并急性并发症者;心力衰竭患者;肝、肾功能不全患者;严重感染性疾病患者;发热患者;肿瘤患者;原发性肾病患者;尿路感染患者。3组受检者的性别构成、年龄比较,差异有统计学意义(P<0.05),具有可比性,见表1。本研究经本院医学伦理委员会审批通过,患者均知情同意并签署知情同意书。
1.2方法 1.1测定所有受检者的身高、体质量、血压,计算体质量指数(BMI)。受检者均禁食、禁水8 h以上,于次日清晨抽取静脉血,检测空腹血糖(FPG)、糖化血红蛋白(HbA1c)、血清总胆固醇(TC)、三酰甘油(TG)、低密度脂蛋白胆固醇(LDL-C)、血UA、血肌酐(Scr)、血尿素氮(BUN)、肾素及血管紧张素Ⅱ水平,并留取晨起第1次尿液检测ACR。Scr、BUN、UA、血脂测定采用酶法,ACR测定采用免疫比浊法,FPG测定采用己糖激酶法,HbA1c测定采用高效液相法,肾素、血管紧张素Ⅱ测定采用化学发光法。
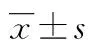
2 结 果
2.13组临床资料比较 3组受检者的FPG、HbA1c及血脂水平比较,差异均无统计学意义(P>0.05);3组BUN、Scr水平比较,差异均有统计学意义(P<0.05),微量蛋白尿组、临床蛋白尿组均高于正常尿蛋白组(P<0.05),见表1。
2.23组UA、肾素及血管紧张素Ⅱ水平比较 3组UA、肾素及血管紧张素Ⅱ水平比较,差异均有统计学意义(P<0.01);且在正常蛋白尿组、微量蛋白尿组、临床尿蛋白组UA、肾素及血管紧张素Ⅱ水平均逐渐升高,组间两两比较,差异均有统计学意义(P<0.05),见表2。
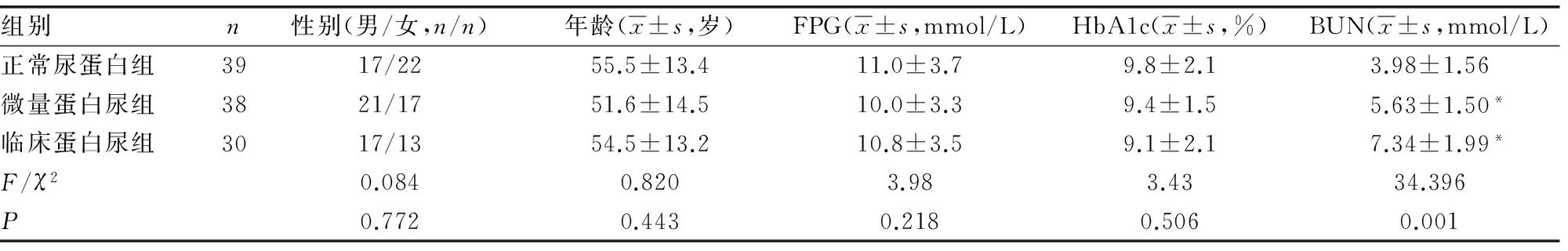
表1 3组患者临床资料比较
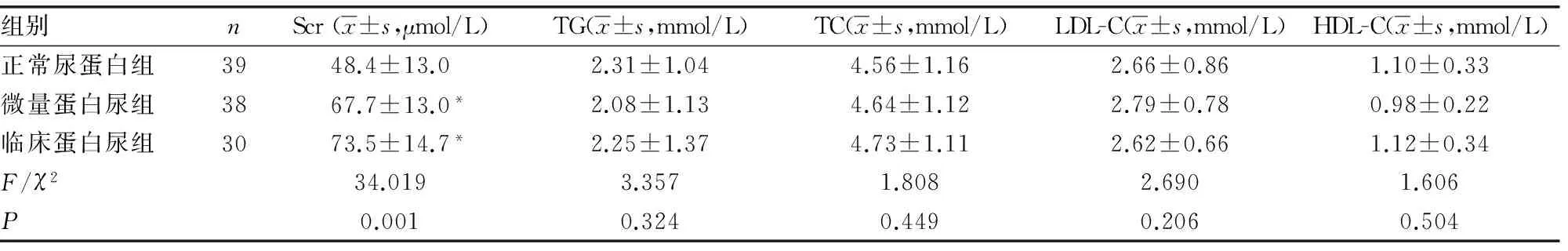
续表1 3组患者临床资料比较
*:P<0.05,与正常尿蛋白组比较

表2 3组患者UA、肾素及血管紧张素Ⅱ水平比较
*:P<0.05,与正常尿蛋白组比较;#:P<0.05,与微量蛋白尿组比较
2.3相关性分析 2型糖尿病肾病患者UA与肾素、血管紧张素Ⅱ水平均呈正相关(r=0.961、0.961,P<0.05)。
3 讨 论
UA作为嘌呤代谢的终产物,主要由细胞代谢分解的核酸和其他嘌呤类化合物,以及食物中的嘌呤经酶作用分解而来。UA的排出减少和生成增多都可能导致高尿酸血症。近年来研究提示,UA是慢性肾脏疾病的预测因素之一,并且可能是慢性肾脏疾病的治疗靶点之一,高水平血UA可能通过肾素-血管紧张素-醛固酮系统(RAAS)激活参与糖尿病肾病的发生、发展[2]。
本研究结果提示,正常蛋白尿组、微量蛋白尿组、临床蛋白尿组患者UA、肾素、血管紧张素Ⅱ水平均逐渐升高,提示高尿酸血症可能通过激活RAAS参与糖尿病肾病的发病。其可能的机制包括:(1)UA可以上调肾素-血管紧张素相关mRNA的表达,促进血管紧张素Ⅱ分泌增多[3];(2)UA可以通过有机阴离子转运体进入人脐静脉内皮细胞,并快速诱导氧化应激反应,反过来进一步激活局部的肾素-血管紧张素系统,并使血管紧张素Ⅱ产生增多[4];(3)升高的血管紧张素Ⅱ可以改变肾小球内血流动力学,诱导系统高血压和肾小球内高压及肾小管间质损伤,最终导致肾小球硬化和间质纤维化[5-6];(4)有研究表明,高尿酸血症也可在不依赖血压升高的情况下引起大鼠肾脏入球肾小动脉病变及小管间质纤维化,而应用肾素-血管紧张素抑制剂后,肾脏肾小动脉及小管间质病变得到改善[7]。
综上所述,临床上给予T2DM合并高尿酸血症患者降UA治疗,可能改善患者体内RAAS激活状态,并预防糖尿病肾病的发生、发展,但仍需大规模临床研究以进一步证实。
[1]Liang CC,Lin PC,Lee MY,et al.Association of serum uric acid concentration with diabetic retinopathy and albuminuria in taiwanese patients with type 2 diabetes mellitus[J].Int J Mol Sci,2016,17(8):1248.
[2]Jalal DI,Maahs DM,Hovind P,et al.Uric acid as a mediator of diabetic nephropathy[J].Semin Nephrol,2011,31(5):459-465.
[3]Zhang JX,Zhang YP,Wu QN,et al.Uric acid induces oxidative stress via an activation of the renin-angiotensin system in 3T3-L1 adipocytes[J].Endocrine,2015,48(1):135-142.
[4]Yu MA,Sánchez-Lozada LG,Johnson RJ,et al.Oxidative stress with an activation of the renin-angiotensin system in human vascular endothelial cells as a novel mechanism of uric acid-induced endothelial dysfunction[J].J Hypertens,2010,28(6):1234-1242.
[5]Feig DI,Madero M,Jalal DI,et al.Uric acid and the origins of hypertension[J].J Pediatr,2013,162(5):896-902.
[6]Johnson RJ,Lanaspa MA,Gabriela Sanchez-Lozada L,et al.The discovery of hypertension:evolving views on the role of the kidneys,and current hot topics[J].Am J Physiol Renal Physiol,2015,308(3):F167-178.
[7]Mazzali M,Kanellis J,Han L,et al.Hyperuricemia induces a primary renal arteriolopathy in rats by a blood pressure-independent mechanism[J].Am J Physiol Renal Physiol,2002,282(6):F991-997.
10.3969/j.issn.1671-8348.2017.35.037
承德市科学技术研究与发展计划项目(20132046)。
何建秋(1980-),主治医师,硕士,主要从事糖尿病、垂体疾病研究。△
,E-mail:wangyanxinnur@163.com。
R587.2
B
1671-8348(2017)35-5014-02
2017-06-15
2017-08-24)
