FID-HPLC法测定木耳中维生素B2的含量
2018-01-04郭航宏王雪丹张念洁
郭航宏,王雪丹,张念洁
维生素B2又叫核黄素(化学式:C17H20N4O6,式量376.37),微溶于水,在中性或酸性溶液中加热亦可保持稳定。为体内黄酶类辅基的组成部分(黄酶在生物氧化还原中发挥递氢作用),当维生素B2缺乏时,会影响机体的生物氧化,引发代谢障碍,故维生素B2是维持人体正常生理所必需的物质。维生素B2通常不能在人体内合成,且体内维生素B2的储存极为有限,故须每天通过饮食摄取。黑木耳是一种味道鲜美、营养丰富的食用菌,含丰富的蛋白质、维生素、膳食纤维及铁、钙等微量元素。而黑木耳中维生素B2含量更为蔬菜中其含量的10倍有余,被称为“素中之荤”[1]。目前维生素B2含量常用测定方法有HPLC-PDA、HPLC-UVD、毛细管电泳—激光诱导荧光检测法(CE-LIF)、离子对高效液相色谱检测法及高效液相荧光检测器法(FID-HPLC)[2-5]等。本研究中笔者采用FID-HPLC测定木耳中的维生素B2的含量。
1 仪器与试药
1.1 仪器 包括赛多利斯电子天平220S(北京赛多利斯仪器系统有限公司),超声波清洗仪(型号KQ-100B,昆山市超声仪器有限公司),高效液相色谱仪(日本日立公司,包括HITACHI Pump L-2130,HITACHI Autosampler L-2200,Organizer,HITACHI UV-VIS Detector L-2420)。
1.2 试药 维生素B2标准品CAS:BW3601(中国计量科学院提供),木瓜蛋白酶CAS:9001-73-4(上海生物西宝有限公司提供)、高峰淀粉酶CAS号:9004-07-3(上海生物沪宇有限公司提供) ,甲醇为色谱纯,其他试剂均为分析纯。
2 方法与结果
2.1 色谱分析条件[1,2]色谱柱:ZORBAX Eclipse XDB-C8(250mm×4.6mm,5μm),流动相:乙酸钠溶液(0.05mol/L):甲醇=65:35,荧光检测的激发波长462nm,发射波长522nm,流速:1mL/min,进样量:20μL,柱温:室温。
2.2 对照品溶液制备[3,4]精密称维生素B2对照品0.0025mg,置于25mL棕色容量瓶中,先用部分流动相溶解,超声10min,冷却至室温,用流动相定容,超声。得0.2μg/mL的对照品溶液。
2.3 精密度实验[5]取1mL对照品溶液,用流动相稀释成5mL,超声,得浓度为0.02μg/mL的溶液。在2.1中条件下测定,检查仪器的精密度。结果见表1。
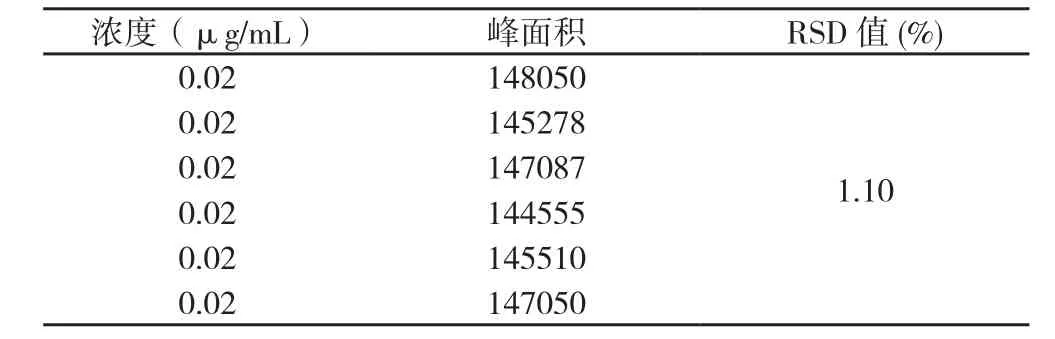
表1 仪器精密度实验Table1 Precision experiment
2.4 标准曲线绘制 分别精密移取对照品溶液1、2、3、4mL,分别置于5mL棕色容量瓶中以流动相稀释,超声,冷却至室温,定容。由面积和浓度进行线性回归,得回归方程为 Y=7.421560×106X-2134.2(0-0.1μg ·mL-1)(R2=0.9999,n=3),在2.1中条件下测定。结果见表2。

表2 浓度与面积关系Table2 Relationship of concentration and peak area
2.5 样品溶液的制备 精密称取样品5g,置于100mL具塞锥形瓶中,加入0.1mol/L盐酸溶液,高压灭菌后,调pH至6.3左右,加入2mL混合酶溶液,摇匀后,过夜酶解。定容100mL容量瓶,先用部分流动相溶解,超声10min,冷却至室温,以流动相定容,取上清液过滤膜作为待测液。
2.6 加样回收率 取维生素B2标准品0.001g,入0.60,1.30,1.90mg,按照2.5项下的方法配制。在2.1中条件下测定。结果见表3。
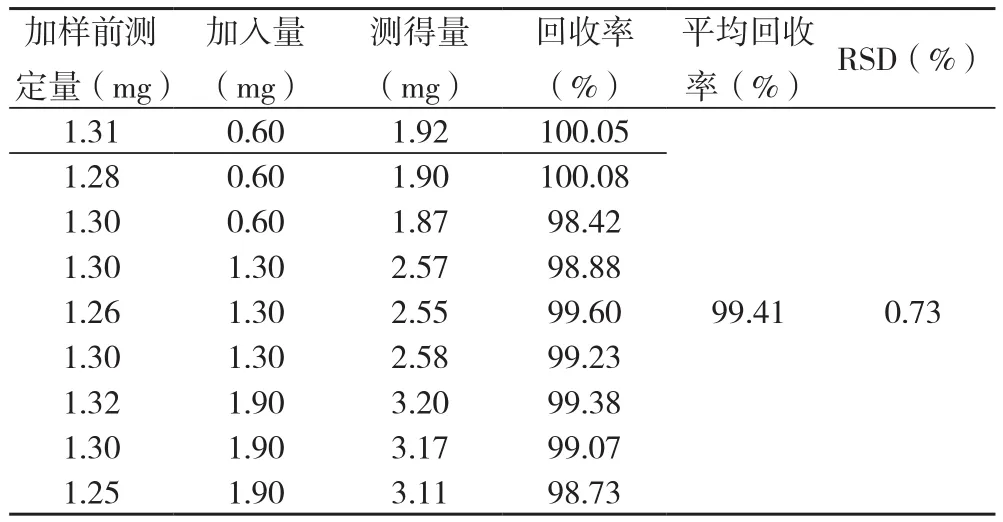
表3 加样回收率实验结果 (n=6)Table3 Results of recovery ratio
2.7 稳定性实验 取浓度为0.02mg/mL的对照品溶液,放置于室温阴暗处1、2、4、8、12h,在2.1中条件下测定。结果表明样品在12h内稳定。见表4。
2.8 样品含量测定 取样品,在2.1中条件下测定。按照回归的方程计算标准的峰面积As,用测定的峰面积Ai与标准峰面积As的比值,进行木耳中维生素B2的含量计算。结果见表5。本实验维生素B2的HPLC色谱图见图1(A)(B)。
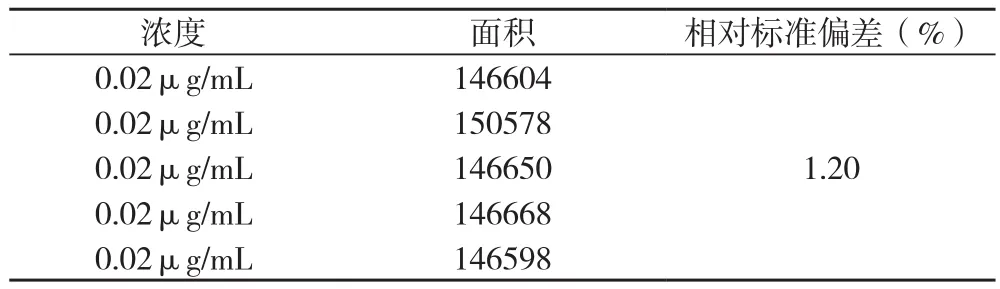
表4 稳定性实验Table4 Stability experiments
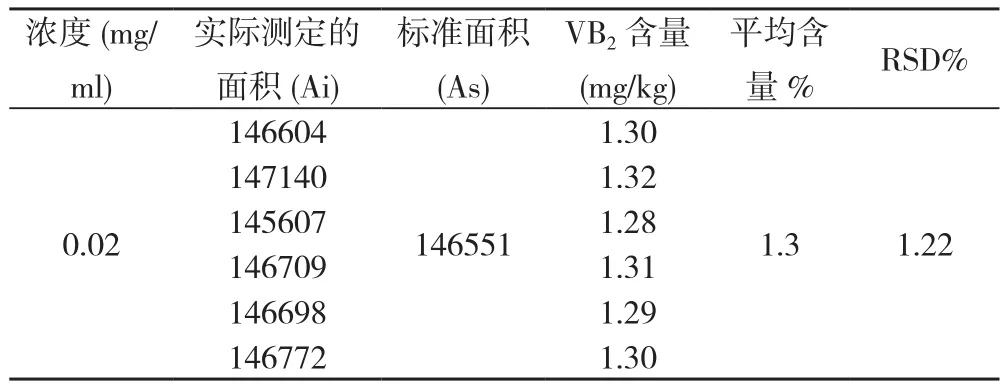
表5 维生素B2含量测定(n=6)Table5 The contents of vitamin b2 in samples
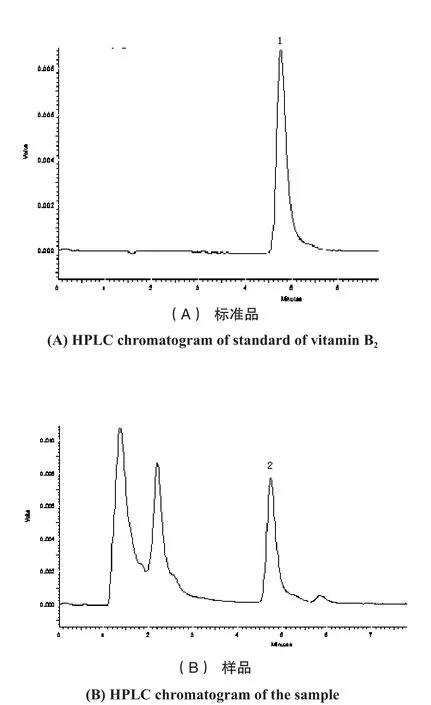
图1 维生素B2的HPLC色谱图Fig.1 HPLC chromatogram
3 讨 论
本实验中需注意维生素B2损失的两个主要因素:(1)可被光破坏:一定波长的光波照射下发出荧光。在pH6~7的溶液中荧光最强,在其他条件恒定时,荧光强度F与维生素B2浓度C成正比;(2)在碱溶液中加热可被破坏,此外实验发现, 维生素B2具有较强的荧光,溶液酸度对维生素B2的荧光光谱有较大影响。溶剂极性对维生素B2的荧光影响较大,极性越小荧光越强。金属离子Fe3+、Ca2+、Mg2+、Cu2+、Al3+等使荧光有不同程度的猝灭,其中Fe3+的猝灭作用最为明显[6],故样品前处理尤为重要。本研究所采用FID-HPLC法具有简便、快捷及重复性好等优点,为测定木耳中维生素B2提供了可靠依据,值得应用推广。
[1]杨文斌.木耳的营养与生长发育条件[J].吉林蔬菜,2016(6):38.
[2]王荣艳,贾丽,钱春燕.HPLC-PDA法同时测定功能性饮料中9种水溶性维生素[J].现代科学仪器,2010,(4):98-101.
[3]国家药典委员会.中华人民共和国药典[M].二部.北京:化学工业出版社:2015232-1233.
[4]张晖,薛洪宝,马涛,等.毛细管电泳—激光诱导荧光法检测维生素B2的研究[J].营养学报,2017,39(1):92-95.
[5]陈光龙,李玉兰,刘敏,等.高效液相色谱法测定复合维生素B片中4种组分的含量[J]中国医院药学杂志,2006,26(10):1256-1258.
[6]范婷婷.维生素的荧光光谱及分析方法研究[D]河北师范大学,2010:9-28.
