恶性中心气道狭窄经支气管镜介入诊疗专家共识
2017-12-27北京健康促进会呼吸及肿瘤介入诊疗联盟
北京健康促进会呼吸及肿瘤介入诊疗联盟
·专家共识·
恶性中心气道狭窄经支气管镜介入诊疗专家共识
北京健康促进会呼吸及肿瘤介入诊疗联盟
恶性中心气道狭窄是指气管、隆突、左右主支气管及中间段支气管因原发或转移的恶性肿瘤引起的气道狭窄,可导致患者在临床上出现不同程度的呼吸困难或窒息死亡[1]。随着介入呼吸病学技术的快速发展,经呼吸内镜介入已成为恶性中心气道狭窄诊疗的主要手段之一[2]。但目前国内各家单位呼吸介入技术诊疗水平参差不齐,治疗方法亦不统一,治疗效果也存在较大差距,有些甚至导致严重并发症发生。国内恶性中心气道狭窄的介入治疗技术亟需规范化,因此北京健康促进会呼吸及肿瘤介入诊疗联盟组织国内相关专家经过数轮充分讨论后制定了本共识。
一、恶性中心气道狭窄的病因
恶性中心气道狭窄的常见病因为气管原发恶性肿瘤和转移性恶性肿瘤。原发性气道肿瘤依次为鳞癌、腺样囊性癌、类癌、黏液表皮样癌及腺癌。转移性肿瘤可来自全身各处,一是气道远端病灶累及近端或食管、纵隔、甲状腺、胸腺等肿瘤累及气管或压迫气管。最易转移至中心气道的肿瘤包括上呼吸道肿瘤、消化道肿瘤、乳腺癌、肾细胞癌、转移性黑色素瘤以及淋巴瘤等[3- 4]。
二、恶性中心气道狭窄的分类和分级
通常根据肿瘤是否为单纯的位于管腔内、管腔外、管腔壁、混合型而将中央气道狭窄分为四类,见图1,分别为:①腔内型,肿瘤局限在管腔内,则称为内生型即腔内型;②腔外型,单纯因气管外肿瘤生长压迫致气管狭窄,且无腔内组织和管壁受损,则称为外压型即腔外型;③管壁型,沿管壁匍匐性生长,基底较宽,管壁较厚,可致管腔狭窄;④混合型,肿瘤有腔内生长,也有管壁、管外累及即称为混合型。混合型肿瘤常源于毗邻气道的组织、侵犯气道壁并进而侵入管腔[5]。
恶性气道狭窄严重程度的分级通常依据管径的狭窄程度(%)进行分级,管径的狭窄程度=狭窄管径/正常管径×100%。狭窄的严重程度用数字代码1~5描述(分为5级),中心气道狭窄的严重程度分级,见表1。
三、恶性中心气道狭窄的分区和定位
通过大数据分析,发现中心气道不同的分区,肿瘤有不同的好发部位。国内王洪武等[7]根据狭窄的解剖部位将恶性中心气道狭窄划分为八个分区,见表2。

表1[6] 中心气道狭窄的严重程度分级
一般认为1级为轻度狭窄,可有轻度咳嗽等症状;2、3级为中度狭窄,可有咳嗽、气短等症状;4、5为重度狭窄,则有严重呼吸困难,可出现三凹征、发绀,甚至窒息死亡[6]。呼吸困难的程度主要取决于狭窄气道的直径大小。一般情况下,当肿瘤堵塞或压迫引起气管狭窄程度>50%时,患者会出现明显的呼吸困难。正常情况下,气道、左、右主支气管的平均直径分别为12~18 mm、8~14 mm及10~16 mm,当气管直径<8 mm时,患者就会出现劳力性呼吸困难,当气管直径<5 mm时,则会出现静息性呼吸困难。左、右主支气管或中间段支气管部分狭窄,甚至完全堵塞,但由于另一侧肺的代偿作用,患者呼吸困难严重程度表现不一。其它常见症状及体征包括咳嗽、喘鸣和哮鸣音,以及反复发生或持续存在的阻塞性肺炎。喘鸣常指示病灶已累及气管或喉部水平,而哮鸣音则提示可能为局部或隆突远端的气道阻塞。

表2 气道病变的部位
一般认为,Ⅰ区最常见的肿瘤是鳞癌和甲状腺癌,Ⅱ、Ⅲ区主要是鳞癌、腺样囊性癌和食管癌,Ⅳ、Ⅴ区是鳞癌和腺样囊性癌,Ⅵ区是鳞癌和黏液表皮样癌,Ⅶ区是鳞癌、食管癌、腺样囊性癌和黏液表皮样癌,而Ⅷ区是腺癌、食管癌和黏液表皮样癌。
四、恶性中心气道狭窄的诊断方法
恶性中心气道狭窄因为临床征象及症状不具有特异性,易被误诊或漏诊,因而对可疑恶性气道狭窄的诊断应引起高度重视,同时要排除引起喘息的其他疾病,尤其是哮喘、结核及其他良性气道狭窄。诊断时应进行详细的病史采集、体格检查、影像学检查、支气管镜、肺功能以及血气分析,这些信息对于选择介入治疗方法、麻醉方式及预测可能的并发症和判断患者预后均具有重要意义。恶性中心气道狭窄诊疗流程图,见图1。
1. 病史采集: 恶性中心气道狭窄的患者可能表现为刺激性干咳和进行性呼吸困难,有时可有痰中带血或咯血。对于出现这些症状,尤其是有各种恶性肿瘤病史的患者应高度考虑是否有气道侵犯或转移。
2. 体格检查: 主要检查呼吸困难的相关体征。恶性中心气道狭窄根据病变部位、大小、生长方式不同而呼吸困难的形式亦有不同,可表现为吸气性、呼气性或二者均存在的呼吸困难,严重者可有三凹征和发绀。肺部听诊可闻及鼾音或哮鸣音。严重的声门下或气管狭窄时常可闻及鼾音,左、右主支气管或中间段支气管狭窄时可闻及局限性哮鸣音、吸气时高调哮鸣音和局部肺不张体征。
3. 胸部影像学检查: 普通的胸部X线片诊断恶性气道狭窄的价值有限。少数患者可显示气管或主支气管病变或不张,另外,间接征象可判断病变的部位和程度,气管、支气管断层显像对狭窄诊断亦有帮助[8]。胸部CT是诊断恶性中心气道狭窄的重要方法,尤其是多排螺旋CT可以重建三维立体图像,建立虚拟气管、支气管图像,并可进行3D打印,可以明确判断病变程度、形态、侵犯深度及其与周围血管的关系,特别是对远端气道的通畅情况及远端肺组织实变和是否存在病变可提供依据[9- 10]。磁共振成像(magnetic resonance imaging, MRI)可以判断支气管狭窄的类型和程度,尤其是对支气管外压性狭窄的判断更为准确,对于争取合理的介入治疗方法有重要的指导作用[11]。应该提醒的是虽然胸部CT是诊断恶性气道狭窄的主要方法,但其对于发现较轻的气道狭窄的能力有限,与支气管检查相比常会低估气道狭窄的长度[12]。
4. 支气管镜检查: 支气管镜检查是诊断恶性中心气道狭窄的金标准[13]。通过病史采集、体格检查及影像学检查考虑为恶性中心气道狭窄的患者,在无支气管镜检查禁忌证的情况下,根据气道狭窄位置、类型、严重程度及患者耐受情况不同,在采取相对安全保护措施下,均应进行支气管镜检查,这样可以直接观察病变的位置、大小、狭窄程度,并可通过吸引、灌洗、活检而进行定性诊断[14]。目前诊断主要是通过支气管镜下活检病理组织学诊断完成。另外,超声支气管镜引导透支气管壁针吸活检术可进行外压性狭窄的定性诊断,还可用于识别是否存在气管软骨外病变及气管软骨受累的程度[15-16]。虚拟支气管镜可以判断狭窄远端支气管和肺组织功能情况。恶性中心气道狭窄的类型,见图2。
5. 肺功能检查: 肺功能检查包括肺活量测定和流量、容量曲线(flow volume line, FVL)分析。由于肺活量测定可诱发呼吸衰竭,对于严重气道狭窄患者可不测定。当气道狭窄直径≤6 mm时,第一秒用力呼气容积(forced expiratory volume in one second, FEV1)检查出现明显下降,因此,FEV变化可能早于FEV1的变化。与FEV1相比,最大呼气流速(peak expiratory flow, PEF)和最大自主通气量(maximal voluntary ventilation, MVV)诊断气道狭窄的敏感度更高。在肺活量测定时,如果PEF下降显著低于FEV1的下降时,应考虑气道狭窄。MVV与FEV1的比值<25%时常见于气道狭窄。当MVV下降而FEV1正常时,也应考虑气道狭窄。但这些气道狭窄都相对较轻,严重气道狭窄是无法进行肺活量检查的。FVL可区分胸腔内和胸腔外中心气道固定或可变性狭窄。FVL有助于评价肺脏基础状况,判断介入手术治疗安全性及决定麻醉方法及手术中需要采取的相应气道处理措施[17]。

图1 恶性中心气道狭窄诊疗流程图
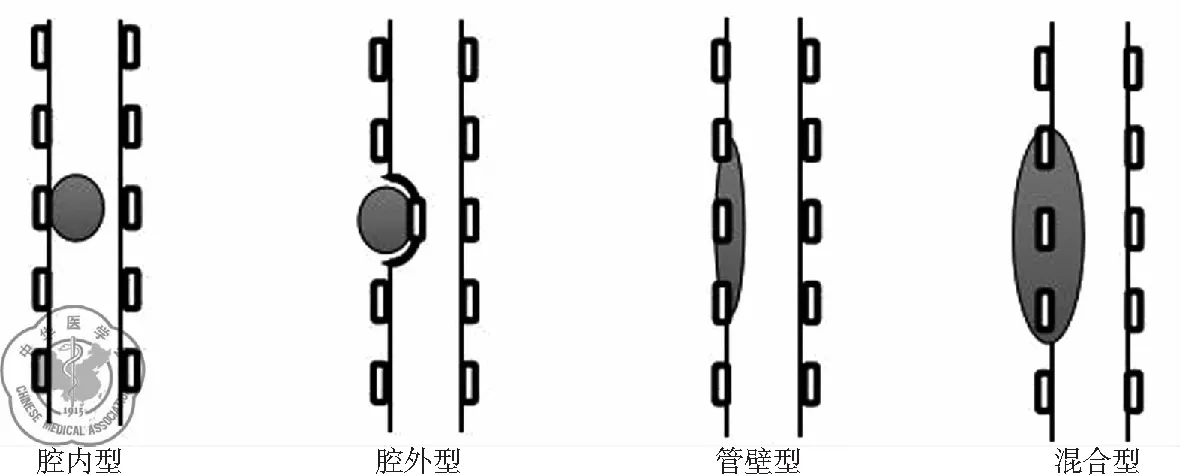
图2 恶性中心气道狭窄的类型
肺功能F-V曲线的形态特征有利于气道阻塞定位诊断、病变的严重程度、治疗效果的评价以及指导相关治疗方案的制定。由于胸腔内外压力受不同呼吸时相的影响,可变胸内型大气道阻塞呼气气流受限,F-V曲线呼气相出现明显平台样改变,吸气相一般正常,病变多局限于胸腔入口以内(如气道肿瘤、支气管结核、气道异物等);可变胸外型大气道阻塞吸气相气流受限,F-V曲线吸气相出现明显平台样改变,呼气相一般正常,病变一般局限于胸腔入口以外(如喉癌、声带功能障碍、喉头水肿、声门狭窄、食管癌、甲状腺肿癌等);固定型大气道阻塞F-V曲线呈双相平台样改变,提示病变范围较大、程度较重。单侧主支气管不完全阻塞可见“双碟影”,见图3。因此,术前肺功能检查有助于预估气道狭窄的位置。也可采用脉冲震荡肺功能法进行测定,根据相应的指标进行判断狭窄的位置及程度。
6. 血气分析: 用于判定肺通气及换气功能、呼吸衰竭类型与缺氧的严重程度,以及各种类型的酸碱失衡状态。但血气分析不能用于判断气道狭窄的严重程度,因为即使为严重的气道狭窄,患者表现为极度呼吸困难,但血气分析,尤其是PaO2可能正常。对于既往无慢性呼吸系统疾病史,肺功能正常的患者,即使PaCO2轻度、中度升高,也应高度重视并紧急处理。术中、术后出现的血氧饱和度和PaO2下降要寻找原因、评估病情并积极处理。总之,血气分析是呼吸内镜介入治疗术前、术中和术后对患者进行功能评价的一项重要指标,动脉血气的动态监测对于患者手术的安全性有极其重要的作用。
五、恶性中心气道狭窄的治疗方法
恶性中心气道狭窄早期无症状或症状轻微,往往可被忽视,一旦出现呼吸困难加重,狭窄就会很重,给治疗带来一定的风险和困难。恶性气道狭窄治疗包括外科手术治疗和经支气管镜引导下的介入治疗。
1. 传统的外科治疗方法: 袖状切除、支气管切除并行气道重建是外科切除气管癌的主要方法。对于因其他肿瘤如甲状腺癌、胸腺恶性肿瘤、纵隔恶性肿瘤等压迫气管引起的气道狭窄应以外科手术切除原发肿瘤。但手术切除创伤大、风险高、加之部分患者病变部位解剖学限制,如病变区域太大(超过两个区)、管壁全层侵犯及混合性狭窄、转移癌等,或全身基础条件差限制手术等原因,使得外科手术的适应证非常有限,对于大部分恶性气道狭窄外科手术是无法解决的。部分患者术后端端吻合口还可发生疤痕增生而致再狭窄。
2. 介入治疗方法: 随着介入呼吸病学技术在我国的迅速发展和广泛应用,选择适当的介入治疗技术可使恶性气道狭窄患者获得良好效果。目前经支气管镜介入治疗恶性中心气道狭窄的方法主要是通过热消融(激光、电刀、氩气刀等)、冷消融(冻融或冻切)、机械性切除(硬质镜铲除术)和气道扩张(支架置入或硬质镜扩张)技术,这些技术的目的是快速达到通畅气道、改善通气和防止窒息的作用[18-20]。
(1)消融技术:通过热或冷消融使肿瘤组织坏死、碳化、甚至汽化,达到祛除病灶的目的。主要包括热消融和冷消融[21]。热消融指使用微波、激光、高频电刀(电烧或电切)和APC的方法,使组织加热、坏死、汽化,从而达到减少组织体积的方法[22-24]。冷消融是指通过冻融或冻切的方式使组织破坏、坏死或经冻切方式祛除肿瘤病灶的目的。
(2)机械性切除术:通过硬质镜、光镜的前端直接切除肿瘤或部分肿瘤,或通过硬质镜下较大的活检钳直接钳取肿瘤,以达到快速通畅气道的目的[25]。
(3)气道扩张技术:主要有三种扩张气道的方法,包括高压球囊扩张、硬质支气管镜体的机械扩张和支架置入[26-27]。
高压球囊扩张术在临床上主要用于良性气道狭窄,但对于部分恶性气道狭窄的患者,尤其是外压和管壁软骨受损的患者可以使用[28]。现有专为气道扩张而设计的球囊,也可用各种型号的血管、食道球囊进行扩张。推注生理盐水将球囊直径扩充到预设的气道直径值,并持续施压至气道组织上30~60 s,如此反复进行。扩张气管时,患者在整个球囊充盈期间处于窒息状态,需在全麻下进行。球囊直径过大或过度充盈会导致气道撕裂,应引起重视。球囊还可用于置入支架张开不良时对支架的迅速扩张。
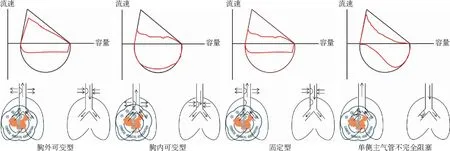
图3 上气道梗阻流量-容量曲线变化图
硬质支气管镜本身可以用于气道扩张,尤其适用于近端大气道。全麻配合高频通气下进行扩张,当硬质镜通过阻塞部位后,留置数分钟以便充分扩张,其优点是在整个操作过程中允许患者通气。此外,在操作过程中,可利用硬质支气管镜的镜身铲除管腔内的部分肿瘤[29]。操作时必须保持在同一层面,防止镜身偏离方向导致气道穿孔。
支架置入术可起到持续扩张气道的作用。当高压球囊扩张、硬质镜扩张及腔内病灶清理后仍达不到气道通畅作用时,可考虑放置支架。如何选择最合适的支架需考虑术者的经验、所需费用、病灶的结构以及患者病情。中央型气道的八分区方法对选择气道支架的形状有重要指导意义。对Ⅰ、Ⅵ、Ⅷ区病变适合放置直筒型支架,而对隆突附近的Ⅱ、Ⅲ、Ⅳ、Ⅴ、Ⅶ区则适合放置分叉支架(L或Y型)。硅酮支架需要全麻并在硬质镜下放置,同时硅酮支架较柔软,支撑力度不足,容易移位,曲线形的病灶不适合放置,因为有可能会突入气道中央扩张不良而引起阻塞[30]。所以,对于恶性气道狭窄患者最好选用合适的金属支架。硅酮支架和金属支架的特点比较,见表3。

表3 硅酮和金属支架比较
六、恶性中心气道狭窄介入治疗规范与原则
恶性中心气道狭窄介入治疗是一项复杂的技术,应从以下六个方面严格执行规范和原则,确保介入手术顺利和病人的安全。
1. 选择患者的原则: 对于不能外科手术或者拒绝手术的原发恶性肿瘤或转移恶性肿瘤导致的中心气道狭窄患者可选择介入手术。同时对病人狭窄远端气管、支气管和肺组织功能应进行评价,如果病变远端支气管和肺组织功能丧失且预计气道开放后仍无法恢复,应该放弃介入治疗[31]。
2. 选择急诊或择期治疗的原则: 根据狭窄的部位、程度以及呼吸困难的程度,决定急诊或择期手术。对于气管、隆突、左右主支气管严重狭窄、一侧支气管狭窄而对侧肺脏切除或肺功能明显障碍或肺不张等严重呼吸困难而随时危及生命的患者应选择急诊手术。而对于其他各种类型的轻、中度狭窄,不会在短期内危及生命的患者可选择择期手术[32]。
3. 选择麻醉和通气方式的原则
(1)全身麻醉: 全身麻醉简称全麻,是指麻醉药经呼吸道吸入、静脉或肌肉注射进入体内,产生中枢神经系统的暂时抑制,临床表现为神志消失、全身痛觉消失、遗忘、反射抑制和骨骼肌松弛。对中枢神经系统抑制的程度与血液内药物浓度有关,并且可以控制和调节。这种抑制是完全可逆的,当药物被代谢或从体内排出后,患者的神志及各种反射逐渐恢复。全身静脉麻醉是在静脉麻醉诱导后,采用多种短效静脉麻醉药复合应用,以间断或连续静脉注射法维持麻醉,是目前支气管镜下介入治疗较为广泛采用的麻醉方式,具有时间可控性强,麻醉苏醒时间短的特点。而在监控静脉麻醉设计腔内介入治疗手术方案时,首先要考虑如何保障气道的通畅和氧合。对于有以下情况者,最好采取全麻,并建立人工气道和进行机械通气: ①气管、隆突、左右主支气管严重狭窄、一侧支气管狭窄而对侧肺脏切除或肺功能明显障碍或肺不张等严重呼吸困难的患者; ②患者全身一般情况差,心肺功能不全,手术风险大; ③气道内出血或病变血供丰富,治疗中可能出现大出血的患者; ④病变大、需要长时间手术、局麻下患者难以耐受或不能完成手术者; ⑤患者心里恐慌不能接受局麻手术者。在手术过程中可有两种全麻形式: ①全身麻醉、人工气道、密闭通气加软质支气管镜。这是一种相对安全的治疗方式。气管插管方法要求病灶距离声门较远(>7 cm),如此才可保证气管插管球囊在声门下,并且气管插管下端不至遮挡病灶。如果病灶距离声门较近(<5 cm),气管插管不易固定或气管插管易遮挡病灶,应该选择喉罩; ②全身麻醉、硬质支气管镜加开放通气,或全麻+硬质支气管镜联合软质支气管镜+开放通气,这对严重的气道狭窄患者来说是安全的治疗方式。硬质气管镜的通气方法有两种: 其一是用喷射呼吸机进行开放通气,采用高频通气的患者有二氧化碳潴留的风险,因此需术中进行二氧化碳浓度监测,对于有二氧化碳潴留风险的患者(如伴有COPD的基础疾病或肺功能较差者),亦可采用常频通气(14~18次/min)以有助于二氧化碳的排出; 其二是用麻醉机或呼吸机进行密闭或半密闭式通气(经通气管路的延长管活塞进入),也可起到较好的通气效果,同样建议术中监测呼气末二氧化碳浓度。
(2)局部麻醉: 对于健康状况良好,气管轻度阻塞或单侧支气管阻塞病变,局麻下可在短时间内完成手术。另外患者保持在清醒状态下有咳嗽反射,可咳出气道分泌物或出血,也易于主动配合手术,是临床上最常用的一种麻醉方法。如果患者耐受性差,难以进行配合,可加用镇静剂。
4. 选择介入手术的分次原则: 根据病变大小与外周组织的关系以及出血量的不同应选择单次或分次进行介入手术。较小病变,或带蒂的较大病变均可一次切除干净并处理残端; 如病变较大,与周围组织分界不清,出血量较大者宜分次进行,从表及里分层处理,待坏死组织脱落,正常组织暴露或病变分解清晰后,再进行后续治疗。
5. 选择软、硬支气管镜单用或联合使用原则: 根据病变性质、大小、部位、呼吸困难情况的不同,以及内镜操作者的经验不同而选择软质或硬质镜。如果病变大,短时间内不能移除病灶,或随时可能大咯血或窒息,或患者无法耐受长时间操作者可选用全麻硬质支气管镜下操作,其特点是能保持气道开放并进行侧支通气,而且有大型的光学钳、异物钳、氩气刀喷头和冷冻探头等特殊治疗器械,能快速摘除气道内病变或异物,快速开放气道[33]。另外,还可进行一些特殊操作,如放置或摘除金属或硅酮支架等。对于气道远端和角落的病变,可采取软、硬质支气管镜相结合,让软镜通过硬质镜通道进行操作[34]。另外,因为气道内某些异物及断裂的金属支架等造成的气道狭窄必须用硬质镜才能处理,不建议应用软镜[35]。
6. 介入治疗方法选择的原则: 对于恶性气道狭窄介入治疗方法的选择最好是根据狭窄的类型去决定: ①对于累及气道的单纯性腔内型肿瘤,内镜下采用热、冷消融术清除或用硬质镜尖端直接切除即可,见图4~6;②如果为混合性狭窄,内镜下可应用冷热消融术清除部分管腔内病灶,然后置入支架,最好用金属支架,如果支架扩张效果不好,可用球囊扩张支架,见图7~11;③如果为单纯性外压性狭窄,可直接置入支架,如重度狭窄可行支气管镜下球囊扩张术,术后再置入支架,见图12~13;④如果外压性狭窄伴气管壁侵犯,可置入带膜支架,不仅可阻止肿瘤再生,而且可对抗肿块的压迫效应,见图14~15。
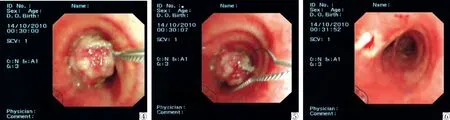
图4 气管内球形新生物,带蒂,随呼吸上下活动 图5 电圈套器套切新生物 图6 套切后的基底部
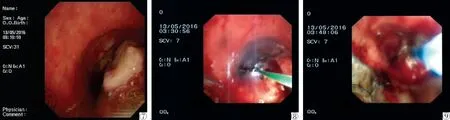
图7 气管内新生,管壁增厚、隆起伴有新生 图8 激光烧灼 图9 氩气刀烧灼

图10 针形电刀切割 图11 置入金属支架 图12 右上叶楔形术后8天,右主支气管塌陷性狭窄

图13 置入金属支架 图14 食管癌术后14月,气管黏膜鱼鳞样新生改变伴管腔外压性狭窄 图15 置入覆膜支架
关于最佳腔内介入治疗时机要根据患者具体情况而定。总之,如果原发的气管内肿瘤,时机为越早越好,而在许多的晚期恶性肿瘤患者往往出现严重呼吸困难时才入院治疗,其原则是通畅气道,改善通气,介入治疗作为一种过渡,以缓解狭窄,为更进一步治疗,如放疗、化疗提供机会,尤其是对化、放疗敏感的肿瘤,如小细胞肺癌的后续治疗是很有帮助的。
综上所述,恶性中心气道狭窄可见于多种疾病,包括肺癌和其它实体瘤等肿瘤的发病过程中。阻塞气道发展到一定程度时,患者出现以呼吸困难为主的临床症状。除传统的外科手术、放疗和化疗治疗外,介入呼吸病学技术,如腔内消融术、支架置入等有快速通畅气道,改善通气的作用。要强调气道介入治疗恶性气道狭窄大多是姑息性治疗,能缓解症状、减少痛苦、延续生命,有些可为后续治疗提供时机。腔内介入技术方法多种多样,疗效相似,具体的选择需综合考虑治疗团队的经验、能力以及可利用的资源、患者病情、费用及可能发生的并发症。随着我国越来越多的受过良好培训的介入呼吸病学和危重症医学医师的增多以及临床经验的积累,未来一定会使恶性气道狭窄的患者得到更好的内镜下的诊断及治疗。
专家组成员(按姓氏汉语拼音排序)
白冲(第二军医大学长海医院)
蔡志刚(河北医科大学第二医院)
陈良安(解放军总医院)
冯靖(天津医科大学总医院)
冯起校(南方医科大学中西医结合医院)
郭述良(重庆医科大学第一附属医院)
侯刚(中国医科大学附属第一医院)
黄海东(第二军医大学长海医院)
金发光(第四军医大学唐都医院)
赖国祥(解放军福州总医院)
李时悦(广州医科大学附属第一医院)
李王平(第四军医大学唐都医院)
孙劲文(煤炭总医院)
王昌惠(上海市第十人民医院)
王洪武(煤炭总医院)
谢宝松(福建省立医院)
曾奕明(福建医科大学附属第二医院)
张楠(煤炭总医院)
周锐(中南大学湘雅二医院)
周云芝(煤炭总医院)
执笔人(按姓氏汉语拼音排序)
金发光、李时悦、王洪武
1 Ernst A, Feller-Kopman D, Becker HD, et al. Central airway obstruction[J]. Am J Respir Crit Care Med, 2004, 169(12): 1278-1297.
2 李强. 介入肺脏病学及其用于呼吸系统疾病诊治临床现状[J]. 中国实用内科杂志, 2013, 33(2): 98-101.
3 金发光, 李王平. 中心气道狭窄的诊断及介入治疗[J]. 医学与哲学, 2008, 29(22): 7-9.
4 王洪武, 张楠, 李冬妹, 等. 中央型气道恶性肿瘤881例分析[J]. 中华结核和呼吸杂志, 2014, 37(2): 148-149.
5 王洪武. 现代介入肺脏医学概况[J]. 国际呼吸杂志, 2012, 32(4): 269-274.
6 王洪武. 恶性原发性中央型气道肿瘤新的分型和支气管镜新的诊断方法探讨[J/CD]. 中华临床医师杂志(电子版), 2013, (21): 9423-9426.
7 王洪武. 中央型气道新的八分区方法和恶性气道肿瘤的治疗策略[J]. 临床荟萃, 2016, 31(11): 1167-1169.
8 早期中央型肺癌的影像诊断研究进展[J]. 实用肿瘤杂志, 2014, 29(2): 196-198.
9 Remy-Jardin M, Remy J, Deschildre F, et al. Obstructive lesions of the central airways: evaluation by using spiral CT with multiplanar and three-dimensional reformations[J]. Eur Radiol, 1996, 6(6): 807-816.
10 Ferretti GR, Knoplioch J, Bricault I, et al. Central airway stenoses: preliminary results of spiral-CT-generated virtual bronchoscopy simulations in 29 patients[J]. Eur Radiol, 1997, 7(6): 854-859.
11 Rimell FL, Shapiro AM, Meza MP, et al. Magnetic resonance imaging of the pediatric airway[J]. Arch Otolaryngol Head Neck Surg, 1997, 123(9): 999-1003.
12 路融, 董进文, 严志刚. CT及纤维支气管镜等检查诊断中央型肺癌的价值研究[J]. 人民军医, 2015, 58(2): 168-169.
13 王广发. 中心气道狭窄的介入治疗[J]. 中华结核和呼吸杂志, 2010, 33(1): 14-16.
14 Finkelstein SE, Summers RM, Nguyen DM, et al. Virtual bronchoscopy for evaluation of airway disease[J]. Thorac Surg Clin, 2004, 14(1): 79-86.
15 Paone G, Nicastri E, Lucantoni G, et al. Endobronchial ultrasound-driven biopsy in the diagnosis of peripheral lung lesions[J]. Chest, 2005, 128(5): 3551-3557.
16 Medford AR, Bennett JA, Free CM, et al. Endobronchial ultrasound-guided transbronchial needle aspiration (EBUS-TBNA): applications in chest disease[J]. Respirology, 2010, 15(1): 71-79.
17 Lunn WW, Sheller JR. Flow volume loops in the evaluation of upper airway obstruction[J]. Otolaryngol Clin North Am, 1995, 28(4): 721-729.
18 Sohrab S, Mathur PN. Management of central airway obstruction[J]. Clin Lung Cancer, 2007, 8(5): 305-312.
19 金发光, 刘伟, 殷凯生. 复杂中心气道狭窄的诊断及综合介入治疗现状[J]. 生物医学工程与临床, 2010, 14(2): 176-179.
20 金发光, 李王平, 傅恩清, 等. 介入性肺脏病学技术在中心气道狭窄治疗中的作用及安全性分析:附389例报告[J]. 解放军医学杂志, 2008, 33(11): 1352-1355.
21 Moorjani N, Beeson JE, Evans JM, et al. Cryosurgery for the treatment of benign tracheo-bronchial lesions[J]. Interact Cardiovasc Thorac Surg, 2004, 3(4): 547-550.
22 Miller SM, Bellinger CR, Chatterjee A. Argon plasma coagulation and electrosurgery for benign endobronchial tumors[J]. J Bronchology Interv Pulmonol, 2013, 20(1): 38-40.
23 Puchalski J, Musani AI. Tracheobronchial stenosis: causes and advances in management[J]. Clin Chest Med, 2013, 34(3): 557-567.
24 王辰飞, 李强, 白冲, 等. 支气管镜下腔内高频电刀治疗中央气道良、恶性肿瘤的临床疗效[J]. 第二军医大学学报, 2007, 28(5): 554-556.
25 Shojaee S, Dawson J, Shepherd RW, et al. Palliative interventional pulmonology procedures in the incarcerated population with cancer: a case series[J]. Lung, 2014, 192(6): 915-920.
26 Shitrit D, Kuchuk M, Zismanov V, et al. Bronchoscopic balloon dilatation of tracheobronchial stenosis: long-term follow-up[J]. Eur J Cardiothorac Surg, 2010, 38(2): 198-202.
27 Lund ME, Garland R, Ernst A. Airway stenting: Applications and practice management considerations[J]. Chest, 2007, 131(2): 579-587.
28 Liang YL, Liu GN, Zheng HW, et al. Management of Benign Tracheal Stenosis by Small-diameter Tube-assisted Bronchoscopic Balloon Dilatation[J]. Chin Med J (Engl), 2015, 128(10): 1326-1330.
29 王洪武, 周云芝, 李冬妹, 等. 电视硬质气管镜下治疗中央型气道内恶性肿瘤[J]. 中华结核和呼吸杂志, 2011, 34(3): 230-232.
30 Tonn H, Mall W, Schneider KD, et al. [Tracheobronchial stents: a retrospective analysis of indications, results and in particular complications][J]. Pneumologie, 2008, 62(10): 611-615.
31 党斌温. 中心气道管腔狭窄的病变类型和介入技术选择[J]. 国际呼吸杂志, 2009, 29(14): 888-890.
32 金发光. 中心气道狭窄规范性诊治策略[J/CD]. 中华肺部疾病杂志(电子版), 2015, 8(5): 1-4.
33 Beaudoin EL, Chee A, Stather DR. Interventional pulmonology: an update for internal medicine physicians[J]. Minerva Med, 2014, 105(3): 197-209.
34 Huret B, Perez T, Dhalluin X, et al. Treatment of malignant central airways obstruction by rigid bronchoscopy[J]. Rev Mal Respir, 2015, 32(5): 477-484.
35 Kim HJ, Kim SW, Lee HY, et al. Clinical experience of rigid bronchoscopy in single center[J]. Tuberc Respir Dis (Seoul), 2012, 72(6): 486-492.
10.3877/cma.j.issn.1674-6902.2017.06.004
国家公益性行业科研专项课题(201402024)
金发光 710038,西安,第四军医大学唐都医院呼吸与
危重症医学科
Email: jinfag@fmmu.edu.cn
2017-09-27)
张大春)
北京健康促进会呼吸及肿瘤介入诊疗联盟. 恶性中心气道狭窄经支气管镜介入诊疗专家共识[J/CD]. 中华肺部疾病杂志(电子版), 2017, 10(6): 647-654.
