制备可促进干细胞增殖的三维取向电纺纤维膜
2017-12-22王丹丹钟惠湘轩留洋马双双李燕蒋乐伦蒋庆
王丹丹,钟惠湘,轩留洋,马双双,李燕,蒋乐伦,蒋庆
(1.中山大学工学院生物医学工程系,广东 广州 510006;2.广东省传感和医疗器械重点实验室,广东 广州 510006;3.广东省便携式普及型先进实用医疗器械工程技术研究中心,广东 广州 510006)
制备可促进干细胞增殖的三维取向电纺纤维膜
王丹丹1,2,3,钟惠湘1,2,3,轩留洋1,2,3,马双双1,2,3,李燕1,2,3,蒋乐伦1,2,3,蒋庆1,2,3
(1.中山大学工学院生物医学工程系,广东 广州 510006;2.广东省传感和医疗器械重点实验室,广东 广州 510006;3.广东省便携式普及型先进实用医疗器械工程技术研究中心,广东 广州 510006)
为模拟体内三维微环境,比较脂肪干细胞(adipose derived stem cells, ADSCs)在二维与三维取向纤维膜的增殖速率,通过改进静电纺丝收集装置,制备三维聚己内酯(poly caprolactone, PCL)取向电纺纤维。缠绕在毛细管(直径300 μm)的电纺纤维取向性优良,纤维直径300~400 nm。将ADSCs种于经表面改性的电纺纤维上,黏附良好。在取向纤维膜上,细胞均沿纤维取向方向铺展。与2D纤维膜相比,细胞在3D纤维模型支架上增殖速率较快,表明3D纤维支架在组织工程应用中更有优势。
三维取向纤维;静电纺丝;脂肪干细胞;骨组织工程
细胞外基质(extra cellular matrix, ECM)是细胞在体内生存微环境的重要组成部分。近年来有关生物支架材料的研究多致力于模拟ECM的结构和性能,从而调控特殊的细胞应答,如细胞黏附、迁移、增殖和分化。静电纺丝、自组装和相分离法都可以制备出具有类似于ECM的微纳米结构的纤维支架[1-3]。其中,静电纺丝技术因操作简单、所得纤维结构易于控制,纤维尺寸范围分布广(从纳米至微米级别),被广泛应用于纳米纤维支架领域[4]。静电纺丝技术所制备的纳米纤维支架除具有类似ECM的纳米网状结构外,还具有高孔隙率和高比表面积等优点。在生物学性能方面,纳米纤维支架还可促进细胞黏附、增殖和分化等[5]。
静电纺丝技术是在聚合物溶液和接收装置之间施加一个高电压,一旦表面电位电荷超过一个临界值,静电引力就会克服溶液表面张力,产生直径在纳米到微米尺度的连续性纤维[6-7]。纺丝过程中,聚合物溶液的浓度、黏度、电场强度、挤出速率、接收装置等会影响纤维的直径和形状。因此可以通过改变静电纺丝条件,来控制支架的结构和形态[8]。
最近,一些研究报告指出支架的表面形貌可以影响干细胞命运[9-10]。由合成或天然可降解聚合物制备出的取向纳米纤维,其表面形貌类似于原生骨组织中高度取向的胶原纤维束,被广泛作为骨再生支架[11]。Duque等[12]发现:干细胞可以沿着高度取向的纤维方向生长。与无规纤维相比,在取向纤维上表现出增强的成骨分化潜能。高比表面积和高孔隙率的支架材料,对于细胞生长和组织再生起着至关重要的作用。大量研究表明,2D纤维膜可允许细胞粘附和增殖[13-15]。然而,这种传统纤维支架为平面结构,严重阻碍了细胞的生长和迁移。通过改变实验策略,不少研究者制备出了所需形态和结构的三维电纺纳米纤维支架,并将之应用于组织工程领域。Swaminathan等[16]制备出取向的聚乙丙交酯(poly lactide-co-glycolide, PLGA)纳米纤维,将其用于神经工程修复;同时,相关研究也证明:相比于无规纤维,取向纤维降解速率较慢,可促进细胞增殖。Bosworth等[17]的研究发现3D电纺支架较2D支架材料能够承载更大的拉伸载荷,表现出良好的机械性能。此外,3D电纺膜可更好地模拟层次紧密的肌腱组织结构,促进肌腱成纤维细胞的黏附和增殖。Xu 等[18]利用热诱导纳米纤维,在冷冻干燥条件下通过自集聚的方式制备出了聚己内酯(poly caprolactone, PCL)三维纳米支架,其具有高孔隙率和相互关联的孔洞结构。体外实验结果表明:该支架不仅可提高细胞存活率,还可有效的促进BMP-2诱导的软骨细胞的成骨分化,在骨组织工程中具有优良的应用前景。尽管在3D纳米纤维支架领域已经累积了一定的研究成果,但关于细胞对纳米纤维取向的响应,却鲜有报道。而细胞取向与细胞增殖、分化等行为密切相关。且,3D培养是否优于2D培养,仍有待进一步研究阐明。
在众多干细胞中,脂肪干细胞(adipose-derived stem cell, ADSCs)具有很强自我更新能力和高度分化潜能,在一定条件下可诱导分化为成骨细胞、软骨细胞、肌细胞、内皮细胞等[19],进一步借助于组织工程技术可构建出骨组织[20]、软骨组织[21]、肌肉组织[22]、内皮等。此外,ADSCs来源丰富,取材较方便,成为国内外学者的研究热点[23]。因此,在本研究中ADSCs被选为模型细胞。本研究构建了具有大比表面积和高孔隙率的3D纳米纤维支架模型,探索其对细胞粘附和增殖等方面的影响。为制备3D取向纳米纤维,我们改进了纺丝接收装置,制备出取向良好的电纺纤维。经表征后,选择具有合适性能的3D电纺纤维膜作为基底材料,研究其对ADSCs黏附和增殖的影响。
1 3D取向纳米纤维支架模型的制备
1.1 实验材料
聚己内酯(PCL,Mn~80000)购自Sigma公司;二氯甲烷(DCM)、N,N-二甲基甲酰胺(DMF),均为分析纯级别,购自广州化学试剂厂;细胞基础培养基(DMEM/F12)和链霉素-青霉素双抗溶液,购自Hyclone公司;胎牛血清(FBS)、胰蛋白酶(EDTA-Trypsin)、3-(4,5-二甲基噻唑)-2,5-二苯基四氮唑溴盐,噻唑蓝(MTT),购自GIBCO公司。
1.2 实验方法
制备取向和无规纳米电纺纤维膜的原理相同,只是在接收装置上有所区别。先将PCL溶于体积比为3∶1的DCM/DMF混合溶液中,质量分数为12%。电纺参数设置如下进行电纺:正极高压喷射头采用21#短针头(φ=0.22 mm),电压+14 kV, 接收距离为10 cm, 推进速度为2 mL/h。收集3D取向(3D-A)纳米纤维的装置如图1所示,该装置利用电机带动毛细管旋转收集取向纳米纤维。毛细管外径为300 μm,转速为900 r/min。在每根毛细管接收取向纳米纤维30 s后取下,如此重复。用同样的电纺溶液、纺丝参数制备对照样品。2D无规(2D-R)电纺膜用平面铝箔收集,2D取向(2D-A)电纺膜在接地金属片的狭缝处收集[24]。

图1 三维取向纳米纤维的电纺装置示意图Fig.1 Schematic diagram of the electrospinning setup for 3D aligned nanofibers
2 实验方法与结果
2.1 3D取向纳米纤维支架的形貌观察
2.1.1 测试方法 3D取向纤维支架模型经香豆素染色后,采用日本Olympus公司LX71荧光显微镜观察取向纤维整体形貌;然后,使用日本日立S-4800扫描电镜(SEM)在20 kV电压下观察喷金后的纳米纤维的表面形貌。2D无规和取向电纺纤维膜,亦采用S-4800型扫描电镜观察形貌。最后,用图像处理软件Image J分析纤维直径与取向分布。纤维取向由纤维与取向方向间的夹角表征,夹角越小,取向越单一。
2.1.2 测试结果 如图2,毛细管中段所收集的纤维直径分布最均匀,纤维取向最单一,几乎全部与毛细管轴向呈垂直。而上段所收集的纳米纤维取向和毛细管轴向夹角不为90°,有少许偏差。毛细管下段的纳米纤维厚度比中段薄,纤维取向不均一。这可能是因为毛细管各段与注射针头间的距离有差别,加上纺丝过程中还受重力作用,导致了毛细管不同段纤维取向不同。综上所述,本文选择毛细管中段的纳米纤维构建三维支架模型。

图2 毛细管上、中和下段取向电纺纤维荧光图Fig.2 Fluorescence microscope images of 3D aligned electrospun fibers on the top, middle and bottom of glass capillaries
纤维表面形貌进一步由SEM表征。如图3所示,3种纤维均连续,无结点。样品2D-R的纤维平均直径为(776±238)nm,~72.5%的纤维其直径分布在500~1 000 nm范围内,且取向随机。而样品2D-A的纤维平均直径及分布与2D-R较接近,平均值为760 nm,~77.2%的纤维直径分布在500-1 000 nm范围内。但,2D-A纤维具有高度取向性,~58.7%纤维取向角分布在-5°~5°范围内。由图3(c)可知,毛细管上的3D-A纳米纤维亦取向性良好。纤维平均直径为(333±68) nm,61.1%的纤维直径分布在300~400 nm范围内,表明该样品纤维直径分布较窄。~41.7%的纤维取向角度分布在-5°~5°范围内,表明该纤维取向性良好。综上所述,通过旋转的毛细管可收集连续性良好,取向单一的3D取向纳米纤维,且纳米纤维堆积厚度可通过纺丝时间控制。且与2D电纺膜相比,3D-A纤维较粗,直径分布较宽。
2.2 细胞在2D纤维膜上黏附与增殖检测
2.2.1 测试方法 细胞实验前,先将2D纤维膜灭菌(体积分数为75%酒精浸泡3 h),在超净台中风干后,室温下用0.1 mg/mL的PLL溶液包被过夜,后用PBS清洗。为观察细胞黏附情况,将ADSCs(ATCC)按密度104cells/cm2种于2D纤维膜上,待细胞增殖3 d后,将Calcein-AM存储液与PBS按1∶1 000比例混合加入细胞培养孔板,在37 ℃避光条件下孵育30 min,后用PBS清洗3遍,在荧光显微镜下观察细胞形貌。

图3 3种纤维的形貌、直径和取向分布图Fig.3 Fiber morphology (SEM image) and diameter, orientation distribution of three different electrospun nanofibers
为追踪细胞增殖,将ADSCs按密度为5×103cells/cm2种于2D纤维膜上。相比于MTT法,Alamar Blue法稍灵敏,且不影响细胞活性,可用于追踪同一组细胞的增殖[25]。因此,对于2D纤维膜,先用Alamar Blue法追踪细胞增殖行为。
2.2.2 测试结果 本文首先研究ADSCs在经表面改性的2D电纺纤维膜上的粘附与增殖。如图4所示,在无规与取向纤维膜上,细胞均铺展良好;在样品2D-R上,细胞随机分布,取向无规;而在样品2D-A上,细胞取向较规律,沿着纤维方向呈伸展形态。采用Alamar Blue法追踪了细胞的增殖行为。如图5所示,在前5 d,2D-R与2D-A样品间的吸光值无显著性差异,但在第7天,2D-R纤维膜上吸光值明显增加,表明其上细胞显著增殖;而2D-A上吸光值仍然维持在与前5 d较接近的数值。上述对比表明,在2D电纺纤维膜上,无规纤维膜较取向纤维膜更利于ADSCs的增殖。

图4 ADSCs在2D纤维膜上的荧光显微照片Fig.4 Fluorescence microscope images of ADSCs on 2D electrospun membranes after Calcein-AM staining
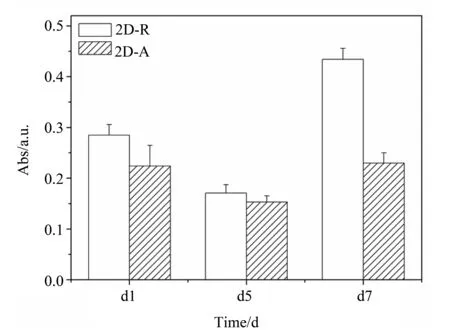
图5 ADSCs在2D-R和2D-A纤维支架上的增殖行为Fig.5 Monitoring proliferation of ADSCs on 2D-R and 2D-A electrospun membranes
2.3 细胞在3D纳米纤维支架模型上的粘附与增殖检测
2.3.1 测试方法 通过对3D取向纳米纤维的形貌观察,本文选用毛细管中间段的纳米纤维来构建用于细胞粘附与增殖研究的支架模型,将3D取向纳米纤维和毛细管一起,用硅胶粘在玻片(适于12孔板)上(样品3D-A)。作为对照组,先将无规纤维膜固定在毛细管上,后用同样的方式粘在玻片上(样品3D-R)。灭菌、PLL表面处理、细胞种植以及Calcein-AM染色参数同2.2.1。
对于3D支架模型,用MTT法表征细胞增殖行为。检测步骤如下:先配置质量浓度为5 mg/mL的MTT储存溶液,溶剂为PBS,加入细胞时,MTT储存液与培养基按1∶10的比例混合,在37 ℃避光条件下孵育4 h,后将培养基移除,每孔加入200 μL DMSO,置摇床上80 r/min震荡10 min,使结晶物甲瓒充分溶解,在将溶液移入96孔板中,使用美国BioTek Synergy4酶标仪检测490 nm处的吸光度。
2.3.1 测试结果 如图6,细胞在具有曲率的取向纤维上能够很好的黏附及铺展,且细胞沿着纤维取向的方向生长。
为了追踪细胞在3D纳米纤维支架模型上的增殖情况,采用MTT法检测细胞相对活性,结果如图7所示。图7中,两种模型支架的吸光值均随增殖时间逐渐增加,表明细胞在这两种模型支架上均有所增殖。3D-R与3D-A支架模型在所表征的时间范围(6 d内)无显著差异。但细胞在3D-A支架模型上的活性较高。以上结果表明,对于3D纤维支架模型,纤维呈取向分布时更利于ADSCs黏附及增殖。

图6 3D-A电纺纤维支架模型上ADSCs荧光显微照片Fig.6 Fluorescence microscope images of ADSCs on 3D-A electrospun scaffold model

图7 ADSCs在3D-R纤维支架模型上的增殖行为Fig.7 Monitoring proliferation of ADSCs on 3D electrospun scaffold models
3 分析与讨论
除了细胞内部的调控机制,细胞外基质(ECM)对细胞行为的信号调控作用具有重要意义。电纺纤维膜,因具有与ECM相似的结构与形貌,被广泛用于组织工程研究[26]。本研究构建了3D取向纤维支架模型来模拟体内ECM结构,进而研究其对ADSCs增殖的影响。通过改变接收装置获得了3D取向PCL纳米纤维支架。与2D电纺膜相比,3D纤维直径较小,取向更为规整。
ADSCs在2D纤维膜上可良好粘附,但与在无规纤维基底上(2D-R)相比,在取向纤维基底上(2D-A)细胞增殖速率较慢。这一发现与文献中结果较接近。人源间充质干细胞(hMSC)在具有纳米沟槽结构的基底上可沿着沟槽结构取向生长,但增殖速率却低于在平面无纳米拓扑结构的基底[27]。
当将ADSCs种于3D纤维模型支架时,发现细胞在3D-A支架上仍然沿纤维取向方向生长,而增殖速率与在3D-R支架上接近并在第2、6天略高。即使对于无规纤维,ADSCs在3D模型上增殖速率比在2D上更快。尽管对于在3D支架与2D纤维膜上细胞增殖的表征所用方法不同,但经对比发现,两种不同检测方式所展现出的趋势是一致的,如图8所示。3D支架模型,可为细胞提供了一个利于吸收氧及营养成分以及输出代谢废物的微环境。 因此ADSCs在3D模型支架上表现出更快的增殖趋势。

图8 Alamar Blue法和MTT法表征ADSCs在孔板(TCP)上增殖行为的对比Fig.8 Comparing Alamar Blue assay and MTT assay on monitoring proliferation of ADSCs on tissue culture plates (TCP)
4 结 论
本研究构建了3D取向纳米支架模型,探索了该模型对ADSCs黏附和增殖的影响。实验证明了细胞可沿着纤维丝取向方向生长。与2D纤维膜相比,3D模型支架包括3D取向支架,均具有更优的促细胞增殖能力。而间充质干细胞在取向基底上具有更优的成骨分化能力。因此,本研究的发现为骨组织工程支架的设计提供了新思路,即制备具有取向纳米结构如纳米纤维的三维支架材料,在修复骨缺损领域更具潜力。
[1] HOLZWARTH J M, MA P X. Biomimetic nanofibrous scaffolds for bone tissue engineering[J]. Biomaterials,2011, 32(36): 9622-9629.
[2] LIU X, JIN X, MA P X. Nanofibrous hollow microspheres self-assembled from star-shaped polymers as injectable cell carriers for knee repair[J]. Nat Mater,2011, 10(5): 398-406.
[3] WANG X, DING B, LI B. Biomimetic electrospun nanofibrous structures for tissue engineering[J]. Mater Today (Kidlington),2013, 16(6): 229-241.
[4] RIEGER K A, BIRCH N P, SCHIFFMAN J D. Designing electrospun nanofiber mats to promote wound healing -a review[J]. Journal of Materials Chemistry B,2013, 1(36):4531.
[5] LUO Y, SHEN H, FANG Y, et al. Enhanced proliferation and osteogenic differentiation of mesenchymal stem cells on graphene oxide-incorporated electrospun poly(lactic-co-glycolic acid) nanofibrous mats[J]. ACS Appl Mater Interfaces,2015, 7(11): 6331-6339.
[6] CHEW S Y, WEN Y, DZENIS Y, et al. The role of electrospinning in the emerging field of nanomedicine[J]. Curr Pharm Des,2006, 12(36): 4751-4770.
[7] VENUGOPAL J, LOW S, CHOON AT, et al. Interaction of cells and nanofiber scaffolds in tissue engineering[J]. J Biomed Mater Res B, Appl Biomater,2008, 84(1):34-48.
[8] BARNES C P, SELL S A, BOLAND E D, et al. Nanofiber technology: designing the next generation of tissue engineering scaffolds[J]. Adv Drug Deliv Rev,2007, 59(14):1413-1433.
[9] ABAGNALE G, STEGER M, NGUYEN V H, et al. Surface topography enhances differentiation of mesenchymal stem cells towards osteogenic and adipogenic lineages[J]. Biomaterials, 2015,61: 316-326.
[10] TASKIN M B, XU R, ZHAO H, et al. Poly(norepinephrine) as a functional bio-interface for neuronal differentiation on electrospun fibers[J]. Phys Chem Chem Phys, 2015, 17(14): 9446-9453.
[11] MA B, XIE J, JIANG J, et al. Rational design of nanofiber scaffolds for orthopedic tissue repair and regeneration[J]. Nanomedicine (Lond), 2013, 8(9):1459-1481.
[12] DUQUE S L, BRACK N, POSTMA A, et al. Surface modification of electrospun fibres for biomedical applications: A focus on radical polymerization methods[J]. Biomaterials, 2016, 106: 24-45.
[13] SCHNELL E, KLINKHAMMER K, BALZER S, et al. Guidance of glial cell migration and axonal growth on electrospun nanofibers of poly-epsilon-caprolactone and a collagen/poly-epsilon-caprolactone blend[J]. Biomaterials, 2007, 28(19): 3012-3025.
[14] LI W J, LAURENCIN C T, CATERSON E J, et al. Electrospun nanofibrous structure: a novel scaffold for tissue engineering[J]. J Biomed Mater Res,2002, 60(4):613-621.
[15] KUMBAR S G, JAMES R, NUKAVARAPU S P, et al. Electrospun nanofiber scaffolds: engineering soft tissues[J]. Biomed Mater, 2008, 3(3): 034002.
[16] SUBRAMANIAN A, KRISHNAN U M, SETHURAMAN S. Fabrication of uniaxially aligned 3D electrospun scaffolds for neural regeneration[J]. Biomed Mater, 2011, 6(2): 025004.
[17] BOSWORTH L A, ALAM N, WONG J K, et al. Investigation of 2D and 3D electrospun scaffolds intended for tendon repair[J]. J Mater Sci Mater Med, 2013,24(6): 1605-1614.
[18] XU T, MISZUK J M, ZHAO Y, et al. Electrospun polycaprolactone 3D nanofibrous scaffold with interconnected and hierarchically structured pores for bone tissue engineering[J]. Adv Healthc Mater, 2015, 4(15): 2238-2246.
[19] CHENG K H, KUO T L, KUO K K, et al. Human adipose-derived stem cells: Isolation, characterization and current application in regeneration medicine[J]. Genomic Medicine, Biomarkers, and Health Sciences,2011, 3(2): 53-62.
[20] JONES E, YANG X. Mesenchymal stem cells and bone regeneration: current status[J]. Injury, 2011, 42(6): 562-568.
[21] SALGADO A, OLIVEIRA J, PEDRO A, et al. Adult stem cells in bone and cartilage tissue engineering[J]. Current Stem Cell Research & Therapy. 2006, 1(3): 345-364.
[22] STERODIMAS A, DE Faria J, NICARETTA B, et al. Tissue engineering with adipose-derived stem cells (ADSCs): current and future applications[J]. J Plast Reconstr Aesthet Surg, 2010, 63(11):1886-1892.
[23] GOMILLION C T, BURG K J. Stem cells and adipose tissue engineering[J]. Biomaterials,2006, 27(36):6052-6063.
[24] LI D, WANG Y L, XIA Y N, et al. Electrospinning of polymeric and ceramic nanofibers as uniaxially aligned arrays[J]. Nano Letters, 2003, 3(8):1167-1171.
[25] HAMID R, ROTSHTEYN Y, RABADI L, et al. Comparison of alamar blue and MTT assays for high through-put screening[J]. Toxicology in Vitro, 2004, 18(5): 703-710.
[26] YIN Z, CHEN X, SONG H X, et al. Electrospun scaffolds for multiple tissues regeneration in vivo through topography dependent induction of lineage specific differentiation[J]. Biomaterials,2015, 44:173-185.
[27] WATARI S, HAYASHI K, WOOD J A, et al. Modulation of osteogenic differentiation in hMSCs cells by submicron topographically-patterned ridges and grooves[J]. Biomaterials,2012, 33(1): 128-136.
Fabricationof3Dalignedelectrospunnaofiberstoenhancetheproliferationofstemcells
WANGDandan1, 2,3,ZHONGHuixiang1, 2,3,XUANLiuyang1, 2,3,MAShuangshuang1, 2,3,LIYan1, 2,3,JIANGLelun1, 2,3,JIANGQing1, 2,3
(1. Department of Biomedical Engineering, School of Engineering, Sun Yat-sen University, Guangzhou 510006, China;(2. Guangdong Provincial Key Laboratory of Sensor Technology and Biomedical Instrument, Guangzhou 510006, China;3. Guangdong Province Portable Universal Advanced Medical Equipment Engineering Technology Research Center, Guangzhou 510006, China)
In order to mimic theinvivo3D micro environment and compare proliferation rate of adipose derived stem cells (ADSCs) on 2D and 3D aligned nanofiber sheets, 3D aligned poly(caprolactone) (PCL) fiber scaffolds were prepared by improving the collector for electrospinning. The fibers were around capillaries in diameter of 300 μm, which were aligned very well and with fiber diameter in the range of 300~400 nm. After surface modification, ADSCs were seeded and it was found these cells were spread very well. Regardless 2D or 3D scaffolds, on aligned fibers cells were nearly all aligned along the fiber direction. When compared with that on 2D membranes, cells proliferated faster on 3D fiber scaffolds, showing the higher potential of 3D fiber scaffolds to be applied for tissue engineering applications.
three-dimensional oriented fibers; electrospinning; adipose derived stem cells; bone tissue engineering
10.13471/j.cnki.acta.snus.2017.06.012
2017-03-23
国家自然科学基金(51303216)
王丹丹(1992年生),女;研究方向静电纺丝;E-mail:wangdd_bme@163.com
钟惠湘(1991年生),女;研究方向:干细胞扩增;E-mail:huixiang34@163.com
(以上2位作者并列第1作者)
李燕(1984年生),女;研究方向生物材料;E-mail:liyan99@mail.sysu.edu.cn
R318.08
A
0529-6579(2017)06-0076-07
