利伐沙班关键杂质的合成
2017-12-15罗海荣顾荣领
罗海荣, 顾荣领, 王 蓉
(1. 铜仁学院 材料与化学工程学院,贵州 铜仁 554300; 2. 浙江海正药业股份有限公司,浙江 台州 318000)
·制药技术·
利伐沙班关键杂质的合成
罗海荣1*, 顾荣领2, 王 蓉1
(1. 铜仁学院 材料与化学工程学院,贵州 铜仁 554300; 2. 浙江海正药业股份有限公司,浙江 台州 318000)
以对溴硝基苯为原料,经偶联、胺基保护、亲核取代、硝基还原、环氧开环、环合、脱保护和胺基酰化反应合成了利伐沙班的二胺杂质——5-氯-N-【【(5S)-2-氧代-3-{4-[5-氯-噻吩-2-甲酸-N-(2-甲基氨基甲酰基甲氧基乙基)酰胺基]苯基}-1,3-噁唑烷-5-基】甲基】-2-噻吩甲酰胺,其结构经1H NMR,13C NMR, DEPT135°,1H-1HCOSY, HSQC, HMBC和MS(ESI)确证。
对溴硝基苯; 利伐沙班; 关键杂质; 二胺; 合成
利伐沙班(Rivaroxaban)[1],化学名为5-氯-N-【{(5S)-2-氧代-3-[4-(3-氧代-4-吗啉基)苯基]-1,3-噁唑烷-5-基}甲基】-2-噻吩甲酰胺(1, Chart 1),是由拜耳和强生公司共同研发的一种高效FXa抑制剂,主要用于进行择期髋关节或膝关节置换手术的成年患者。1对预防静脉血栓形成有良好的功效[2]。2008年,1在加拿大和欧盟获得批准上市,商品名为Xarelto[3]。与传统的抗凝药相比,1的服用方法简单,选择性高,可直接抑制Xa因子,是一种具有较好应用前景的新型抗凝药物[4]。
为控制1的质量,蔡正艳等[5]根据1的结构特征和合成工艺,合成了8种相关化合物。Mangion等[6]阐述了1的两种可能杂质的合成方法。李维思等[7]合成了1的对映异构体杂质。为了进一步控制1的原料药中的相关杂质,保证药物质量,本文参考药品杂质分析指导原则[8]和1的进口注册标准[9],合成了1进口注册标准中的一种相关物质(二胺杂质):5-氯-N-【【(5S)-2-氧代-3-{4-[5-氯-噻吩-2-甲酸-N-(2-甲基氨基甲酰基甲氧基乙基)酰胺基]苯基}-1,3-噁唑烷-5-基】甲基】-2-噻吩甲酰胺(A)。
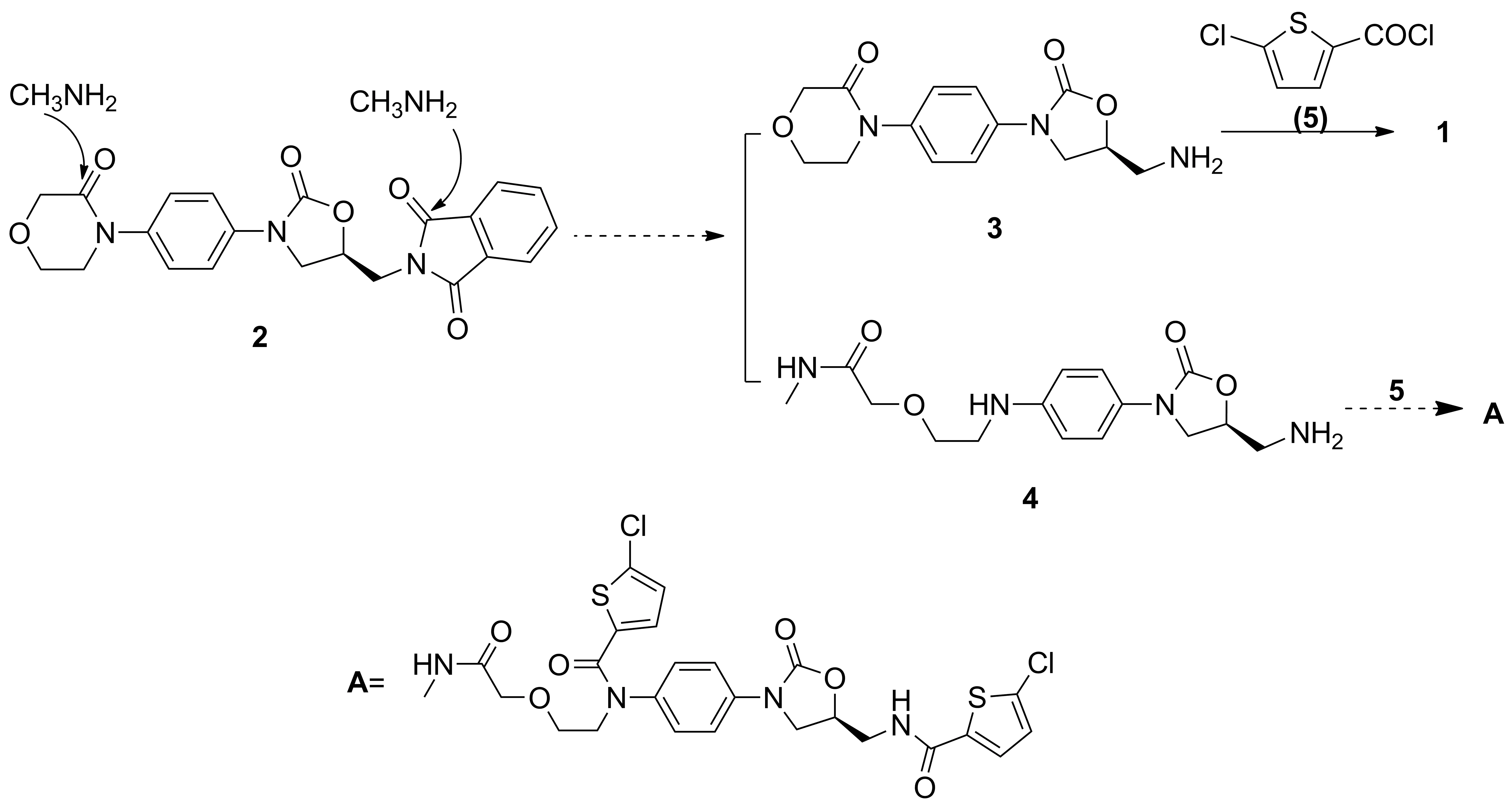
Scheme 1
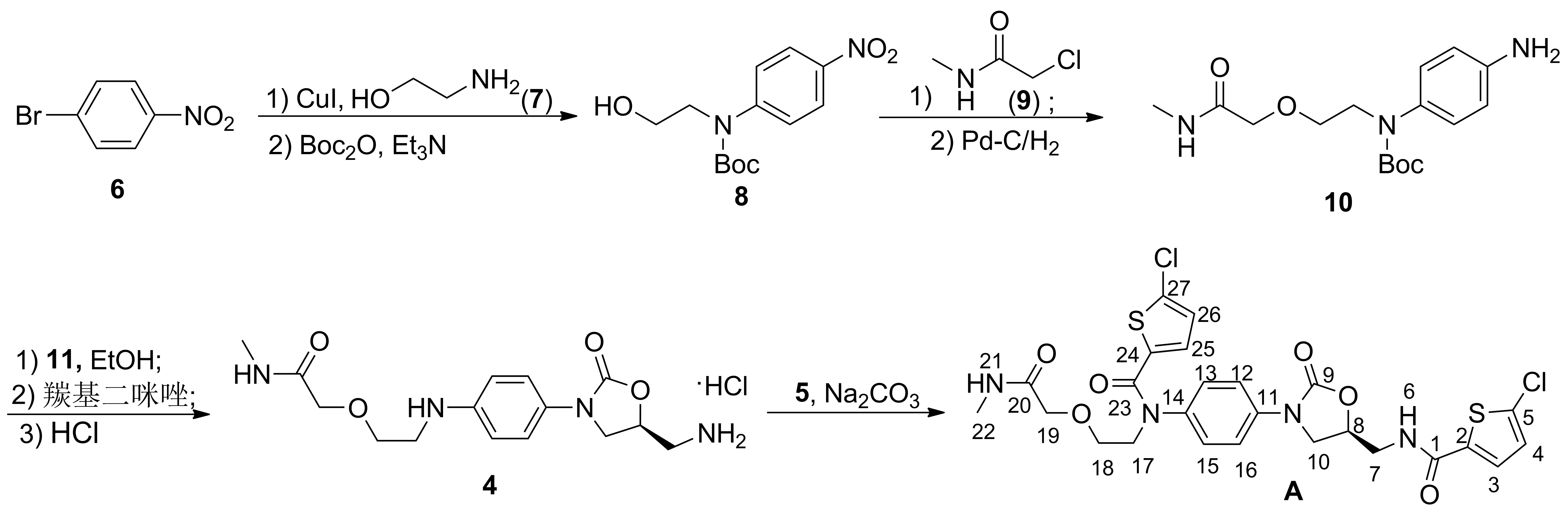
Scheme 2
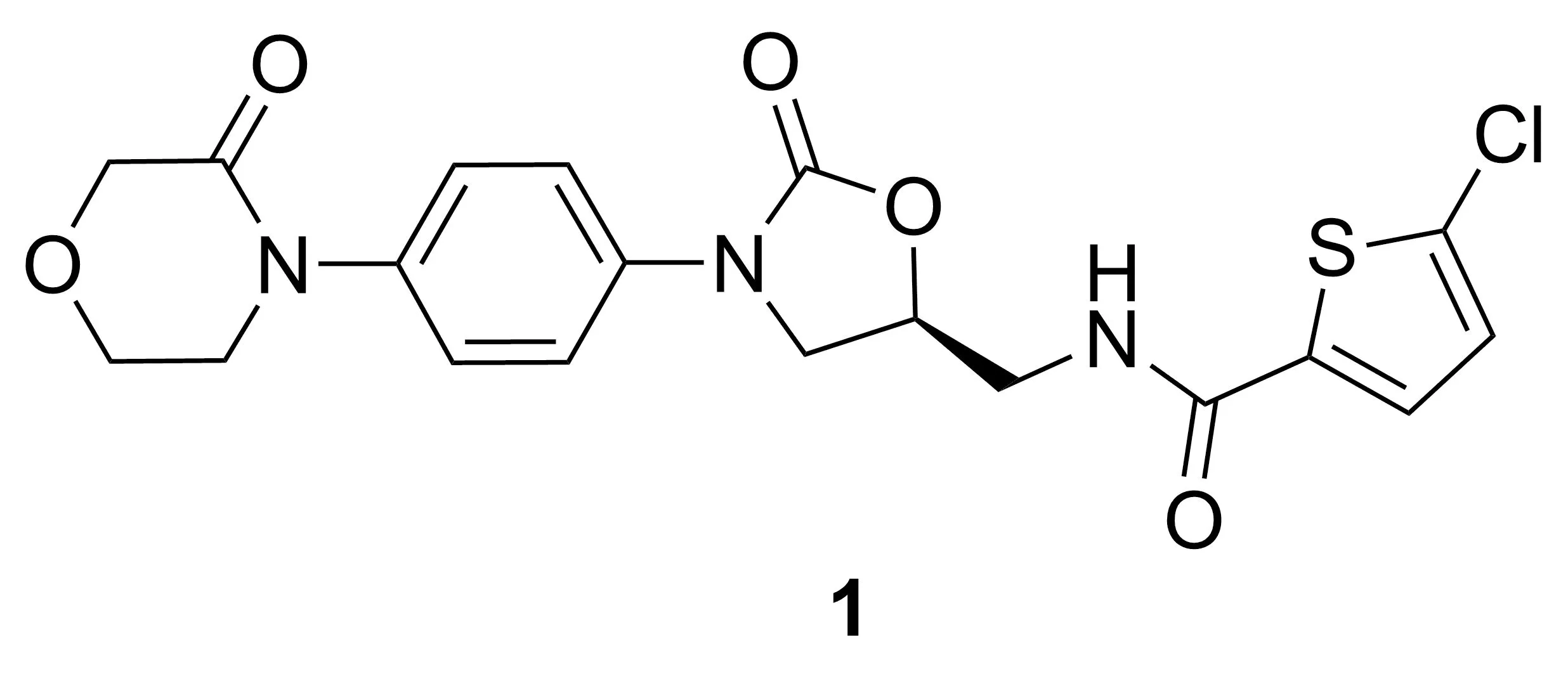
Chart 1
A与1的结构相似,其可能的合成方法如Scheme 1所示。1的合成过程[10]涉及2的氨解反应,主要产物为3,该氨解反应同时可能有少部分甲胺对2的吗啉酮基进行氨解开环得到4,所得化合物继续参与后续反应生成A。郑继宇等[11]报道了A的合成方法,以1为原料,经多步反应合成了A,但该专利并未对A的结构进行确证。冯汝洁等[12]以叔丁基-4-氨基苯胺甲酸酯和(S)-N-环氧丙基邻苯二甲酰亚胺为原料,经8步反应合成了A。该专利只公布了1H NMR数据。
本文以对溴硝基苯(6)为原料,与2-氨基乙醇(7)缩合后经氨基保护得化合物(8);8与2-氯-N-甲基乙酰胺(9)缩合后经钯碳氢化还原硝基得化合物(10);10与(S)-N-环氧丙基邻苯二甲酰亚胺(11)缩合,再在羰基二咪唑作用下环合,然后经盐酸脱胺基保护得到盐酸盐(4);4与5-氯-2-酰氯噻吩(5)反应合成了A(Scheme 2)。
1 实验部分
1.1 仪器与试剂
Perkin-Elmer-314型自动旋光仪;Bruker Avance 400 MHz型核磁共振仪(DMSO-d6为溶剂,TMS为内标);Agilent 1260 LC-6540 Q-TOF MS型质谱仪;Agilent 1260型[HPLC归一法,Merck RP-18色谱柱(4.0 mm×55 mm, 3 μm);流动相A:0.01 mol·L-1磷酸溶液/乙腈=92/8,V/V,流动相B:0.01 mol·L-1磷酸溶液/乙腈=51/49,V/V;检测波长:250 nm;柱温:45 ℃;流速:1.0 mL·min-1]。
所用试剂均为分析纯或化学纯。
1.2 合成
(1)8的合成
在三颈烧瓶中依次加入对溴硝基苯5 g(24.7 mmol),乙醇胺20 mL(334 mmol)和碘化亚铜0.5 g(2.6 mmol),搅拌下于120 ℃(浴温)反应2 h。冷却至室温,倒入冰水(100 mL)中,析出黄色片状结晶,剧烈搅拌,析晶完全后抽滤,用乙酸乙酯重结晶得淡黄色片状晶体M 4.0 g(22.0 mmol)[13]。将M 4.0 g,二碳酸二叔丁酯(Boc2O)7.2 g(32.9 mmol),四氢呋喃40 mL和三乙胺4.4 g(43.9 mmol)加入单口烧瓶中,搅拌下于室温反应10 h。旋蒸除溶,残余物经硅胶柱层析(洗脱剂:A=石油醚/乙酸乙酯=15/1,V/V)纯化得无色液体85.9 g,收率85%;1H NMRδ: 1.44[s, 9H, OC(CH3)3], 3.32(t, 2H, CH2), 3.80(m, 2H, CH2), 4.01(brs, 1H, OH), 6.82(d,J=9.3 Hz, 2H, ArH), 8.18(d,J=9.3 Hz, 2H, ArH)。
(2)10的合成
在三颈烧瓶中依次加入85.5 g(19.5 mmol),乙腈25 mL,碳酸钾4.1 g(30.0 mmol)和92.3 g(21.5 mmol),搅拌下于80 ℃(浴温)反应5 h(TLC检测)。冷却至室温,倒入冰水(100 mL)中,用乙酸乙酯(2×25 mL)萃取,合并有机相,用无水硫酸钠干燥,过滤,滤液经减压浓缩,所得残余物用甲醇(30 mL)溶解,加入钯碳0.2 g,氢气氛围下于0 ℃反应3 h(TLC检测)。滤除钯碳,滤液浓缩,残余物经硅胶柱层析(洗脱剂:A=3/1)纯化得无色液体104.7 g,收率75%, m.p.108~110 ℃。
(3)4的合成
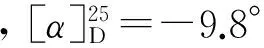
(4)A的合成

2 结果与讨论
2.1 表征
表1和表2为A的结构表征结果。由表1和表2可见,A的结构与文献[12]报道基本一致。
2.2 合成
(1)8的合成
合成8时,参考了文献[10]方法,即采用对溴硝基苯和乙醇胺在CuI作用下合成2-(4-硝基苯基胺基)乙醇。表3为反应温度对反应的影响。由表3可见,反应温度由80 ℃升至120 ℃,可以有效缩短反应时间。合成的黄色晶体产物蒸除溶剂后,不需重结晶,可直接进行胺基保护反应,不会对收率产生不良影响。

表1 1H NMR和相关性解析结果Table 3 1H NMR and correlation analysis result
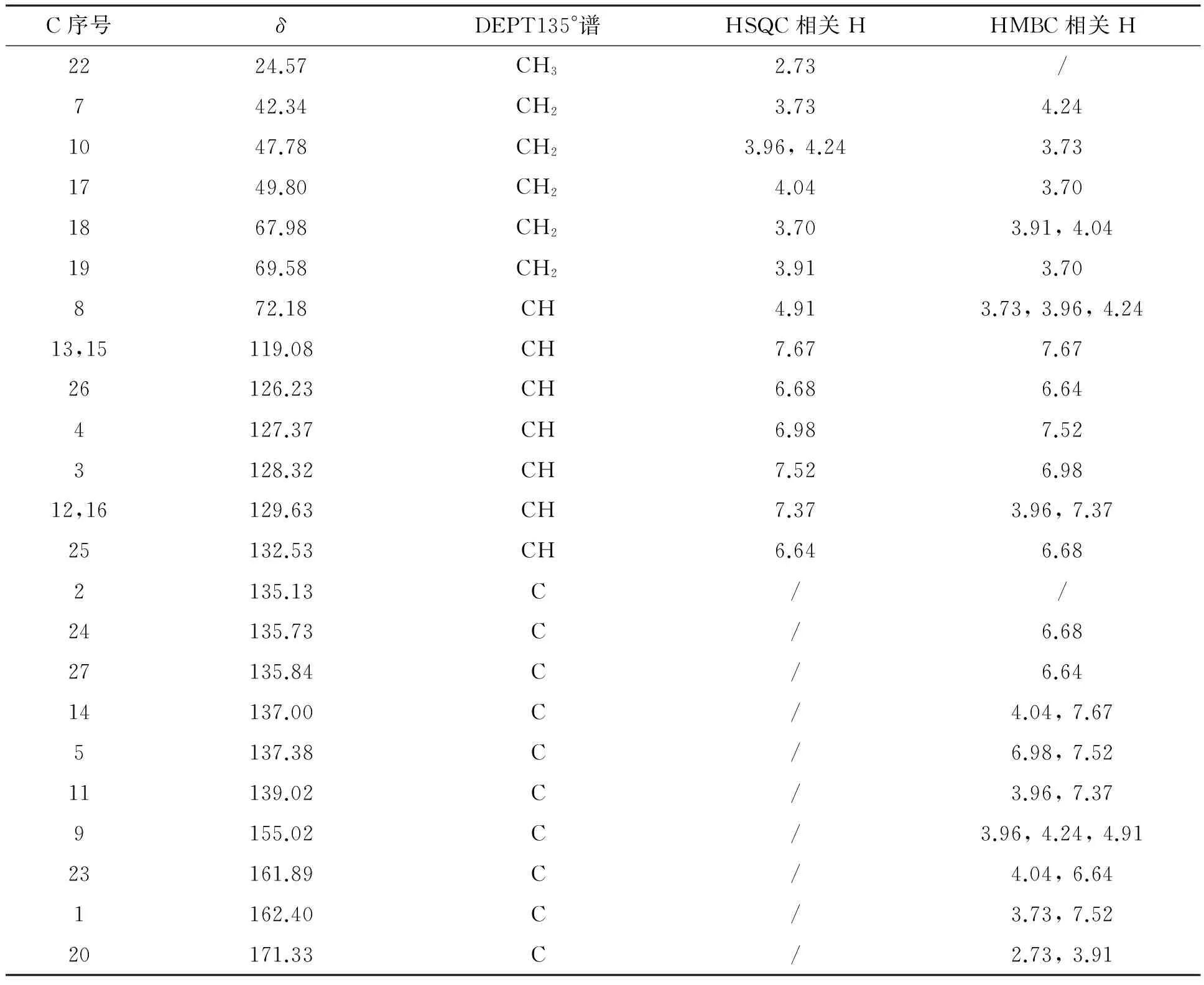
表2 13C NMR和相关性解析结果Table 2 13C NMR and correlation analysis result
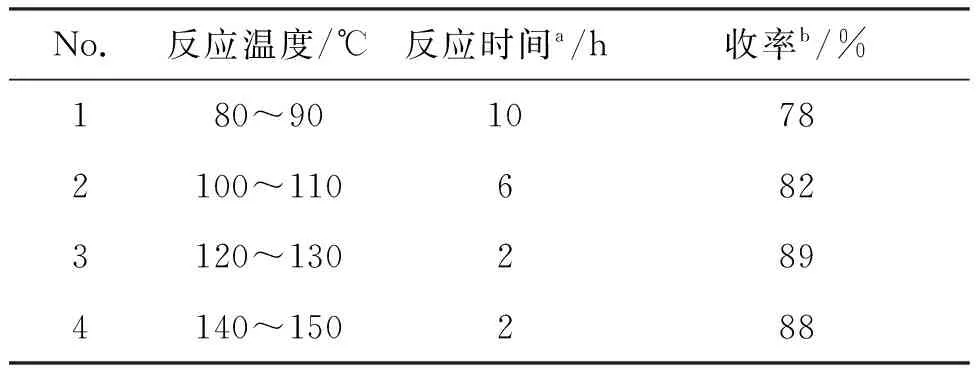
表3 反应温度对反应的影响Table 3 Effect of temperature on the reaction
aTLC监控;b摩尔收率。

表4 钯碳加氢温度对反应的影响Table 4 Effect of Pd-C/H2 temperature on the reaction
aTLC监控;b摩尔收率。
(2)10的合成
8先在碳酸钾的作用下与9发生氧烷基化反应,再经钯碳氢化还原硝基得化合物10。我们研究了钯碳还原反应温度对10收率的影响,结果见表4。由表4可见,反应温度为0~5 ℃时,收率最高(95%)。其可能原因为:冷却后的氢气与反应底物接触较为充分。
(3)4的合成
合成4时,我们采用甲胺脱胺基保护,收率偏低。采用盐酸可以同时脱除伯胺和肿胺的保护,而且产物成盐析出,免去了柱层析纯化的步骤。
合成了5-氯-N-{{(5S)-2-氧代-3-{4-[5-氯-噻吩-2-甲酸-N-(2-甲基氨基甲酰基甲氧基乙基)酰胺基]苯基}-1,3-噁唑烷-5-基}甲基}-2-噻吩甲酰胺(A),并确证了其结构。A的合成对利伐沙班的生产、贮存和检验均有一定的实际意义。
[1] ROEHRIG S, STRAUB A, POHLMANN J,etal. Discovery of the novel antithrombotic agent 5-chloro-N-({(5S)-2-oxo-3-[4-(3-oxomorpholin-4-yl)phenyl]-1,3-oxazolidin-5-ylmethyl)thiophene-2-carboxamide(BAY 59-7939):An oral,direct factor Xa inhibitor[J].J Med Chem,2005,48(19):5900-5908.
[2] THOMAS T F, GANETSKY V, SPINLER S A. Rivaroxaban:An oral factor Xa inhibitor[J].Clin Ther,2013,35(1):4-27.
[3] 利伐沙班在加拿大和欧盟获得上市批准[J].中国医药导刊,2008,(7):1061-1061.
[4] 田国祥,魏万林,张灵,等. 后华法林时代口服抗凝新秀:达比加群、利伐沙班、阿哌沙班[J].中国循证心血管医学杂志,2011,12(3):403-406.
[5] 蔡正艳,温颖玲,张顺利,等. 利伐沙班有关物质的合成及结构确定[J].中国医药工业杂志,2014,45(4):303-307.
[6] MANGION B, DURAN L E. Process for determining the suitability for distribution of a batch of a thiophene-2-carboxamide derivative:WO 2012035057A[P].2012.
[7] 李维思,徐强,王华,等. 利伐沙班异构体杂质的合成[J].山东化工,2016,45(10):34-36.
[8] 国家药典委员会. 中华人民共和国药典:二部[M].北京:中国医药科技出版社,2010:204-205.
[9] 国家食品药品监督管理局. 利伐沙班片进口注册标准JX20080077[S].北京:中国医药科技出版社,2009.
[10] 袁静,黄长江,张俊伟,等. 利伐沙班的合成[J].中国新药杂志,2010,19(23):2185-2187.
[11] 郑继宇,孙长山,孙铁民,等. 一种利伐沙班相关物质二胺的合成方法:CN 104844588A[P].2015.
[12] 冯汝洁,施涯邻,吴毅武,等. 一种利伐沙班的有关物质f、g的合成方法:CN 104892593A[P].2015.
[13] 罗玲艳,申东升,周宗洲,等. 4-(4-氨基苯基)-3-吗啉酮的合成[J].中国医药工业杂志,2011,42(2):93-95.
SynthesisofTheKeyImpurityofRivaroxaban
LUO Hai-rong1*, GU Rong-lin2, WANG Rong1
(1. School of Material and Chemical Engineering, Tongren University, Tongren 554300, China; 2. Zhejiang Hisunpharm Co., Ltd., Taizhou 318000, China)
The key diamine impurity of Rivaroxaban, 5-chloro-N-{{(5S)-2-oxo-3-{4-[5-chloro-thiophene-2-carboxylic acid-N-(2-methylcarbamoxylmethoxyethyl)-amide]phenyl}-1,3-oxazolidin-5-yl}methyl}-thiophene-2-carboxamide, was synthesized from 4-nitrobromobenzeneviathe reaction of coupling, amino group protection, nucleophilic substitution, nitro reduction, epoxy ring opening, cyclization, deprotection and amine acylation. The structure was confirmed by1H NMR,13C NMR, DEPT135°,1H-1HCOSY, HSQC, HMBC and MS(ESI).
4-nitrobromobenzene; Rivaroxaban; key impurity; diamine; synthesis
2017-04-25;
2017-09-20
贵州省科技合作计划项目(黔科合LH字[2016] 7309号); 铜仁学院博士科研启动基金(trxyDH1605)
罗海荣(1976-),男,汉族,江西宜春人,副教授,主要从事药物合成工艺的研究。 E-mail: luohair@163.com
O621.3; R914.5
A
10.15952/j.cnki.cjsc.1005-1511.2017.12.17096
