盐酸右美托咪定对颅内动脉瘤介入手术患者术中及苏醒期血流动力学的影响
2017-12-15史记刘雅张娜娜周长浩
史记 刘雅 张娜娜 周长浩
·论著·
盐酸右美托咪定对颅内动脉瘤介入手术患者术中及苏醒期血流动力学的影响
史记 刘雅 张娜娜 周长浩
目的本研究拟观察盐酸右美托咪定复合七氟醚吸入进行全身麻醉用于颅内动脉瘤介入治疗术的效果。方法40例接受颅内动脉瘤栓塞术的患者,根据麻醉维持用药不同随机分为R组(瑞芬太尼)和D组(盐酸右美托咪定)。记录麻醉诱导前(T0)、气管插管完成后(T1)、盐酸右美托咪定输注15 min(T2)、输注30 min(T3)及手术结束时(T4)各时点患者MAP(平均动脉压)、心率(HR)及血氧饱和度(SPO2)数值。麻醉苏醒期,记录带管耐受(S1)、指令配合(S2)、拔除气管插管(S3)及出手术室时(S4)各时点血流动力学数值并根据riker镇静和躁动评分(SAS)评估分值,记录各组拔管时间。结果2组患者一般情况比较差异无统计学意义(Pgt;0.05)。 2组患者血流动力学指标在麻醉维持期的比较:T1、T2、T3及 T4时间点MAP,D组均高于R组(Plt;0.05);HR值比较,D组较 R组明显降低(Plt;0.05)。2组患者血流动力学指标在麻醉苏醒期比较:S1、S2、S3及S4时间点HR及MAP, D组均低于R组(Plt;0.05)。与基础值相比,MAP及HR的变化幅度D组明显低于R组(Plt;0.05)。苏醒期Riker镇静和躁动评分(SAS),D组明显低于R组(Plt;0.05)。拔管时间,D组较R组明显延长(Plt;0.05)。结论盐酸右美托咪定用于颅内动脉瘤介入手术患者全麻维持期间的血流动力学稳定,维持了良好的脑组织灌注能力。盐酸右美托咪定在全麻苏醒期血流动力学稳定,躁动评分降低,减少了随着麻醉作用减弱出现的剧烈应激反应。
右美托咪定;血流动力学;组织灌注;应激;保护;镇静
颅内动脉瘤介入治疗是目前广泛开展的神经外科微创手术,其对围麻醉期血流动力学稳定性要求苛刻,麻醉苏醒期有必要患者配合进行神经系统检查评估手术效果。以往颅内动脉瘤介入治疗采用的麻醉方法多是瑞芬太尼复合七氟烷静吸全麻。瑞芬太尼超短时效,镇痛作用强,但作用消失快,疼痛发生早,疼痛和苏醒迅速带来的不适可引起烦躁,甚至是心脑血管系统意外[1]。七氟烷术中血流动力学较平稳,减少肌肉松弛剂用量,术后苏醒快而彻底,但恢复期易发生躁动[2,3]。右美托咪定是高选择性α2肾上腺素能受体激动剂(α2∶α1为1 600∶1),具有中枢性降压、催眠镇静、镇痛、抗焦虑等作用[4],能抑制中枢交感神经系统活性,减少应激反应,同时通过降低脑组织中儿茶酚胺的浓度减轻对神经元的毒性而发挥脑保护作用[5,6]。右美托咪啶的优良药理特点在于采用右美托咪啶镇静的患者更容易被唤醒以配合进行各种操作及神经学评估[7]。被誉为是最理想的全麻苏醒期麻醉管理协助性用药以及有助于患者顺利脱机拔管最有价值的选择用药[8]。本研究拟观察右美托咪定复合七氟醚吸入进行全身麻醉用于颅内动脉瘤介入治疗术的临床效果。
1 资料与方法
1.1 一般资料 选择河北医科大学第一医院2014年5月至2015年1月40例接受颅内动脉瘤栓塞术的患者,随机分为D组[右美托咪定(dexmedetomidine)]和R组[瑞芬太尼(remifentanil)]。2组患者一般情况比较无统计学差异(Pgt;0.05)。见表1。

表1 2组一般情况比较 n=20
1.2 纳入及排除标准
1.2.1 纳入标准:①经本院医学伦理委员会批准同意和患者(或授权委托人)书面知情同意,选取本院实施行颅内动脉瘤介入治疗术的患者;②经MRI或全脑血管造影术诊断明确的颅内动脉瘤实施介入治疗的患者;③ASA评分Ⅱ~Ⅲ级的患者。
1.2.2 排除标准:①有严重的心、肺、肝、肾和代谢性疾病的患者;②有精神异常,不能合作的患者;③术前已经出现意识障碍,嗜睡,昏迷,不能配合指令完成检查动作的患者;④有长期使用镇静镇痛药,或者酒精,精神药品依赖的患者;⑤有心动过缓或缓慢性心律失常的患者;⑥有休克、严重的脱水或电解质紊乱的患者;⑦手术时间gt;3 h,手术治疗操作时有意外情况出现的患者。
1.3 麻醉实施方案 所选取病例均不予术前用药,患者入室开放静脉液路。常规监测心电图(以Ⅱ导为主,必要时多导联监测显示),连续血压监测(频率3 min/次,必要时连续测压),血氧饱和度(SPO2)。麻醉诱导采用咪达唑仑0.05 mg/kg,舒芬太尼0.3 μg/kg,顺式阿曲库铵0.2 mg/kg及依托咪酯0.15 mg/kg静脉注射。麻醉维持:R组:1.5%~3%七氟烷吸入,瑞芬太尼0.1~0.2 μg·kg-1·min-1持续输注;D组:1.5~3%七氟烷吸入,右美托咪定负荷量0.5 μg/kg,10 min输注完毕,之后0.4 μg·kg-1·h-1持续输注。(术中维持BIS值在40~60)。麻醉苏醒:手术结束前约10 min,2组均静脉给予舒芬太尼0.1 μg/kg。同时关闭蒸发器,降低新鲜气体流量至0.3~0.5 L/min,至外科缝皮时方增加新鲜气体流量至4 L/min。术中心血管调节药物使用的管理方案:低血压定义为MAPlt;65 mm Hg (年龄lt;65岁)或MAPlt;70 mm Hg (年龄≥65岁),或者与患者术前基础血压值比较MAP下降gt;30%,并持续1 min。处理:适当减浅麻醉深度,进行容量调节,必要时静脉注射去甲肾上腺素2~4 μg。心动过缓定义为:HRlt; 50次/min静脉注射阿托品0.25~0.5 mg。如果MAP增高超过基础值20%并且持续3 min,则先适当加深麻醉深度,必要时静脉注射乌拉地尔5~10 mg。HR gt;100次/min静脉注射艾司洛尔10~20 mg。
1.4 观察指标 观察记录麻醉诱导前(T0),气管插管完成后(T1),盐酸右美托咪定输注15 min(T2),盐酸右美托咪定输注30 min(T3)及手术结束时(T4)各时点患者平均动脉压,心率及血氧饱和度数值。麻醉苏醒期,根据riker镇静和躁动评分(SAS)记录苏醒即刻(S1)、指令配合(S2)、拔除气管插管(S3)及出手术室时(S4)各时点血流动力学数值及评分,2组拔管时间。拔管时间定义为:停用使用麻醉药物到拔管的时间。见表2。
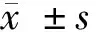

表2 SAS具体内容
2 结果
2.1 2组患者血流动力学指标在麻醉维持期比较 T0时点2组患者MAP及HR无明显差异(Pgt;0.05)。T1、T2、T3及 T4时间点MAP,右美托咪定组均高于瑞芬太尼组(Plt;0.05)。同时点HR值右美托咪定组较瑞芬太尼组明显降低(Plt;0.05)。见表3,图1、2。
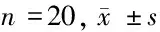
表3 2组麻醉维持期各时点MAP 和HR比较
注:与T0比较,*Plt;0.05;与R组比较,#Plt;0.05
2.2 2组患者血流动力学指标在麻醉苏醒期比较 S1、S2、S3及S4时间点MAP及HR,右美托咪定组低于瑞芬太尼组(Plt;0.05)。与基础值相比,MAP及HR的变化幅度明显低于瑞芬太尼组(Plt;0.05)。见表4,图3、4。
2.3 2组苏醒期SAS比较 苏醒期SAS右美托咪定组明显低于瑞芬太尼组(Plt;0.05)。见表5。
2.4 2组拔管时间比较 拔管时间,右美托咪定组较瑞芬太尼组明显延长(Plt;0.05)。见表6。

图1 2组患者麻醉维持期MAP比较
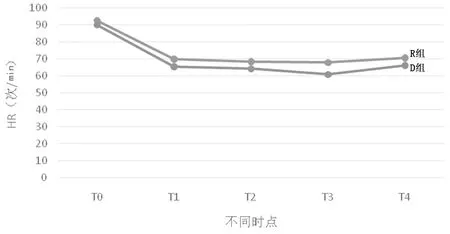
图2 2组患者麻醉维持期HR比较
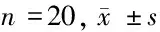
表4 2组患者麻醉恢复期MAP和HR比较
注:与S1比较,*Plt;0.05;与R组比较,#Plt;0.05
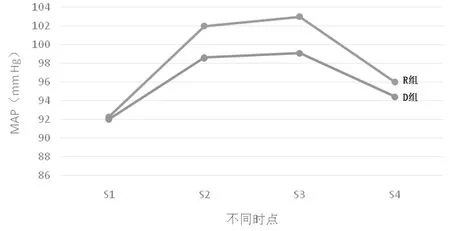
图3 2组患者麻醉恢复期MAP比较

图4 2组患者麻醉恢复期HR比较

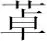
表5 2组患者苏醒期SAS评分 n=20,分
注:与R组比较,*Plt;0.05
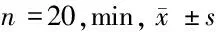
表6 2组患者拔管时间比较
注:与R组比较,*Plt;0.05
3 讨论
颅内动脉瘤介入治疗手术属微创手术,患者的基本麻醉要求是制动可靠,术中充分镇静镇痛,麻醉期间血流动力学表现稳定,保证重要脏器的灌注能力。术毕,患者可以平稳苏醒,并能够在耐受气管插管的前提下,可以进行自主配合的神经查体检查,及时评估手术治疗效果。期间患者要求不能躁动,避免发生对手术结果影响较大的恶性事件,比如疼痛刺激,气管导管耐受不良引起躁动,挣扎反抗,导致循环剧烈波动,容易诱发围术期心脑血管意外。
颅内动脉瘤的患者大都伴有长期的高血压疾病,在长期慢性高血压疾病的发展过程中,患者的血压压力感受性反射功能曲线向右移位,即压力感受性反射的调定点上移,使患者的基础动脉血压维持在了一个高于正常水平的状态。因此,患者术中维持的循环灌注压力也需要保持在一个正常的较高平稳水平,从而不至于发生麻醉管理期间组织器官的缺血缺氧损伤。另一方面,该类患者的交感神经兴奋性及依赖性增强,导致该类患者对于不良的外因刺激会产生更加剧烈的应激反应,而发生意外事件,所以必须保证可靠的麻醉深度。矛盾之处在于,不恰当的麻醉抑制又会导致交感神经兴奋可依赖能力的减弱,患者出现生理功能的急性失代偿而导致灌注指标平均动脉压数值持续偏低最终导致灌注不良。
右美托咪定作为麻醉镇痛镇静的协助性用药,在本次试验研究中用于麻醉维持期间使用,表现出了良好的血流动力学平稳性,虽然给予负荷量期间,由于药物自身作用的影响发生了较为明显的心率改变,但是对于平均动脉压力的影响是有限的。对比瑞芬太尼这一经典的阿片类麻醉药品,瑞芬太尼确实能够提供完善可靠的镇痛,从而在麻醉过程中表现出良好的血流动力学稳定性,但是对于疼痛刺激较轻的微创操作而言,这种镇痛的效能相对更多的表现为了麻醉的过度抑制,导致患者术中平均动脉压力明显偏低。在麻醉管理过程中,考虑到可能出现的组织器官灌注不良,无法给予充分的麻醉深度保证,容易出现“低血压状态掩盖的浅麻醉状态”。伴随着七氟烷吸入剂量的调整,不可完全避免术中知晓的发生。而必要时不得不使用升压药物替代治疗来保证麻醉深度,这就增加了麻醉实施的难度,同时又容易在调整麻醉深度和升压药物共同作用维持下的血流动力学动态平衡时,发生不可预期的血压波动,增加了手术麻醉的风险。而右美托咪定配伍组合全身麻醉中可起到协同镇静镇痛作用,节俭全身麻醉药物的用量。且有研究表明右美托咪定可减少七氟烷的用量达17%[9]。同时,七氟醚吸入复合0.4 μg·kg-1·h-1右美托咪定可以显著降低患者BIS值,增强麻醉深度,减少术中知晓发生率[10]。
另一方面,全身麻醉苏醒期拔管时,由于气管插管、吸痰等刺激气道引起呛咳反射,Kim等[11]发现苏醒期呛咳发生率为76%,对于苏醒期管理也是最常见的问题。而右美托咪定是一种新型的 α2高选择性肾上腺素能受体激动剂,具有明显的抗交感神经兴奋作用,发挥增强围术期心血管稳定性,具有镇静、镇痛且无呼吸抑制作用。其可减少脑血流、不增加颅内压、改善麻醉恢复过程,是一种值得推广的神经外科麻醉辅助药[12]。在以前的麻醉方案中,瑞芬太尼具有超短时效,镇痛作用强的优点;缺点是作用消失快,疼痛发生早,疼痛刺激和苏醒迅速带来的不适感可引起烦躁,甚至心脑血管系统意外。七氟醚优点具有术中血流动力学较平稳,肌肉松弛药用量小,术后苏醒快而彻底。缺点是恢复期躁动发生率较高。本试验研究的结果中也显示,瑞芬太尼组的血压骤升幅度远远高于右美托咪定组的波动范围,这一危害显而易见。术毕追加小剂量的舒芬太尼,并没有达到完全理想的治疗效果。
右美托咪定主要兴奋脑干蓝斑核内α2A受体产生镇静作用,兴奋脊髓内α2C 受体则产生镇痛作用。其镇静特点不同于其他镇静药物:右美托咪定可使患者产生类似自然睡眠状态,并可随时被唤醒且合作良好。在产生镇静镇痛的同时,右美托咪定几乎不影响患者呼吸[16]。在本次试验的苏醒期神经查体过程中,手术患者即表现了良好的指令配合,完成了检查目的。所观察的病例中没有发生呼吸抑制的不良事件发生。本研究中,右美托咪定的持续输注时间在1.5~2.5 h范围内,该组患者拔管时间长于瑞芬太尼组,与右美托咪定的药代动力学特点有关。
综上所诉,我们认为盐酸右美托咪定用于颅内动脉瘤介入手术患者全麻维持期间的血流动力学稳定,维持了良好的脑组织灌注能力。盐酸右美托咪定在全麻苏醒期血流动力学稳定,镇静评分满意,躁动评分降低。减少了随着麻醉作用减弱出现的剧烈应激反应。
1 熊源长,王恒跃,林福清,等.瑞芬太尼复合丙泊酚持续泵注在颅内动脉瘤 GDC 栓塞术的应用.第二军医大学学报,2006,27:808-809.
2 徐莉,郭浪涛.异丙酚预防七氟烷全麻后躁动的临床研究.现代临床医学,2011,37:104-110.
3 Skopets AA,Lomivorotov VV,Karakhalis NB,et al.Oxygen-transporting function of the blood circulation system in sevoflurane anesthesia during myocardial revasculariza-tion under extracorporeal circulation.AnesteziolRean-imatol,2009,41:713-715.
4 丁晶晶,徐秋美,陈秋萍,等.国产右美托咪啶用于高血压患者全麻气管拔管临床研究.南通大学学报,2010,30:263-265.
5 MA D,Hossain M,Rajakumaraswamyn N,et al.Dexme-detomidine produces its neuroprotective effect via the alpha2A-adrenoceptor subtype.Eur J Pharmacol,2004,502:87-97.
6 Yagmurdur H,Ozcan N,Dokumaci F,et al.Dexmedetomi-dine reduces the ischemia-reperfusion injury markers during upper extremity surgery with tourniquet.J HandSurg Am,2008,33:941-947.
7 Urban MK,Wukovits B,Flynn E.Dexmedetomidineversuspropofol for sedation of ventilated spinalpatients.Anesthesiology,2004,101:A 158.
8 中华医学会麻醉学分会.右美托咪定临床应用指导意见.中华医学杂志,2013,93:2775-2777.
9 Fragen RJ,Fitzgerald PC.Effect of dexmedetomidine on the minimum alveolar concentration(MAC) of sevoflurane in adults age 55 to 70 years.J ClinAnesth,1999,11:466-470.
10 周涛.右旋美托咪呢对七氟醚复合瑞芬太尼麻醉期间麻醉深度的影响.中国实用医,2014,9:15-16.
11 Kim ES,Bishop MJ.Cough during emergence from isoflurane anaesthesia.I AnesthAnalg,1998,87:117-241.
12 李征,邵贵骞,于宏志,等.右美托咪定在颅内动脉瘤栓塞术中的应用.实用医学杂志,2012,28:290-292.
13 Sun S,Huang SQ.Effects of pretreatment with a small dose ofdexmedetomidineon sufentanil-induced cough during anestheticinduction.J Anesth,2013,27:25-28.
14 Lee W,Shin JD,Choe K,et al.Comparison of dexmedetomidine andketamine for the analgesic effect using intravenous patient-controlledanalgesia after gynecological abdominal surgery.Korean J Anesthesiol,2013,65:132-134.
15 Nie Y,Liu Y,Luo Q,et al.Effect of dexmedetomidine combined withsufentanil for post-caesarean section intravenous analgesia:arandomised,placebo-controlled study.Eur J Anaesthesiol,2014,31:197-203.
16 姚月勤.右美托嘧啶预防谵妄的研究进展及机制.中国当代医药,2009,16:5.
10.3969/j.issn.1002-7386.2017.24.010
项目来源:河北省医学科学研究重点课题计划(编号:20160693)
050031 石家庄市,河北医科大学第一医院(史记、张娜娜、周长浩);河北医科大学第二医院(刘雅)
周长浩,050031 石家庄市,河北医科大学第一医院;E-mail:1558986296@qq.com
R 651.122
A
1002-7386(2017)24-3719-04
2017-06-10)
