毛黄堇药材的质量标准研究Δ
2017-12-13吴佳胡娟娟张德伟重庆市食品药品检验检测研究院重庆401121重庆医药高等专科学校中药学院重庆4011重庆万州食品药品检验所重庆404000
吴佳,胡娟娟,张德伟(1.重庆市食品药品检验检测研究院,重庆401121;2.重庆医药高等专科学校中药学院,重庆 4011;.重庆万州食品药品检验所,重庆 404000)
毛黄堇药材的质量标准研究Δ
吴佳1*,胡娟娟2#,张德伟3(1.重庆市食品药品检验检测研究院,重庆401121;2.重庆医药高等专科学校中药学院,重庆 401331;3.重庆万州食品药品检验所,重庆 404000)
目的:建立毛黄堇药材的质量标准。方法:从原植物形态、性状特征、显微特征、薄层色谱(TLC)方面对药材进行定性鉴别;检测药材水分、总灰分和水浸出物的含量;采用高效液相色谱法测定药材中脱氢卡维丁的含量:色谱柱为Agilent C18,流动相为乙腈-磷酸盐缓冲液(含20 mmol/L磷酸二氢钾、10 mmol/L二乙胺、0.1%磷酸)(28∶72,V/V),流速为1.0 mL/min,检测波长为347 nm,柱温为35℃,进样量为10µL。结果:原植物为多年生草本,药材常皱缩成团,被毛,主根圆锥形,根茎和根部有明显的干裂,叶卷曲而多碎落,花呈黄白色;花粉粒类圆形,可见方晶和柱晶,非腺毛众多,可见具缘纹孔、螺纹及网纹导管,亦可见木纤维。药材样品TLC图斑点清晰,分离度好。水分为7.5%~18.5%,总灰分为20.5%~26.2%,水浸出物为29.9%~46.4%。脱氢卡维丁检测进样量线性范围为0.040 08~2.404 8 μg(r=0.999 9),精密度、稳定性、重复性试验的RSD<2.0%;加样回收率为95.6%~102.5%(RSD=2.3%,n=9)。结论:该研究所建标准可用于毛黄堇药材质量标准评价。
毛黄堇;质量标准;薄层色谱法;高效液相色谱法;脱氢卡维丁
毛黄堇Corydalis tomentella Franch.系罂粟科紫堇属植物,产于湖北西部、四川东部至南部、重庆和陕西南部,又名干岩矸(重庆),其全草皆可入药,为民间贵重中草药,具有抗菌、消炎、镇痛和镇静作用,主治疮痈肿毒、肝炎、肝硬化、肝癌等症[1-3],作为地方民族用药用途广泛,疗效显著。随着重庆市药物种植研究所对毛黄堇药材人工驯化研究的初步成功,毛黄堇药材的系统研究需求也愈加迫切。目前,国内外尚未见有关该药材活性和成分的相关报道。本试验对毛黄堇药材进行原植物形态性状特征、显微特征、薄层色谱(TLC)定性鉴别,拟定药材水分、总灰分和水浸出物限度,通过高效液相色谱法(HPLC)建立其活性成分脱氢卡维丁含量测定方法[4-9],以期为建立毛黄堇药材的质量标准提供依据。
1 材料
1.1 仪器
1260型HPLC仪,包括四元泵、自动进样器、柱温箱、二极管阵列检测器,Agilent 1260工作站(美国Agilent公司);BP221S、MSA225S-100-DU型电子分析天平(德国Sartorius公司);KQ-500B型超声波清洗器(昆山市超声仪器有限公司)。
1.2 试剂
脱氢卡维丁对照品(中国食品药品检定研究院,批号:111667-200401,纯度:100%);硅胶G薄层板(青岛海洋化工厂);乙腈为色谱纯,二乙胺、甲醇、盐酸、磷酸二氢钾、磷酸为分析纯,水为纯化水。
1.3 药材
试验用10批毛黄堇药材样品(S1~S10)由重庆市药物种植研究所采集(采集地:重庆市南川区金佛山)提供并确认基源,由重庆市药物种植研究所蒋万浪副主任中药师鉴定为真品。
2 方法与结果
2.1 原植物形态与性状鉴别
2.1.1 原植物形态 本品为多年生草本,全体密被白色毛茸;主根肉质,圆锥形,灰黄色;茎1~3 mm,直立或倾斜;叶基生,具长柄;叶片轮廓狭三角形,二回羽状复叶,一回裂片11~13枚,具短柄;二回裂片9~11枚;末回裂片宽倒卵形,先端钝圆或再2~3深裂。总状花序顶生,疏生花10余朵;苞片短小,卵状披针形;花冠金黄色,无毛,外轮上瓣先端具浅凹,距圆筒形,长约占全瓣长的2/3,末端略下弯[4]。原植物形态见图1。

图1 原植物形态Fig 1 Original plant morphology
2.1.2 药材性状 与原植物相比较,毛黄堇药材全草常皱缩成团,被毛;主根圆锥形,表面棕黄色至棕褐色,有明显的皱纹及须根痕,质硬而脆,断面黄绿色至绿棕色;根茎和根部有明显的干裂,呈片层结构;叶柄多成束卷曲,绿灰色,干硬、脆而易碎;叶卷曲而多碎落,呈现灰绿色;花呈黄白色;气微臭,味酸苦。药材性状见图2。

图2 药材性状Fig 2 Medicinal materials properties
2.2 显微鉴别
取药材样品适量,粉碎,粉末因各组织部位的比例不同,呈现的颜色也稍有差别,介于深绿色至棕色之间,花粉粒类圆形,具3个萌发孔;可见方晶和柱晶;非腺毛众多,多碎断,顶端钝圆;可见具缘纹孔、螺纹及网纹导管,亦可见木纤维。显微特征见图3。

图3 药材粉末显微特征图Fig 3 Microscopic characteristics of medicinal materials powder
2.3TLC鉴别
取药材样品粉末(过2号筛)0.25 g,加1%盐酸甲醇溶液50 mL,超声(功率:250 W,频率:40 kHz,下同)处理30 min,滤过,取续滤液作为供试品溶液。另取脱氢卡维丁对照品,加甲醇制成脱氢卡维丁质量浓度为0.5 mg/mL的对照品溶液。按TLC法[2015年版《中国药典》[10](四部)]试验,吸取上述2种溶液各2 μL,分别点于同一硅胶G薄层板上,以环己烷-乙酸乙酯-异丙醇-甲醇-水-三乙胺(3∶3.5∶1∶1.5∶0.5∶1,V/V/V/V/V/V)为展开剂,置于氨蒸气饱和的展开缸内,展开,取出,晾干,置紫外光灯(365 nm)下检视。结果,供试品色谱中,在与对照品色谱相应位置上显相同颜色的斑点,详见图4。
2.4 水分测定
取10批药材样品粉末(过2号筛)适量,精密称定,按照2015年版《中国药典》(一部)“附录ⅨH水分测定法”的第一法(烘干法)[10]测定药材样品水分,每批平行测定3份,详见表1。结果表明,药材样品水分为7.5%~18.5%,平均值为12.5%。初步拟定毛黄堇药材水分不得过15.0%。
2.5 总灰分测定

图4 薄层色谱图Fig 4 TLC chromatograms
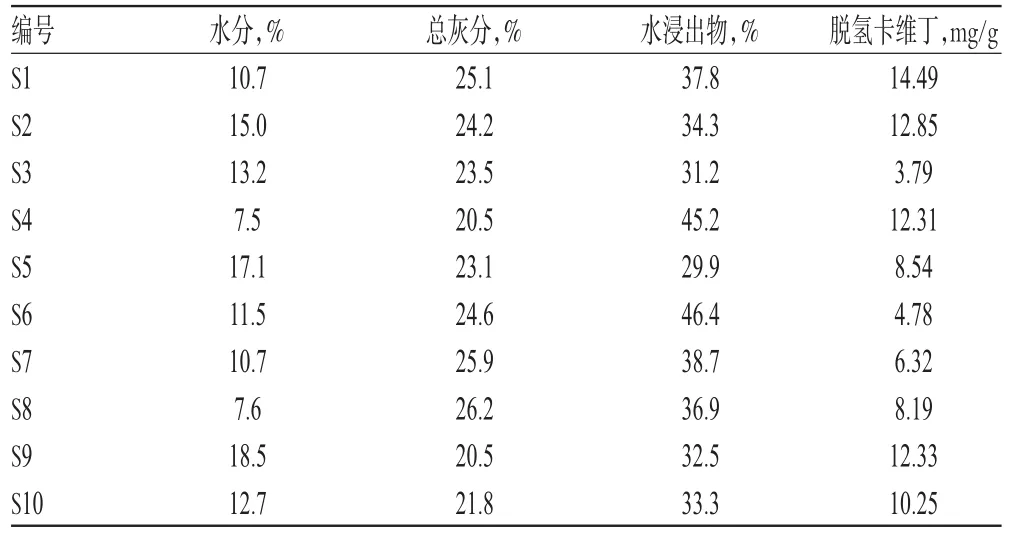
表1 水分、总灰分、水浸出物和脱氢卡维丁含量测定结果(n=3)Tab 1 Results of determination of moisture,total ash,water-soluble extract and dehydrocavidine(n=3)
取10批药材样品粉末(过2号筛)适量,精密称定,按照2015年《中国药典》(一部)“附录ⅨK灰分测定法[10]”测定药材样品总灰分。每批平行测定3份,详见表1。结果表明,药材样品总灰分为20.5%~26.2%(过2号筛),平均值为23.5%。初步拟定毛黄堇药材总灰分不得过26.0%。
2.6 水浸出物
取10批药材样品粉末(过2号筛)适量,精密称定,按照2015年版《中国药典》(一部)“附录ⅩA浸出物测定法[10]”测定药材样品浸出物。每批平行测定3份,详见表1。结果表明,药材样品水浸出物为29.9%~46.4%,平均值为36.6%。初步拟定毛黄堇药材水浸出物不得少于30.0%。
2.7 含量测定
2.7.1 色谱条件 色谱柱:Agilent C18(250 mm×4.6 mm,5 μm);流动相:乙腈-磷酸盐缓冲液(含20 mmol/L磷酸二氢钾、10 mmol/L二乙胺、0.1%磷酸)(28∶72,V/V);流速:1.0 mL/min;检测波长:347 nm;柱温:35 ℃;进样量:10 μL。在上述色谱条件下,理论板数以脱氢卡维丁峰计>4 000;脱氢卡维丁基线分离良好,分离度>1.5,详见图5。

图5 高效液相色谱图Fig 5 HPLC chromatograms
2.7.2 对照品溶液的制备 精密称取五氧化二磷中减压干燥至恒质量的脱氢卡维丁对照品适量,加1%盐酸甲醇溶液制成脱氢卡维丁质量浓度为0.200 4 mg/mL的对照品溶液。
2.7.3 供试品溶液的制备 取药材样品粉末(过2号筛)约0.2 g,精密称定,置于具塞锥形瓶中,加1%盐酸甲醇溶液50 mL,称定质量,超声处理30 min,放置室温,用甲醇补足减失的质量,摇匀,经0.45 μm微孔滤膜滤过,取续滤液,即得。
2.7.4 线性关系考察 分别精密量取“2.7.2”项下对照品溶液0.2、0.5、1、2、4、8、12 µL,按“2.7.1”项下色谱条件进样测定,记录峰面积。以脱氢卡维丁进样量(x,μg)为横坐标、峰面积(y)为纵坐标进行线性回归,得脱氢卡维丁回归方程y=2 833.6 x+99.236(r=0.999 9)。结果表明,脱氢卡维丁检测进样量线性范围为0.040 08~2.404 8 μg。
2.7.5 精密度试验 取“2.7.2”项下对照品溶液适量,按“2.7.1”项下色谱条件连续进样测定6次,记录峰面积。结果,脱氢卡维丁峰面积的RSD=0.3%(n=6),表明仪器精密度良好。
2.7.6 稳定性试验 取“2.7.3”项下供试品溶液(编号:S2)适量,分别于室温下放置0、2、4、8、12 h时按“2.1”项下色谱条件进样测定,记录峰面积。结果,脱氢卡维丁峰面积的RSD=0.9%(n=5),表明供试品溶液室温放置12 h内基本稳定。
2.7.7 重复性试验 精密称取药材样品(编号:S2)适量,按“2.7.3”项下方法制备供试品溶液,共6份,再按“2.7.1”项下色谱条件进样测定,记录峰面积。结果,脱氢卡维丁峰面积的RSD=1.8%(n=6),表明本方法重复性良好。
2.7.8 加样回收率试验 取已知含量药材样品(编号:S2)适量,共9份,分别加入低、中、高质量的脱氢卡维丁对照品,按“2.7.3”项下方法制备供试品溶液,再按“2.7.1”项下色谱条件进样测定,记录峰面积并计算加样回收率,结果见表2。
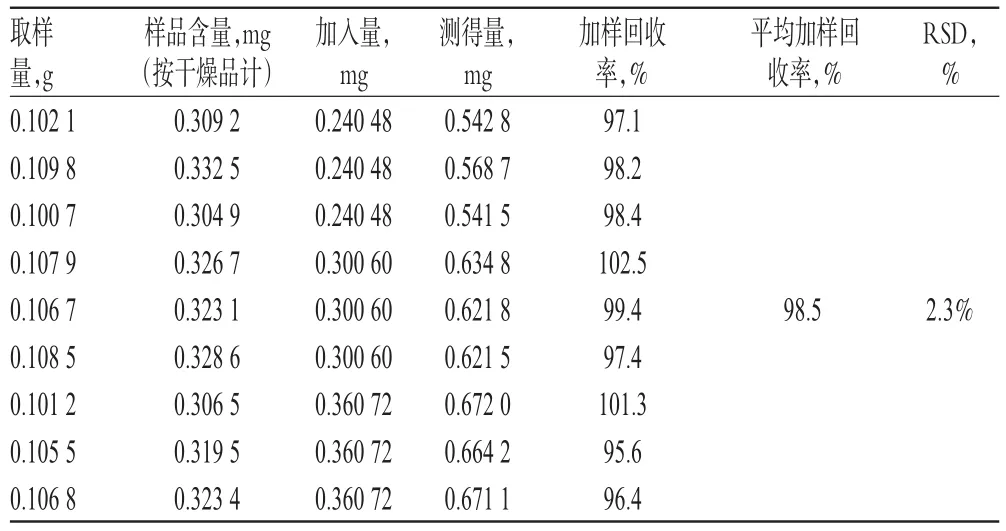
表2 加样回收率试验结果(n=9)Tab 2 Results of recovery tests(n=9)
2.7.9 样品含量测定 取10批药材样品各适量,分别按“2.7.3”项下方法制备供试品溶液,再按“2.7.1”项下色谱条件进样测定,记录峰面积并计算样品含量,结果见表1。
3 讨论
毛黄堇原为野生,近年重庆市药物种植研究所对毛黄堇人工驯化研究已初步成功(在性状上考察了野生品与家种品异同,结果两者性状均一致)。笔者对多批药材样品进行TLC检测,结果均检出脱氢卡维丁对照品相应的色谱斑点。结果表明,本研究TLC条件合理,方法可行,专属性强。因本药材样品为全草类药材,各部位占比不同,造成水分、总灰分及水浸出物含量差异较大;故在制定限度时,范围稍有放宽。
本试验含量测定供试品溶液的制备项下,笔者对提取溶剂类型、提取溶剂体积及提取时间均进行考察,结果用50 mL 1%盐酸甲醇溶液提取30 min药材样品即可提取完全,且杂质较少。笔者分别以乙腈-0.05 mol/L磷酸二氢钾溶液(28∶72,V/V)和乙腈-磷酸盐缓冲液(含20 mmol/L磷酸二氢钾、10 mmol/L二乙胺、0.1%磷酸)(28∶72,V/V)为流动相所得的供试品色谱峰分离度均能达到要求;其中,正文收载的流动相所得到的色谱峰形相对较好。笔者对脱氢卡维丁进行全波长扫描,发现有2个较大的紫外吸收峰,最强吸收峰在274 nm,次强吸收峰在347 nm;但采用274 nm作为检测波长时,杂质干扰较多,故最终选用347 nm作为检测波长。
综上所述,本研究所建标准可用于毛黄堇药材质量标准评价。
[1]国家药典委员会.中华人民共和国药典:一部[S].2015年版.北京:中国医药科技出版社,2015:303.
[2]南京中医药大学.中药大辞典:上册[M].2版.上海:上海科学技术出版社,2006:105.
[3]中国科学院四川分院中医中药研究所.四川中药志:第1册[M].1982年版.成都:四川人民出版社,1982:52.
[4]叶勇,黄秋洁,刘华钢.高效液相色谱法测定不同来源岩黄连中不同部位脱氢卡维丁含量[J].医药导报,2015,34(1):99-101.
[5]吴杨,陆兔林,季德,等.岩黄连中生物碱的分离和结构鉴定[J].南京中医药大学学报,2015,31(1):81-83.
[6]叶勇,黄秋洁,刘华钢.超滤法测定脱氢卡维丁的血浆蛋白结合率[J].中国医院药学杂志,2015,35(1):12-15.
[7]龚志强,谢丽莎,黄茂春.HPLC测定广西4个产地野生岩黄连药材中脱氢卡维丁的含量[J].中国医药指南,2013,11(3):480-481.
[8]胡芳,陆兔林,毛春芹,等.HPLC测定岩黄连生物总碱中脱氢卡维丁、盐酸巴马汀和盐酸小檗碱[J].中国实验方剂学杂志,2011,17(7):68-71.
[9]程华,熊斌,丁碧军,等.RP-HPLC法测定岩黄连注射液中脱氢卡维丁的含量[J].中国药房,2008,19(33):2601-2602.
[10]国家药典委员会.中华人民共和国药典:四部[S].2015年版.北京:中国医药科技出版社,2015:57、103、202、204.
Study on Quality Standard of Corydalis tomentella
WU Jia1,HU Juanjuan2,ZHANG Dewei3(1.Chongqing Institute for Food and Drug Control,Chongqing 401121,China;2.TCM College,Chongqing Medical and Pharmaceutical College,Chongqing 401331,China;3.Wanzhou Institute for Food and Drug Control,Chongqing 404000,China)
OBJECTIVE:To establish the quality standard of Corydalis tomentella.METHODS:The medicinal material was identified in respects of property,microscopic characteristics and TLC.The contents of moisture,total ash and water soluble extract were determined.The content of dehydrocavidine was determined by HPLC.The determination was performed on Agilent C18column with mobile phase consisted of acetonitrile-phosphate buffer solution(containing 20 mmol/L monopotassium phosphate,10 mmol/L diethylamine,0.1%phosphoric acid)(28∶72,V/V)at the flow rate of 1.0 mL/min.The detection wavelength was set at 347 nm,and the column temperature was 35℃.The sample size was 10µL.RESULTS:The original plant is perennial herbs.The medicinal material often shrank into a ball.The main root was in conical shape;the rhizomes and roots were distinctly chapped;leaves curled and broken,and flowers were yellowish-white.The pollen grains were round-like in shape;square and columnar crystals were found;there were a large number of nonglandular hairs.The bordered pit,threaded and reticulate catheter were found;wood fiber was also found.TLC spots were clear and well-separated.The content of moisture were 7.5%-18.5%,total ash were 20.5%-26.2%,and extract were 29.9%-46.4%.The linear range of dehydrocavidine were 0.040 08-2.404 8 μg(r=0.999 9);RSDs of precision,stability and reproducibility tests were lower than 2.0%.The recoveries were 95.6%-102.5%(RSD=2.3%,n=9).CONCLUSIONS:The established standard can be used for quality evaluation of C.tomentella.
Corydalis tomentella;Quality standard;TLC;HPLC;Dehydrocavidine
R927
A
1001-0408(2017)33-4695-04
DOI 10.6039/j.issn.1001-0408.2017.33.24
国家科技重大专项课题(No.2014ZX09304307)
*主管中药师。研究方向:中药质量检验及标准起草、化学成分分析。E-mail:37358772@qq.com
#通信作者:讲师。研究方向:中药化学成分分析。E-mail:4651520@qq.com
(编辑:张 静)
2017-05-09
2017-07-03)
