微乳液中四氯化硅水解制备二氧化硅微球*
2017-12-11徐华,陈强
徐 华,陈 强
(常州大学材料科学与工程学院,江苏常州213100)
微乳液中四氯化硅水解制备二氧化硅微球*
徐 华,陈 强
(常州大学材料科学与工程学院,江苏常州213100)
利用阳离子表面活性剂十六烷基三甲基溴化铵(CTAB)和非离子表面活性剂聚乙二醇辛基苯基醚(TritonX-100)配制微乳体系,并利用工业生产单晶硅副产物四氯化硅制备粒径分别为45 nm和60~120 nm的二氧化硅微球。探讨了加水量、氨水浓度、四氯化硅用量、搅拌转速、反应温度对微球粒径及表面形貌的影响。研究表明,在CTAB乳液体系中,微球粒径随含水量的增加而减小,随通入四氯化硅气体量的增加而增大,且只有在碱性条件下才能得到硅球;在TritonX-100乳液体系中,微球粒径随含水量的增加呈现先减小后增大的趋势,随四氯化硅液体加入量的影响较小,碱性越高颗粒成球度越好、分散性能越好。微乳液反应过程不宜搅拌,且反应温度不易高于四氯化硅沸点。
四氯化硅;油包水微乳液;单分散;纳米二氧化硅
改良西门子法制备多晶硅,第一步将气相氯化氢与冶金级硅粉反应制备三氯氢硅,第二步在高温条件下用高纯氢气还原三氯氢硅,两步反应都有副产物四氯化硅生成。科学工作者对副产物四氯化硅进行了综合利用研究。赵云等[1]采用四氯化硅液相鼓泡的方式制备白炭黑。张向京等[2-3]采用四氯化硅水解法制备纳米二氧化硅粉体。微乳法是近年来制备纳米微粒的新方法。王玉琨等[4]利用正硅酸乙酯(TEOS)水解,在油包水(W/O)型 TritonX-100/正辛醇/环己烷/氨水微乳液中获得粒径为40~50 nm的单分散球形 SiO2。 陈小泉等[5]亦在 H2O(HNO3)/Span80-Tween60/环己烷酸微乳液体系中催化水解TEOS,得到粒度在110~550 nm的单分散酸性超细SiO2。但是利用四氯化硅作为硅源制备纳米二氧化硅微球还未见报道。笔者利用工业生产单晶硅副产物SiCl4制备粒径在100 nm以下的二氧化硅粒子。在前人研究基础上,采用最佳配制微乳液方法(所以对形成微乳最佳条件对颗粒的影响不作过多叙述),主要探讨加水量、氨水浓度、SiCl4用量、搅拌转速、反应温度等外部条件对颗粒粒径及形貌的影响。
1 实验部分
1.1 反应原理
反相微乳液是一种在表面活性剂和少量表面活性剂助剂作用下形成的以油相为连续相水为分散相的W/O乳液。将SiCl4加入微乳液中反应得到SiO2及HCl,HCl与加入的氨水反应生成氯化铵挥发除去。
在阳离子表面活性剂体系CTAB/正丁醇/环己烷/NH3·H2O中制备SiO2颗粒,由于SiCl4活性非常大,会在乳液体系中因反应过于剧烈而得不到理想的硅球,因此采用鼓泡的方式将四氯化硅以气态形式通入乳液中制备硅球,使得反应温和。在非离子表面活性剂 TritonX-100/正己醇/环己烷/NH3·H2O 中制备SiO2颗粒,由于水核被紧密束缚于表面活性剂分子的氧乙烯基上而阻止了水核间的物质交换,故气体SiCl4分子进入反胶束水核中较少不利于其水解和成核,所以该反应采用直接滴加液体四氯化硅的方式也不会发生很剧烈的反应。
1.2 主要原料及仪器
原料:无水乙醇、氨水(质量分数为25%)、正己醇、正丁醇、环己烷(C6H12)、十六烷基三甲基溴化铵(CTAB)、聚乙二醇辛基苯基醚(TritonX-100)均为分析纯,四氯化硅为工业级。仪器:D/MAX-2500 X射线衍射仪(XRD)、Vector22型傅里叶变换红外光谱仪(FT-IR)、ZEN3600型纳米激光粒度及zeta电位分析仪、JEM-100CXⅡ透射电镜(TEM)。
1.3 实验过程
1)在CTAB/正丁醇/环己烷/H2O微乳液中制备SiO2纳米颗粒。根据文献[6-7],称取 3.94 g CTAB加入环己烷中,再滴入7.3 mL表面活性剂助剂正丁醇,超声20 min,在磁力搅拌下缓慢滴入3 mL蒸馏水,得澄清蓝光透明乳液,加入2 mL氨水,继续搅拌1 h。将气态SiCl4通入乳液中,鼓泡后静置30 min使反应完全。加入乙醇破乳,采用无水乙醇超声离心洗涤,得产物。
2)在 TritonX-100/正己醇/环己烷/H2O 微乳液中制备SiO2纳米颗粒。根据文献配制0.3 mol/L的TritonX-100环己烷溶液40 mL,加入8.5 mL表面活性剂助剂正己醇,超声20 min,在磁力搅拌下缓慢滴入1.2 mL蒸馏水,得澄清蓝光透明乳液,加入2 mL氨水,继续搅拌1 h。缓慢滴入液体SiCl4,静置30 min使产物沉淀完全。加入乙醇破乳,采用无水乙醇超声离心洗涤,得产物。
2 结果与讨论
2.1 实验条件对产品粒径的影响
1)水含量的影响。SiO2粒子的形成是一个复杂的过程,可通过调节反相微乳液组成等参数,如:水与表面活性剂物质的量比(R)、氨水用量、原料用量,来调控SiO2尺寸和形貌及微观结构[8-10]。反相微乳液中结合水、捕获水和自由水是其中常存在的3种水,R为水与表面活性剂物质的量比,是表征乳液的首要结构参数。固定氨水用量为2 mL、通入SiCl4气体量为100 mL,在微乳液增溶水量范围内改变加水量分别为2、3、4、5 mL,考察水含量对产品粒径的影响,结果见图1a。由图1a看出,产品粒径随水含量增加而减小。一般来说,自由水的增加有利于水核数量的增加。随R增大,胶束尺寸、界面层的不稳定性在静电作用下使硅源水解成核数增多、粒子尺寸减小。在TritonX-100反胶团体系中,固定氨水用量为2 mL、滴入SiCl4液体量为0.8 mL,在微乳液增溶水量范围内改变加水量分别为 0.4、0.8、1.2、1.6 mL,考察水含量对产品粒径的影响,结果见图1b。由图1b看出,产品粒径随水含量增加先减小后增大,当加水量为1.2 mL时,产品粒径存在最小值45 nm。水含量较少时,体系中胶束所含有的自由水分子数较少,且低的水含量也会受到空间效应的限制,水核被胶束紧密包覆,表面活性剂尾链也阻止SiCl4分子进入胶束中参与反应,使胶团间的成核几率变得很低,只有进入胶束中的四氯化硅才能水解成核最终长成较大颗粒。相反,反胶团体系中水含量较高时,大部分水核处在自由良好的水环境中,有利于SiC4水解成核及核生长,由于水的存在颗粒间也有团聚现象。

图1 加水量和四氯化硅加入量对二氧化硅产品粒径的影响
2)四氯化硅加入量的影响。对于反相微乳法,增大SiCl4气体量将有利于大颗粒二氧化硅生成。固定加水量为3 mL、氨水用量为2 mL,改变通入SiCl4气体量分别为 20、60、100、140 mL,考察气体加入量对产品粒径的影响,结果见图1c。由图1c看出,在CTAB体系中,颗粒粒径随通入SiCl4气体量增加而增大。这是由于,当通入SiCl4气体量较少时,乳液中水核水解四氯化硅有限,所以成核较少及核生长较小;随着通入SiCl4气体量增加,碱性水核使得水解的硅酸根带负电在阳离子表面活性剂亲水端通过静电吸引使核生长。过量四氯化硅导致乳液呈酸性产生硅酸,得不到多余颗粒。在TritonX-100反胶团体系中,固定加水量为1.2 mL、氨水用量为2 mL,改变滴入 SiCl4液体量分别为 0.2、0.5、0.8、1.1 mL, 考察滴入SiCl4液体量对产品粒径的影响,结果见图1d。由图1d看出,随着四氯化硅用量增加,产品粒径变化不明显。这是因为,大部分水分子被束缚于表面活性剂分子中,很大程度上阻止了水核间物质交换传输,有效防止了粒子间团聚及核生长,而且该乳液中成核生长空间较小,也限制了颗粒粒径的长大。
2.2 实验条件对产品形貌规整度的影响
1)氨水用量的影响。用反相微乳液CTAB体系制备SiO2颗粒过程中,氨水不仅为SiCl4水解缩合反应提供了碱性环境,而且其本身也参与反应。在碱性环境中,SiCl4水解不再生成溶胶而是产生沉淀,副产盐酸和氨水作用生成氯化铵挥发除去。此外,硅酸单体间缩聚、脱水反应也需要碱性条件。不加氨水时将得不到SiO2颗粒,因为四氯化硅水解产生盐酸使乳液呈酸性,水解后硅酸溶解于水核中没有成核。氨水用量较少时,产品颗粒分散性和规整度均较差。图2a为加入2 mL及1 mL氨水所得产品TEM照片。由图2a看出,加入2 mL氨水时,产品呈球形,颗粒规整度高、单分散性好,分布范围为62~120 nm;氨水用量较少时,产品颗粒有团聚现象。用反胶团法TritonX-100乳液制备SiO2颗粒过程中,氨水对颗粒形貌有较大的影响。图2b为加入2 mL氨水及未加氨水制得产品TEM照片。由图2b看出,加入2mL氨水时,产品粒度分布规整、分散性良好、基本呈球形,平均粒径约为45 nm;未加入氨水时,硅球表面粗糙、球形度差,颗粒大部分团聚严重。TritonX-100乳液增溶水量很小,形成的水核呈现几十纳米,在狭小的反应空间中SiCl4易于成核,故在酸性条件下也能得到小球。氨水的加入,排除了反应产生的氯化氢气体,有利于硅原子和羟基之间缩合反应,使得成球性更好。

图2 氨水用量对二氧化硅产品形貌规整度的影响
2)搅拌转速的影响。在反相微乳液CTAB体系中,鼓入四氯化硅气体后,改变搅拌转速分别为0、300、600 r/min,搅拌时间为30 min。研究发现,随着搅拌转速增大硬团聚较为严重,乙醇破乳后大颗粒难以通过超声波重新分散。在反胶团法TritonX-100乳液中,滴入SiCl4反应后,经搅拌沉淀消失,乳液呈现蓝光,生成的纳米颗粒又重新分散到反胶团乳液中。随着搅拌转速增加,颗粒软团聚较为严重,即使用超声波分散开,停止后又会立即团聚。不管在CTAB乳液中还是在TritonX-100乳液中,搅拌使得乳液中水核间相互碰撞便有物质交换,而纳米粒子比表面积大、活性高,搅拌后团聚严重。所以四氯化硅气相水解不需要搅拌便可得到单分散性较好的纳米粒子。
3)乳液温度的影响。其他条件不变,将配制好的微乳密封,放入不同温度(20、50、80℃)的水浴中保温,然后进行反应对比。研究发现,在反相微乳液CTAB体系中,随着温度升高反应未有变化,当温度为80℃时瓶口pH试纸颜色变得更深,说明有更多未反应的SiCl4气体溢出。这是因为,CTAB乳液中水核较大、自由水较多,在温度高于SiCl4沸点情况下依然能与所接触的SiCl4剧烈反应生成粒子,但是由于温度过高还是有大量蒸汽接触不到反应水核而溢出。在反胶团法TritonX-100乳液中,在不同乳液温度下滴入SiCl4,温度升高反应变得剧烈,颗粒沉降加快,对产物形貌没有影响。这是因为,液体SiCl4浓度大,而且其气化过程相对缓慢,故反应速度相对于气化速率快很多。乳液温度对反应产物形貌规整度的影响不大,温度超过SiCl4沸点57.6℃时原料易挥发,反应在常温下就可以实现。
3 产品IR、XRD表征
图3为二氧化硅IR图。用TritonX-100乳液制备的二氧化硅(图3a),Si—O—Si键的弯曲振动峰在464 cm-1处;Si—O—Si对称伸缩振动峰在806 cm-1左右;Si—OH弯曲振动峰在943cm-1左右;1088cm-1附近强而宽的吸收带是Si—O—Si反对称伸缩振动峰;水的H—O—H弯曲伸缩振动峰在1 631 cm-1附近;3 427 cm-1左右为Si—OH键导致的反对称伸缩振动吸收峰。这些峰均为二氧化硅特征峰。用CTAB乳液制备的二氧化硅(图 3b),2929cm-1和 2854cm-1处出现的—CH3、—CH2—吸收峰主要是由SiO2微球中残留的CTAB所致,因为表面活性剂难以通过乙醇和水的洗涤而被完全除去[11]。
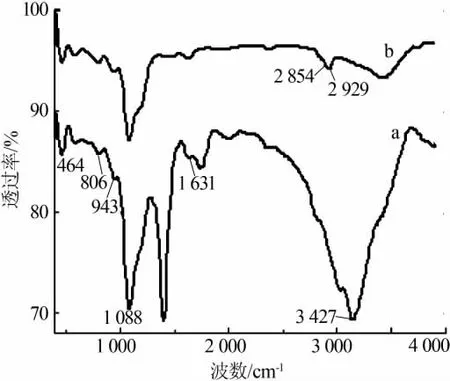
图3 二氧化硅纳米颗粒IR图
图4为二氧化硅XRD谱图。在TritonX-100乳液(图4a)及CTAB乳液(图4b)中制备的二氧化硅样品,在2θ为22~24°处都出现了相同的宽化衍射峰。此宽化衍射峰是非晶态的特征峰,表明通过四氯化硅水解制得的样品为无定形二氧化硅。

图4 二氧化硅纳米颗粒XRD谱图
4 结论
反相微乳液CTAB体系制备二氧化硅颗粒,在增溶水量范围内随着水含量增加,颗粒粒径减小;增加氨水浓度,硅球团聚少、规整度好;二氧化硅微球粒径与通入四氯化硅气体量成正相关关系。这也解决了王玲玲等[7]用TEOS在阳离子表面活性剂CTAB乳液中得不到二氧化硅球的难题。在TritonX-100乳液体系中,制得硅球的粒径很小、分散性很好,是制备纳米级材料理想的反应容器;其颗粒粒径随水含量增加先减小后增大,当加入水量为1.2 mL时,其粒径最小(45 nm);反胶团法在酸性条件下也能得到颗粒,但产物易团聚、规整度很差;氨水的加入使得颗粒的分散性及规整度提高;四氯化硅加入量对颗粒粒径的影响很小。微乳液法制备纳米颗粒过程中不宜搅拌,搅拌将导致纳米粒子间碰撞而易团聚;反应温度不宜高于四氯化硅沸点,因为温度过高易导致原料挥发而浪费。利用四氯化硅也能像正硅酸乙酯一样成功制备分散性较好的纳米硅球。
[1] 赵云,杨旭,但建明,等.四氯化硅液相鼓泡法制备纳米白炭黑工艺研究[J].无机盐工业,2014,46(8):28-32.
[2] 张向京,郝丛,靳悦淼,等.四氯化硅水解制纳米二氧化硅粉体工艺研究[J].无机盐工业,2013,45(10):20-22.
[3] 乔永志,马瑞平,张志昆,等.表面活性剂存在下四氯化硅水解制备二氧化硅[J].无机盐工业,2012,44(5):44-46.
[4] 王玉琨,钟浩波,吴金桥.微乳液法制备条件对纳米SiO2粒子形貌和粒径分布的影响[J].精细化工,2002,19(8):466-468.
[5] 陈小泉,古国榜.W/O微乳体系酸催化水解硅酸乙酯合成单分散酸性超微二氧化硅[J].现代化工,2002,22(3):26-30.
[6] 陈龙武,甘礼华,岳天仪,等.微乳液反应法制备α-Fe2O3超细粒子的研究[J].物理化学学报,1994,10(8):750-754.
[7] 王玲玲,方小龙,唐芳琼,等.单分散二氧化硅超细颗粒的制备[J].过程工程学报,2001,1(2):167-172.
[8] Zhang Q,Huang F,Li Y.Cadmium sulfide nanorods formed in microemulsions[J].Colloid.Surface.A,2005,257-258:497-501.
[9] Garti N,Holmberg K.Reactions in microheterogeneous media[J].Curr.Opin.Colloid In.,2003,8(2):135-136.
[10] Arriagada F J,Osseo-Asare K.Synthesis of nanosize silica in a nonionic water-in-oil microemulsion:Effects of the water/surfactant molar ratio and ammonia concentration[J].J.Colloid Interf.Sci.,1999,211(2):210-220.
[11] 陈和生,孙振亚,邵景昌.八种不同来源二氧化硅的红外光谱特征研究[J].硅酸盐通报,2011,30(4):934-938.
Preparation of silica microspheres by hydrolysis of silicon tetrachloride in microemulsion
Xu Hua,Chen Qiang
(School of Material Science and Engineering,Changzhou University,Changzhou 213100,China)
Microemulsion system was prepared through cationic surfactant cetyltrimethyl ammonium bromide and nonionic surfactant polyoxyethylene octyl phenyl ether(TritonX-100).Then silica microspheres with particle sizes of 45 nm and 60~90 nm were prepared respectively,by silicon tetrachloride,a by-product of industrial monocrystalline silicon production.The factors,such as the amount of water,ammonia concentration,SiCl4amount,stirring rate,and temperature affecting on the microsphere particle size and surface topography of silica were investigated.The results showed that the particle size decreased with the increase of water content in CTAB W/O microemulsion,increased with the amount of SiCl4gas,and only in the alkaline condition to get the silicon ball.In a TritonX-100 W/O microemulsion,the particle size decreased and then increased with increasing water content.The amount of SiCl4added had little effect on the particle size.The higher the basicity,the better the sphericity and dispersion properties.Microemulsion reaction process should not be stirred and the reaction temperature should not be higher than the boiling point of SiCl4.
silicon tetrachloride;W/O microemulsion monodisperse;nano sized silica
TQ127.2
A
1006-4990(2017)12-0029-04
2017-06-22
徐华(1992— ),男,硕士研究生,主要研究利用四氯化硅制备二氧化硅微球。
陈强,高级工程师。
联系方式:chem100@nju.edu.cn
