钙基脱硫剂固硫特性的试验研究
2017-12-11程乐鸣王勤辉方梦祥
蔡 毅,程乐鸣,王勤辉,方梦祥
(1.浙江浙能技术研究院有限公司,杭州 310013;2.浙江大学 能源清洁利用国家重点实验室,杭州 310027)
钙基脱硫剂固硫特性的试验研究
蔡 毅1,程乐鸣2,王勤辉2,方梦祥2
(1.浙江浙能技术研究院有限公司,杭州 310013;2.浙江大学 能源清洁利用国家重点实验室,杭州 310027)
利用热重分析法、微观结构表征法研究了2种钙基脱硫剂(石灰石Ⅰ,Ⅱ)固硫反应特性,揭示了钙基脱硫剂固硫反应机理,并通过等效粒子法模型分析了石灰石固硫反应动力学特性。研究结果表明:在800~900℃温度范围内,石灰石钙转化率随温度提高而增强;石灰石粒径越小,钙转化率越高。石灰石Ⅰ钙利用率对温度敏感,而石灰石Ⅱ对粒径敏感。石灰石煅烧后在晶粒表面形成的裂纹促进SO2的扩散,有利于固硫反应的进行。动力学计算结果表明,石灰石Ⅱ在扩散控制阶段有较高的有效扩散系数,最终钙利用率高于石灰石Ⅰ。
循环流化床;吸收剂;脱硫;动力学
0 引言
SO2(二氧化硫)是燃煤电站发电过程中产生的一种主要大气污染物。目前,我国燃煤发电机组正处于全面实现超低排放[1]的阶段,环境保护部在《燃煤电厂超低排放烟气治理工程技术规范(征求意见稿)》中建议:循环流化床锅炉SO2超低排放路线,可采用以炉内喷钙脱硫为基础,结合炉后湿法脱硫或烟气循环流化床脱硫的工艺。
钙基脱硫剂因含CaO和MgO等碱性物质[2-3],具有脱除酸性物质的基本能力,而被应用于循环流化床炉内脱硫。
目前研究的钙基脱硫剂主要以矿物岩类为主,分为石灰石、白云石以及磷酸岩。
石灰石在循环流化床炉内首先发生煅烧反应,煅烧后生成的CaO进一步与烟气中SO2反应[4-6]。其反应过程如下:
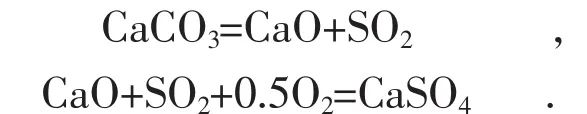
对于白云石,在脱硫反应过程中,首先发生缓慢煅烧:
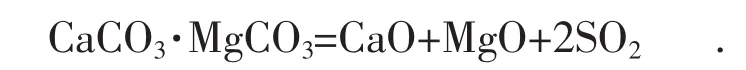
由于MgO在炉内高温条件下与SO2反应极慢,因此MgO可以被作为惰性物质,白云石中实际参与脱硫的仍然是CaO。
与白云石类似,磷酸岩中主要活性成分同样为CaCO3,其煅烧反应如下[7-9]:
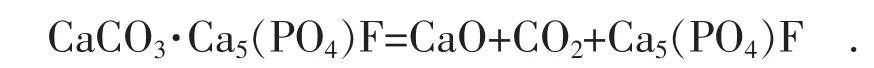
磷酸岩分解产生的CaO作为主要活性物质,与SO2反应生成CaSO4[10-12]。
由于不同钙基脱硫剂形成条件和自身物理微观性质不同,其脱硫效果仍存在显著差距。因此,选择经济、高效的钙基脱硫剂是优化循环流化床锅炉SO2超低排放工艺路线的重要基础。
以下选用2种石灰石脱硫剂,研究了循环流化床锅炉运行温度及粒径范围内,石灰石的微观特征、固硫特性以及反应动力学特性,揭示了石灰石脱硫反应机理,并为合理选择石灰石脱硫剂提供理论参考。
1 试验装置与方法
1.1 试验样品
试验选用2种石灰石,利用化学成分分析法对上述2种脱硫剂进行分析,结果如表1所示。
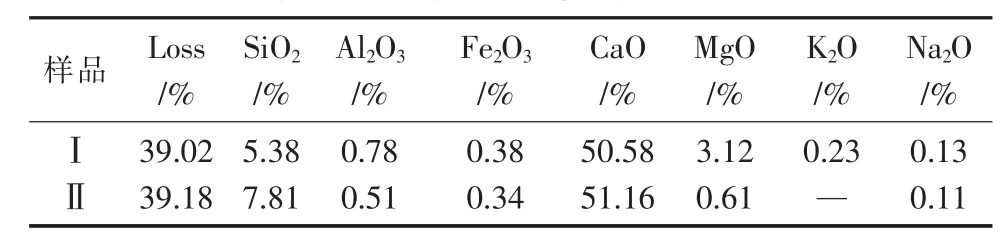
表1 脱硫剂化学成分分析
石灰石经研磨、干燥、筛分后,取所需粒径范围内颗粒作为试验物料,装于干燥瓶中备用。
1.2 试验方法
固硫试验在NETZSCH STA 449F3热重分析仪中进行,固硫温度分别为800℃,850℃和900℃,粒径范围选择为 0.1~0.3 mm,0.3~0.5 mm,0.5~0.7 mm。取5 mg样品置于热重分析仪中,在空气气氛中,连续升温使样品分解,待样品在反应温度下恒重后,通入模拟烟气(成分为5%O2+15%CO2+0.3%SO2,剩余平衡气为N2),为克服样品反应时存在的外扩散阻力,反应气体总流量控制为100 mL/min。
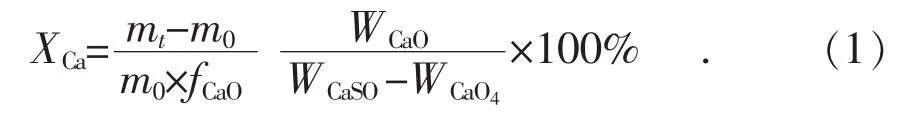
实验过程中记录不同时刻t时反应物重量,计算其最终钙转化率。钙转化率表示脱硫剂中吸收SO2的CaO占吸收剂中总CaO的比例:式中:XCa为钙利用率;mt为反应过程中t时刻样品质量;m0为初始时刻样品质量;fCaO为样品中CaO质量分数;和CaO的摩尔质量。
煅烧前后石灰石样品采用SEM(SIRON场发射扫描电镜)对其微观形貌进行测试。
2 结果与分析
2.1 反应温度对固硫特性影响
选取反应温度800℃,850℃和900℃,对粒径0.3~0.5 mm范围内2种石灰石固硫特性进行试验。其钙利用率与反应时间之间关系曲线如图1所示。
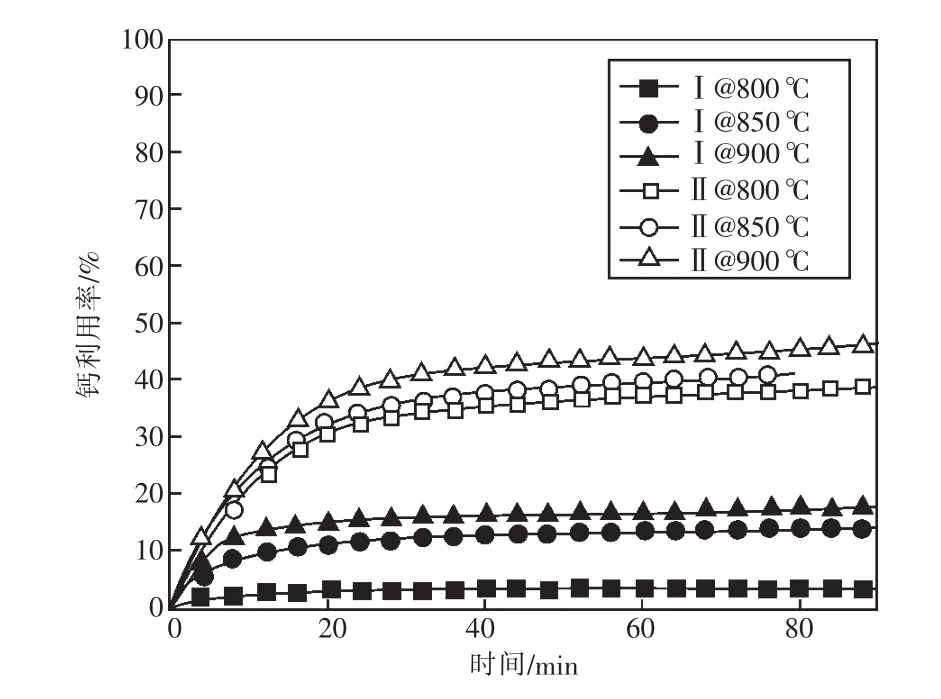
图1 石灰石固硫反应随温度变化特性曲线
由图1可知,对于所选的2种石灰石,在试验选取的温度范围内,随着反应时间增加,石灰石的钙利用率逐渐增加,但增加的程度逐渐降低,反应一段时间后,钙利用率基本不再变化。表明脱硫剂内部微孔随反应时间增加而逐渐堵塞,阻碍了SO2与CaO的进一步反应,降低了脱硫剂的反应程度。
如图1所示,不同反应温度条件下,石灰石Ⅱ的最终钙利用率均高于石灰石Ⅰ。石灰石Ⅱ相比于石灰石Ⅰ,从初始反应至最终反应所经历的时间较长,导致脱硫反应速率及最终钙利用率明显高于石灰石Ⅰ。
试验结果表明:对于同一种脱硫剂,反应温度较低时,脱硫剂与SO2之间化学反应速率慢,钙利用率较低。随着反应温度升高,脱硫反应速率逐渐提高,钙利用率相应增加。
对于选用的石灰石Ⅰ、石灰石Ⅱ,适当提高床温有利于促进炉内脱硫反应。脱硫反应过程中,石灰石Ⅰ比石灰石Ⅱ有更高的温度敏感性。反应温度提高,石灰石Ⅰ钙利用率提高幅度高于石灰石Ⅱ。
2.2 粒径对固硫特性影响
粒径是脱硫剂反应的另一个重要参数,反应温度850℃,选择粒径分别为0.1~0.3 mm,0.3~0.5 mm和0.5~0.7 mm的脱硫剂进行固硫实验,其结果如图2所示。
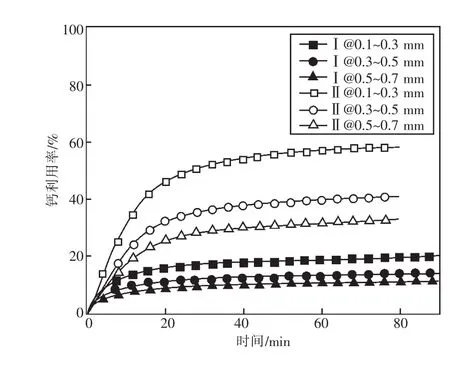
图2 石灰石固硫反应随粒径变化特性曲线
由图2可知,降低脱硫剂粒径,可提高石灰石钙利用率。颗粒粒径减小,一方面增加了反应颗粒的比表面积,促进脱硫剂与SO2化学反应;另一方面,由于脱硫产物CaSO4摩尔体积较大,会导致产物层外壳内孔隙堵塞,阻碍SO2与CaO进一步反应,该现象对大粒径颗粒影响明显,使颗粒中CaO不能完全被利用,而小粒径颗粒则可以相对减少未反应的CaO含量,总体提高脱硫剂钙利用率。
试验结果表明,石灰石Ⅱ比石灰石Ⅰ有更高的粒径敏感性。反应物粒径减小,石灰石Ⅱ钙利用率提高幅度高于石灰石Ⅰ。
2.3 固硫反应机理
石灰石固硫反应机理如图3所示,随着SO2扩散的形式改变,石灰石与SO2反应分为3个阶段:第一阶段,SO2扩散至石灰石颗粒表面;第二阶段,SO2在石灰石晶粒间扩散,反应在固体晶粒表面进行,此阶段称为化学反应控制阶段;第三阶段,随着SO2与CaO反应进行,在晶粒表层形成产物层,产物层将固体表面与反应气体分隔,此时反应通过气体在内部孔之间扩散或固体离子扩散方式继续进行,此阶段为产物层扩散控制阶段。
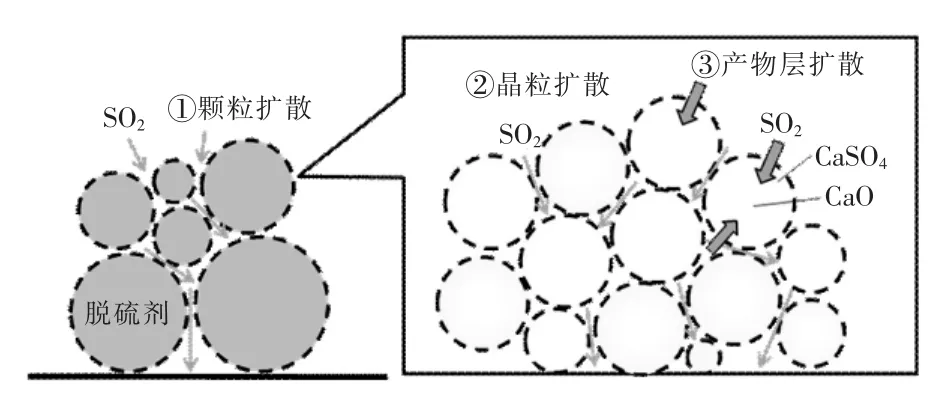
图3 石灰石固硫反应机理
对2种石灰石在850℃条件下煅烧前后样品进行表面微观特征分析。由图4可知,煅烧前2种石灰石表面形态结构主要由多面体晶粒堆积组成,晶粒与晶粒之间存在圆形通孔。

图4 石灰石煅烧前后微观特征
煅烧之后,脱硫剂晶粒形态、大小变得不规则,并且在晶粒表面均出现明显的裂痕。由此可见煅烧后,由于热应力和CO2内部释放,造成的裂痕改变了脱硫剂的表面微观特性,增加了脱硫剂孔隙数量,并使孔隙间连通特性得到增强。当SO2扩散至石灰石晶粒表面,强化了固硫反应。
2.4 固硫反应动力学分析
对于钙基脱硫剂,可采用等效粒子法对石灰石固硫反应动力学进行分析。
等效粒子法提出,气固反应发生在反应物与产物之间的界面上[13-15]。随着时间改变,产物层厚度相应发生变化。对于脱硫反应,反应初期,粒子的产物层薄,反应通过化学反应因素控制;随着反应的进行,产物层厚度增加,扩散阻力增大。该模型可表述为:
表面化学反应控制阶段

产物层扩散控制阶段

其中:
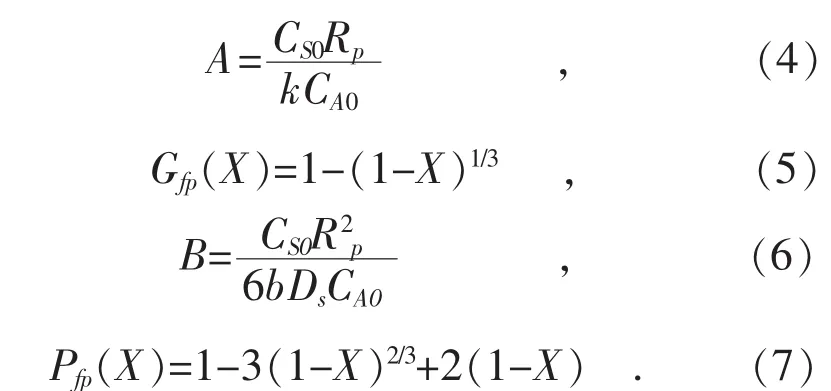
表面反应速率常数k和有效扩散系数Ds可通过Arrhenius方程表述为:

式中: A1和 B1为时间校正因子; Gfp(X)和 Pfp(X)分别为表面化学反应控制阶段、扩散反应控制阶段转化率函数;CS0为固硫剂中CaO浓度;Rp为颗粒半径;b为反应计量系数;CA0为SO2浓度;k为表面反应速率常数;Ds为有效扩散系数;Ea为表面化学反应活化能;Rg为气体普适常量;T为反应温度;k0和D0为对应的指前因子;Ep为扩散反应活化能。
通过最小二乘法进行线性拟合,其拟合结果如图5所示。依据拟合结果可知,各阶段的转化率均与时间t呈良好的线性关系。
依据等效粒子法分别计算2种石灰石脱硫剂在不同反应温度下表面反应速率常数k和有效扩散系数Ds,其结果如表2所示。
由表2可知,虽然石灰石Ⅱ在反应初期,化学反应控制阶段的表面反应速率常数k略有降低,但在扩散控制阶段的有效扩散系数Ds显著高于石灰石Ⅰ。因此,当固硫反应处于扩散控制阶段时,石灰石Ⅱ具有较好的固硫特性,最终钙利用率更高。
3 结论
(1)对于选用的2种石灰石,提高反应温度和降低石灰石粒径,石灰石钙利用率均会相应提高,石灰石Ⅰ温度敏感性高,而石灰石Ⅱ粒径敏感性高。
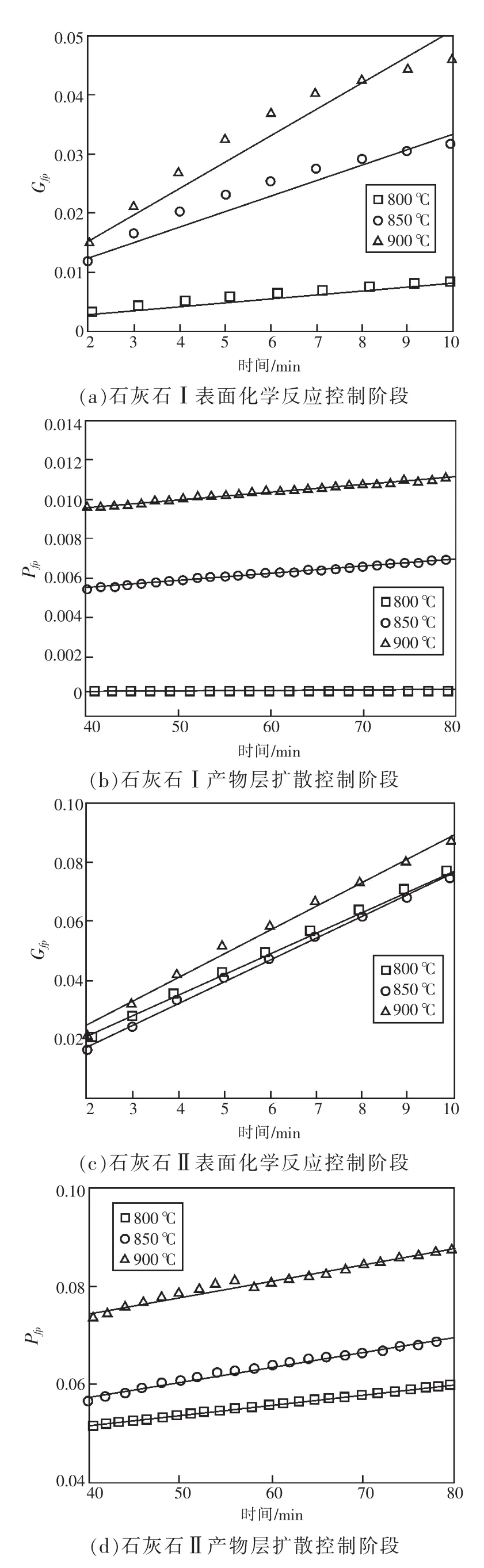
图5 石灰石各反应阶段拟合
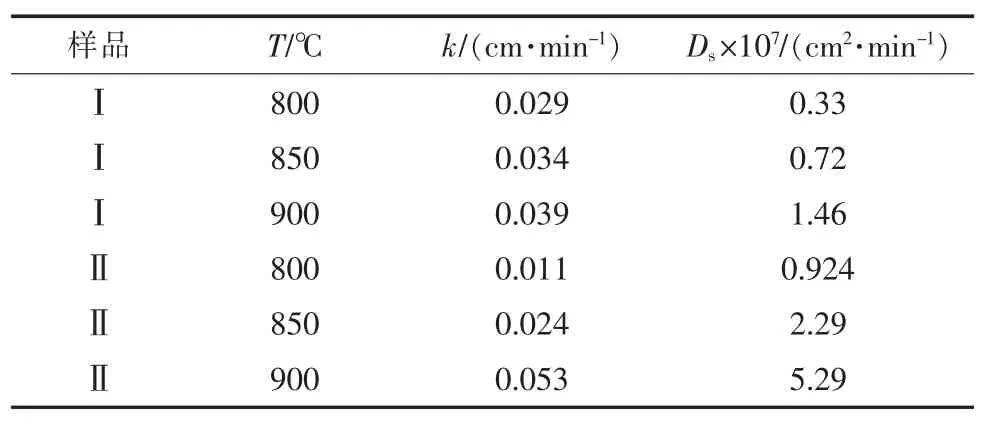
表2 不同反应温度下k与Ds计算值
(2)通过对脱硫剂微观特性分析可知,煅烧后的石灰石产物呈疏松多孔状,晶粒间存在明显裂缝,促进了石灰石固硫反应的进一步发生。
(3)动力学计算结果表明,在扩散控制阶段,因石灰石Ⅱ有较高的有效扩散系数,石灰石Ⅱ最终钙利用率明显高于石灰石Ⅰ。
[1]张军,郑成航,张涌新,等.某1 000 MW燃煤机组超低排放电厂烟气污染物排放测试及其特性分析[J].中国电机工程学报,2016(5)∶1310-1314.
[2]MURA G,LALLAI A,OLLA P.On the kinetics of dry desulfurization with calcium oxide[J].The Chemical Engineering Journal,1991,46(3)∶119-128.
[3]ADÁNEZ J,LABIANO F G,ABÁNADES J C,et al.Methods for characterization of sorbents used in fluidized bed boilers[J].Fuel,1994,73(3)∶355-362.
[4]ERSOY MERIÇBOYU A,KÜÇÜKBAYRAK S,YAMAN S.Sulphation capacities of natural Turkish limestones and dolomites[J].Environmental Technology,1993,14(8)∶787-794.
[5]FAN L,SATIJA S,WILSON W I,et al.Thermogravimetric analysis of sulfation kinetics of calcined limestones or dolomites[J].The Chemical Engineering Journal,1984,28(3)∶151-162.
[6]DE DIEGO L F,DE LAS OBRAS-LOSCERTALES M,GARCIA-LABIANO F,et al.Characterization of a limestone in a batch fluidized bed reactor for sulfur retention under oxy-fuel operating conditions[J].International Journal of Greenhouse Gas Control,2011,5(5)∶1190-1198.
[7]CHAN R K,MURTHI K S,HARRISON D.Reaction of sulfur dioxide with calcined limestones and dolomites[J].Environmental Scienceamp;Technology,1971,5(9)∶776-781.
[8]REID W T.BASIC FACTORS in the Capture of Sulfur Dioxide by Limestone and Dolomite[J].Journal of Engineering for Gas Turbines and Power,1970,92(1)∶11-15.
[9]SCALA F,SALATINO P.Dolomite attrition during fluidized-bed calcination and sulfation[J].Combustion Science and Technology,2003,175(12)∶2201-2216.
[10]ÖZER A K,GÜLABO■IU M S,BAYRAKÇEKEN S,et al.Flue gas desulfurization with phosphate rock in a fluidized bed[J].Fuel,2002,81(1)∶41-49.
[11]ÖZER A K,GÜLABO■IU M S,BAYRAKCEKEN S.Physical Structure and Chemical and Mineralogical Composition of the Mazidag1(Turkey) Phosphate Rock[J].Industrialamp;Engineering Chemistry Research,2000,39(3)∶679-683.
[12]ÖZER A K,GÜLABO■IU M S,BAYRAKCEKEN S,et al.Changes in physical structure and chemical composition of phosphate rock during calcination in fluidized and fixed beds[J].Advanced Powder Technology,2006,17(5)∶481-494.
[13]HAN K,LU C,CHENG S,et al.Effect of characteristics of calcium-based sorbents on the sulfation kinetics[J].Fuel,2005,84(14-15)∶1933-1939.
[14]LI Y,QI H,YOU C,et al.Kinetic model of CaO/fly ash sorbent for flue gas desulphurization at moderate temperatures[J].Fuel,2007,86(5-6)∶785-792.
[15]KARATEPE N,ERDOGAN N,ERSOY-MERICBOYU A,et al.Preparation of diatomite/Ca(OH)2sorbents and modelling their sulphation reaction[J].Chemical Engineering Science,2004,59(18)∶3883-3889.
2017-09-22
蔡 毅(1989),男,工程师,从事煤炭清洁利用及污染物控制研究。
(本文编辑:徐 晗)
Experimental Study on of Desulfurization Characteristics of Calcium-based Sorbents
CAI Yi1, CHENG Leming2, WANG Qinhui2, FANG Mengxiang2
(1.Zhejiang Energy Group Ramp;D CO.,Ltd.,Hangzhou 310013,China 2.State Key Laboratory of Clean Energy Utilization of Zhejiang University, Hangzhou 310027, China)
The desulfurization characteristics of two calcium-based sorbents(limestoneⅠandⅡ)were investigated by thermogravimetry and microstructure characterization technique to reveal the reaction mechanism of desulfurization.The equivalent particle approach model was used to analyze the reaction kinetics.The results show that the calcium utilization increases with the temperature increase in a temperature range of 800~900℃,and increases with the particle diameter decreases.The limestoneⅠ is sensitive to the temperature while limestoneⅡ is sensitive to particle diameter.After calcinations of limestone,the cracks on the grains increase the SO2diffusion,which is conducive to the desulfurization process.The kinetic analysis shows that the large effective diffusivity in the diffusion controlled stage contributes to the higher calcium utilization for limestoneⅡ,which is superior to limestone I in calcium utilization.
circulating fluidized bed; sorbent; desulfurization; kinetics
10.19585/j.zjdl.201711013
1007-1881(2017)11-0073-05
X701.3
B
