美罗培南延长输注时间治疗老年人医院获得性肺炎的临床研究
2017-12-02张勇,丁荣,张景
张 勇, 丁 荣, 张 景
美罗培南延长输注时间治疗老年人医院获得性肺炎的临床研究
张 勇, 丁 荣, 张 景
目的比较美罗培南常规输注(30 min)和延长输注时间(3 h)两种给药方法治疗老年人医院获得性肺炎(HAP)的临床疗效和安全性,观察肾清除率增加(ARC)对临床疗效的影响。方法采用开放性随机对照临床单盲研究。选择2015年9月-2016年8月住院的需要使用美罗培南治疗的老年HAP患者40例。随机分为对照组、研究组各20例。对照组给药方案为美罗培南1 g加入0.9% NaCl 溶液100 mL中,使用静脉输液泵匀速维持30 min,每8小时给药1次;研究组给药方案为美罗培南1 g加入0.9% NaCl 溶液100 mL中,使用输液泵匀速维持3 h,每8小时给药1次。两组至少用药7 d。比较两组患者的临床疗效和药物不良反应。进一步将40例患者中肌酐清除率(Ccr)≥130 (mL/min)/1.73 m2的患者列为A1组,其余患者列为A2组。将对照组和研究组中Ccr≥130 (mL/min)/1.73 m2的患者分别列为B1组和B2组。单独比较A1组和A2组,B1组和B2组的临床疗效。结果与对照组比较,研究组临床治愈率和28 d生存率明显升高[临床治愈率:70.00%(14/20)比50.00%(10/20);28 d生存率:85.00%(17/20)比65.00%(13/20),P均<0.05],临床肺部感染评分(CPIS)、降钙素原(PCT)明显改善[CPIS降低值(分):(2.88±2.51)比(1.25±1.67);PCT降低值(μg/ L):(2.43±0.68)比(1.05±0.27),P均<0.05],而美罗培南治疗天数、住院时间无明显差异(P > 0.05)。两组患者的主要不良反应为血清丙氨酸转氨酶升高及腹泻,不良反应发生率无明显差异(P>0.05)。进一步分析,与A2组比较,A1组临床治愈率,28 d生存率明显降低[临床治愈率:44.44%(4/9)比64.52%(20/31);28 d生存率:66.67%(6/9)比77.42%(24/31),P均<0.05],CPIS评分及PCT下降值亦有明显差异[CPIS降低值(分):1.62±1.61比2.19±2.2;PCT降低值(μg/L):(1.41±0.39)比(1.84±0.5),P均<0.05],而美罗培南治疗天数、住院时间无明显差异。与B1组比较,B2组的临床治愈率、28 d生存率明显提高(临床治愈率:3/5比1/4;28 d生存率:4/5比2/4,P均<0.05),CPIS评分、PCT值明显改善[CPIS降低值(分):(2.56±2.29)比(0.68±0.93);PCT降低值(μg/L):(2.21±0.63)比(0.61±0.15),P 均<0.05],美罗培南治疗天数、住院时间无明显差异(P>0.05)。结论与30 min常规输注给药方法相比,延长美罗培南输注时间至3 h可以提高老年HAP患者的临床疗效,不良反应未增加。ARC导致患者临床疗效下降,通过延长美罗培南输注时间可提高ARC患者的临床疗效。
美罗培南; 延长输注时间给药; 医院获得性肺炎; 肾清除率增加
医院获得性肺炎(HAP)是我国第1位的医院感染,发病率达1.3%~3.5%,在各部位感染构成比中约占1/3[1]。老年人(年龄≥65岁)由于年龄或伴有基础疾病其HAP的发病率更是高达15%。老年人HAP往往病情发展迅速,并发症多、死亡率高、预后差,需要及时有效的治疗。而治疗的关键在于选择有效、安全的抗菌药物。
美罗培南是碳青霉烯类抗生素的代表药物,对临床上常见的需氧菌和厌氧菌均有较强的抗菌活性,对产酶(包括ESBL和AmpC酶)的细菌亦有强大的抗菌活性,是HAP特别是初始治疗无效的HAP的适宜选择。但随着细菌耐药现象不断加重,美罗培南治疗细菌感染的疗效也逐年下降。因此,如何通过优化给药方法提高美罗培南的疗效,成了目前临床上的一大课题。本研究通过延长美罗培南输注时间来观察其对老年人HAP的有效性和安全性,同时观察肾脏清除率增加(ARC)对临床疗效的影响。
1 材料与方法
本研究为开放性随机对照临床单盲研究,经过泰州市第四人民医院伦理委员会批准。
1.1 研究对象
选择2015年9月-2016年8月,因HAP入住我科应用美罗培南治疗的患者40例。入选病例均符合2016年美国感染病协会(IDSA)指南HAP的诊断标准[2],具体标准如下:①体温上升,> 38℃;②咳嗽、咯脓痰或呼吸道吸出脓性分泌物,可有肺部啰音、叩浊等体征;③咳嗽、咯痰,白细胞计数增高,血氧分压降低;④X线胸片新出现的或进展性肺浸润影,可伴有空洞;⑤起病于住院72 h、术后24 h、机械通气48 h后或拔除气管插管48 h之内(VAP)。④、⑤ + ①~③中的2项可确诊。
1.2 方法
1.2.1分组及给药方案 40例患者按照计算机抽选随机纳入对照组和研究组,每组20例,除给予化痰、对症支持等常规治疗外;①对照组采用传统输注方式给药,美罗培南1 g加入0.9% NaCl 溶液100 mL中,使用静脉输液泵匀速泵入,维持30 min,每8小时给药1次;②研究组采用延长输注方式给药,美罗培南 1 g 加入0.9% NaCl 溶液100 mL中,使用静脉输液泵匀速维持3 h,每8小时给药1次。两组至少用药7 d。③亚组:将40例患者中肌酐清除率(Ccr)≥130 (mL/min)/1.73 m2的患者纳入A1组,其余患者纳入A2组;将对照组中Ccr≥130 (mL/min)/1.73 m2的患者纳入B1组,研究组中Ccr≥130 (mL/min)/1.73 m2的患者纳入B2组。
1.2.2观察指标及临床疗效评价 ①主要评价指标为临床疗效和28 d生存率。②次要评价指标包括用药疗程、住院时间、临床肺部感染评分(CPIS)、血清降钙素原(PCT)等。其中临床疗效依据2015年国家食品药品监督管理局(CFDA)颁布的《抗菌药物临床试验技术指导原则》[3]进行评价,临床疗效分为临床治愈及临床无效,评价时间点在抗菌药物疗程结束后7~14 d。
1.2.3不良反应评价 在治疗期间随时监察药物不良反应的发生,按不良反应/事件分析的5条标准将关联性评价分为肯定有关、很可能有关、可能有关、可疑有关、不可能有关5级。肯定有关、很可能有关、可能有关记为不良反应。
1.2.4数据分析及处理 采用SPSS17.0软件统计分析数据,计量资料用均数±标准差(±s)表示,采用t检验,计数资料用χ2检验;以P<0.05为差异有统计学意义。
2 结果
2.1 基线资料比较
①对照组、研究组:两组患者性别比例、年龄、基础疾病、治疗前的器官衰竭数、CPIS评分、PCT值及Ccr、Ccr≥130 mL/(min·1.73 m2)患者的比例等指标差异均无统计学意义(P>0.05)。大部分患者(70%~75%)使用美罗培南之前均应用其他抗菌药物,分别为第三、第四代头孢菌素,哌拉西林-他唑巴坦或喹诺酮类药物,两组间比较差异无统计学意义(P>0.05)。40例患者中检出病原菌8株,阳性率20%,分别为肺炎克雷伯菌3株、铜绿假单胞菌2株、大肠埃希菌1株、阴沟肠杆菌1株、鲍曼不动杆菌1株。药敏结果显示大多对美罗培南敏感,1株鲍曼不动杆菌中介。②亚组:分析A1、A2、B1、B2组基线资料,发现A1与A2组比较,年龄、Ccr差异明显(P <0.05),性别比例、CPIS评分、PCT值以及采用传统和延长输注方式给药患者比例无明显差异(P > 0.05)。B1与B2组比较,各项指标均无明显差异(P>0.05)。见表1~3。
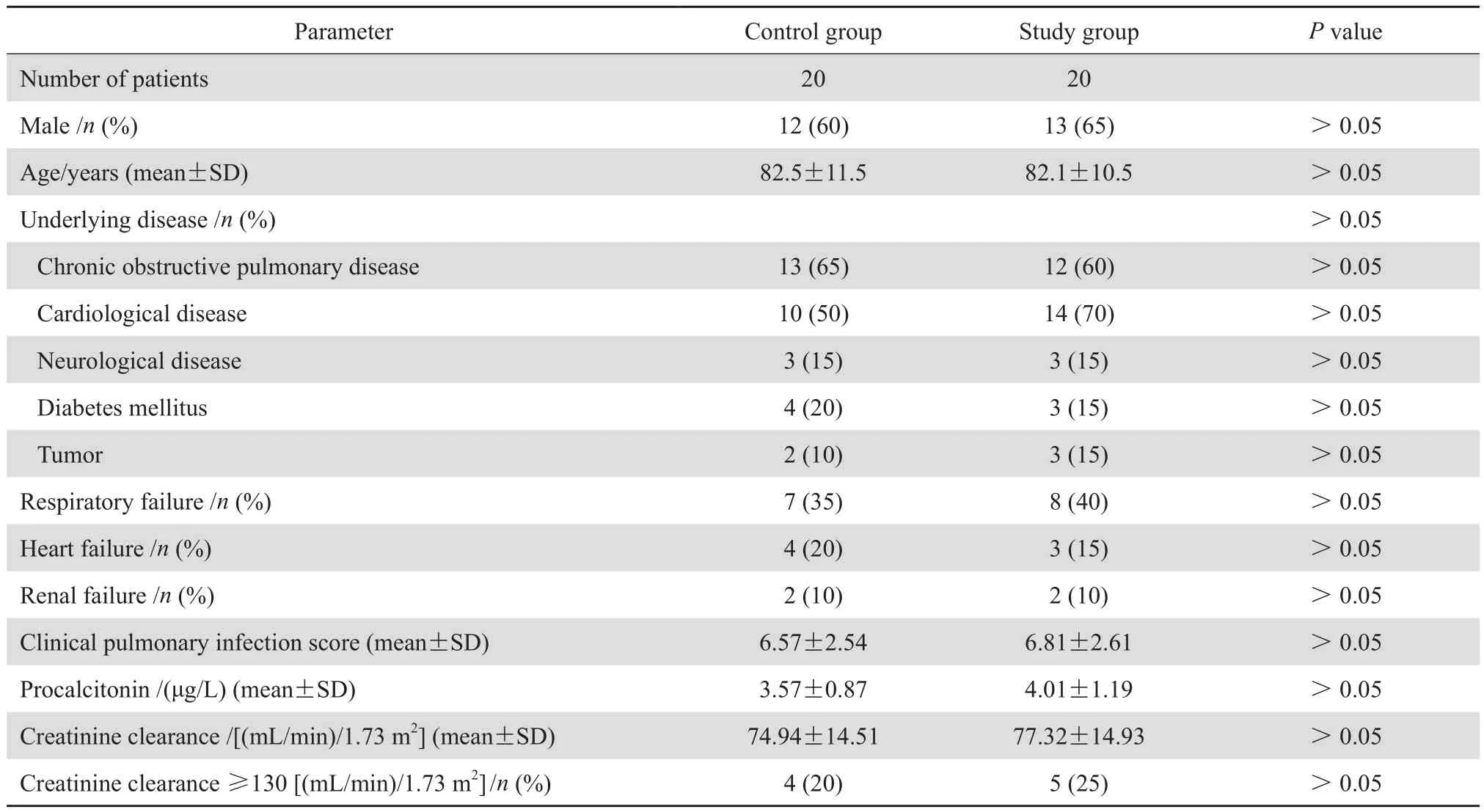
表1 两组患者基线资料比较Table 1 Baseline clinical data of the patients in study and control groups
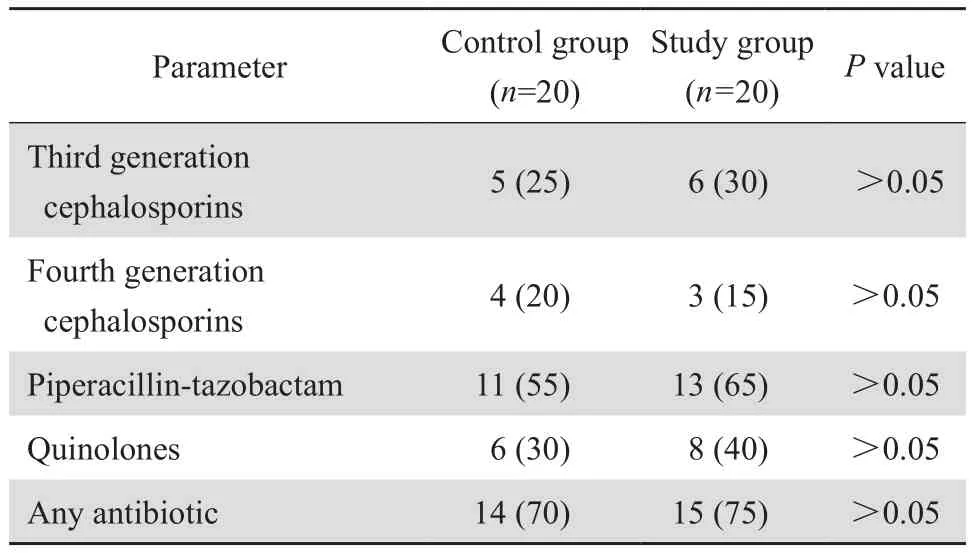
表2 对照组、研究组患者使用美罗培南之前应用抗菌药物情况比较Table 2 Prior antibiotic use before meropenem treatment[n(%)]
2.2 临床疗效比较
研究组临床治愈率70.00%(14/20),28 d生存率85.00%(17/20),对照组临床治愈率50.00%(10/20),28 d生存率65.00%(13/20)。研究组临床治愈率、28d生存率明显高于对照组(P <0.05),治疗后CPIS评分、PCT下降值亦明显高于对照组(P<0.05)。两组患者美罗培南治疗天数、住院时间无明显差异(P>0.05),见表4。经治疗,8株检出的细菌中,3株肺炎克雷伯菌、1株大肠埃希菌、1株阴沟肠杆菌均完全清除,2株铜绿假单胞菌清除1株,1株鲍曼不动杆菌未清除。
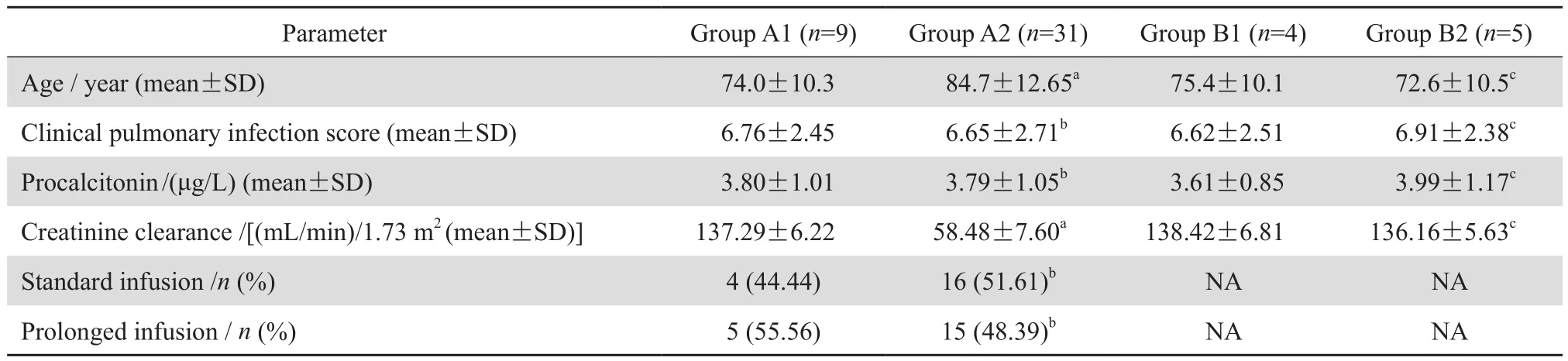
表3 亚组患者的基线资料比较Table 3 Baseline clinical data in the subgroups
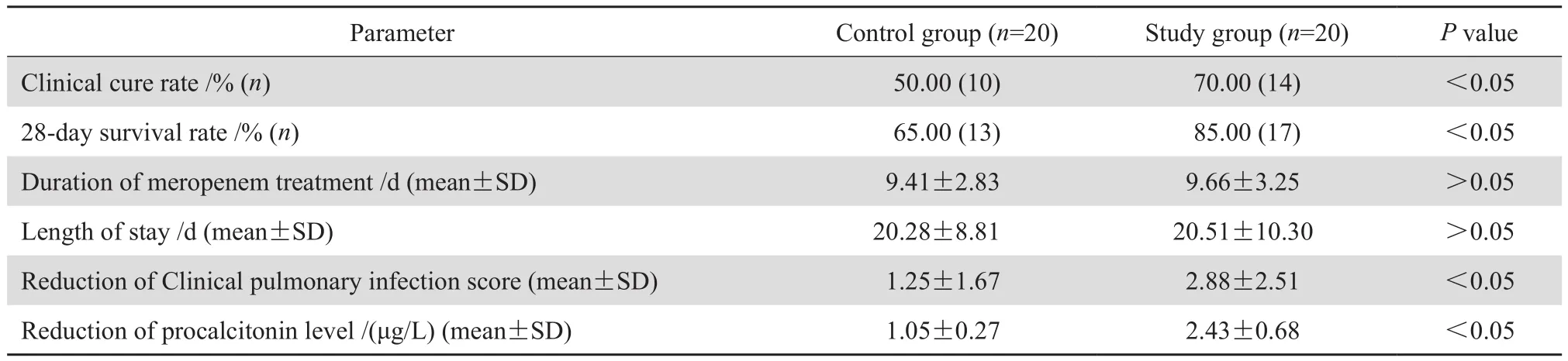
表4 对照组、研究组患者临床疗效比较Table 4 Clinical efficacy compared between study group and control group
进一步进行亚组分析,A1组临床治愈率4/9,28 d生存率6/9,A2组临床治愈率64.52%(20/31),28 d生存率77.41%(24/31)。A1组临床治愈率、28 d生存率明显低于A2组(P <0.05),治疗后CPIS评分、PCT下降值亦明显低于A2组(P<0.05),美罗培南治疗天数、住院时间无明显差异(P>0.05)。B1组临床治愈率1/4,28 d生存率2/4,B2组临床治愈率3/5,28 d生存率4/5。B2组临床治愈率、28 d生存率明显高于B1组(P<0.05),治疗后CPIS评分、PCT下降值亦明显高于B1组(P<0.05),美罗培南治疗天数、住院时间无明显差异(P>0.05)。见表5。
2.3 不良反应
两组均按照肯定有关、很可能有关、可能有关、可疑有关、不可能有关进行分层。两组患者主要不良反应为血清丙氨酸转氨酶升高、腹泻,两组间不良反应发生率无明显差异(P>0.05),经保肝、调节肠道菌群等处理后症状改善,均未停止使用美罗培南。见表6。
3 讨论
HAP尤其是老年人HAP病原菌以革兰阴性菌为主。中国医院感染的抗菌药物耐药性监测计划(CARES)显示,铜绿假单胞菌、大肠埃希菌和肺炎克雷伯菌等革兰阴性杆菌是导致HAP感染最常见的病原菌[4],入住ICU患者鲍曼不动杆菌感染比例增加。因此初始经验治疗必须覆盖革兰阴性杆菌。

表5 亚组患者临床疗效比较Table 5 Clinical efficacy compared between subgroups
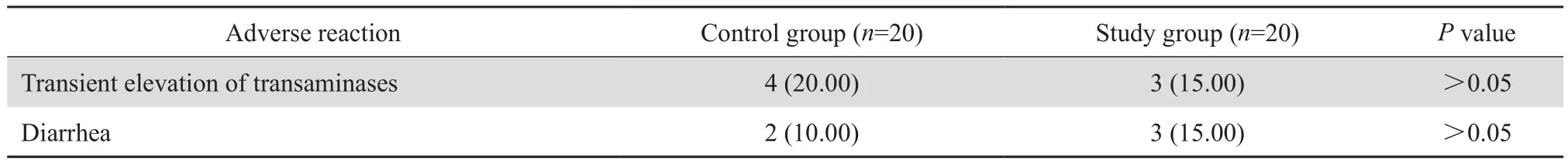
表6 对照组、研究组患者不良反应比较Table 6 Incidence of adverse reactions compared between study group and control group[n(%)]
对老年人HAP来说,不恰当的初始治疗是病死率增加和住院时间延长的主要因素[6]。在患者HAP诊断明确后,进一步判断患者的病情严重程度和细菌耐药的风险。对病情严重,细菌耐药风险高的患者,直接使用美罗培南治疗。对其他患者,根据情况选择第三、第四代头孢菌素或哌拉西林-他唑巴坦等药物治疗。72 h后判断疗效,如疗效不佳,则改为美罗培南治疗。本研究中两组患者中70%~75%为后来升级为美罗培南治疗。
美罗培南为时间依赖性抗菌药物,半衰期较短,常以给药间隔内血药浓度超过致病菌最低抑菌浓度(MIC)的持续时间(T>MIC)作为药动学(PK)/药效学(PD)参数。T>MIC为20%时对敏感菌有抑菌效应,T>MIC为40%时可对敏感菌表现出最大杀菌效应[6]。随着细菌耐药现象的不断加重,由于美罗培南常规剂量不足、常规30 min输注时间不够等原因,常常难以使T>MIC超过40%,而延长美罗培南输注时间能够更好地延长T>MIC时间,提高临床疗效。Jaruratanasirikul等[7]通过对接受美罗培南治疗呼吸机相关性肺炎(VAP)患者的PK/PD进行研究,发现美罗培南1 g每8小时1次,每次静脉输注30 min的T>MIC在MIC为l6、8、4和l mg/ L 时分别占给药间隔的28.33%、45.89%、57.00%和74.67%,而每次静脉输注3 h则数据分别为37.78%、58.1l%、72.67%和93.56%。本研究结果表明,将美罗培南输注时间从30 min延长至3 h,可以提高老年人HAP的临床疗效,改善预后。
ARC[8]是近年提出的一个新概念,指危重症患者肾小球滤过率(Ccr)增加,对循环溶质的清除能力增强,通常定义为Ccr≥130(mL/ min) /1.73 m2[9]。ARC常见于重症但血肌酐正常的患者,一般年龄较轻(<55岁)。ARC的发生率不同研究之间报道不一,最低为28%[10],最高为57.7%[11]。本研究中ARC的发生率为22.5%(9/40),明显低于既往文献报道,可能与入选患者年龄大(≥65岁)有关。多项研究表明,ARC显著降低抗菌药物血药浓度和疗效。Claus等[12]前瞻性研究表明,在128例ICU患者中,51.6%患者存在ARC,其治疗失败率显著高于非ARC患者,分别为27.3%和12.9%,P=0.04。对于ARC患者,通过合理增加给药剂量,延长输注时间可提高抗菌药物PK/PD达标率,改善预后。对亚组进行分析后发现:①基线资料。A1组较A2组年龄轻,但病情相近。②临床疗效。分析A1组与A2组疗效,可以发现ARC导致患者临床疗效下降。两组患者虽采用了两种不同给药方式,但使用比例无明显差异,疗效具有可比性;分析B1组与B2组疗效,可以发现,将美罗培南输注时间从30 min延长至3 h,可以提高ARC患者的临床疗效。
观察药物的不良反应可以发现,两组的主要不良反应为血清丙氨酸转氨酶升高及腹泻,发生率差异无统计学意义。提示延长输注时间给药并不增加不良反应的发生率。
综上所述,对老年人HAP来说,将美罗培南输注时间从30 min延长至3 h给药方法可以提高患者的临床疗效,同时不增加不良反应的发生率。ARC导致患者的临床疗效下降,通过延长美罗培南输注时间可提高ARC患者的临床疗效。但本研究是单中心临床研究,入组病例少,尤其是ARC病例少,故尚需多中心、多样本的随机对照研究。
[1]何礼贤. 重症医院获得性肺炎的经验性抗菌治疗策略[J]. 内科急危重症杂志,2001,7(1):4-5.
[2]KALIL AC,METERSKY ML,KLOMPAS M,et al.Executive Summary: Management of adults with hospitalacquired and ventilator-associated pneumonia: 2016 Clinical Practice Guidelines by the Infectious Diseases Society of America and the American Thoracic Society [J]. Clin Infect Dis,2016,63(5):757-582.
[3]国家食品药品监督管理局. 抗菌药物临床试验技术指导原则 [EB/OL]. [2015-04-03]. http://www. sda. gov. cn/WS01/CL1616/117281. html.
[4] 汪复,朱德妹,胡付品,等. 2009年中国CHINET细菌耐药性监测[J]. 中国感染与化疗杂志,2010,10(4):325-334.
[5]PARKER CM,KUTSOGIANNIS J,MUSCEDERE J,et al.Ventilator-associated pneumonia caused by multidrug-resistant organisms or Pseudomonas aeruginosa:prevalence,incidence,risk factors,and outcomes[J]. J Crit Care,2008,23(1):18-26.
[6] DRUSANO GL. Prevention of resistance:a goal for dose selection for antimicrobial agents[J]. Clin Infect Dis,2003,36(Suppl 1):s42-s50.
[7]JARURATANASIRIKUL S,SRIWIRIYAJAN S,PUNYO J.Comparison of the pharmacodynamics of meropenem in patients with ventilator associated pneumonia following administration by 3-hour infusion or bolus injection[J]. Antimicrob Agents Chemother,2005,49(4):1337-1339.
[8]UDY AA,ROBERTS JA,BOOTS RJ,et al. Augmented renal clearance: implications for antibacterial dosing in the critically ill[J]. Clin Pharmacorinet,2010,49(1):1-16.
[9]UDY AA,PUTT MT,BOOTS RJ,et al. ARC-augmentedrenalclearance[J]. Curr Pharm Biotechnol,2011,12(12):2020-2029.
[10]CAMPASSI ML,GONZALEZ MC,MASEVICIUS FD,et al.Augmented renal clearance in critically ill patients:incidence,associated factors and effects on vancomycintrea tment[J]. Rev Bras TerInteasiva,2014,26(1):13-20.
[11]UDY AA,ROBERTS JA,SHORR AF,et al. Augmented renal clearance in septic and traumatized patients with normal plasma creatinine concentrations: identifying at-risk patients[J].Crit Care,2013,17(1):R35.
[12]CLAUS BO,HOSTE EA,COLPAERT K,et al. Augmented renal clearance is a common finding with worse clinical outcome in critically ill patients receiving antimicrobial therapy[J]. J Crit Care,2013,28(5):695-700.
Clinical evaluation of prolonged infusion versus standard infusion of meropenem in the treatment of hospital-acquired pneumonia in elderly patients
ZHANG Yong, DING Rong, ZHANG Jing.
(Department of Respiratory Medicine, Taizhou No. 4 People's Hospital, Taizhou Jiangsu 225300, China)
ObjectiveTo compare the clinical efficacy and safety of meropenem administered by standard 30-minute infusion or prolonged 3-hour infusion regimen in treatment of hospital acquired pneumonia (HAP) in elderly patients, and evaluate the effect of augmented renal clearance on clinical efficacy.MethodsAn open-label randomized controlled clinical trial was conducted. A total of 40 elderly patients (≥65 years of age) with HAP requiring meropenem therapy were enrolledfrom September 1, 2015 to August 31, 2016. The patients were randomly assigned to receive meropenem 1.0 g in 100 mL of 0.9%NaCl solution by constant-rate continuous intravenous infusion over 3 hours (study group, n=20) or by constant-rate intravenous infusion over 30 minutes (control group, n=20), every 8 hours, for at least 7 days. Clinical efficacy and safety were compared between groups. According to the level of creatinine clearance (Ccr), the 40 patients were further divided into group A1 [Ccr≥130(mL/min)/1.73 m2]and A2 [Ccr<130 (mL/min)/1.73 m2]. The patients with Ccr≥130 (mL/min)/1.73 m2in control group belonged to group B1, and those in study group belonged to group B2. Clinical efficacy was compared between group A1 and A2, and between group B1 and B2.ResultsThe clinical cure rate was 70.00% (14/20) in study group and 50.00% (10/20) in control group (P<0.05).The 28-day survival rate was 85.00% (17/20) in study group and 65.00% (13/20) in control group (P<0.05). The clinical pulmonary infection score (CPIS) was improved significantly in study group (reduction of 2.88±2.51) than in control group (reduction of 1.25±1.67) (P<0.05). Procalcitonin (PCT) level was more improved in study group [reduction of (2.43±0.68) μg/L]than in control group [reduction of (1.05±0.27) μg/L](P<0.05). The duration of meropenem treatment and days of hospital stay did not show significant difference between study group and control group (P>0.05). The common adverse reactions were transient elevation of serum transaminases and diarrhea in both groups. The incidence of adverse reactions did not show significant difference between groups (P>0.05). Further analysis indicated that the clinical cure rate was 44.44% (4/9) in group A1 and 64.52% (20/31) in group A2 (P<0.05). The 28-day survival rate was 66.67% (6/9) in group A1 and 77.42% (24/31) in group A2 (P<0.05). CPIS reduction was 1.62±1.61 in group A1 and 2.19±2.2 in group A2 (P<0.05). The reduction of PCT level was (1.41±0.39) μg/L in group A1 and (1.84±0.5) μg/L in group A2 (P<0.05). The duration of meropenem treatment and days of hospital stay did not show significant difference between group A1 and group A2. The clinical cure rate was 1/4 in group B1 and 3/5 in group B2 (P<0.05). The 28-day survival rate was 2/4 in group B1 and 4/5 in group B2 (P<0.05). CPIS reduction was 0.68±0.93 in group B1 and 2.56±2.29 in group B2 (P<0.05). The reduction of PCT level was (0.61±0.15) μg/L in group B1 and (2.21±0.63) μg/L in group B2 (P<0.05).The duration of meropenem treatment and days of hospital stay did not show significant difference between group B1 and group B2 (P>0.05). Conclusions Prolonged intravenous infusion of meropenem over 3 hours provides better clinical efficacy than the standard 30-minute infusion of meropenem in the treatment of HAP in elderly patients without increase of adverse reactions. Augmented renal clearance may reduce the clinical efficacy of meropenem, which can be improved by 3-hour prolonged infusion of meropenem.
meropenem; prolonged intravenous infusion; hospital acquired pneumonia; augmented renal clearance
R563.11
A
1009-7708 ( 2017 ) 06-0623-06
10.16718/j.1009-7708.2017.06.002
江苏省泰州市第四人民医院呼吸内科,江苏泰州 225300。
张勇(1974—),男,学士,主任医师,主要从事肺部感染性疾病、慢性阻塞性肺疾病研究。
张勇,E-mail:7773330083@sina.com。
2016-11-01 修回日期:2017-05-08
