超高效凝胶色谱法测定聚乙二醇衍生物的分子量及其分布
2017-11-29谢梦婷黄晓兰罗辉泰朱志鑫吴惠勤
谢梦婷,黄晓兰,罗辉泰,黄 芳,朱志鑫,李 兴,吴惠勤
(广东省测试分析研究所 广东省分析测试技术公共实验室,广东 广州 510070)
超高效凝胶色谱法测定聚乙二醇衍生物的分子量及其分布
谢梦婷,黄晓兰*,罗辉泰,黄 芳,朱志鑫,李 兴,吴惠勤
(广东省测试分析研究所 广东省分析测试技术公共实验室,广东 广州 510070)
采用超高效聚合物色谱(APC)技术,以单甲氧基聚乙二醇丙醛(mPEG_pALD)为代表,测定了聚乙二醇衍生物的相对分子质量及其分布和杂质含量,优选了色谱柱和流动相,考察了样品质量浓度变化以及溶解时间等对测定结果的影响。优化后3根超高效凝胶色谱柱串联,在柱温40 ℃,流动相95%甲醇,流速0.5 mL/min,示差折光检测条件下,对mPEG_pALD的分子量及其分布进行测定,同时得到杂质的相对含量。结果测得mPEG_pALD主成分的重均分子量(Mw)为19 444,分布指数(D)为1.01;杂质1的Mw为38 703,D为1.01,含量为1.31%;杂质2的Mw为61 036,D为1.00,含量为0.70%。与常规凝胶渗透色谱(GPC)相比,该方法分辨率高,分析速度快,能快速测定mPEG_pALD的相对分子量及其分布,并能得到其纯度和杂质含量,为其工艺研发、质量控制提供了科学的依据,同时也可用于其它PEG衍生物的相对分子量及其分布和纯度的测定。
超高效凝胶色谱法;聚乙二醇衍生物;相对分子量;杂质含量;单甲氧基聚乙二醇丙醛
蛋白药物具有多种优点,目前已被广泛应用于临床。但蛋白药物存在易被酶水解、循环半衰期短、免疫原性高以及溶解度低等缺点[1-2],为了维持一定的疗效需要大剂量、频繁用药,但长期、反复的用药不仅增加了病人的痛苦而且会引发一系列的副反应。这些缺点严重制约了蛋白类药物的发展,通过化学修饰可以改善这些问题。用作蛋白药物的修饰剂很多[3],其中应用最广泛的是聚乙二醇(Polyethylene glycol,PEG)及其衍生物[4-7]。PEG及其衍生物不仅可以修饰蛋白药物,还可用于修饰其他药物而改善其性能(增加水溶性、延长半衰期等),其分子量及分布和杂质含量对修饰后药物的性能有较大影响[8-10]。因此,亟需建立一种快速有效的方法测定其分子量及分布和杂质的含量。
目前,测定PEG及其衍生物相对分子质量的方法有粘度法[11]、红外光谱法[12]、凝胶色谱(GPC)法[13-15]、基质辅助激光解吸电离-飞行时间质谱(MALDI-TOF MS)法[16-18]、快原子轰击质谱(FAB-MS) 法[18-19]、核磁共振 (NMR) 法[20]等。PEG相对分子质量的测定方法报道较多,而测定PEG衍生物分子质量的方法则较少报道。粘度法测定高聚物分子量操作繁琐、花费时间较长,与红外光谱法的准确度均较差,且无法得到分子量分布;而MALDI-TOF MS法需要选择合适的基质,FAB-MS法的分子量测定上限为2 000 Da[18],这两种方法的仪器昂贵,难以普及;NMR法只能测定PEG衍生物的相对分子量,对样品纯度要求高。GPC法不仅可以测定聚合物的相对分子质量,同时可得到分布系数(D,Mw/Mn),并可根据GPC色谱峰面积大小测定杂质的相对含量,是目前测定高分子聚合物分子量的首选方法。
本文采用近两年最新发展起来的超高效聚合物色谱(Advanced polymer chromatography,APC)技术,以单甲氧基聚乙二醇丙醛(Monomethoxy polyethylene glycol propyl aldehyde,mPEG_pALD)为代表,建立了PEG衍生物相对分子质量及其分布和杂质含量的快速测定方法,以期为其工艺研发、质量控制提供科学依据。
1 实验部分
1.1 仪器与试剂
超高效聚合物系统(Waters Acquity APC):Acquity APC溶剂管理器,Acquity APC 样品管理器,Acquity APC Column Manager-30S 柱温箱,Acquity UPLC 示差折光(RI)检测器。
聚乙二醇(PEG,美国 Sigma Fluka 公司),峰位分子量(Mp)分别为600、1 500、2 010、3 120、6 240、8 600、12 000、23 000、40 000、230 000、478 000 Da。甲醇(色谱纯,美国Thermo Fisher公司);蒸馏水(广州屈臣氏饮料食品有限公司)。
1.2 实验条件与方法
色谱条件:色谱柱:Acquity APC XT 450(4.6 mm×150 mm,2.5 μm),测定分子量量程:20 000~400 000 Da;Acquity APC XT 200(4.6 mm×150 mm,2.5 μm),测定分子量量程:3 000~70 000 Da;Acquity APC XT 45(4.6 mm×150 mm,1.7 μm),测定分子量量程:200~5 000 Da,3根色谱柱串联。柱温:40 ℃;流动相:95%甲醇;流速:0.5 mL/min;示差折光检测器:40 ℃;进样量:10 μL。
标准溶液的制备:取PEG标准品(2.25 mg)加入1.5 mL流动相,室温放置24 h,待标准品完全溶解后测定。
样品溶液的制备:称取mPEG_pALD 50 mg置于10 mL容量瓶中,加入流动相溶解定容。
1.3 标准曲线的建立
在上述色谱条件下,取标准溶液进行测定,以聚乙二醇标样的峰位分子量(Mp)的对数为纵坐标(lgw),以淋洗体积为横坐标(V),用三阶方程拟合标准曲线,用于计算待测样品的相对分子量及其分布,标准曲线方程为lgw=16.6-8.13V+1.92V2-0.165V3,r=0.999。
1.4 样品质量浓度对测量结果的影响
分别称取 mPEG_pALD 5、10、20、50、100、200 mg各置于10 mL容量瓶中,加入流动相至刻度,室温放置24 h待其溶解。在相同实验条件下进行分析。
1.5 不同溶解时间对测量结果的影响
称取mPEG_pALD适量,配制成质量浓度均为 5 mg/mL的待测样品,在室温下分别放置0、4、24 h,于相同实验条件下进行分析。
1.6 重复性试验
称取 mPEG_pALD 6份,按上述条件重复测定6次,得到重均分子量、分布系数和杂质相对含量。
2 结果与讨论
2.1 凝胶色谱系统的选择
mPEG_pALD(约20 kDa)在合成过程中会产生2倍(或3倍)目标分子量的杂质,因其主成分与杂质均为聚合物,两者之间有部分物质的分子量较接近,如果色谱柱分辨率不高,则主成分与杂质分离度不好,无法准确测定其分子量,也无法定量主成分含量。传统的GPC色谱柱因填料颗粒较大(≥5 μm),导致分辨率无法提高,不能有效分离mPEG_pALD主成分与杂质1(分子量约为40 kDa),且对于分子量为600、1 500、2 010、3 210 Da的PEG标样也无法得到很好的分离。
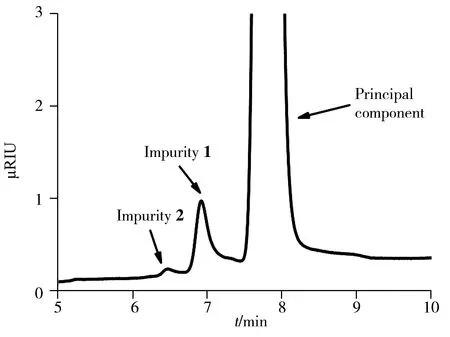
图1 mPEG_pALD的APC系统分析色谱图Fig.1 Chromatogram of mPEG_pALD using APC
因APC系统的总体扩散低,色谱柱的填料颗粒较小(≤2.5 μm),而将最新的超高效聚合物色谱技术与 Acquity APC 系列超高效色谱柱相结合,能显著提高分辨率。在分离低分子量聚合物时分辨率提高尤为显著,不仅使mPEG_pALD(20 kDa)主成分与杂质1得到有效的分离,同时还发现了杂质2(见图 1),这在传统GPC中无法看到;而且对于分子量较为接近的PEG标样(分子量为600、1 500、2 010、3 210 Da)也能得到良好分离。因此实验选择APC凝胶色谱系统分析mPEG_pALD。
2.2 色谱柱及流动相的选择
Acquity APC系列超高效色谱柱主要包括AQ水系色谱柱和XT有机系色谱柱等。AQ系列色谱柱填料是未键合的亚乙基桥杂化(BEH)颗粒,表面有较多的游离羟基,能与聚乙二醇类物质相互作用,使分离作用并非单纯的体积排阻作用,故有可能导致结果偏差。因而本实验选择填料为键合高覆盖率三甲基硅烷的亚乙基桥杂化颗粒的Acquity APC XT系列色谱柱。
因PEG衍生物易溶于极性有机溶剂,故采用极性有机溶剂作为流动相。传统的脂溶性GPC色谱柱填料通常为聚苯乙烯-二乙烯基苯,需进行老化,以使填料在流动相内膨胀到适当大小,平衡时间较长;而且GPC使用的流动相通常固定不变,如果改变流动相则需进行长时间的置换及平衡,并可能导致柱效下降。新型的Acquity APC XT系列色谱柱的填料为亚乙基桥杂化聚乙氧基硅烷颗粒,属刚性填料,适用于有机溶剂,在不同溶剂内的膨胀程度极小或不膨胀,因此能使用多种常见的有机溶剂(四氢呋喃、二氯甲烷、N,N-二甲基甲酰胺)作为流动相而保持柱效不变,并且可以添加少量的水作为改善剂优化方法。根据mPEG_pALD的溶解性,选择甲醇作流动相,并加入5%的水增加流动相对mPEG_pALD的溶解性,最终确定甲醇-水(9∶5,体积比)作为流动相。
2.3 样品浓度的影响
不同浓度的mPEG_pALD分子量及其分布测定结果见表 1,随着样品质量浓度(0.5~5 mg/mL)的增加,主成分的数均分子质量(Mn)、重均分子质量(Mw)、峰位分子质量(Mp)、粘均分子质量(Mz)呈减小趋势,这说明随着质量浓度的减小,分子链更易展开。当浓度达到10 mg/mL 以上时,主峰已变形,这是由于样品量已超过色谱柱载量所致,因而影响分子量及其分布的测定。
当质量浓度较小时(≤2 mg/mL),含量较少而分子量较大的杂质检测不到,会导致丢失一部分信息(见表 1),因此,选择样品质量浓度为5 mg/mL。
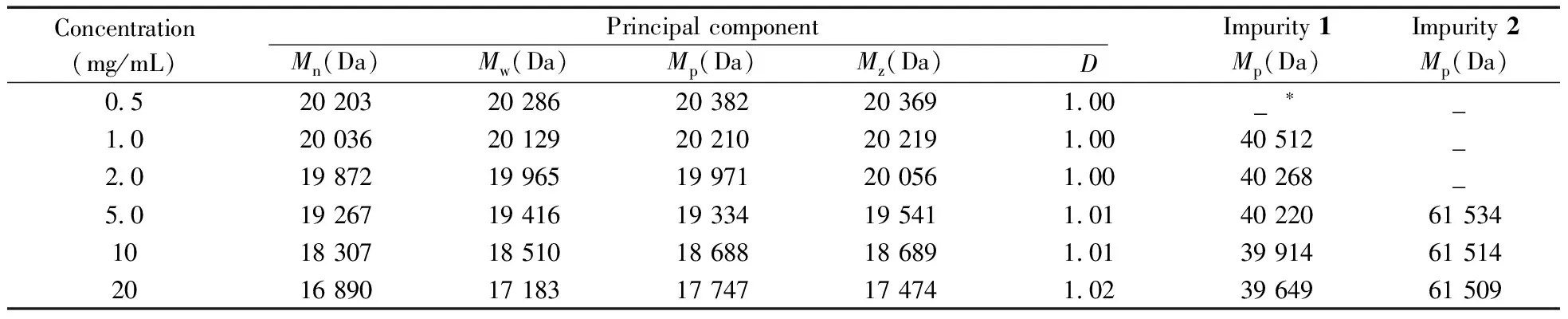
表1 不同质量浓度的mPEG_pALD主成分和杂质分子量及其分布测定结果Table 1 Results of the molecular weight and its distribution of the principal component and impurities of mPEG_pALD at various concentrations
*not detected
2.4 溶解时间的影响
大部分聚合物的溶解需一定的溶胀时间,样品溶解时间的不同有可能导致其分子量及分布的检测结果不一致,因而考察了样品溶解10 min、4 h、24 h对mPEG_pALD分子质量及分布检测的影响。结果表明:随着溶解时间的增加,mPEG_pALD分子质量及分布均无明显变化,说明mPEG_pALD在流动相中溶解性较好,溶解时间对mPEG_pALD在分子质量及分布的测定影响不大。
2.5 流速的影响
考察了流速为0.3、0.5、0.8 mL/min对PEG标样分离度的影响,3种流速下标样均能进行有效分离。当流速为0.3 mL/min时所需分析时间较长;当流速为0.8 mL/min时,分析时间较短但系统压力较高,因此选择0.5 mL/min作为测试流速。此时分析1个样品所需时间为10 min,而传统的GPC 3根色谱柱串联分析1个样品需要60 min以上。与传统的GPC相比,APC技术不仅能提高分离效率,还可以缩短分析时间,减少有机溶剂的使用,降低成本。
2.6 重复性试验结果
对 6 份mPEG_pALD样品溶液用上述条件进行测定,测得重均分子量(Mw)的相对标准偏差(RSD)为1.1%,分布系数(D)的RSD为0.07%,表明该方法重复性良好。
2.7 不同PEG衍生物样品的检测结果
对5个不同的PEG衍生物样品用上述条件进行测定,结果见表 2。由表 2 可知,本文建立的超高效凝胶色谱法除了可以测定mPEG_pALD的分子量及其分布外,还可以用于其他PEG衍生物的分子量及其分布的测定,同时可以得到其杂质的分子量及其分布。
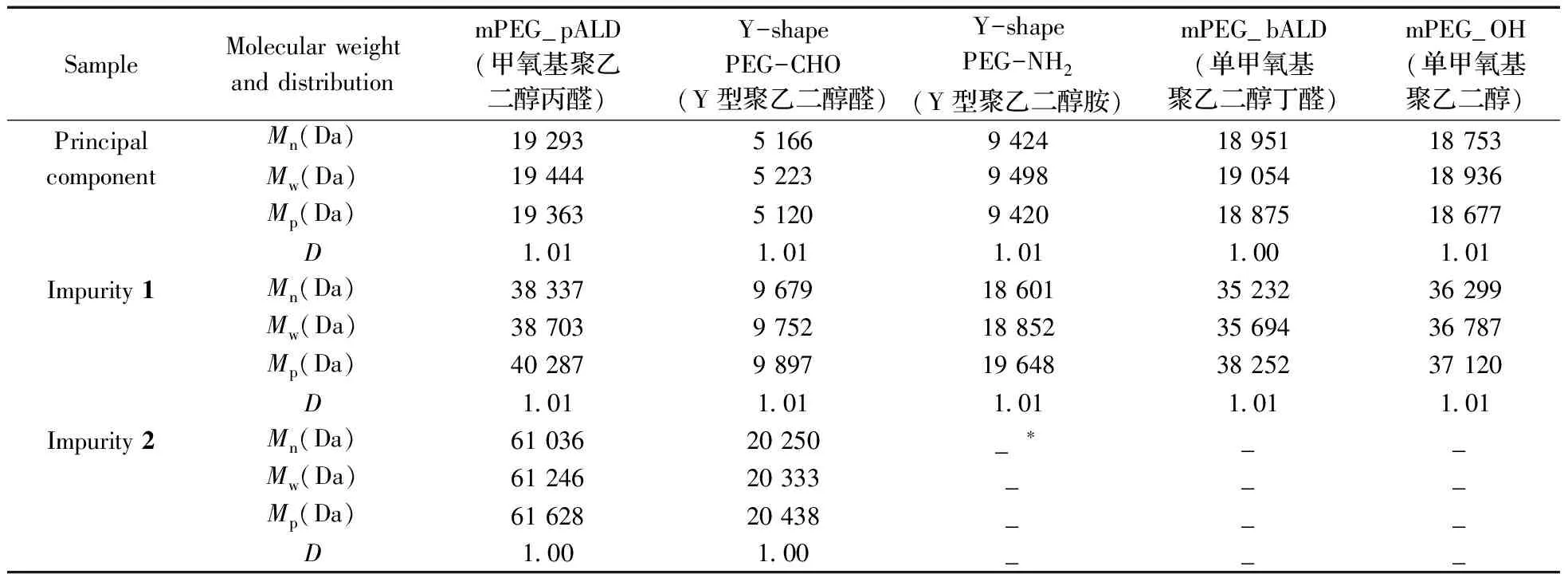
表2 不同PEG衍生物样品的分子量及其分布的检测结果Table 2 Results of the molecular weight of different PEG derivatives
*not detected
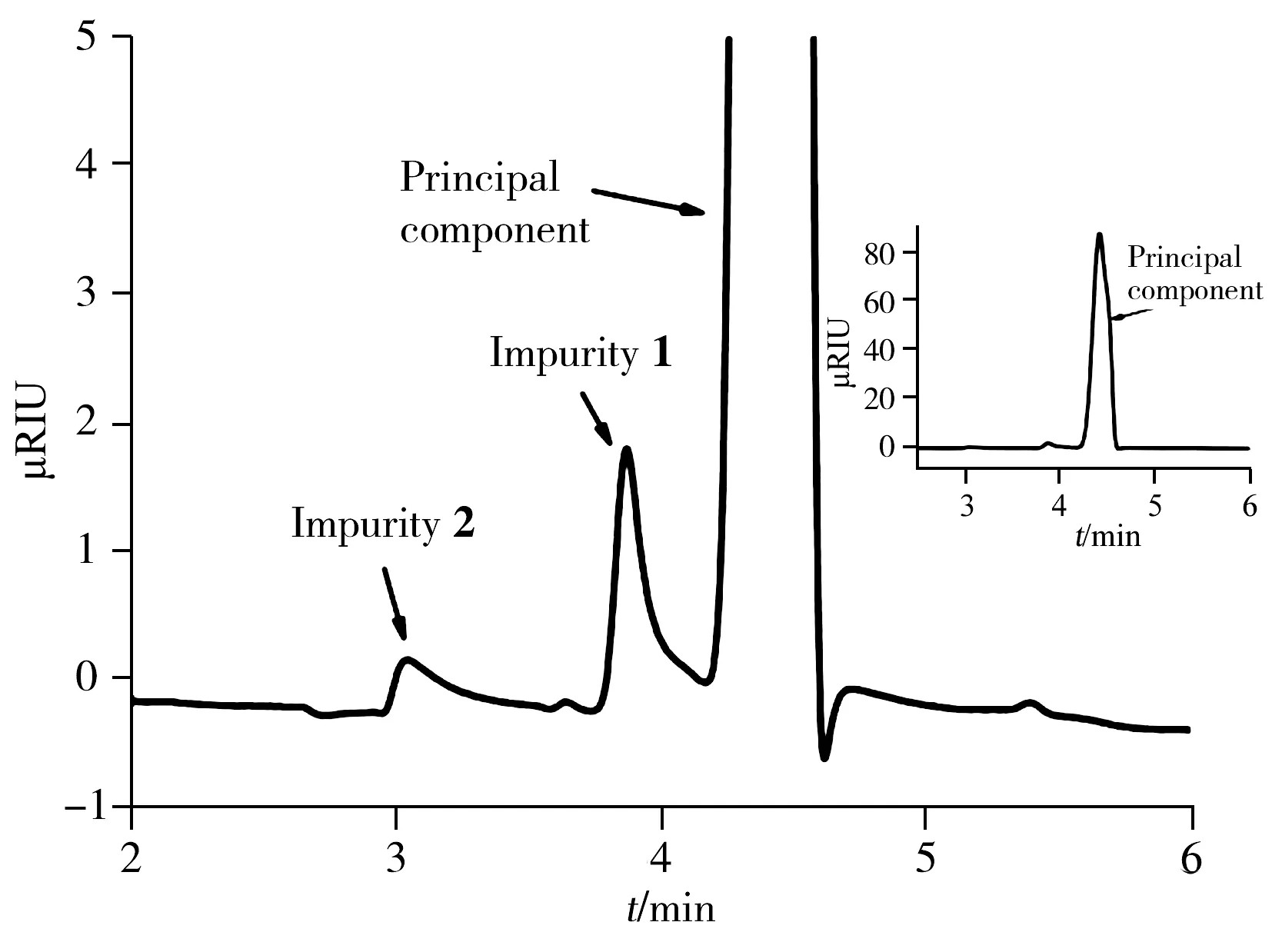
图2 mPEG_pALD(5 mg/mL)用两根色谱柱(AcquityAPC XT 200和Acquity APC XT 45)分析的色谱图Fig.2 Chromatogram of mPEG_pALD(5 mg/mL) with 2 gel columns(Acquity APC XT 200 and Acquity APC XT 45)
2.8 杂质含量的测定
由于样品目标分子量主要在20 kDa左右,因此选择两根色谱柱Acquity APC XT 200和 Acquity APC XT 45串联(分离分子量范围:200~70 000 Da)对样品进行分析,结果发现,杂质2已接近色谱柱的排阻极限,而且主峰已变形(图2)。为得到更准确的结果,选择3根色谱柱串联(分子量范围:200~400 000 Da),不仅可用于mPEG_pALD的分子量及其分布和杂质含量的测定,还可用于其他PEG及其衍生物的分子量及分布和杂质含量的测定。由面积归一化法得出杂质的相对含量,结果见表3。由表3可知,本方法测得杂质1的含量为1.32%,RSD为0.44%;杂质2的含量为0.073%,RSD为7.9%,说明本方法测定mPEG_pALD的杂质含量重复性良好。
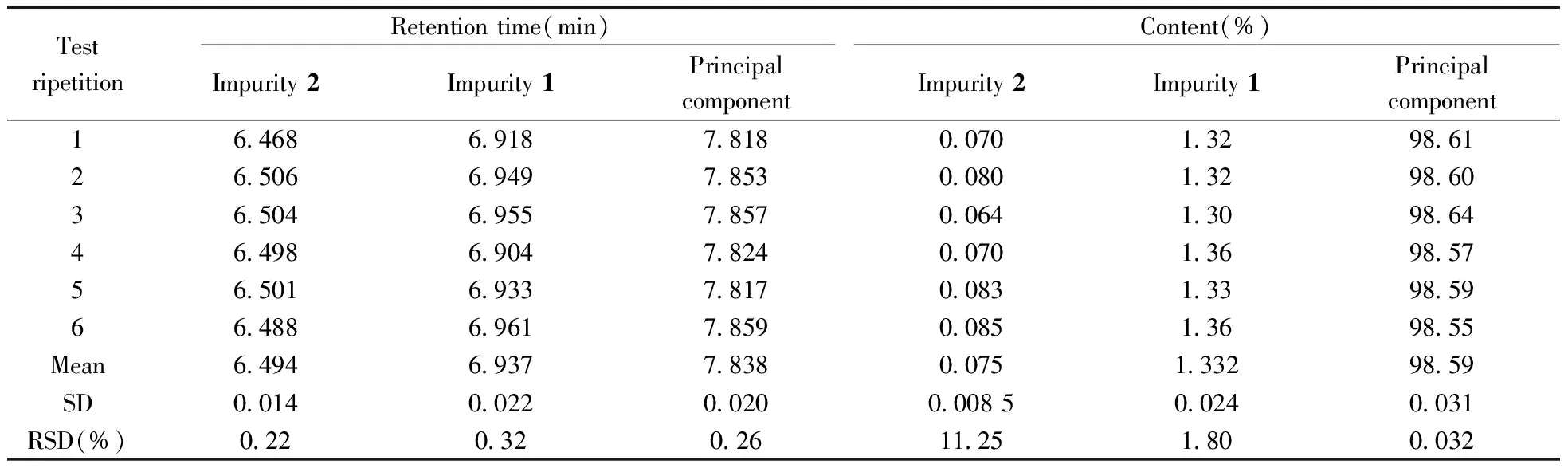
表3 APC系统测定mPEG_pALD(5 mg/mL)主成分和杂质含量结果Table 3 Results of content of the principal component and impurities of mPEG_pALD(5 mg/mL)using APC
3 结 论
本文采用APC技术,以mPEG_pALD为代表,建立了快速测定PEG衍生物相对分子量及其分布的超高效凝胶渗透色谱新方法。与传统的GPC法相比,本方法的分辨率高、分析速度快、重复性好,同时可对PEG衍生物中的杂质进行定量,为其工艺研发、质量控制提供了科学依据。
[1] Choonara B F,Choonara Y E,Kumar P,Bijukumar D,Du Toit L C,Pillay V.Biotechnol.Adv.,2014,32(7):1269-1282.
[2] Park K,Kwon I C,Park K.React.Funct.Polym.,2011,71(3):280-287.
[3] Ding T T,Fan Y,Lin G M.Pharm.Biotechnol.(丁婷婷,范洋,林贵梅.药物生物技术),2014,23(5):417-421.
[4] Wu Y X,Zhai Y Q,Lei J D,Ma G H,Su Z G.Chin.J.Biotechnol.(吴影新,翟艳琴,雷建都,马光辉,苏志国.生物工程学报),2008,24(9):1658-1663.
[5] Wang D X,Wang Y H,Zhou X Y,Zhang Z.Chin.J.Exp.Surg.(王德兴,王艳红,周小芸,张哲.中华实验外科杂志),2009,26(10):1301-1303.
[6] Zhu J,Wang S M,Shen W M,Wu Z R,Liu Y K.Chin.J.NewDrugsClin.Rem.(朱珺,王松梅,沈炜明,吴自荣,刘银坤.中国新药与临床杂志),2005,24(9):723-726.
[7] Chen J W,Wang R H,Rong L F,Song L H.Chin.Pharm.J.(陈金武,王荣海,戎隆富,宋礼华.中国药学杂志),2007,42(10):777-780.
[8] Zhou J J,Zhou Q S,Sun R F,Li X R.Chin.J.Pharmacol.Bull.(周婧婧,周庆颂,孙若飞,李笑然.中国药理学通报),2016,32(10):1446-1451.
[9] Zhang F,Liu M R,Wan H T.J.ZhejiangChin.Med.Univ.(张钒,刘沐荣,万海同.浙江中医药大学学报),2014,38(6):759-763.
[10] Zhou Q S,Jiang X H,Li K J,Fan X X.J.Biomed.Eng.(周庆颂,蒋学华,李珂佳,樊新星.生物医学工程学杂志),2006,23(2):353-356.
[11] Wang L M.Chem.Eng.(王丽梅.化学工程师),2010,(8):18-20.
[12] Deng K L,Zhang R Z.J.HebeiUniv.:Nat.Sci.Ed.(邓奎林,张荣珍.河北大学学报:自然科学版),1996,35(2):62.
[13] Cheng G W,Fan X D,Zhou Z Y,Tian W.Polym.Mater.Sci.Eng.(程广文,范晓东,周志勇,田威.高分子材料科学与工程),2008,24(10):127-130.
[14] Yu X Y.ValueEng.(于小焱.价值工程),2015,34(36):234-236.
[15] Kou D,Manius G,Zhan S D,Chokshi H P.J.Chromatogr.A,2009,1216(28):5424-5428.
[16] Liu Y Q,Zou J K,Qiu Y Y.Res.Exp.Lab.(刘雅琴,邹建凯,裘雅渔.实验室研究与探索),2015,34(10):183-186.
[17] Woldegiorgis A,Löwenhielm P,Björk A,Roeraade J.RapidCommun.MassSpectrom.,2004,18(23):2904-2912.
[18] Mincheva Z,Hadjieva P,Kalcheva V,Seraglia R,Traldi P,Przybylski M.J.MassSpectrom.,2001,36(6):626-632.
[19] Seraglia R,Traldi P,Mendichi R,Sartore L,Schlavon O,Veronese F M.Anal.Chim.Acta,1992,262(2):277-283.
[20] Izunobi J U,Higginbotham C L.J.Chem.Edu.,2011,88(8):1098-1104.
Determination of the Molecular Weight and Molecular Weight Distribution of Polyethylene Glycol Derivatives by Advanced Polymer Chromatography
XIE Meng-ting,HUANG Xiao-lan*,LUO Hui-tai,HUANG Fang,ZHU Zhi-xin,LI Xing,WU Hui-qin
(Guangdong Provincial Public Laboratory of Analysis and Testing Technology,Guangdong Institute of Analysis,Guangzhou 510070,China)
A method of advanced polymer chromatography(APC) was established for the determination of the molecular weights and their distributions of polyethylene glycol derivatives and the impurity contents,with monomethoxy polyethylene glycol propyl aldehyde(mPEG_pALD) as the representation for polyethylene glycol derivatives.The chromatographic conditions such as chromatographic column and mobile phase were optimized,while the effects of the concentration of sample(within the concentration range of 0.5-20 mg/mL) and dissolution time were also investigated.The optimized chromatographic conditions were as follows:three ultra-high performance gel columns were connected in series at 40 ℃ with methanol-water (95∶5,by volume) as mobile phase at a flow rate of 0.5 mL/min,and a refractive index detector was selected.The result showed that the weight-averaged molecular weight(Mw) of mPEG_pALD was 19 444 and its distribution index(D) was 1.01,while theMwfor impurity1was 38 703 with itsDindex of 1.01 and its content of 1.31%,and theMwfor impurity2was 61 036 with itsDindex of 1.00 and its content of 0.70%.Compared with the traditional GPC method,this APC method could obtain the molecular weight and its distribution of mPEG_pALD with higher resolution and less time,and the content of impurity could also be acquired.The method provides a scientific basis for the research,development and quality control of PEG derivatives,and is applicable for the determination of molecular weight,molecular weight distribution and purity of other PEG derivatives.
ultra high performance gel chromatography;polyethylene glycol derivatives;relative molecular weight;impurity content;mPEG_pALD
2017-07-04;
2017-08-10
广东省科学院科研平台环境与能力建设专项资金项目(2016GDASPT-0308)
*
黄晓兰,研究员,研究方向:色谱-质谱分析技术,Tel:020-87312430,E-mail:wenhxl@126.com
10.3969/j.issn.1004-4957.2017.11.004
O657.7;O631.6
A
1004-4957(2017)11-1312-06
