孤儿药研发的经济学分析Δ
2017-11-29俞江婷王艳翚南京中医药大学卫生经济管理学院南京210023
俞江婷,王艳翚,华 东(南京中医药大学卫生经济管理学院,南京 210023)
孤儿药研发的经济学分析Δ
俞江婷*,王艳翚#,华 东(南京中医药大学卫生经济管理学院,南京 210023)
目的:从经济学角度对我国孤儿药的研发问题进行分析,为我国孤儿药的发展与政策制定提供建议。方法:利用外部性理论和交易费用理论,分析我国药品企业对孤儿药研发积极性不高的原因,并针对这些原因提出相应的解决办法。结果:孤儿药在我国尚缺乏认定标准,其外部经济性、众多的交易费用以及较大的研发风险都会加重药品企业的经济负担,打击企业研发和生产的积极性。结论:我国药品企业可以对孤儿药实行合作研发的策略,并发挥中医药治疗的传统优势,以减少研发成本。政府应建立并发展孤儿药的制度体系,发挥税收及医保的作用,加速审批,给予医药企业市场独占权,鼓励合作研发。
孤儿药;外部性;交易费用;研发;经济学分析
罕见病是指发病率极低的疾病,诊疗难度大,且具有治疗的不可替代性[1]。孤儿药主要是指用于预防、诊断、治疗罕见病的药物。虽然其需求数量少,但由于可以满足罕见病患者的需求,所以具有较高的社会效益。目前,我国尚无针对孤儿药的鼓励性政策,这使得我国药品企业对孤儿药的研发和生产积极性不高,孤儿药的研究进展缓慢,导致罕见病患者无法得到及时、有效的治疗,其用药不得不依赖国外进口,而这类药物通常价格昂贵,会给患者家庭带来沉重的经济负担。因此,探索并寻求适合我国国情的孤儿药发展政策具有重要的现实意义。
1 孤儿药在我国的研发现状
1.1 缺乏认定标准
有关罕见病和孤儿药的认定标准,多数西方发达国家都已有明确界定。如美国《罕见病法案》认定,每年患病人数低于20万的疾病为罕见病;欧盟《孤儿药品管理法》认定,每年患病人数低于24.6万的危及生命或慢性渐进性的疾病为罕见病[2]。此外,美国FDA和欧洲药品管理局(EMA)均通过孤儿药认定五项标准(低发病率、无有效的治疗手段、真实有效的临床有效性或优越性证据、低投资回报率、创新的治疗技术或手段)对孤儿药的含义进行了界定[2]。
目前,我国并没有罕见病和孤儿药的官方认定标准。2010年中华医学会的遗传学分会上,曾有与会学者将罕见病定义为“一种患病率低于五十万分之一、新生儿发病率低于万分之一的遗传病”[3],然而由于缺乏官方的认定,虽然该定义具有较高的科学性,却仅止于学术研究的范畴,并没有普遍的适用性,因此依然不利于企业制定研发决策。
1.2 研发风险较大
孤儿药的研发风险较大,主要表现在:第一,孤儿药的研发周期长,且研究结果有较大的非预测性。新药的研发和上市需要经过临床试验,但孤儿药的治疗对象是罕见病患者,因此与其他新药相比,孤儿药研发所拥有的资料较少,试验对象的寻找也比较困难。这些因素导致其研发周期长,加上研究技术复杂,因此研究结果的成败与否也很难预测。第二,孤儿药的成本回收率低。由于研发成本高、风险大,一旦研究失败,高昂的研发成本将给研究企业带来巨大的经济损失。即使药物能够研发成功,由于其针对的病种罕见,真正能够使用这种药物的患者数量很少。需求量少、利润低,使得企业很难收回成本。这也是我国药品企业不愿意投资孤儿药研发的重要原因。
1.3 缺失激励性政策
从1999年开始,我国陆续出台过一些有关于孤儿药的政策,例如允许减免申报单位的临床研究、实行孤儿药的快速审批、特殊审批制度等[1]。但这些制度都是零散的,不能形成一套完整的激励孤儿药研发的政策体系。虽然它们在一定程度上减少了研发企业的时间成本消耗,但由于没有其他相关鼓励性政策配套,仍然无法弥补企业的研发成本,无法提高我国药品企业对孤儿药研发的兴趣与积极性。
2 孤儿药研发的经济学视角分析
2.1 孤儿药研发的外部性与资源配置分析
从社会效益角度分析,孤儿药的研发能够给予罕见病患者获得救治的途径和希望,其研发所获得的临床数据以及知识经验的积累有利于推动药物创新,从而有利于后期研发成本的降低,进而在客观上促进社会整体健康水平的提高。因此,孤儿药的研发具有较大的正外部性。按照经济学理论,这种因增加某单位的某种物品或服务的消费而给第三者所带来的额外效益可以用外部边际效益(Marginal external benefit,MEB)来表示[4]。对于这种具有正外部性的物品或服务,需要政府的财政补贴予以扶持,以实现正外部效应的内在化。孤儿药研发的正外部性与资源配置分析见图1。
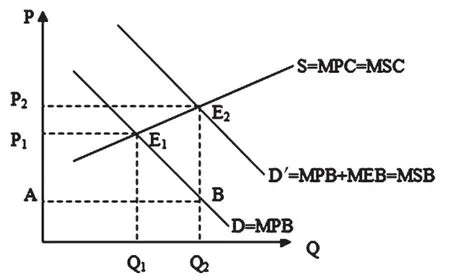
图1 孤儿药研发的正外部性与资源配置分析Fig 1 Analysis of positive externalities and resource allocation of orphan drug research and development
如图1所示,通常情况下,孤儿药的需求曲线D与供给曲线S相交于市场均衡点E1,Q1和P1分别代表均衡数量与均衡价格。由于孤儿药具有明显的外部经济效益,所以不将边际损害考虑在内,因此本研究假设孤儿药研发的私人边际成本(Marginal private cost,MPC)等于社会边际成本(Marginal social cost,MSC)。考虑到孤儿药所带来的MEB,E1点的社会边际效益(Marginal social benefit,MSB)是大于私人边际效益(Marginal private benefit,MPB)的,这就会导致孤儿药研发主体研发和投资的积极性不高,甚至放弃药品研发,因此就需要通过政府的矫正性财政补贴使需求曲线D向右上方平移,让市场均衡点由E1移至E2。由图1可以看出,E2点的均衡价格P2虽然有所增加,但患者得到补贴后所支付的净价格事实上却是下降的,这就有助于减少罕见病患者因为药品价格过于昂贵而放弃治疗的几率,一定程度上增加了需求量。这时市场均衡点E2所代表的孤儿药的MSB就等于其MSC,能够实现私人福利的最大化。图1中矩形ABE2P2的面积为政府的财政补贴。
同样,政府部门也可以通过减少税收等激励性政策对孤儿药的研发企业进行补贴。以税收为例,政府部门可以按照孤儿药研发和生产的数量从量减税[5]。如图2所示,若政府部门减少税收,则研发企业的MPC和MSC都会相应地减少,即供给曲线S就会向右下方移动至S′,达到新的市场均衡点Q2和P2。此时药品企业会适当增加孤儿药的研发生产,并适当减少药品的价格。同时,随着税收的减少,生产者剩余和消费者剩余都会有一定数量的增加,即社会总效益会有所提升。图2中矩形P1ACF的面积代表政府所减少的税收;三角形ABC的面积代表生产者剩余和消费者剩余增加的总和。
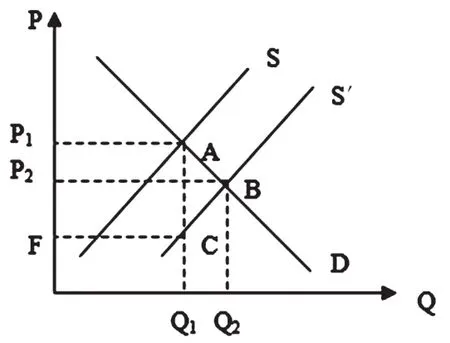
图2 政府减少税收对孤儿药研发企业行为的影响分析Fig 2 Analysis of the effects of government tax reduction on orphan drug research and development enterprises
2.2 孤儿药研发的交易费用构成分析
新制度经济学的一个突出特点是坚持交易费用的存在。关于交易费用的含义,目前学术界还没有统一。科斯、威廉姆森等人从契约的角度对交易费用进行探讨,认为交易费用是合同形成的过程中所产生的诸如谈判、签约及履行合同等的成本;肯尼斯·阿罗、张五常等人从社会经济系统的层面出发,认为交易费用是“所有与制度或组织的建立或变迁,和制度或组织的使用有关的费用”[6]。据此,笔者认为交易费用是在资源或所有权转移的过程中所产生的,为了维持组织或制度运行,实现组织或制度目标的费用。具体如下:
(1)信息搜集费用。药品企业在孤儿药研发之前首先需要做药品的研发决策[7],内容包括哪些病种属于罕见病范围,哪种罕见病患者的需求量相对较大,孤儿药研发能给企业带来多少收益等;同时,还需要确定相关技术人员及相应的研发方案。在孤儿药的研发阶段,科研人员需要对无数的分子结构进行筛选、合成,以产生新的化合物,然后还要对新化合物的活性继续筛选。此过程不断循环,直至找出企业所需且活性足够理想的化合物。之后还需要进行3期的临床试验。在此过程中,企业会产生大量的与信息搜集有关的人、财、物的转移,也因此会产生大量的交易费用。
(2)签约与谈判费用。新药的研发需要具有专业知识和经验的科学家的参与。由于孤儿药的临床资料较少、研究技术难度较高,其所需的研究者的专业素质要求也比较高,因此相关科研机构或药品企业需要与专业的技术人员进行谈判并签约,以获得他们在专业上的协助。同时,孤儿药在临床试验阶段还需要受试者的协助,为了吸引并保障受试者的权益,相关机构与受试者之间也会产生相应的谈判与签约费用。孤儿药的上市流通阶段还需要大量的销售、监督、管理决策等人员参与,与他们之间进行谈判与签约所产生的费用也不容小觑。此外,存在合作、转让、投资等关系的企业之间也会产生相应的签约与谈判费用。
(3)管理型交易费用。这部分费用常见于企业内部发号施令的过程中,通常表现为企业的间接费用,可以通过合理的管理来减少。该费用主要包括药物原料流动时产生的命令、执行和确认的费用,保证供应药品生产的费用,保证药物质量的费用,基础性生产信息体制变更的费用等[8]。
还有一些管理型交易费用会以“专用性投资”的形式出现[8]。这里所说的专用性投资指的是“交易专用性投资”,即为执行交易所产生的专用性资产的投入[9]。孤儿药在研发生产的过程中很有可能会涉及到专用性资产投资的问题,例如投入专用的人力资源、器材设备等。资产的专用性会使得该资产在移作他用时价值降低,因此投资主体在交易时会处于被动地位,极有可能因对方的机会主义而遭受损失,从而增加其潜在的市场交易费用,且资产专用性程度越高,交易费用也越高。
(4)知识产权维护费用。为了保护核心技术秘密,确保市场竞争优势,孤儿药的研发企业必然会借助专利、商标、商业秘密等知识产权形式设定法律保护,其权利维护费用也是一笔不小的开支。笔者认为,可以将这种法律保护关系看成一种知识产权所有者与国家之间的交易关系。以专利保护为例,专利所有者每年按时向国家缴纳一定的专利保护费用,以此换来国家给予的一定期限的市场独占权。在这种保护之下,专利所有者可以在规定的期限内尽可能多地收回药品研发所产生的成本。
(5)法律纠纷解决费用。这主要指的是相关企业或机构为了保护权益或者解决纠纷所花费的费用,包括和解、调解、仲裁和诉讼等过程中产生的相应的交易费用。
3 讨论与建议
3.1 明确罕见病与孤儿药的认定标准
我国目前缺乏对罕见病的认定标准,有关孤儿药的界定也比较模糊,这就为药品企业确定市场需求、制定研发决策带来困难,也使得政府无法确定哪些药品能够享受孤儿药的优惠政策。为此,国家卫生管理机构有必要对罕见病和孤儿药的认定标准予以明确,可以考虑通过召开听证会的方式,听取各方面专业人士的意见,并结合各地诸如各病种发病率等相关报告,以法律或法规的形式确定符合我国国情的罕见病认定标准。对于孤儿药,政府也需要借鉴国外的经验以及相关领域专家的意见,并通过市场调查了解我国孤儿药的研发生产及市场交易等相关情况,为孤儿药官方标准的确认及其他政策的制定提供参考。
3.2 鼓励合作研发,减少交易费用
针对孤儿药研发创新动力不足的现状,笔者认为,可以考虑采取企业之间合作的方式,鼓励合作研发。一方面,合作研发有利于减少信息搜集与传递的费用。合作研发的相关企业可以避免对同一信息的重复搜索,从而减少不必要的成本支出。在上市流通阶段,相关合作企业还可以通过信息共享而迅速、高效地找到交易对象,或者通过费用共担的方式减少信息传递的成本。另一方面,合作研发还有利于减少签约、谈判与监督的费用。企业间合作可以促进技术人员的流动,实现人力资源共享,减少不必要的人力消耗;同时,鉴于机会主义和交易频率会影响交易费用的高低[6],企业间合作得越频繁,企业间的了解程度越会加深,不但可以减少为了预防对方的机会主义而支出的费用和时间,还可以促使双方为维持合作关系而约束自己的机会主义行为,减少因此而产生的交易费用,加快合同的形成。
我们可以借鉴日本的合作研发模式,主要有参与者签订协议共同承担研发费用和成立技术研究组合两种[10]。其中,前者属于垂直合作形式,指的是某一产品从研发到使用过程中所有参与机构共同分担研发费用;后者属于平行合作形式,指的是各个不同的技术研发企业组成临时的研发合作联盟,实现技术共享、风险共担。笔者认为,鉴于我国创新力不足的情况,我国应更加注重技术创新方面的合作,降低失败风险,因此企业间的平行合作可以作为首选。
目前,我国也发展出一种“政、产、学、研”的新合作模式,即由学校或科研机构作为供给方提供技术研究成果,企业作为需求方购买该成果的所有知识产权[11],而政府则在其中进行协调与引导,以维护研发技术合作联盟的稳定。在这种合作模式中,政府的支持十分重要。笔者认为,政府可以考虑:在资金支持方面,给予合作研发的企业或组织一定的税收优惠或财政补偿,以及一定数量的科研经费投入;在信息支持方面,为了促进合作主体之间的信任与合作,特别是产、学、研这种异质性主体之间的合作,减少因信息不对称而产生的交易风险,可以建立和提供官方的信息交流平台,并提供经审批合格的药品生产厂家的相关信息,包括其拥有的生产条件及技术等,以帮助研发机构选择合适的合作伙伴,同时实现合作主体之间科研技术成果与技术团队的信息公开和信息交流;在法律政策的支持方面,国家需要完善相关的政策法规以明确知识产权的归属,规范市场交易行为和产业结构等,为研发合作提供良好的法律环境。
3.3 发挥税收及医保的作用,解决外部性问题
孤儿药的正外部性会导致孤儿药市场的失灵,因此需要政府的财政补贴将其内部化。在这方面,笔者认为可以考虑采取税收减免和医保报销的鼓励性政策。孤儿药的价格与其他药品相比相对较高,若政府予以税收减免或给予财政补贴,有助于客观上降低该类药品的支付价格,从而减轻患者的经济负担,提高购买量。
将孤儿药纳入医保的报销范围能够降低患者实际支付的药品价格,有利于罕见病患者的治疗,也可以鼓励企业的研发。政府需要制定相应的计划,将重点孤儿药纳入报销的范围;同时考虑借助相关基金项目的设置,进行必要的资金投入;还可以通过商业医疗保险来实现补偿。
3.4 制定激励性政策,加速审批,给予市场独占权
为激励孤儿药的研发,很多国家都制定了诸如加速审批以及给予市场独占权的激励性政策,例如美国和日本通过实施优先审评、快速审批的制度为孤儿药开通快速通道;欧盟通过集中审批制度加速孤儿药的上市时间等[3]。为此,我国政府也有必要为孤儿药开通“加速通道”,简化审批程序,缩短审批时间。
此外,西方国家普遍给予孤儿药生产企业7~10年的市场独占期,在此期间不批准其他任何同类药品生产,除非证明其在临床上更具优越性[12],以给予研发企业一定的利润空间。我国也可以借鉴该做法。当然,由于市场独占权有可能给企业制造攫取超额经济利益的空间,因此在政策施行时仍需慎重,可以考虑配套出台相应的限制措施。不过就目前我国相关政策法规还处于空白的状况来看,我国可以以适当延长孤儿药专利保护期的形式来给予市场独占权。
3.5 发挥中医药治疗的传统优势,减少研发成本
“罕见病”属于中医“疑难杂症”的一部分[13],因此研发企业可以考虑对中医药中治疗疑难杂症的配方和治疗手段等进行研究。将中医药运用于孤儿药的研发具有两大优势:一是中医疗法具有简、便、验、廉的特点,可减少一定的研发成本;二是中医在治疗疑难杂症方面积累的经验可以为孤儿药的研发提供有价值的参考。因此,研发企业可以考虑将中医古籍上所记载的疑难杂症的治疗手段和药物配方作为参考,并结合当代罕见病的具体情况进行更深一步的研究;或选择与中医药院校等专业的研究机构进行合作,从而在一定程度上降低研发的难度,减少研发的风险成本。
4 结语
虽然我国对孤儿药的重视程度正逐渐加强[14],但到目前为止,我国依然在制度方面存在较大缺陷。本文从经济学的角度,在理论上对孤儿药的研发问题进行了分析并提出了建议,但在具体实施方面依然需要数据的支持。因此,今后的研究还需要对目前我国各种疾病的发病状况、孤儿药的研发情况等进行进一步的调查研究及数据采集,从而有效支持我国孤儿药制度体系的逐步建立与完善。
[1] 信枭雄,管晓东,陈敬,等.国内外孤儿药注册制度比较研究[J].中国药学杂志,2013,48(15):1323-1328.
[2] 李认书,李鸿彬.美国与欧盟孤儿药研发上市管理制度及对我国的启示[J].中国药事,2014,28(10):1109-1113.
[3] 唐健元,赵夏茵.国外孤儿药管理制度对比研究及对我国的政策建议[J].中国新药杂志,2013,22(14):1638-1642.
[4] 高培勇,崔军.公共部门经济学[M].3版.北京:中国人民大学出版社,2011:36-38.
[5]Tresch RW.公共部门经济学[M].薛涧坡,译.北京:中国人民大学出版社,2014:232.
[6] 胡乐明,刘刚.新制度经济学原理[M].北京:中国人民大学出版社,2014:29-31.
[7] 张锡林,唐元虎.交易费用与企业技术创新战略决策[J].科技进步与对策,2003,20(5):12-14.
[8](美)埃里克·弗鲁博顿,(德)鲁道夫·芮切特.新制度经济学:一个交易费用分析范式[M].姜建强,罗长远,译.上海:格致出版社、上海三联书店、上海人民出版社,2012:57-69.
[9] 周俊,薛求知.交易专用性投资效应及治理机制研究评价[J].外国经济与管理,2009,31(9):18-28.
[10] 宋成华.日本企业共同研发的经济学分析[J].现代日本经济,2005(6):45-48.
[11] 徐向艺,任荣.产学研合作创新与企业间合作创新的比较研究[J].比较管理,2011(1):31-40.
[12] 李丹阳,王健.激励性监管:“孤儿药”的特殊属性与政府监管政策初探[J].中国卫生产业,2013,10(27):186-187.
[13] 易八贤,王广平,吴晓明.基于孤儿药制度的传统疑难杂症药物研发激励策略[J].中国医药工业杂志,2014,45(3):S16-S20.
[14] 曾智,杨悦,令狐昌黎,等.拟建我国罕用药政策制度的探讨与建议[J].中国药房,2009,20(10):737-740.
Economic Analysis of Orphan Drug Research and Development
YU Jiangting,WANG Yanhui,HUA Dong(School of Health Economics and Management,Nanjing University of TCM,Nanjing 210023,China)
OBJECTIVE:To analyze the research and development(Ramp;D)of orphan drug in China from the respect of economics,and to provide suggestions for the development and policy formulation of orphan drug in China.METHODS:The theories of external economy and transaction costs were adopted to analyze the reasons about no enthusiasm in orphan drug Ramp;D,and find some appropriate solutions for them.RESULTS:Orphan drug was still lack of identification standard in China.The external economy,much of transaction costs in orphan drug and Ramp;D risk aggravated the economic burden on pharmaceutical enterprises,combated Ramp;D and production enthusiasm of pharmaceutical enterprises.CONCLUSIONS:Chinese pharmaceutical enterprises can take part in orphan drug cooperative Ramp;D,and play the advantage of TCM treatment so as to reduce Ramp;D cost.The government should establish and develop orphan drug system,play the role of taxation and health insurance,accelerate approval,give market exclusivity for pharmaceutical enterprises and encourage cooperative Ramp;D.
Orphan drug;External;Transaction costs;Research and development;Economic analysis
R956
A
1001-0408(2017)32-4474-05
DOI10.6039/j.issn.1001-0408.2017.32.03
四川省哲学社会科学重点研究基地、四川医事卫生法治研究中心项目(No.YF16-Y08)
*硕士研究生。研究方向:药事管理与医药法。电话:025-85811761。E-mail:yjt85584896@163.com
#通信作者:副教授,硕士生导师,博士。研究方向:中医药知识产权。电话:025-85811761。E-mail:heimi8@163.com
2016-11-05
2017-01-07)(编辑:胡晓霖)
