一种易操作的小鼠肝细胞的分离及培养方法
2017-11-29范仕郡祝元锋鲁永玲
范仕郡,刘 鑫,杨 东,祝元锋,鲁永玲,郑 江
(第三军医大学第一附属医院中心实验室,重庆 400038)
经验交流
一种易操作的小鼠肝细胞的分离及培养方法
范仕郡,刘 鑫,杨 东,祝元锋,鲁永玲,郑 江*
(第三军医大学第一附属医院中心实验室,重庆 400038)
目的在传统肝细胞提取方法的基础上,优化一种易操作、快速实用获取小鼠肝细胞的方法,为从事肝脏功能相关研究人员提供改良的实验方法参考。方法以肝脏分离液逆向灌注小鼠肝脏后,剪碎,肝脏酶消化后密度梯度离心分离肝细胞,转入培养基培养。采用台盼蓝染色计算细胞活力,流式细胞检测技术计算纯度,倒置显微镜观察细胞形态。结果获得较高纯度和活力的肝细胞,具备肝细胞的典型形态特征。结论通过逆向灌注,降低了灌注的难度,同时获得较高纯度、较高活力的肝细胞,经多次实验证明该方法确实是一种易操作、高效适用的肝细胞提取方法。
C57BL/6J小鼠;肝细胞;逆向灌注;活力;纯度
肝脏是人体最大的实质器官和重要的排毒器官。在人体中担负着去氧化、存储肝糖、合成分泌性蛋白质等重要作用。同时也是消化系统中重要的消化腺。它可以制造胆汁来帮助食物的消化,也是尿素合成的主要脏器,更是新陈代谢的重要器官[1]。因此,肝脏对于人体的重要作用不言而喻。肝脏细胞主要由肝细胞(hepatocytes,HC)、枯否细胞(Kupffer cells,KC)、肝星形细胞(liver stellate cells,HSC)和肝血窦内皮细胞(liver sinusoidal endothelial cells,LSEC)构成,肝细胞占肝脏细胞80%以上[2]。其作用主要表现在合成凝血因子和多种消化酶以及胆汁、调节内分泌、代谢储能、清除毒素等方面。肝细胞形态为多角形,直径约几十微米级,具有六至八个面。不同的生理条件下肝细胞大小有差异,在饥饿时肝细胞体积变大。每个肝细胞表面可分为窦状隙面、肝细胞面和胆小管面三种。肝细胞里面含有非常多复杂的细微结构:如肝细胞核、肝细胞质、线粒体、内质网、溶酶体、高尔基氏体、微粒体及饮液泡等组成[3]。然而,在实验中细胞株并不能满足所有的研究需求。本文主要是提供一种实用的肝细胞提取方式,为从事病毒性肝炎、肝硬化和肝癌方面。以及少数从事肝脏的遗传性代谢疾病、免疫性肝病、药物和化学中毒性肝病、肝血管性疾病等研究者提供一些参考。
1 材料和方法
1.1实验动物
SPF级10周龄C57BL/6J雄性小鼠2只,购自北京华阜康生物科技股份有限公司 [SCXK (京) 2014-0004]。实验前禁食12 h,小鼠手术及取材过程均在第三军医大学第一附属医院动物实验室内进行 [SYXK (渝) 2017-0011],按实验动物使用的3R原则给予人道主义关怀。
1.2主要试剂与仪器
VS-1300L-U型洁净工作台(中国苏州安泰空气技术有限公司);1300系列A2生物安全柜(美国Thermo公司);倒置BDS200-P型显微镜(中国重庆奥特光学仪器有限公司);FACSCalibur流式细胞仪(美国BD公司);Harvard 2000型精密注射泵(美国Harvard公司);CO2恒温细胞培养箱(美国Thermo公司);ST-40R台式离心机(美国Thermo公司);Nano Drop 2000分光光度计(美国Thermo公司);CPA2250型电子天平(德国Sartorius公司);蛋白电泳仪(美国Bio-Rad公司);ChemiDocTMXRS+超高灵敏度化学发光成像系统(美国Bio-Rad公司);TC20自动细胞计数仪(美国Bio-Rad公司);微量移液器(美国Millipore公司);Zeiss LSM 780激光扫描共聚焦显微镜(德国Zeiss公司);MS分离柱及MACS分离器(德国Milternyi Biotec公司);漩涡振荡器(中国上海科学仪器厂);电热恒温水浴箱(中国上海科学仪器厂)。
60 mL注射器,静脉输液针(规格0.7 mm),注射器针头,无菌大玻璃平皿,吸耳球,无菌10 mL玻璃吸管,无菌15 mL离心管,无菌1.5 mL离心管,无菌50 mL离心管,眼科手术剪,眼科镊(平口及有齿),酒精灯,止血钳,小动脉夹,微量移液器(规格1000 μL)。
1.2.1 肝细胞分离液I
D-Hank’s平衡溶液(不含钙、镁离子)250 mL为基础液,加入EDTA 46.5 mg和葡萄糖250 mg,振荡溶解后,经0.22 μm超滤,转入50 mL无菌离心管分装。
1.2.2 肝细胞分离液II
Hank’s平衡溶液(含钙、镁离子)250 mL为基础液,加入葡萄糖250 mg、HEPES 1191.5 mg和IV胶原酶40 mg,振荡溶解后,经0.22 μm超滤,转入50 mL无菌离心管分装。
1.2.3 肝细胞分离液III
Hank’s平衡溶液(含钙、镁离子)250 mL为基础液,加入辅助试剂葡萄糖250 mg、HEPES 1191.5 mg、IV胶原酶40 mg和DNase I 2.5 mg,振荡溶解后,经0.22 μm超滤,转入50 mL无菌离心管分装。
1.2.4 肝细胞分离用洗涤缓冲液
取100 mL PBS溶液,加入1 g BSA,振荡溶解后,经0.22 μm超滤,转入50 mL无菌离心管分装。
1.2.5 密度梯度离心液(10% OptiPrep)
无菌生理盐水(V/V=4∶2),即取4 mL OptiPrepTM加入2 mL无菌生理盐水,配成6 mL WS工作液,充分混匀,4℃避光,备用;配置5 mL的10% OptiPrep,即精确吸取1.25 mL WS工作液加入3.75 mL无菌生理盐水,至15 mL无菌离心管内混匀,4℃避光保存。
1.3实验方法
1.3.1 小鼠肝脏的原位灌洗
用60 mL注射器吸取已预温至37℃的原代肝细胞分离液I并连接好静脉输液针与注射器,并将注射器固定在注射泵插槽内,白炽手术灯距其约20 cm加热,进行保温。将预冻冰袋置于不锈钢托盘上。小鼠经脱臼处死后,立即用注射器针头固定四肢置于不锈钢托盘的冰袋上,用75%乙醇消毒腹部皮肤,“U”形切口剪开小鼠腹部、胸,并沿胸廓外沿剪开,完全剪开隔肌,暴露胸、腹器官,并可视心脏下腔静脉,用平口镊将腹部脏器向右外侧牵拉,暴露并识别肝门静脉。第一步灌洗,用止血钳结扎小鼠肝前静脉及心脏下腔静脉后,用静脉输液针穿刺肝后静脉,进入约5 mm,并同时用小动脉夹固定穿刺入针头前端约3 mm位置,剪开肝门静脉,随后开始灌注肝细胞分离液I,设定流速为6 mL/min,灌注体积为20 mL/只,灌流方向从肝后静脉进入,从肝门静脉流出,行逆行灌注;可见肝门静脉缺口有大量血液流出(如图1A),并逐渐减少,肝脏完全变为土灰色。第二步灌洗,待第一步灌洗结束后,随即改用已预温至37℃的原代肝细胞分离液II进行灌洗,设定流速为3 mL/min,灌注体积为20 mL/只,可见肝门静脉缺口已无血液流出,液体清亮,肝脏逐渐变为土黄色(如图1B,体积明显膨胀,用平口镊轻触肝脏表面可见不可复原小坑出现[4, 5]。
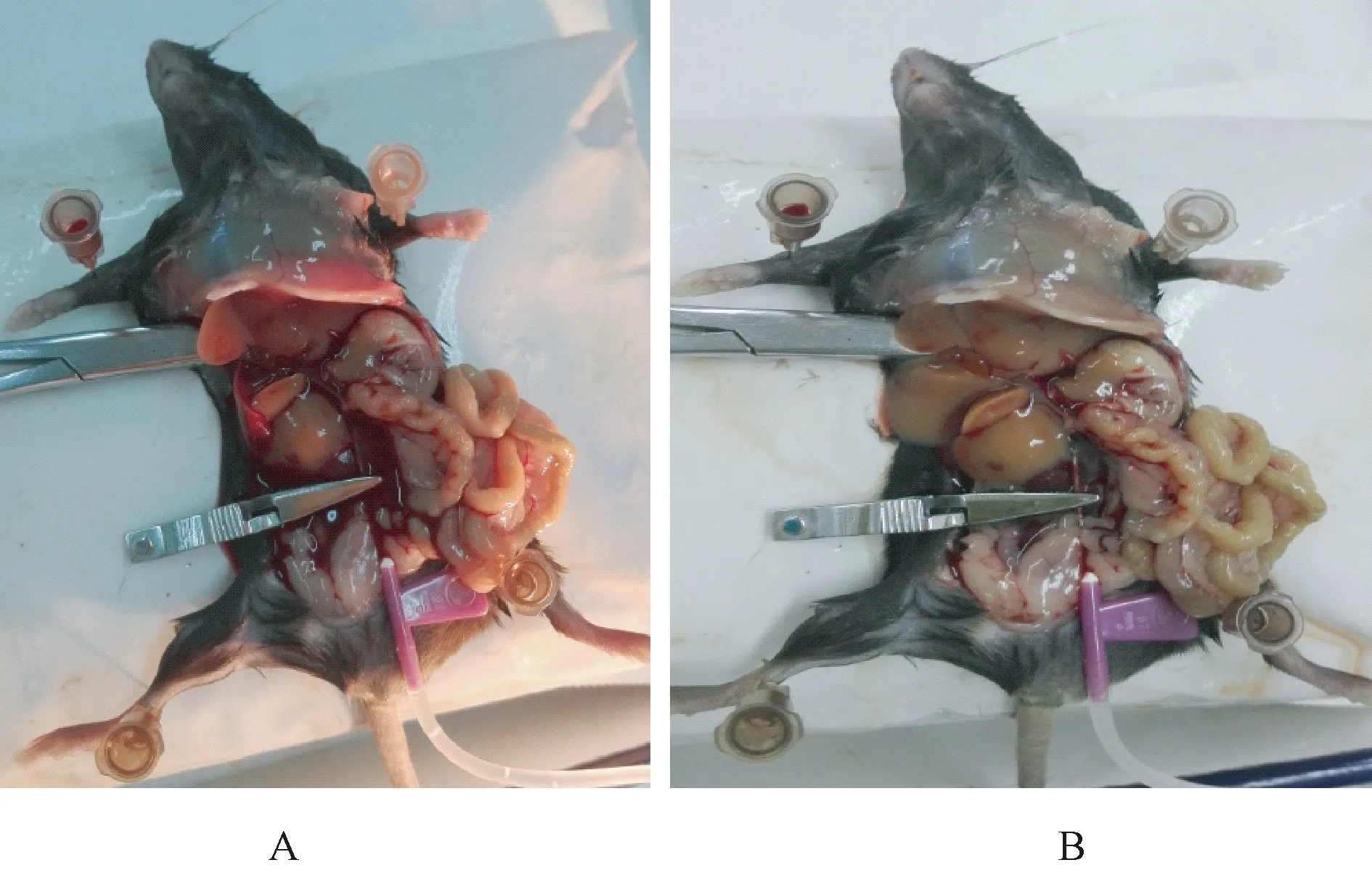
注:A:第一步灌洗开始;B:第二步灌洗结束。图1 小鼠肝脏原位灌洗示意图Note. A: Beginning of the first perfusion; B: Ending of the second perfusion.Fig.1 In situ liver perfusion of a mouse
1.3.2 小鼠肝脏的酶消化
用眼科手术剪无菌剥离全肝(去除胆囊部分),经4℃,含1% FBS的无菌PBS溶液漂洗后,迅速转至盛有已预热至37℃的肝细胞分离液III的15 mL大玻璃平皿;将小鼠肝脏经眼科剪剪至大小1 mm3后转入37℃水浴锅消化15 min;立即向每个肝脏加入5 mL DMEM培养基(含10% FBS)混匀,中止酶消化。
1.3.3 单细胞悬液的制备
消化处理后的肝组织悬液经100 μm细胞滤器过滤后,再经4℃的肝细胞分离用洗涤缓冲液补充体积至30 mL,4℃,750 r/min,5 min离心;吸弃上清,再加入5 mL肝细胞分离用洗涤缓冲液,4℃,750 r/min,3 min离心,洗涤2次,目视上清无明显浑浊出现。
1.3.4 肝细胞的密度梯度离心分离
沿管壁加入5 mL 10% OptiPrep,用微量移液器吹打至获得的细胞沉渣均匀分布,转移至无菌15 mL离心管内;再在上层加入5 mL肝细胞分离用洗涤缓冲液,不混匀,标记并立即进行4℃,750 r/min,10 min离心,吸弃上清后,再加入肝细胞分离用洗涤缓冲液2 mL,4℃,750 r/min,2 min离心洗涤,获得肝细胞。
1.3.5 原代肝细胞的贴壁培养
向获得的肝细胞沉淀中加入1 mL DMEM培养基(含10% FBS)后,混匀,用细胞计数板计算细胞浓度,按接种密度为2 × 105个/mL立即接种于预包被有大鼠鼠尾胶蛋白的六孔板或细胞培养皿中。每个培养皿所加培养基以视培养基厚度为1.6~1.8 mm为准,于37℃,5% CO2细胞培养箱中培养,2 h后细胞贴壁,吸弃上清,加入1 mL DMEM培养基(含10% FBS)小心洗涤未贴壁细胞,再加入DMEM培养基(含10% FBS),37℃,5% CO2细胞培养箱中继续培养(如图2)。

图2 肝细胞培养24 h后形态(× 40)Fig.2 Morphology of hepatocytes after culture for 24 h
1.3.6 TC20自动细胞计数仪计算
分离后获得的肝细胞纯度检测采用流式细胞检测技术,对FITC标记细胞角蛋白18(cytokeratin 18)抗体(FITC-At18)标记的肝细胞进行分析,即分离后的肝细胞悬液约100 μL,分别加入2支无菌15 mL离心管内,标记为阴性对照(negative control,NC)管和FITC-At18标记的肝细胞(FITC-At18-HC)管,再分别加入1 mL 4%多聚甲醛,4℃,避光固定15 min后,分别加入1 mL PBS溶液,混匀,4℃,750 r/min,3 min离心,如此洗涤3次;加入3% BSA,4℃,封闭30 min后,4℃,750 r/min,3 min离心,吸弃上清,再加入500 μL按FITC标记抗细胞角蛋白18抗体原液: 3% BSA(V/V)=1∶300稀释后的抗体,4℃,避光过夜孵育;次日,每次以1 mL PBS溶液进行洗涤,4℃,750 r/min,3 min离心,洗涤3次,再加入200 μL PBS溶液,进行流式细胞仪检测。
1.3.7 原代肝细胞的活力分析
分离肝细胞的活力分析(台盼蓝拒染实验):取0.2 mL 4%台盼蓝母液,加入1.8 mL PBS溶液中,稀释为0.4%作为台盼蓝工作液。取分离后的原代肝细胞悬液约100 μL加入1支无菌1.5 mL离心管内,加入0.9 mL 0.4%台盼蓝工作液,3 min染色后,利用TC20自动细胞计数仪计数未被染色的细胞数,得活细胞数及活细胞率。
2 结果
2.1纯度分析
通过TC20自动细胞计数仪计算,细胞浓度为5.95 × 105个/mL;从检测结果来看,红色为NC组,蓝色为FITC-At18-HC组,测得FITC-At18-HC组阳性细胞百分比为91.3%,表明初次分离获得原代肝细胞纯度为91.3%(见图3)。

图3 分离肝细胞的纯度测定Fig.3 Purity analysis of the isolated hepatocytes
2.2活力分析
通过台盼蓝拒染实验,测得初次分离的原代肝细胞在未贴壁培养前的存活率为90.5%(见图4)。
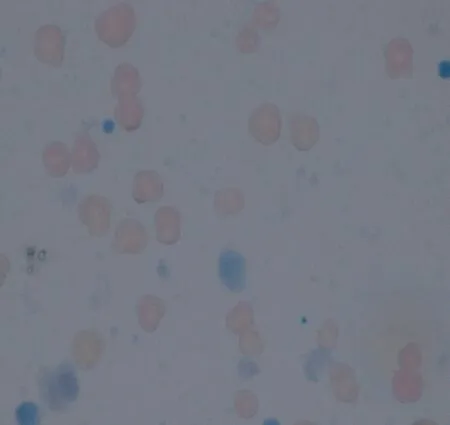
图4 台盼蓝拒染实验测定细胞活力(× 40)Fig.4 Cell viability determined by trypan blue exclusion test
3 讨论
肝脏是生理和病理状态下能量代谢、毒素的生物转化以及血浆蛋白合成的中心器官,是机体最重要的器官之一[6]。肝细胞培养体系可以很好地模拟体内肝脏生理环境,作为研究肝特异代谢过程和肝脏功能的重要工具,被广泛用于毒理学和药理学的研究[7, 8]。因此,建立和改进实验动物肝细胞的提取方法具有重要意义。
从实验对象来看,目前常规的肝细胞提取操作大多在大鼠中开展。主要原因是大鼠体型相对较大,且实验易操作,获取的肝细胞产量较高。然而目前大多数基因敲除或转基因模型均在小鼠中建立,因此优化小鼠肝细胞提取技术对开展生命科学相关研究更具意义。从操作流程来看,常规肝细胞提取主要采用胶原酶浸泡的方法消化组织。该方法虽然操作简单(无需灌注),但是浸泡消化的时间和强度不易掌握,得到的肝细胞质量不好(活力一般低于80%)[9],不能满足有些实验的需求。因此本研究选择了操作复杂但效果更好的酶灌注消化法。灌流在肝细胞提取中又是非常重要的环节,直接决定实验所获取细胞的质量。在实际操作中我们发现,小鼠门静脉非常细小,不易穿刺。经过多次摸索,我们在两步灌洗法的基础上,优化出一种更易操作的方法,即采用下腔静脉进、门静脉出的方式。下腔静脉相对门静脉更粗,因此方便穿刺操作。该改良方法相对降低了实验的操作难度,降低了对实验材料的要求(常见的静脉输液针即可满足需求)。同时经改法获得的肝细胞纯度和活力均在90%以上,能够满足大多数的实验需求。在实验中我们也发现,该方法的主要不足之处在于灌流液体可从门静脉流出,因而增大了细胞污染的几率,故要求实验者在操作时应小心谨慎。课题组在传统肝细胞提取方法的基础上,改变了灌流方式,得到了良好的实验结果,为从事相关研究者提供参考。同时,建立和完善肝细胞长期培养技术将为人工生物肝脏研究及其临床应用提供技术参考,具有重要意义。
[1] Strnad P, Tacke F, Koch A, et al. Liver—guardian, modifier and target of sepsis [J]. Nat Rev Gastroenterol Hepatol, 2017, 14(1): 55-66.
[2] 杨东, 刘鑫, 郑新川, 等. 小鼠肝脏细胞分离和原代培养技术研究进展 [J]. 重庆医学, 2015, 44(34): 4851-4854.
[3] Ueno T, Komatsu M. Autophagy in the liver: functions in health and disease [J]. Nat Rev Gastroenterol Hepatol, 2017, 14(3): 170-184.
[4] 彭齐荣, 袁爱力, 赖卓胜, 等. 肝细胞的大量制备技术 [J]. 中华肝脏病杂志, 1999, 7(4): 246.
[5] 刘学忠, 李慧敏, 王富民, 等. 大鼠肝细胞分离和原代培养的简易方法 [J].江苏农业学报, 2009, 25(1): 222-224.
[6] Liu W, Hou Y, Chen H, et al. Sample preparation method for isolation of single-cell types from mouse liver for proteomic studies [J]. Proteomics, 2011, 11(17): 3556-3564.
[7] Vinken M, Maes M, Oliveira AG, et al. Primary hepatocytes and their cultures in liver apoptosis research [J]. Arch Toxicol. 2014, 88(2): 199-212.
[8] Shulman M, Nahmias Y. Long-term culture and coculture of primary rat and human hepatocytes [J]. Methods Mol Biol, 2013, 945: 287-302.
[9] 王琳, 徐建波, 田元, 等. 一种分离新生小鼠肝细胞的简单方法 [J]. 中国优生与遗传杂志, 2007, 15(1): 10-12.
Asimplifiedmethodforisolationandcultureofprimarymousehepatocytes
FAN Shi-jun, LIU Xin, YANG Dong, ZHU Yuan-feng, LU Yong-ling, ZHENG Jiang*
(Medical Research Center, First Affiliated Hospital, Third Military Medical University, Chongqing 400038, China)
ObjectiveTo simplify and optimize the method for isolation and culture of primary mouse hepatocytes on the basis of conventional extraction method, and to provide a reference for related research.MethodsMouse liver was reversely perfused with the isolation solution (i.e., through the vena cava inferior in, and portal vein out), cut into small pieces and digested with enzymes. Then the hepatocytes were isolated by density gradient centrifugation and transferred into culture medium. The cell viability was detected by trypan blue staining. The purity of the hepatocytes was analyzed by flow cytometry and the cell morphology was observed with an inverted microscope.ResultsThe hepatocytes obtained by this improved method showed high viability and purity, with typical characteristics of cell morphology.ConclusionsThe liver perfusion is facilitated by reversed perfusion, and the isolated hepatocytes are with high viability and purity confirmed by many times of experiments. This optimized procedure is an easy and efficient method for isolation of primary mouse hepatocytes.
C57BL/6J mice; Hepatocytes; Reversed perfusion; Viability; Purity
国家自然科学基金项目(编号:81372089)。
范仕郡(1983 -),男,助理研究员,研究方向:脓毒症的发病机制与拮抗措施研究。E-mail: 574472439@qq.com
郑江(1961 -),男,研究员,研究方向:脓毒症的发病机制与拮抗措施研究。E-mail: zhengj@tmmu.edu.cn
R-33
A
1671-7856(2017) 11-0075-05
10.3969.j.issn.1671-7856. 2017.11.015
2017-03-20
