响应面法优化克氏原螯虾虾壳中乙酸钙的提取工艺
2017-11-21,,,,*,,
,, , ,*,,
(1.中国水产科学研究院 长江水产研究所,湖北武汉 430223; 2.农业部风险评估实验室(武汉),湖北武汉 430223)
响应面法优化克氏原螯虾虾壳中乙酸钙的提取工艺
喻亚丽1,2,周运涛1,2,文平1,2,何力1,2,*,周殿芳1,2,吕磊1,2
(1.中国水产科学研究院 长江水产研究所,湖北武汉 430223; 2.农业部风险评估实验室(武汉),湖北武汉 430223)
为进一步利用虾壳资源,以克氏原螯虾虾壳为原料,采用乙酸提取法从虾壳中进行乙酸钙的提取,探讨了乙酸浓度、液料比、温度和时间4个因素对虾壳钙提取的影响,在此基础上利用响应面法研究各自变量及其交互作用对虾壳中钙提取率的影响。结果表明,影响钙提取率的因素大小顺序为:液料比>温度>乙酸的浓度>酸解时间。乙酸钙提取最优条件是乙酸浓度73.60 g/L,反应时间3 h,反应温度65 ℃,液料比11.60∶1 (mL/g),在此条件下,得到克氏原螯虾虾壳中钙的得率为20.45%。此工艺下钙的得率较高,成本较低。本研究为以虾壳为钙源进行乙酸钙生产提供了技术参考。
克氏原螯虾,乙酸,响应面法,乙酸钙
克氏原螯虾(Procambarusclarkii)俗称小龙虾,隶属甲壳纲(Crustacea),十足目(Decapoda),螯虾科(Cambaridae),原螯虾属(Procambarus)[1]。克氏原螯虾食性广、生长速度快、繁殖力和适应能力强,是目前我国重要的经济水产养殖品种之一[2]。据渔业统计年鉴统计,2014年我国小龙虾产量高达6.60万t,出口额达3.8亿美元。
目前,克氏原螯虾主要以加工成冻熟制虾仁、冻熟整虾的形式进行生产、销售。在加工和食用小龙虾的过程中产生了大量的固体废弃物,这些废弃物的直接丢弃不仅给环境带来了严重的污染,也是一种资源的巨大浪费[4]。研究发现,虾壳中含有丰富的虾青素、蛋白质、甲壳素、钙、不饱和脂肪酸、脑磷脂、卵磷脂等营养成分[5-7]。虾黄含有良好风味物质,是提取风味化合物的一种重要来源[8]。因此,充分利用虾壳、虾头这些优质资源,开发相关副产品,不仅可以增加产品的附加值,还对保护环境具有重要意义。
虾壳是含钙量很高的天然食物成分之一,是一种优质的钙源[9]。目前从虾壳中提取钙的方法主要有:煅烧法、直接中和法和酶法。利用煅烧法,能耗大,成本高,过程复杂,而且在煅烧过程会产生大量的废气,带来严重的环境污染[10]。以直接中和法从虾壳中提取钙是使用强酸、强碱,该方法不仅会带来严重的环境污染而且还会降低虾壳中甲壳素的聚合度和质量,最终会影响到虾壳的综合利用[11-12]。利用酶法提取对虾虾壳钙,该方法反应温和,对环境污染较小,但该方法提取的虾壳钙含量较低,仅有12.33%[13]。因此,利用有机酸进行钙的提取备受关注,该方法不仅简单易操作,提取成本低,而且对环境影响较小,产物也具有广泛的应用前景[14]。乙酸钙属于有机酸钙,具有溶解性比无机酸钙要好、pH近中性、对胃肠刺激较小、吸收利用好等方面的优点[15],在临床、食品工业上都有广泛的应用。目前制备乙酸钙主要通过直接法和间接法,间接法是经高温煅烧石灰石同乙酸进行反应[16];直接法是利用碳酸钙与乙酸进行反应[17]。因此,利用虾壳代替碳酸钙开发相关的乙酸钙产品逐步成为该领域的研究热点。
现有研究表明,酸的浓度、酸解的温度、时间以及液料比对虾壳钙的酸解的工艺和钙的提取率都有一定的影响。本文采用乙酸酸解的方法制备乙酸钙,通过单因子实验,研究乙酸的浓度、酸解温度和时间、液料比对虾壳钙的得率的影响,并通过响应面法优化制备乙酸钙的工艺条件。以期为克氏原螯虾虾壳综合利用提供一种环保、高产、高附加值的技术支持。
1 材料与方法
1.1材料与仪器
克氏原螯虾 武汉市新竹路菜市场;去离子水 实验室自制;乙酸、氨水、乙二胺基四乙酸二钠、铬黑T、氯化铵 国药集团,分析纯试剂。
DHG-9003BS电热恒温鼓风干燥箱 上海新苗;滴定仪 瑞士万通;HH6电热恒温水浴锅 国华电器有限公司;粉碎机 上海顶帅电器有限公司。
1.2实验方法
1.2.1 虾壳粉的制备 取克氏原螯虾除去全部肉质,虾壳用蒸馏水反复清洗,直至无浮液,置于100 ℃鼓风干燥箱中烘干24 h。将干燥好的虾壳用粉碎机进行粉碎,过100目筛,贮存备用。
1.2.2 虾壳营养成分分析 水分含量测定:采用常压干燥法(GB 5009.3-2010),粗蛋白含量测定:采用凯氏定氮法(GB 5009.5-2010),粗脂肪含量测定:采用索氏抽提法(GB/T 5009.6-2003),灰分含量测定:采用灼烧称重法(GB 5009.4-2010)。
1.2.3 制备乙酸钙的工艺流程 称取一定量粉碎后的虾壳粉,按比例加入乙酸混合均匀,置于水浴锅上,在不同的酸解温度、酸解时间、乙酸浓度、液料比条件下进行酸解反应。待反应结束后,用蒸馏水定容酸解液至25 mL。然后进行钙得率的测定。
1.2.4 钙得率的测定 取酸解液1 mL于锥形瓶中,加入9 mL去离子水,再分别加入3 mL三乙醇胺和4 mL氨性溶液,加入铬黑T指示剂约0.05 g,再用标定过的EDTA溶液滴定至溶液由紫红色转变为蓝色。记录EDTA的消耗量,并计算钙的得率w。钙的得率计算公式[18]:
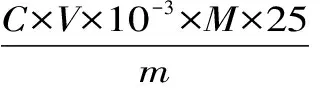
式中:C-标准EDTA溶液的浓度,mol/L;V-滴定钙元素总量消耗的EDTA溶液的体积,mL;M-钙的相对分子质量,g/mol;m-称取的样品量,g。
1.3单因素实验
1.3.1 温度对钙得率的影响 取0.50 g虾壳粉,按照10∶1 (mL/g)的液料比,加入50 g/L的乙酸5 mL。分别置于45、55、65、75、85 ℃的水浴锅中进行酸解反应1 h,将酸解液定容,测定钙的得率。
1.3.2 酸解时间对钙得率的影响 取0.50 g虾壳粉,按照10∶1 (mL/g)的液料比,加入50 g/L的乙酸5 mL,置于75 ℃水浴锅中进行酸解反应,分别反应2、3、4、5、6 h,将酸解液定容,测定钙的得率。
1.3.3 液料比对钙得率的影响 取0.50 g虾壳粉,分别按照6∶1、8∶1、10∶1、12∶1、14∶1 (mL/g)的液料比,加入50 g/L的乙酸3、4、5、6、7 mL,置于75 ℃的水浴锅进行酸解反应3h,将酸解液定容,测定钙的提取率。
1.3.4 乙酸浓度对钙得率的影响 取0.50 g虾壳粉,按照10∶1 (mL/g)的液料比,分别加入10、30、50、70、90、110 g/L的乙酸5 mL,置于75 ℃的水浴锅进行酸解反应3 h,将酸解液定容,测定钙的得率。
1.4响应面法优化钙得率工艺的实验
根据单因素实验结果,选择乙酸浓度、液料比、酸解温度、酸解时间4个因素与钙的得率进行响应面实验设计,优化虾壳中乙酸钙的提取工艺,设计因素水平见表1。
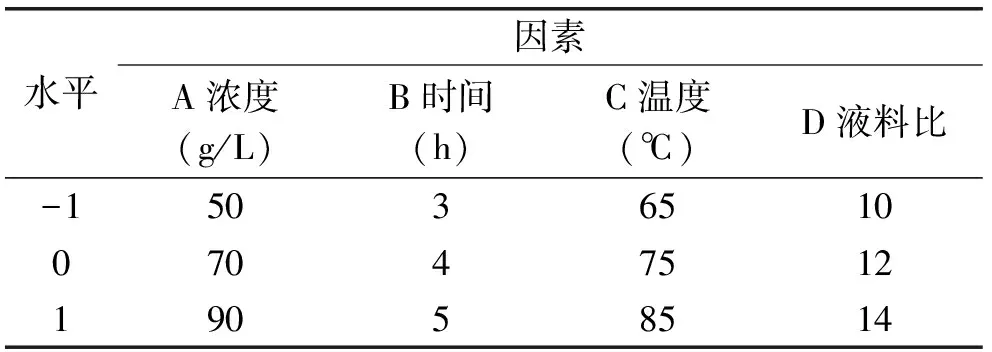
表1 响应面因素与水平表Table 1 Factors and levels table of response surface methodology
1.5数据统计分析
实验数据方差分析采用SPSS 19.0软件进行处理,利用Design Expert 8.0.5b对实验数据进行回归分析。
2 结果与分析
2.1基本营养成分

表2 克氏原螯虾虾壳基本营养成分(以鲜重计%)Table 2 The general nutritional of the shrimp shell(by wet weight %)
克氏原螯虾虾壳中的基本营养成分如表2所示,其中水分含量为36.21%、灰分含量高达31.74%、粗蛋白含量为4.92%、粗脂肪含量为6.57%。克氏原螯虾虾壳中的灰分高达31.74%,远远高于南极磷虾虾头和虾壳中的12.48%、14.26%[19],凡纳对虾虾壳中的灰分含量较高有20.11%[20]。克氏原螯虾虾壳中灰分含量较高,虾壳灰分中的主要成分是碳酸钙[21]。因此提取虾壳中的钙成分,充分利用克氏原螯虾虾壳中的钙资源,是开展克氏原螯虾虾壳废弃物综合利用的有效途径。
2.2虾壳中钙提取单因素实验
2.2.1 酸解温度对钙得率的影响 温度影响化学反应的速率,随着温度的上升,分子运动加剧,加大了分子间的碰撞几率,从而影响钙的得率。由图1可知,随着酸解温度的上升,钙的得率也不断的升高。当酸解温度达到75 ℃时,钙的得率达到最大,此时钙的得率为12.34%。继续增加酸解温度,钙的得率反而会下降。这可能是由于随着温度继续的升高,乙酸分子的运动速度加快,导致乙酸大量的挥发,从而使得乙酸的实际浓度下降,进而影响钙的得率[22]。
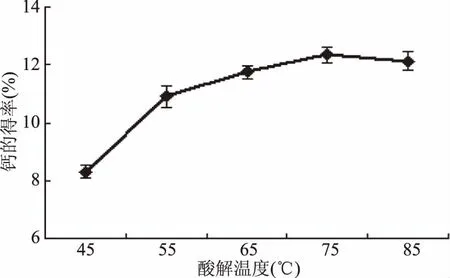
图1 酸解温度对钙得率的影响Fig.1 Effect of temperature on extraction yield of calcium
2.2.2 酸解时间对钙得率的影响 由图2可知,虾壳粉中钙的得率随时间的延长而增大,当酸解反应达到4 h时,钙的得率达到最大,为18.02%。随着酸解时间的延长,钙的得率开始下降。这可能是由于随着酸解反应进行的同时,乙酸也有一定的挥发,从而使反应系统中的乙酸浓度下降,使反应向逆反应方向进行,从而使钙的得率有下降的趋势。

图2 酸解时间对钙得率的影响Fig.2 Effect of time on extraction yield of calcium
2.2.3 液料比对钙得率的影响 由图3可知,当虾壳粉的量一定时,随着反应体系中乙酸用量的增加,钙的得率随之变大,当液料比达到12∶1时,钙的得率达到最大,为20.11%。继续增加乙酸的用量,钙的得率呈下降趋势。这可能是由于在液料比达到12∶1时,用乙酸从克氏原螯虾虾壳中提取乙酸钙已经达到了一种平衡状态,继续增加乙酸的量对钙的提取影响不大。因此,液料比最佳为12∶1。
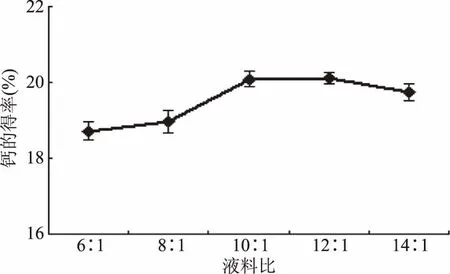
图3 液料比对钙得率的影响Fig.3 Effect of ratio of liquid to solid on extraction yield of calcium
2.2.4 乙酸浓度对钙得率的影响 由图4可知,当乙酸浓度增加到70 g/L时,钙的得率增加到最大。继续增大乙酸浓度,钙的得率呈下降的趋势。这可能是由于当乙酸浓度不断增大时,乙酸中的氢离子不能完全游离出来与碳酸钙进行反应[23],从而导致虾壳粉中钙的得率下降。因此,乙酸的最佳浓度为70 g/L。

图4 乙酸浓度对钙得率的影响Fig.4 Effect of acetic acid concentration on extraction yield of calcium
2.3响应面法优化钙提取率工艺
2.3.1 响应面法优化实验结果 表3列出了乙酸进行酸解提取钙的实验设计、结果及其预测值。利用Design-Expert 8.05b对表3中的实验数据进行多元回归拟合,得到钙的得率(Y)对自变量乙酸浓度(A)、酸解时间(B)、酸解温度(C)、料液比(D)的二次回归模拟方程:
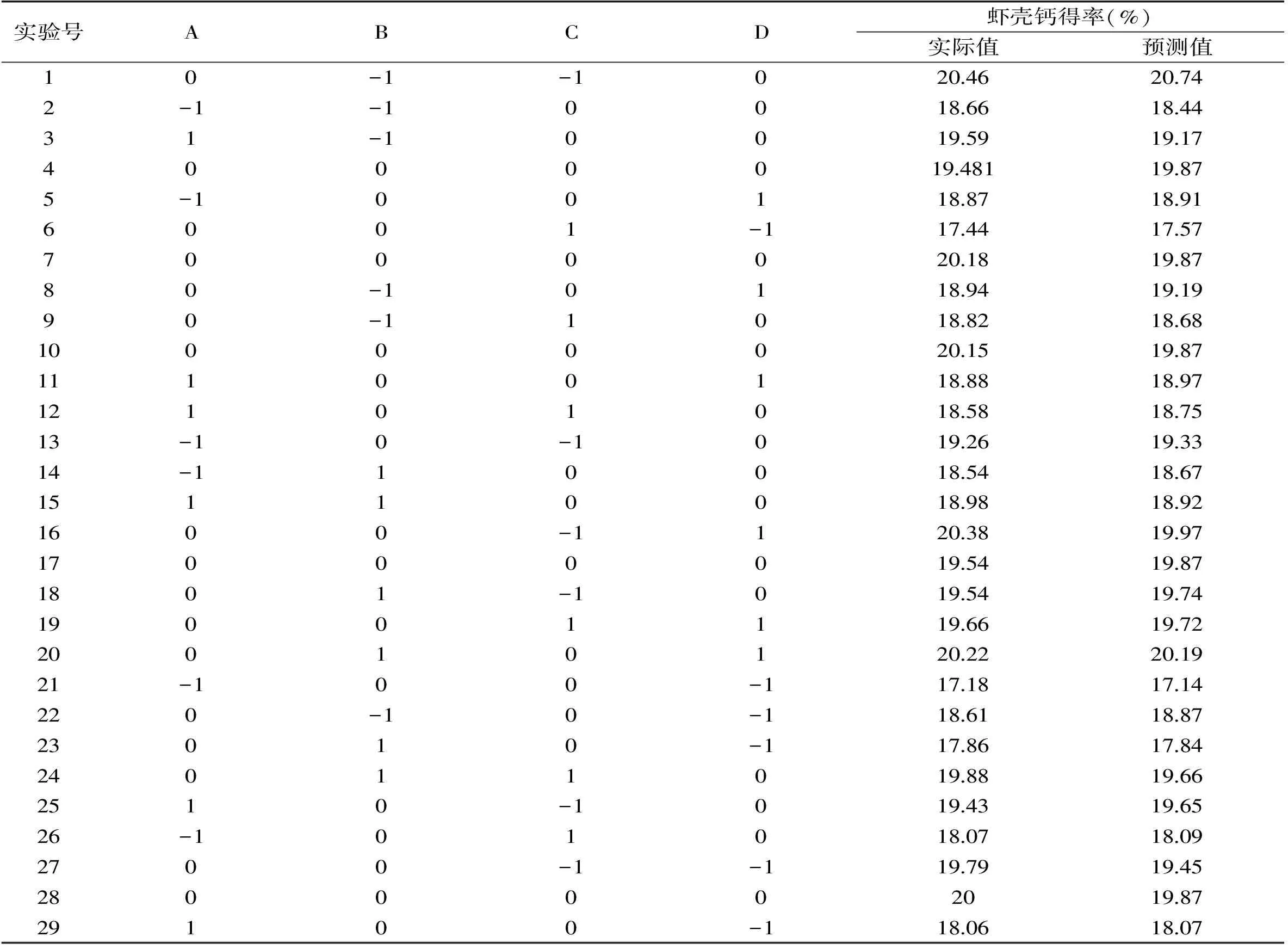
表3 响应面试验设计及结果Table 3 Experimental design and corresponding results for response surface analysis
Y=19.87+0.245A-0.005B-0.534C-0.668D-0.123AB+0.085AC+0.218AD+0.495BC-0.508BD-0.408CD-0.910A2-0.1620B2-0.009C2-0.686D2。
对该回归模拟方程进行方差分析和差异显著性检验,结果见表4。
由表4可知模型的F=14.262,p<0.0001,表明该实验的二次回归模型是极显著的;失拟项F=0.8442,p=0.625>0.05,该失拟项不显著;实验无失拟因素存在,能充分反映实际情况;决定系数R2=0.9345,表明响应值表中93.45%来源于所选因素;精密度是有效信号与噪声的比值,大于4.0视为合理,本实验精密度达到15.765。因此,该模型的拟合度较好,能充分反映出各因素与响应值之间的关系,可以用该模型对钙的得率结果进行分析和预测。
回归方程中的一次项C、D,交互项BC、BD及二次项A2、D2对钙的得率影响极显著(p<0.01),一次项A、交互项CD对钙的得率影响较显著(p<0.05)。因此,实验因素对钙的得率的影响不是简单的线性关系。各因素对响应值的影响的顺序为D>C>A>B,即液料比对钙的得率影响最大,其次是温度和乙酸的浓度,酸解时间对钙的得率的影响最小。
2.3.2 响应面结果分析 根据多元二次回归模型得到响应面和等高线图,响应面图是响应值对应的实验因素A、B、C、D所构成的三维空间曲线图。将两个因素固定在零水平,考察另外两个因素交互对钙得率的影响。曲线的走势能反映因素对钙得率的影响,曲线走势越陡峭,表明响应值对因素改变越敏感,该因素对钙得率的影响越大;反之则越小[24-26]。

表4 响应面实验方差分析Table 4 The variance analysis of response surface
注:*表示p<0.05,差异显著;**表示p<0.01,差异极显著。
2.3.2.1 乙酸浓度和酸解时间的交互作用对虾壳中钙得率的影响 由图5可知,酸解时间相同,当乙酸浓度在50~70 g/L时,随着乙酸浓度的升高,钙的得率增大。因为乙酸与虾壳粉的反应为非均相反应,随着乙酸浓度的增加,虾壳中碳酸钙单位表面积上的乙酸浓度也随之增大,单位体积内活化分子数增加,虾壳中钙的得率不断的增加。当进一步增加乙酸的浓度,钙的得率反而下降。这可能与乙酸是挥发性酸有关,当乙酸浓度达到一定值时,继续增大乙酸的浓度,其挥发性也随之增加,使实际参与反应的乙酸的浓度反而减小[22],从而使钙的得率降低。

图5 乙酸浓度和酸解时间对钙得率的影响Fig.5 Effect of the concentration of acetic acid and time on extraction yield of calcium
乙酸浓度一定时,酸解时间在3~4 h时,随着酸解时间的延长,钙的得率缓慢提高;之后随着酸解时间的延长,钙的得率则缓慢下降。这可能是由于酸解反应进行的同时,乙酸有一定的挥发,从而使反应系统中的乙酸浓度下降,使反应向逆反应方向进行,最终使钙的得率有下降的趋势。范峥以废弃牡蛎壳为原料制备食品级醋酸钙研究发现,反应时间对醋酸钙的含量影响显著,醋酸钙含量及收率随着反应时间的增加而延长,当反应时间大于150 min时,醋酸钙的含量及收率无明显变化[27]。本研究关于酸解时间对钙的得率的影响同范峥的研究结果一致。
2.3.2.2 乙酸浓度和酸解温度的交互作用对虾壳中钙的得率的影响 由图6可知,当乙酸浓度一定时,随着酸解温度的升高,钙的得率一直呈下降趋势。这可能是由于随着温度的升高,乙酸分子的运动速度加快,导致乙酸大量的挥发,从而使得参与到反应中乙酸的实际浓度下降,进而导致钙得率的下降。同时,由于酸解反应温度的升高,也会使钙盐的水溶性下降,最终导致钙的得率下降[28]。
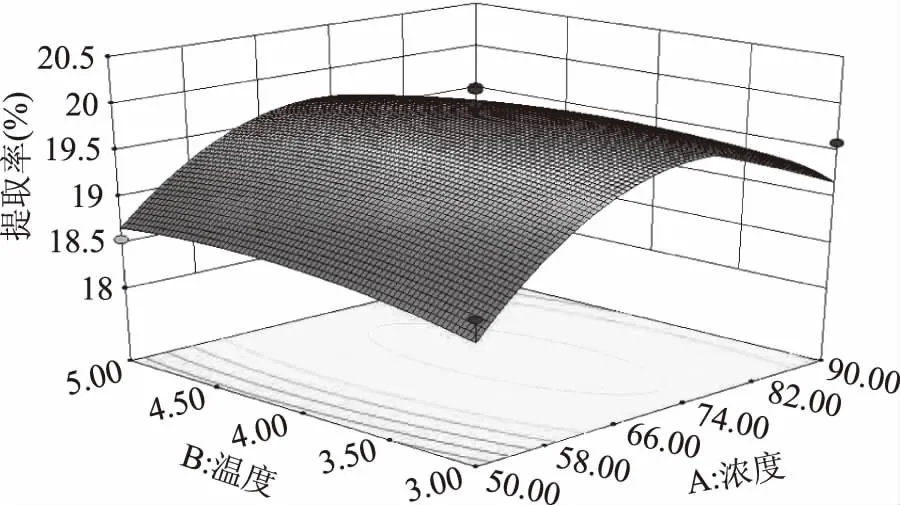
图6 乙酸浓度和酸解温度对钙得率的影响Fig.6 Effect of the concentration of acetic acid and temperature on extraction yield of calcium
2.3.2.3 乙酸浓度和料液比对钙得率的影响 液料比为13∶1时,钙的提取率达到极值,之后随着液料比的增加而钙的得率变化不大。这可能是由于当液料比增加到一定的值,钙的得率趋于稳定,反应趋于完全,增加反应体系中乙酸的量,对虾壳中钙的得率影响不大。该研究结果与刘洪玲的研究结果一致[29]。

图7 乙酸浓度和液料比对钙得率的影响Fig.7 Effect of the concentration of acetic acid and ratio of liquid to solid on extraction yield of calcium
2.3.2.4 酸解时间和温度对虾壳中钙的得率的影响 由图8可知,时间和温度的交互作用极显著。随着温度的上升和酸解时间的延长,钙的得率一直在下降。
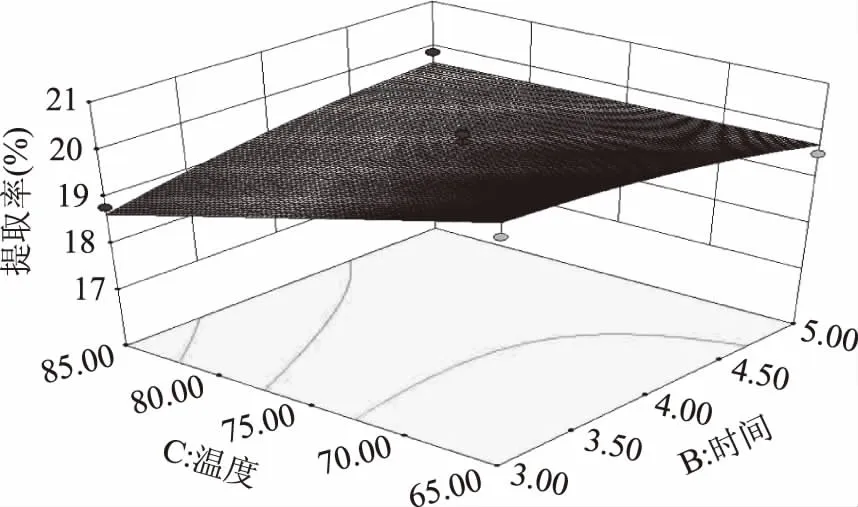
图8 酸解时间和酸解温度对钙得率的影响Fig.8 Effect of time and temperature on extraction yield of calcium
2.3.2.5 酸解时间和液料比对钙的得率的影响 由图9可知,酸解时间和液料比的交互作用显著。随着酸解时间的延长,钙的得率一直在下降。当液料比在12∶1~14∶1之间时,随着酸解时间的延长,钙的得率逐渐增大。
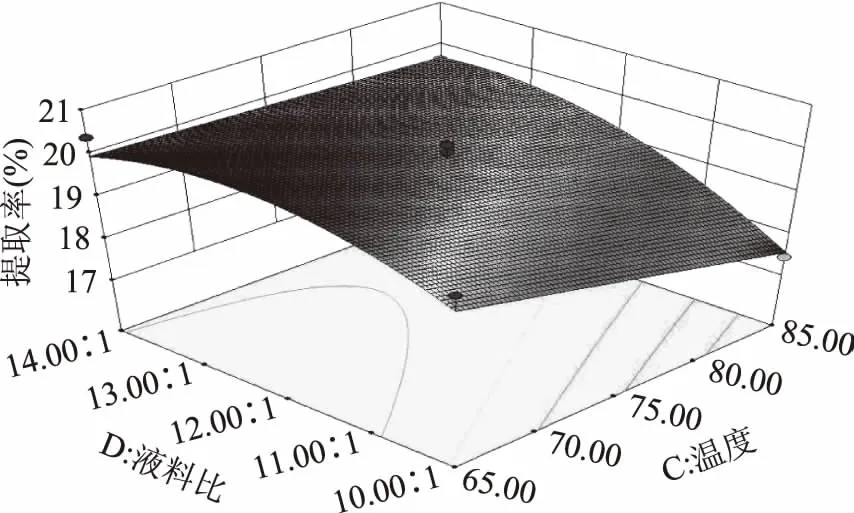
图9 酸解时间和液料比对钙得率的影响Fig.9 Effect of time and ratio of liquid to solid on extraction yield of calcium
2.3.2.6 酸解温度和液料比对钙得率的影响 由图10可知,温度和液料比的交互作用显著。随着液料比的增加,钙的得率也不断的增大;当料液比增大到12∶1时,继续增加液料比,钙的得率反而下降。随着反应体系温度的升高,钙的得率不断的下降,这可能是由于温度的升高,乙酸的大量挥发,从而使乙酸的浓度下降,最终导致钙得率的下降。

图10 酸解温度和液料比对钙得率的影响Fig.10 Effect of temperature and ratio of liquid to solid on extraction yield of calcium
2.4最佳工艺参数确定及验证性实验
用Design-Expert 8.05b软件对二次多项式回归方程进行计算,确定最合适的工艺条件为:浓度73.58 g/L,反应时间3 h,反应温度65 ℃,液料比为11.58∶1 (mL/g),此条件下乙酸钙的得率为20.79%。考虑实际操作的局限性,工艺最终修正为:浓度为73.60 g/L,反应时间为3 h,反应温度为65 ℃,液料比为11.60(mL/g)条件下进行验证实验,经过3组平行实验得到克氏原螯虾虾壳中的钙的得率为20.45%。
3 讨论
乙酸钙极易溶于水,是水溶性最高的一种钙剂,具有有效钙含量高、吸收利用率好、补钙效果快等特点,目前广泛应用于医药化工及食品领域。
本实验利用乙酸对克氏原螯虾虾壳中的钙进行提取,最佳的钙的得率为20.45%。该方法钙的得率较高,而且对环境的影响较小。王迪将虾头虾壳进行高温煅烧,后进行酸溶,与柠檬酸钠反应从而提取柠檬酸钙,最终生成柠檬酸钙的质量高达7.49 g。该方法产率较高,但过程繁琐,增加了能量的消耗,进行工业化生产的成本也较高[30]。王大巾利用菠萝蛋白酶从对虾虾壳中进行钙的提取,在0.65 g/100 mL的菠萝酶水解上清液中钙的提取率为12.33%[13]。使用酶法进行虾壳中钙的提取,该反应温和,环境污染较小,但对钙的提取率较低,而且反应的条件不易于控制。魏颖采用乳酸提取法从虾壳中提取乳酸钙,经研究发现,乳酸钙的最高提取量达7.62%[31]。与以往工艺相比,该方法耗能较低,反应时间较短,具有良好的研究前景。但该方法提取得到的乳酸钙溶解度较低仅有70 mg/100 mL,人体吸收利用率仅有32%[32]。因此,使用该方法提取得到的乳酸钙作为补钙制剂时,不利于钙的吸收利用。陈珊珊等采用盐酸法提取南美白对虾虾壳中的钙,其中虾壳钙的最佳提取率为9.4%[33]。该方法在提取过程中使用了盐酸,当将该法大量应用于工业生产中,不仅会带来环境污染,而且该方法得到的钙的提取率也略低。
本方法使用乙酸进行提取,不但可以降低因大量使用无机酸给环境带来的影响,还可以提高资源利用率。通过该方法制得的乙酸钙具有较高的溶解度(3850 mg/100 mL)和人体吸收利用率(78.51%)[32],具有较好的开发利用前景。同时利用响应面法对乙酸钙的提取工艺进行优化,得到的工艺条件合理可行,可以进一步应用于工业化生产中。因此,本研究选用乙酸进行虾壳中钙的提取该制备工艺可显著节能减排,又兼具高值化利用克氏原螯虾加工废弃物的双重功效,产品具有较好的推广应用潜力。
4 结论
响应面法分析结果可见:酸解反应时间和反应温度,酸解时间和液料比的交互作用对钙的得率影响极显著;酸解温度和液料比的交互作用对钙的得率影响较显著;乙酸浓度和酸解时间,乙酸浓度和液料比,乙酸浓度和温度的交互作用对钙的得率影响不显著。
响应面法优化克氏原螯虾虾壳中乙酸钙的提取实验,在最佳工艺条件:浓度73.58 g/L,反应时间3 h,反应温度65 ℃,液料比为11.58∶1 (mL/g),此条件下乙酸钙的得率为20.79%。考虑实际操作的局限性,工艺最终修正为:浓度为73.60 g/L,反应时间为3 h,反应温度为65 ℃,液料比为11.60∶1 (mL/g)条件下得到克氏原螯虾虾壳中的钙的得率为20.45%。
[1]丁建英,康琎,徐建荣. 东北螯虾和克氏原螯虾肌肉营养成分比较[J]. 食品科学,2010,31(24):427-431.
[2]汤靓颖. 小龙虾产业发展研究[J]. 现代农业科技,2009(22):306-309.
[3]CRUSTACEAN F.ranching and culture[M]. 2nd edn. Oxford:Blackwell Science Ltd,2002:181-199.
[4]罗梦良,钱名权. 虾仁加工废弃物的头、壳的综合利用[J].淡水渔业,2003,33(6):59-60.
[5]Fanimo AO,Oduguwa OO,Onifade AO,et al. Protein quality of shrimp-waste meal[J]. Bioresource Technology,2000,72:185-188.
[6]Sachindra NM,Mahendrakar NS. Process optimization forextraction of carotenoids from shrimp waste with vegetable oils[J].Bioresource Technology,2005,96:1195-1200.
[7]Rødde RH,Einbu A,Vårum K M. A seasonal study of the chemical composition and chitin quality of shrimp shells obtainedfrom northern shrimp(Pandalus borealis)[J]. Carbohydrate Polymers.doi:10.1016/j.carbpol.2007.06.006.
[8]BABU CM,CHAKRABARTI R,SAMBASIVARAOK RS. Enzymatic isolation of carotenoid-protein complex from shrimp head waste and its use as a source of carotenoids[J]. LWT,2008,41:227-235.
[9]秦燕,林炜,宁正祥,等. 虾壳钙蛋白的生物利用率研究[J]. 食品科学,1996,17(12):42-45.
[10]李峰. 以牡蛎壳为原料制备食品级添加剂丙酸钙的工艺研究[D]. 西安:西北大学图书馆,2008.
[11]Mahmoud NS,Ghaly AE,Arab F. Unconventional approach for demineralization of deproteinized crustacean shells for chitin production[J].American Journal of Biochemistry and Biotechnology,2007,3:1-9.
[12]李亚楠,王海滨,王琦. 小龙虾副产物中钙的提取条件研究[J]. 武汉工业学院学报,2013,32(2):19-21.
[13]王大巾,何露,祁鹏飞,等. 利用菠萝蛋白酶提取对虾虾壳蛋白质和钙的工艺研究[J]. 浙江理工大学学报(自然科学版),2016,35(2):304-308.
[14]韩凯宁,王盼盼,林海,等. 有机酸中虾壳中钙的溶出特性研究[J]. 广州化工,2013,41(8):71-72.
[15]李久成. 醋酸钙的保健及医疗功能[J]. 论文选刊,2000(11):30-31.
[16]陈延信,田增愿,赵博. 碳酸钙渣悬浮态和堆积态煅烧产品的理化性能比较[J]. 硅酸盐通报,2014,33(5):1193-1197.
[17]高新,韩伟,李稳宏,等. 循环法制备高纯碳酸钙工艺研究[J]. 西北大学学报(自然科学版),2007,37(1):63-66.
[18]周爱梅,张祥刚,陈毅雯,等. 内、外源复合酶解南美白对虾虾头、虾壳的研究[J]. 食品工业科技,2010,31(5):241-244.
[19]宋翔. 南极磷虾虾头、虾壳营养成分分析及氟安全性初探[D]. 上海:上海海洋大学图书馆,2013.
[20]唐红枫,吴郭燚,严月,等. 凡纳对虾干虾壳营养成分检测分析[J]. 饲料工业,2013,34(2):34-37.
[21]梁玉佳. 南极磷虾虾壳中甲克素的制取与应用[D]. 大连:大连工业大学图书馆,2013.
[22]白艳,谈小登,黄晓,等. 鳗鱼骨钙酸法提取工艺的研究[J]. 食品科技,2010,35(8):274-276.
[23]李彦坡. 利用鸡蛋壳制取乙酸钙的研究[D]. 武汉:华中农业大学图书馆,2010.
[24]赵强,索有瑞,李天才,等. 响应面法优化苦荞皮中总黄酮超声波提取工艺的研究[J]. 食品科学,2014,35(16):64-70.
[25]陈红梅,谢翎. 响应面法优化半枝莲黄酮提取工艺及体外抗氧化性分析[J]. 食品科学,2016,37(2):45-50.
[26]全沁果,杨明,林菲,等. 响应面法优化鸡蛋壳柠檬酸钙的制备工艺[J]. 核农学报,2016,30(1):79-85.
[27]范峥,杨栩,关嘉庆,等. 以废弃牡蛎壳为原料制备食品级醋酸钙[J]. 食品工业科技,2015,36(10):254-258.
[28]谭文溢,聂乾忠,管维. 响应面法优化草鱼鱼鳞柠檬酸-苹果酸钙提取工艺响应面法优化草鱼鱼鳞柠檬酸-苹果酸钙提取工艺[J]. 河南工业大学学报(自然科学版),2015,36(3):51-54.
[29]刘洪玲. 柠檬酸-苹果酸钙复合盐的制备和应用[D]. 泰安:山东农业大学,2007.
[30]王迪,牟建楼,牛万坤,等. 高温煅烧酸溶法从虾头虾壳中制取柠檬酸钙的研究[J]. 食品科技,2015,40(11):75-79.
[31]魏颖,刘华,陈丽丽,等. 响应面法优化克氏原螯虾虾壳中钙提取工艺的研究[J]. 河南工业大学学报(自然科学版),2014(4):50-54.
[32]梁春娜. 鸡蛋壳为原料制备醋酸钙的工艺研究[D]. 兰州:甘肃农业大学,2006.
[33]陈珊珊,丁俏羽,李佳,等. 响应面法优化虾壳可溶性钙提取工艺[J]. 中国食品学报,2014,14(6):81-89.
Optimizationofcalciumacetateextractionprocessfromprocambarusclarkiashellbyresponsesurfacemethodology
YUYa-li1,2,ZHOUYun-tao1,2,WENPing1,2,HELi1,2,*,ZHOUDian-fang1,2,LVLei1,2
(1.Yangtze River Fisheries Research Institute,Chinese Academy of Fishery Sciences,Wuhan 430223,China; 2.Aquatic Product Safety Risk Assessment Laboratory(Wuhan),Ministry of Agriculture P.R. China,Wuhan 430223,China)
In this paper,for further application of clarkia shell resource,the calcium was extracted from procambarus clarkia by acetic acid inquiring the four factors such as extraction temperature,acid concentration,the reaction time,liquid to solid into the extraction yield of calcium acetate. Based on the single factor experiments,the influence of the variables and their interaction on the impact on the extraction yield of calcium acetate was studied by response surface methodology. The results showed that the effect order of the factors on the extraction yield of calcium acetate from shrimp shell was:liquid to solid,temperature,concentration of acetic acid,and the time. The optimum extraction conditions were as follows:acid concentration 73.60 g/L,the reaction time 3 h,extraction temperature 65 ℃,liquid to solid 11.60∶1 (mL/g)and the most calcium extraction rate was 20.45%. The present method gives an acceptable yield and improved quality of calcium acetate. And this study could be helpful for the production or manufacture of calcium acetate based on shrimp shell as calcium resources.
procambarus clarkia;acetic acid;response surface methodology;calcium acetate
2017-03-24
喻亚丽(1989-),女,硕士,助理研究员,研究方向:水产品加工,E-mail:yali198811@163.com。
*
何力(1963-),男,博士,研究员,主要从事水产品质量安全,E-mail:heli28@sohu.com。
中央级科研院所基本科研业务费项目(2015JBFM34)。
TS254
B
1002-0306(2017)21-0167-07
10.13386/j.issn1002-0306.2017.21.034
