双亲性羧甲基壳聚糖钠盐席夫碱衍生物的合成及其性能研究
2017-11-10郭幼红林水森谢志新谢娜娜陈剑雄
郭幼红,林水森,谢志新,谢娜娜,陈剑雄
(泉州医学高等专科学校 药学院,福建 泉州 362000)
双亲性羧甲基壳聚糖钠盐席夫碱衍生物的合成及其性能研究
郭幼红*,林水森,谢志新,谢娜娜,陈剑雄
(泉州医学高等专科学校 药学院,福建 泉州 362000)
旨在以天然产物为基础,设计与合成具有表面活性和抗菌等特性的多功能高分子,拓宽天然产物应用领域. 首先壳聚糖与一氯乙酸取代反应获得O-羧甲基壳聚糖钠盐,然后依次与柠檬醛、对羟基苯甲醛进行席夫碱反应,最终制得O-羧甲基壳聚糖钠盐缩柠檬醛缩对羟基苯甲醛,并通过1H-NMR和元素分析对产物的结构进行表征. 通过测定终产物的表面张力(γ)、临界胶束浓度(CMC)、亲水亲油平衡值(HLB)、乳化能力和抗菌能力等对其性能进行评价,结果表明:该产物具备表面活性且其水溶液能够抑制细菌增长,具有成为功能性高分子表面活性剂的潜力.
壳聚糖;席夫碱;柠檬醛;抑菌剂;高分子表面活性剂
壳聚糖是一种来源广泛的生物可降解材料,其优越的性能使其经常被加工应用于污水处理、医药卫生等方面[1-3]. 壳聚糖利用其羟基和氨基与活性小分子发生接枝反应,可加强或赋予壳聚糖的多功能辅料特性[4]. 孙萍等[5]认为在壳聚糖结构中引入羧甲基,增加了产物的水溶性,从而增大了其使用的范围. 金晓晓等[6]制备了壳聚糖缩柠檬醛席夫碱,然后对其抗菌活性进行研究,结果表明该产物含有的席夫碱与柠檬醛具备协同抗菌作用,使其活性高于壳聚糖,但因产物仅溶于酸性溶液,故应用受到了限制. 李红霞等[7]以O-羧甲基壳聚糖为原料,经过与不同醛类衍生物发生席夫碱反应,制得一系列具有良好水溶性和pH敏感性的潜在聚合物胶束材料. 据此,壳聚糖接枝羧甲基后,再引入活性脂溶性基团所获得的衍生物具有多种潜力.
本研究拟通过壳聚糖接枝羧甲基获得O-羧甲基壳聚糖钠盐,使其具备更强的水溶性,并将该产物先后与柠檬醛、对羟基苯甲醛反应,制得O-羧甲基壳聚糖钠盐席夫碱衍生物,然后考察终产物的表面活性和抗菌性能.
1 实验部分
1.1 主要原料与仪器
壳聚糖(CS),相对分子质量5.0×104,去乙酰化度≥95%,浙江澳兴生物;柠檬醛、对羟基苯甲醛和一氯乙酸均为化学纯,阿拉丁试剂. 其他试剂均为化学纯,购自国药试剂.
LGJ-18B冷冻干燥机(北京松源华兴);Bruker Avance III 型(500MHz)核磁共振波谱仪(Bruker);Vario Micro 元素分析仪(Elementar);表面张力仪BZY-201(上海方瑞);NDJ-5S旋转黏度计(上海昌吉).
1.2 合成及表征
1.2.1 O-羧甲基壳聚糖钠盐的合成(CMCNa)
参照CHEN等[8]的方法,改动如下:1) 反应溶剂(V(蒸馏水)∶V(异丙醇)=2∶8)增加至150 mL,减少溶液黏度,防止搅拌不均匀;2) 产物烘干后需研磨过筛用以除掉不能粉碎的凝胶状颗粒,备用.
1.2.2 CMCNa缩柠檬醛席夫碱的合成(CMCCNa)
参照JIN等[6]的方法,改动如下:1) 由O-羧甲基壳聚糖钠盐和柠檬醛参与反应;2) 反应在恒温磁力搅拌器中进行;3) 壳聚糖氨基和柠檬醛的物质的量比为1∶3,反应时间为4 h,最后获得淡黄色CMCCNa,合成路线如图1所示.
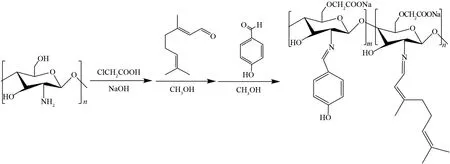
图1 羧甲基壳聚糖钠盐席夫碱衍生物合成路线图Fig.1 Synthesis of carboxymethyl chitosan sodium Schiff’s base
1.2.3 CMCCNa缩对羟基苯甲醛席夫碱的合成(CMCCPNa)
参照JIN等[6]的方法,改动如下:1)由CMCCNa和对羟基苯甲醛参与反应;2)采用恒温磁力搅拌器为反应装置;3)壳聚糖氨基和对羟基苯甲醛的物质的量比为1∶1.5,反应时间依次为1、2、3和4 h,最后获得黄色CMCCPNa(依次编号为CMCCPNa-1、2、3、4),合成反应如图1所示.
1.3 基本性能测试
1.3.1 HLB值测试
准确称取一系列产物各0.5 g,分别置于50 mL比色管中,于25 ℃下采用水数法[9]进行测定,实验重复3次,取平均值.
1.3.2 乳化性能、表面张力(γ)与临界胶束浓度(CMC)测试
[9]的方法进行乳化性能测试,以乳化层占整个液体的体积分数来衡量产物的乳化能力.
参考文献[10]将样品溶解然后稀释获得一系列浓度,静置1 d保证其完全溶解,于(25±0.1) ℃下采用吊片法进行CMC和表面张力测试. 反复冲洗吊片及容器避免干扰.
1.3.3 抗菌能力测试[10-11]
配制一系列产物的母液,浓度为1×104mg/L. 选用LB作为培养基. 培养基和母液均在121 ℃热压灭菌20 min. 选取大肠杆菌(Escherichiacoli)和金黄色葡萄球菌(Staphylococcusaureus)作为试验菌株,菌株须进行培养活化,活化后菌液浓度需与0.5麦氏比浊管比对,使约为108CFU/mL,备用.
采用倍半稀释法用培养基对各母液进行稀释,分别加入10 μL浓度为105~106CFU/mL的菌液,37 ℃摇床增殖1 d,以LB培养基(含对应浓度的样品未加菌液)作参照,测定中性条件下其在600 nm的吸光值. MIC确定依据:该浓度的吸光值是相邻低浓度的吸光值的100倍以上并且溶液呈澄清透明. 实验重复3次,取平均值.
2 结果与讨论
2.1 产物的结构表征
CMCNa、CMCCNa和CMCCPNa-1的1H NMR谱图见图2,其中δ4.79为D2O峰. 参考文献[5-6]的数据可知,δ1.19~2.2属于柠檬醛的CH3和CH2的吸收峰,δ2.06属于壳聚糖单体-COCH3的吸收峰,δ2.73属于壳聚糖单体上的N-CH2-COONa的吸收峰、δ3.40属于壳聚糖单体上的N-CH2-COOD的吸收峰,δ3.6~3.9分别是壳聚糖单体上的H3~6的吸收峰,δ3.95~4.58属于壳聚糖单体上的C-O-CH2-COOD的吸收峰,δ5.20属于柠檬醛上的CH=C吸收峰,δ8.28~8.46属于CH=N亚胺键的吸收峰,δ6.78~7.79属于Ar-H的吸收峰. 上述数据显示,羧甲基已经接枝到壳聚糖单体的C6羟基上,但也有部分C2氨基发生了反应,未反应的氨基分别与柠檬醛、对羟基苯甲醛继续发生了席夫碱反应最终生成O-羧甲基壳聚糖钠盐缩柠檬醛缩对羟基苯甲醛席夫碱CMCCPNa,因此目标产物成功合成.

图2 CMCNa(a)、CMCCNa(b)和CMCCPNa(c)的核磁氢谱Fig.2 1H NMR spectra of CMCNa (a), CMCCNa(b) and CMCCPNa(c) in D2O
2.2 产物的元素分析
通过元素分析获得化合物中C、N的质量分数,接着根据C/N比值与样品化学结构中的重复单元,根据文献[12]的方法对合成物的取代度进行计算,分析数据如表1所示. 表1数据显示,壳聚糖的去乙酰化度为93.75%,较标签注明的95%小,这大概是测试系统误差引起的. CMCNa的中羧甲基取代度达到了64.17%,CMCCNa中柠檬醛的取代程度为18.20%. 此外,因壳聚糖氨基与芳醛的席夫碱反应容易进行,形成的席夫碱衍生物较为稳定. 本研究通过降低投料比和限制反应时间,防止亲脂性基团大量引入而影响产物水溶性,随着反应时间的延长,CMCCNa与对羟基苯甲醛的席夫碱反应逐渐增加,CMCCPNa的取代度逐渐增加,由15.00%增至34.67%.

表1 样品元素分析结果Table 1 Elemental analysis results of samples
注:DS为取代程度.
2.3 产物的HLB值
通过水数法测定CMCCNa和CMCCPNa的HLB值,数据如表2所示. 其中CMCCNa的HLB值为14.93,而CMCCPNa随着取代度的增加,其HLB值不断减小,这可能是引入的疏水性对羟基苯甲醛导致的. 但CMCCPNa的HLB值均大于8,在13.83~14.68之间,表现出良好的水溶性,因此该产物的合成将有利于扩大壳聚糖使用范围. 参照文献[13]可知,HLB值不同则用途也不同,因此CMCCPNa有望作为润湿剂、乳化剂等附加剂使用.

表2 CMCCNa和CMCCPNa的HLB值Table 2 Hydrophile-lipophile balance of CMCCNa and CMCCPNa
2.4 临界胶束浓度(CMC)与表面张力(γ)分析
图3所示为CMCCNa和CMCCPNa水溶液的表面张力随浓度的变化曲线. 由图3可知,两种产物均可使表面张力减小,且浓度增加,与之对应的表面张力则逐渐减小,当浓度达到一定程度后,溶液的γ值出现拐点,此后数值变化比较平缓,该转折点对应的浓度即为CMC,CMCCNa和CMCCPNa-1-4的CMC依次为2.54×10-2、2.27×10-2、2.06×10-2、1.87×10-2和1.69×10-2g/L,该浓度对应的表面张力值分别为64.7、60.8、59.1、58.2、57.0 mN/m. CMCCPNa降低表面张力的程度略大于CMCCNa,表现出较强的表面活性,CMCCPNa的CMC低于CMCCNa,这可能是由于前者引入了更多的脂溶性基团,从而具备更强的疏水性,倾向于在较低浓度就可形成胶束.

图3 CMCCNa和CMCCPNa的表面张力—浓度曲线图Fig.3 Plot of the surface tension vs the concentration of CMCCNa and CMCCPNa
2.5 乳化能力分析
图4为CMCCNa和CMCCPNa的乳化能力随时间的变化曲线. 图4所示的五种产物中,乳化层体积在开始时最高可达75.4%,一段时间后乳化层的体积在44%~52%之间保持稳定,可见上述产物均具有一定的乳化能力. CMCCPNa的乳化能力较CMCCNa强,这说明对羟基苯甲醛的引入可以提高产物的乳化能力,其中又以CMCCPNa-4的乳化能力最强.

图4 CMCCNa和CMCCPNa的乳化能力图Fig.4 Emulsifying ability of CMCCNa和CMCCPNa
2.6 产物的抗菌能力分析
通过常量肉汤稀释法测定产物的MIC值,数据如表3所示. MIC越小,证明该物质的抑菌活性越强. 因此由表3中可知,CMCCNa的抗菌能力远较CMCNa强,这可能是因为前者接枝了柠檬醛这一脂溶性抗菌活性基团[6,11]. 而CMCCPNa的抗菌能力又比CMCCNa强,这可能是因为CMCCPNa通过席夫碱反应,接枝了具有抗菌活性对羟基苯甲醛[14],起到对羟基苯甲醛固载和释放的作用,这使得产物的抗菌活性增强,并随着取代程度的增加,对羟基苯甲醛接枝增加,从而提高了产物的抗菌能力. 此结果表明,CMCCNa和CMCCPNa均具有作为抑菌剂的潜力.

表3 羧甲基壳聚糖钠盐及其席夫碱衍生物对大肠杆菌和金黄色葡萄球菌的MIC值(mg/L)Table 3 Minimum inhibitory concentration of CMCNa and its Schiff’s base derivatives against Escherichia coli and Staphylococcus aureus (mg/L)
3 结论
以壳聚糖为原料,先后进行取代反应和二次席夫碱反应制得O-羧甲基壳聚糖钠盐缩柠檬醛缩对羟基苯甲醛席夫碱. HLB值测试表明产物的HLB值在13.83~14.93之间,具有良好水溶性;MIC测试表明CMCCNa和CMCCPNa均具备一定的抗菌能力,并随取代程度增加抗菌活性增强,其中CMCCPNa-4对大肠杆菌和金黄色葡萄球菌的MIC分别为7.8和3.9 mg/L. 据此,CMCCPNa同时具备水溶、表面活性和抗菌等特性,有望成为一种多功能的材料用于日用品、生物医药等领域. 可见,对壳聚糖进行水溶性结构改造,然后根据用途,采用席夫碱反应引入不同特性的醛类化合物是一种简便可行的设计思路.
参考文献:
[1] 王楠楠, 张大准, 董发才. 磁性壳聚糖的制备及在脂肪酶固定的应用[J]. 化学研究, 2017, 28(2): 247-253.
WANG N N, ZHANG D Z, DONG F C. Research on pre-paration of magnetic chitosan and immobilization of lipase [J]. Chemical Research, 2017, 28(2): 247-253.
[2] RAVI KUMAR M N V, MUZZARELLI R A A, MUZZARELLI C, et al. Chitosan chemistry and pharmaceutical perspectives [J]. Chemical Reviews, 2004, 104: 6017-6084.
[3] 林水森, 李明春, 辛梅华, 等. 壳聚糖及其衍生物抗菌机理研究进展[J]. 化学通报, 2014, 77(3): 220-226.
LIN S S, LI M C, XIN M H, et al. Progress in antimicrobial mechanism of chitosan and its derivatives [J]. Chemistry, 2014, 77(3): 220-226
[4] ZHANG J L, XIA W S, LIU P, et al. Chitosan modification and pharmaceutical/biomedical applications [J]. Mar Drugs, 2010, 8(7): 1962-1987.
[5] 孙萍, 黄国清, 韩晓娜, 等. O-羧甲基壳聚糖的制备工艺研究[J]. 食品研究与开发, 2015, 36(3): 82-84.
SUN P, HUANG G Q, HAN X N, et al. Research on the preparation of O-carboxymethyl chitosan [J]. Food Research and Development, 2015, 36(3): 82-84.
[6] JIN X X, WANG J T, BAI J. Synthesis and antimicrobial activity of the Schiff base from chitosan and citral [J]. Carbohydrate Research, 2009, 344: 825-829.
[7] 李红霞, 张灿, 尤启冬. N-辛基-N′-亚胺基-O-羧甲基壳聚糖衍生物的合成、表征与体外pH敏感性[J]. 中国药科大学学报, 2009, 40(5): 385-388.
LI H X, ZHANG C, YOU Q D. Synthesis, characterization and pH sensitivity of N-octyl-N′-imino-O-carboxymethyl chitosan derivatives [J]. Journal of China Phuarma-ceutical University, 2009, 40(5): 385-388.
[8] CHEN X G, HYUN J P. Chemical characteristics of O-carboxymethyl chitosans related to the preparation conditions [J]. Carbohydrate Polymers, 2003, 53: 355-359.
[9] 王旭颖, 董安康, 崔玉梅, 等. 壳聚糖表面活性剂的制备及其表面性能[J]. 日用化学工业, 2011, 41(3): 172-175.
WANG X Y, DONG A K, CUI Y M, et al. Preparation and surface performance of chitosan surfactants [J]. China Surfactant Detergent & Cosmetics, 2011, 41(3): 172-175.
[10] 裴立军, 蔡照胜, 商士斌, 等. 脱氢枞胺-壳聚糖阳离子表面活性剂的合成及性能研究[J]. 林产化学与工业, 2014, 34(5): 47-52.
PEI L J, CAI Z S, SHANG S B, et al. Synthesis and performance of dehydroabietylamine-chitosan cationic surfactants [J]. Chemistry and Industry of Forest Products, 2014, 34(5): 47-52.
[11] 周盛全, 辛梅华, 李明春, 等. 新型壳聚糖季铵盐抗菌剂的合成及其性能[J]. 化工进展, 2012, 31(8): 1801-1805.
ZHOU S Q, XIN M H, LI M C, et al. Synthesis and characterization of the novel antibacterial agent from quaternary ammonium chitosan derivatives [J]. Chemical Industry and Engineering Progress, 2012, 31(8): 1801-1805.
[12] 温俊杰, 周莉, 王紫威, 等. 微波法制备O-羟丙基-N-辛基壳聚糖及其性能表征[J]. 应用化学, 2015, 34(2): 192-199.
WEN J J, ZHOU L, WANG Z W, et al. Microwave synthesis and characterization of O-hydroxypropyl-N-octyl chitosan[J]. Chinese Journal of Applied Chemistry, 2015, 34(2): 192-199.
[13] 崔福德, 龙晓英, 吕万良, 等. 药剂学[M]. 北京: 人民卫生出版社, 2013: 39-40.
CUI F D, LONG X Y, LÜ W L, et al. Pharmaceutics [M]. Beijing: People’s Medical Publishing House, 2013: 39-40.
[14] 孙国峰, 夏烈文, 杨录, 等. 对羟基苯甲醛改性纳米二氧化硅的抗菌性能研究[J]. 西部皮革, 2011, 33(8): 24-27.
SUN G F, XIA L W, YANG L, et al. Study on anti-microbial property of modified Nano-silica by p-hydroxyben-zaldehyde [J]. West Leather, 2011, 33(8): 24-27.
PreparationandperformanceofSchiffbasesfromO-carboxymethylchitosansodium,citralandp-hydroxybenzaldehyde
GUO Youhong*, LIN Shuisen, XIE Zhixin, XIE Nana, CHEN Jianxiong
(DepartmentofPharmacy,QuanzhouMedicalCollege,QuanZhou362000,Fujian,China)
Schiff’s base of carboxymethyl chitosan sodium was synthesized by the reaction of carboxymethyl chitosan sodium with citral andp-hydroxy benzaldehyde successively. The structure of these Schiff’s base derivatives were characterized by1H NMR and EA. It showed that the amino groups in carboxymethyl chitosan were reacted with citral andp-hydroxy benzaldehyde to form the Schiff’s base derivatives. The HLB value, surface tension, emulsifying ability and antibacterial properties of the products were also investigated. The results showed that these water-soluble products have potential as polymeric surfactant with macromolecular antimicrobial.
chitosan; Schiff’s base; citral; bacteriostat; polymeric surfactant
O636.9
A
1008-1011(2017)05-0628-05
2017-07-19.
泉州市科技计划项目(2014Z58), 泉州医学高等专科学校“国家骨干院校建设”重点资助科研项目(XJ1303).
郭幼红(1966-), 女, 副教授, 研究方向为大分子化学改性与应用.*
, E-mail:93864575@qq.com.
[责任编辑:吴文鹏]