水环境中磺胺类抗生素的污染现状与处理技术研究进展*
2017-11-10丘锦荣蒋成爱王秀娟
赵 涛 丘锦荣 蒋成爱 王秀娟
(1.广东省环境辐射监测中心,广东 广州 510300;2.环境保护部华南环境科学研究所,广东 广州 510655;3.华南农业大学资源环境学院,广东 广州 510642)
水环境中磺胺类抗生素的污染现状与处理技术研究进展*
赵 涛1丘锦荣2#蒋成爱3王秀娟2
(1.广东省环境辐射监测中心,广东 广州 510300;2.环境保护部华南环境科学研究所,广东 广州 510655;3.华南农业大学资源环境学院,广东 广州 510642)
磺胺类抗生素在医药和养殖业中广泛使用,由于难以在环境中降解,其引起的污染问题得到了广泛关注。为了解磺胺类抗生素污染及处理技术,对其使用现状、危害及其在水环境中的迁移状况进行了阐述;介绍了水环境中磺胺类抗生素的处理技术研究现状,比较了各处理技术的优劣,并对今后的研究方向提出展望。
磺胺类抗生素 污染 处理技术
磺胺类抗生素是一类具有对氨基苯磺酰胺结构且人工合成的药物的总称,主要用于预防和治疗细菌感染性疾病[1]503。从1932年发现磺胺的基本结构以来,现已合成数千种磺胺类抗生素,磺胺类抗生素成为全世界生产和使用量最大的抗生素药物之一。其中,疗效好、毒副作用小且常用的磺胺类抗生素有磺胺嘧啶(SDZ)、磺胺氯哒嗪(SCP)、磺胺甲噁唑(SMX)、磺胺甲基嘧啶(SMR)等几十种。磺胺类抗生素的优点有化学性质稳定、抗菌谱广、使用方便、易于生产、价格低廉等,被广泛应用在医药、畜牧和水产养殖中[2]549,[3]2-5。中国是世界上抗生素生产量和使用量最多的国家,2013年中国抗生素的年生产量达16.2万t以上,其中有52%用于畜牧业,这相当于美国2012年畜牧业抗生素使用量的5.77倍,相当于英国2013年畜牧业抗生素使用量的200倍[4]6774-6775。其中,磺胺类抗生素在2013年的使用量达到了7 920 t[4]6774,市场需求量居高不下。
1 水环境中磺胺类抗生素残留的危害
水环境中磺胺类抗生素的残留浓度大多在ng/L至μg/L级别,但由于其在环境中不易发生降解,会长期存在并累积,残留于畜禽粪便、土壤、水体、植物等环境介质,对生态环境造成一定危害,而且会通过食物链的富集,导致越来越多的耐药菌产生,最终可能会危害人体健康[2]549-550,[3]5-15,[4]6772,[5]735-752。水环境中抗生素种类繁多,不同抗生素及其代谢物同时存在,且抗生素的代谢产物与母体化合物可能具有相同毒性[5]749-752,其危害效应甚至可能产生协同或相加等作用。
2 水环境中磺胺类抗生素的污染现状
磺胺类抗生素经人和动物消化后,大约30%(质量分数,下同)~90%会以母体或代谢物的形式随排泄物排出体外而进入环境中[2]550,[6]974。磺胺代谢物扩散到环境中并未失去生物活性,在一定的条件下可进一步形成母体化合物[1]503。有专家估算,每年有超过2万t的具有抑菌特性的磺胺类抗生素进入生物圈(不包括除草剂)[2]549-550,[3]5。图1为水环境中磺胺类抗生素的污染来源。
磺胺类抗生素可以通过多种途径进入水环境,目前在水环境中的残留现象比较普遍,国内外大量的研究报道了其在各种水环境(地表水、地下水、饮用水、海水等)中的残留情况。表1列举了关于磺胺类抗生素在水环境中的残留质量浓度的研究报道。
3 水环境中磺胺类抗生素的处理技术研究现状
目前,在污水和饮用水中,国内外均没有抗生素类药物的安全标准,但近年来磺胺类抗生素在环境中残留所引起的危害已受到人们的重视,为了降低磺胺类抗生素对生态环境和人类健康的影响,国内外对磺胺类抗生素的研究也在不断深入,但关于磺胺类抗生素处理技术的研究还相对较少。水环境中磺胺类抗生素常用的处理技术主要分为常规处理技术和深度处理技术。常规处理技术主要包括生物法和物化法,而深度处理技术主要包括高级氧化技术、膜处理技术和吸附技术。
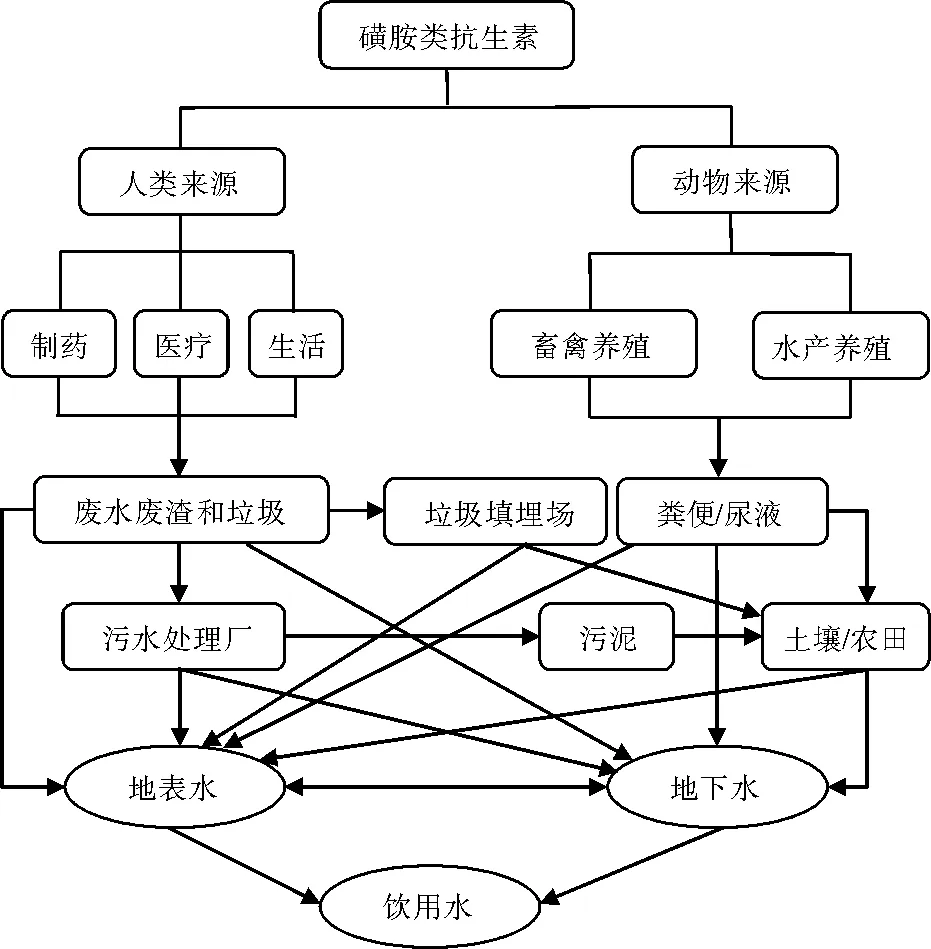
图1 磺胺类抗生素在水环境中的污染来源Fig.1 Pollution pathways for sulfonamides in aquatic environment

表1 磺胺类抗生素在水环境中的残留质量浓度
注:1)ND表示未检出。
3.1 生物法
生物法对水中磺胺类抗生素处理的原理是:在微生物作用下磺胺类抗生素分子结构发生改变,从大分子化合物降解为小分子化合物,最后生成CO2和水,从而实现环境无害化。生物法主要有活性污泥法和人工湿地等。活性污泥法广泛应用于生活污水及工业废水的处理中,是最常用的生物法。但此法主要是针对水中的COD、BOD、N、P等的去除,对水环境中抗生素去除率较低。张从良等[19]通过室内模拟降解水环境中SDZ的实验发现,在猪场废水和湖水中,SDZ的好氧或厌氧微生物降解均较缓慢。RICHTER等[20]在当地灌溉系统的地下水中发现,磺胺类抗生素在有氧条件下才容易被微生物降解去除。还有调查发现,北京6个污水处理厂中多种磺胺类抗生素在缺氧段和好氧段均有一定程度的去除,但去除效率均低于41%[15]。人工湿地的原理是:通过过滤、吸附、离子交换、微生物分解及植物吸收等对废水实现高效净化[13]713-714,[21]1-4。但其用于磺胺类抗生素废水的处理和研究相对较少。磺胺类抗生素在人工湿地中的去除效果取决于基质(黏土、沙土、珍珠岩等)、植物类型等湿地条件,还受水力停留时间(HRT)、pH和温度等运行条件的影响[21]29-40。有研究证实,人工湿地能够去除水环境中的磺胺类抗生素。李丽等[22]利用垂直潜流-水平潜流组合湿地对污水处理厂尾水进行处理,结果表明:有植物的组合湿地去除效率显著高于无植物的组合湿地;3种湿地植物(美人蕉(Cannaindica)、风车草(Cyperusalternifolius)、花叶芦竹(Arundodonaxvar.versicolor))均能吸收和转移磺胺类抗生素,美人蕉积累量最大。HIJOSA VALSERO等[13]714-719研究表明,参与试验的人工湿地对SMX均有较好的去除率。牛瑞华[21]35-37通过建立小型的人工湿地研究了多种因素对人工湿地去除污水中磺胺类抗生素的影响,结果发现,HRT对SDZ、磺胺对甲氧嘧啶(SMD)和SMZ的去除率有显著影响,而对SMR的去除率无显著影响。
3.2 物化法
目前,用于磺胺类抗生素废水处理的物化法主要包括混凝沉淀法和化学氧化法。混凝沉淀法广泛应用于废水中高浓度COD等的去除,其对废水中的磺胺类抗生素的去除未见报道。但有研究表明,加入FeCl3絮凝剂可以使药物和个人护理用品(PPCPs)的去除率提高4%~13%,但其对SMX的去除率并没有显著影响[23]。因此,混凝沉淀法处理抗生素废水的整体效果一般,所以不是处理水环境中磺胺类抗生素的理想方法,但该法可作为污水前处理工艺。化学氧化法通过氧化剂(如O3、Cl2、KMnO4、ClO2等)产生氧化性很强的自由基(主要是羟基自由基(·OH))来提高水环境中磺胺类抗生素的可生化性,实现抗生素的完全降解,其去除效果与氧化剂浓度、氧化时间等有关。
3.3 高级氧化技术
常用的高级氧化技术包括臭氧氧化技术(O3、O3/H2O2等)、光催化氧化技术(紫外(UV)/H2O2、UV/O3、UV/TiO2等)、Fenton法(Fe2+/H2O2)及改进Fenton法(光Fenton法、电Fenton法等)、超声氧化技术等。其机理均是通过·OH来氧化分解水环境中磺胺类抗生素。周宁娟等[24]用羟基化锌(ZnOOH)为催化剂研究其催化O3氧化去除水中SDZ的效能,结果表明,ZnOOH对O3氧化水中的SDZ有较强的催化活性,SDZ去除率高达98.83%,比单独O3氧化提高了47.7%。赵方等[25]采用微波辐照技术辅助H2O2氧化来降解水中SMZ,在最佳条件下去除率可达到96.5%。近年来,国内外兴起了通过改变光照条件(如光强、光照时间、水体pH、催化剂等)来降解水环境中的磺胺类抗生素的研究[26]41,[27-28],[29]1958-1959。BATISTA等[26]44研究发现,UV能够在165 min内使0.1 mmol/L的磺胺类抗生素完全降解。高乃云等[29]1958采用UV/TiO2工艺研究对SMX的光催化去除效果,结果表明,此工艺可以有效地去除水中的SMX,在最佳反应条件下SMX去除率高达98.76%。符荷花等[30]研究表明,在最佳的Fenton氧化条件下,水溶液中SPD、SMZ和SMX的去除率接近100%。GUO等[31]研究表明,超声/O3氧化处理能显著增强SMX的臭氧化,产生更多的·OH,从而大大提高了去除率。BATISTA等[26]40的研究结果表明,水溶液中SDZ、SMR和SMZ的光Fenton反应比UV光解和H2O2/UV光解更高效。通过电Fenton[32]和γ辐照[33]来降解水中磺胺类抗生素均能显著提升去除率。高级氧化技术对水环境中的磺胺类抗生素的降解有较高的去除率,但由于磺胺类抗生素及其代谢物转化的中间产物可能具有毒性,会带来二次污染,且目前高级氧化技术去除水环境中磺胺类抗生素仅停留在实验室研究阶段,其普遍适用性有待论证;高级氧化技术在大规模应用中的技术水平保障不完善,可能需要高额费用,所以仍需要进一步研究和探讨。
3.4 膜处理技术
膜处理技术主要包括微滤(MF)、超滤(UF)、纳滤(NF)和反渗透(RO)。因UF和MF孔径较大(0.01 μm以上),对水中磺胺类抗生素的截留率很低[34],因此去除效果并不理想,但其可用于其他膜处理技术的预处理中;而NF和RO的膜孔径一般小于2 nm,能够有效截留去除水中的磺胺类抗生素。张晗等[35]采用NF膜研究去除水环境中SMX,在最佳的条件下SMX的去除率能够达到96%。ADAMS等[36]研究RO对河水中磺胺类抗生素的去除,结果表明,在两级和三级RO处理中磺胺类抗生素的去除率均在99%以上。可见,膜处理技术中NF和RO是去除水中磺胺类抗生素的有效方法,并且有研究证实了多种膜处理技术的组合(如MF/RO、NF/RO等)有更好的去除率[37]。但是,膜处理技术需要消耗较多能量,成本较高,在处理抗生素废水时应用也少。
3.5 吸附技术
吸附技术是现在研究应用较多且比较成熟的技术之一,也是一种高效、简便的水处理技术。根据作用力的不同可分为物理吸附、化学吸附和离子交换吸附[38]。自从有研究表明抗生素会给生态系统及人类的健康带来危害以来,有关抗生素的吸附降解研究已成为环境科学研究的热点。目前,已有许多研究报道了采用树脂[39]、碳纳米管[40],[41]104、复合材料[41]104,[42]402、活性炭[43]194-195,[44]、生物炭[6]975,[45]890,[46]129等高效的吸附材料来吸附去除水环境中的磺胺类抗生素。鲍晓磊等[42]401-407研究发现,某种新型的磁性纳米复合材料CoFeM48对水中常见的5种磺胺类抗生素表现出了良好的吸附性能,且具有较高的吸附容量。ZHANG等[43]193-196利用粉末活性炭分别去除水中13种磺胺类抗生素,其对抗生素(50 mg/L)的去除率均高于92.0%。而关于利用固体废弃物(木屑、秸秆、药渣和畜禽粪便等)来研究去除水环境中磺胺类抗生素的方法也已成为环境领域的热点[6]974-975,[45]891-892,[46]128-129,[47]2232,[48]60-61。段伦超等[47]2231-2235利用火力发电厂产生的飞灰来吸附水溶液中磺胺,在最佳吸附条件下,去除率可达到92.8%。TZENG等[6]975-982利用牛粪制成的生物炭吸附去除水环境中的SMZ,实验结果表明,800 ℃下制备的生物炭对SMZ的去除率能够达到87.70%。ZHENG等[48]60-66利用芦竹在不同的温度条件(300~600 ℃)下制备成生物炭来吸附水中的SMX,结果表明,高温(600 ℃)制备的生物炭对SMX的吸附效果最好。而LIAN等[46]128-134利用中药渣在不同温度(250~800 ℃)下制备生物炭吸附水中的SMX,结果表明,在250 ℃下制备的生物炭的吸附能力是其他温度下的2~7倍。两者的研究结果不同,可能是研究选择的生物炭原材料不同所致。吸附技术具有能耗低、无副产物、可重复利用、对环境友好等特点,且一些高效的吸附材料具有独特的物理化学性质和较强的吸附特性,可用于去除水环境中的无机和有机污染物,降低这些污染物的环境风险,有利于缓解这些污染物对动植物和人类健康的影响,因而吸附技术是去除磺胺类抗生素较理想的技术。
常规处理技术、高级氧化技术、膜处理技术和吸附技术的各项比较如表2所示。
4 结语与展望
已在多种水环境(医院污水、生活污水、养殖场污水、地表水、地下水和饮用水等)中检测出磺胺类抗生素,其对生态环境和人类健康带来潜在危害。鉴于中国水环境中的磺胺类抗生素污染状况还不甚清楚,需进一步对中国各地区的水环境进行全面而广泛的调查和检测,确定中国磺胺类抗生素的污染水平和主要的磺胺类抗生素种类。
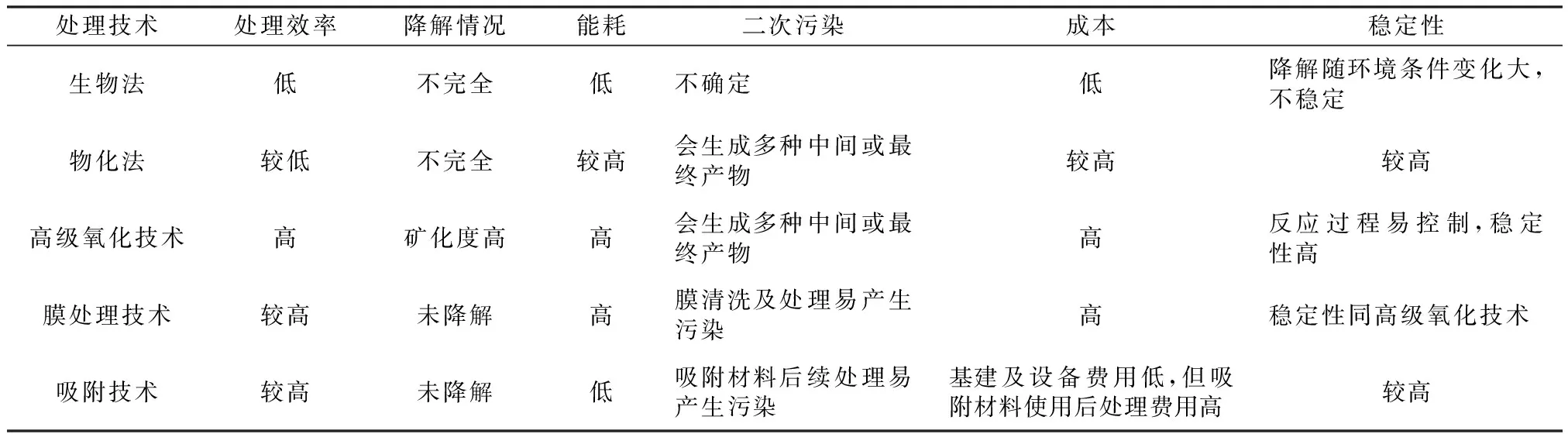
表2 水环境中磺胺类抗生素处理技术比较
目前,国内外关于磺胺类抗生素去除的研究还未广泛开展,而现有的处理技术也不能完全去除磺胺类抗生素,进入水环境的磺胺类抗生素会对水资源的安全利用造成巨大挑战。现有的常规处理技术、高级氧化技术、膜处理技术和吸附技术都存在各自的优势。然而,对于常规处理技术,提高处理效率是关注重点;对于高级氧化技术和膜处理技术,在高效去除的同时,有效控制成本和降低二次污染是重点;对于吸附技术,寻找到一种高效、经济的吸附材料是研究磺胺类抗生素吸附技术的一个发展趋势。总而言之,在强化现有技术的基础上,开发新技术、去除水环境中磺胺类抗生素的污染、保障饮用水安全,均值得高度关注。
[1] YANG W B,ZHENG F F,XUE X,et al.Investigation into adsorption mechanisms of sulfonamides onto porous adsorbents[J].Journal of Colloid and Interface Science,2011,362(2).
[2] QIU J R,ZHAO T,LIU Q Y,et al.Residual veterinary antibiotics in pig excreta after oral administration of sulfonamides[J].Environmental Geochemistry and Health,2016,38(2).
[3] BARAN W,ADAMEK E,ZIEMIANSKA J,et al.Effects of the presence of sulfonamides in the environment and their influence on human health[J].Journal of Hazardous Materials,2011,196.
[4] ZHANG Q Q,YING G G,PAN C G,et al.Comprehensive evaluation of antibiotics emission and fate in the river basins of China:source analysis,multimedia modeling,and linkage to bacterial resistance[J].Environmental Science & Technology,2015,49(11).
[5] SARMAH A K,MEYER M T,BOXALL A B.A global perspective on the use,sales,exposure pathways,occurrence,fate and effects of veterinary antibiotics (VAs) in the environment[J].Chemosphere,2006,65(5).
[6] TZENG T W,LIU Y T,DENG Y,et al.Removal of sulfamethazine antibiotics using cow manure-based carbon adsorbents[J].International Journal of Environmental Science and Technology,2016,13(3).
[7] BARTELT HUNT S,SNOW D D,DAMON POWELL T A.Occurrence of steroid hormones and antibiotics in shallow groundwater impacted by livestock waste control facilities[J].Journal of Contaminant Hydrology,2011,123(3/4):94-103.
[9] 周爱霞,苏小四,高松,等.高效液相色谱测定地下水、土壤及粪便中4种磺胺类抗生素[J].分析化学,2014,42(3):397-402.
[10] GARCIA G J,DIAZ CRUZ M S,BARCELO D.Occurrence of sulfonamide residues along the Ebro river basin:removal in wastewater treatment plants and environmental impact assessment[J].Environment International,2011,37(2):462-473.
[11] ZHOU L J,YING G G,LIU S,et al.Simultaneous determination of human and veterinary antibiotics in various environmental matrices by rapid resolution liquid chromatography-electrospray ionization tandem mass spectrometry[J].Journal of Chromatography A,2012,1244:123-138.
[12] HOA P T P,MANAGAKI S,NAKADA N A,et al.Antibiotic contamination and occurrence of antibiotic-resistant bacteria in aquatic environments of northern Vietnam[J].Science of the Total Environment,2011,409(15):2894-2901.
[13] HIJOSA VALSERO M,FINK G,SCHLUESENER M P,et al.Removal of antibiotics from urban wastewater by constructed wetland optimization[J].Chemosphere,2011,83(5).
[14] SIM W J,LEE J W,LEE E S,et al.Occurrence and distribution of pharmaceuticals in wastewater from households,livestock farms,hospitals and pharmaceutical manufactures[J].Chemosphere,2011,82(2):179-186.
[15] 常红,胡建英,王乐征.城市污水处理厂中磺胺类抗生素的调查研究[J].科学通报,2008,53(2):159-164.
[16] KIM Y,LEE K B,CHOI K.Effect of runoff discharge on the environmental levels of 13 veterinary antibiotics:a case study of Han River and Kyungahn Stream,South Korea[J].Marine Pollution Bulletin,2016,107(1):347-354.
[17] XU W H,ZHANG G,ZOU S C,et al.Determination of selected antibiotics in the Victoria Harbour and the Pearl River,South China using high-performance liquid chromatography-electrospray ionization tandem mass spectrometry[J].Environmental Pollution,2007,145(3):672-679.
[18] ZHENG Q,ZHANG R J,WANG Y H,et al.Occurrence and distribution of antibiotics in the Beibu Gulf,China:impacts of river discharge and aquaculture activities[J].Marine Environmental Research,2012,78:26-33.
[19] 张从良,王岩,王福安.磺胺嘧啶在水中的微生物降解研究[J].生态环境,2007,16(6):1679-1682.
[20] RICHTER D,MASSMANN G,TAUTE T,et al.Investigation of the fate of sulfonamides downgradient of a decommissioned sewage farm near Berlin,Germany[J]. Journal of Contaminant Hydrology,2009,106(3/4):183-194.
[21] 牛瑞华.人工湿地对磺胺类抗生素的去除效果及影响因素研究[D].上海:东华大学,2014.
[22] 李丽,杨扬,陶然,等.垂直流-水平潜流组合湿地对磺胺类抗生素的去除[J].安全与环境学报,2014,14(3):233-239.
[23] SUAREZ S,LERNA J M,OMIL F.Pre-treatment of hospital wastewater by coagulation-flocculation and flotation[J].Bioresource Technology,2009,100(7):2138-2146.
[24] 周宁娟,薛罡,卜聃,等.羟基化锌催化臭氧氧化去除水中痕量磺胺嘧啶[J].中国环境科学,2011,31(2):233-238.
[25] 赵方,张从良,王岩.微波辅助双氧水氧化降解水中磺胺二甲嘧啶[J].环境工程学报,2012,6(11):4074-4078.
[26] BATISTA A P,PIRES F C,TEIXEIRA A C.Photochemical degradation of sulfadiazine,sulfamerazine and sulfamethazine:relevance of concentration and heterocyclic aromatic groups to degradation kinetics[J].Journal of Photochemistry and Photobiology A - Chemistry,2014,286.
[27] GARCIA G J,DIAZ CRUZ M S,BARCELO D.Kinetic studies and characterization of photolytic products of sulfamethazine,sulfapyridine and their acetylated metabolites in water under simulated solar irradiation[J].Water Research,2012,46(3):711-722.
[28] 陈伟,陈晓旸,于海瀛.磺胺二甲嘧啶在水溶液中的光化学降解[J].农业环境科学学报,2016,35(2):346-352.
[29] 高乃云,张晏晏,马艳.UV/TiO2去除水中磺胺甲噁唑的动力学及影响因素分析[J].中国环境科学,2013,33(11).
[30] 符荷花,陈猛,熊小京.Fenton氧化法对磺胺类抗生素的降解动力学[J].环境工程学报,2014,8(3):972-976.
[31] GUO W Q,YIN R L,ZHOU X J,et al.Sulfamethoxazole degradation by ultrasound/ozone oxidation process in water:kinetics,mechanisms,and pathways[J].Ultrasonics Sonochemistry,2015,22:182-187.
[32] DIRANY A,SIRES I,OTURAN N,et al.Electrochemical abatement of the antibiotic sulfamethoxazole from water[J].Chemosphere,2010,81(5):594-602.
[33] LIU Y K,HU J,WANG J L.Fe2+enhancing sulfamethazine degradation in aqueous solution by gamma irradiation[J].Radiation Physics and Chemistry,2014,96:81-87.
[34] SNYDER S A,ADHAM S,REDDING A M,et al.Role of membranes and activated carbon in the removal of endocrine disruptors and pharmaceuticals[J].Desalination,2007,202(1/2/3):156-181.
[35] 张晗,周珺如,董秉直.DOM对纳滤膜去除磺胺甲恶唑效果影响研究[J].中国环境科学,2011,31(7):1159-1165.
[36] ADAMS C,WANG Y,LOFTIN K,et al.Removal of antibiotics from surface and distilled water in conventional water treatment processes[J].Journal of Environmental Engineering,2002,128(3):253-260.
[37] KOSUTIC K,DOLAR D,ASPERGER D,et al.Removal of antibiotics from a model wastewater by RO/NF membranes[J].Separation and Purification Technology,2007,53(3):244-249.
[38] 高廷耀,顾国维,周琪.水污染控制工程[M].北京:高等教育出版社,2007.
[39] 郑芳芳.树脂吸附去除水中抗生素的行为与机理[D].南京:南京师范大学,2012.
[40] INYANG M,GAO B,ZIMMERMAN A,et al.Sorption and cosorption of lead and sulfapyridine on carbon nanotube-modified biochars[J].Environmental Science and Pollution Research,2015,22(3):1868-1876.
[41] ZHANG C,LAI C,ZENG G M,et al.Efficacy of carbonaceous nanocomposites for sorbing ionizable antibiotic sulfamethazine from aqueous solution[J].Water Research,2016,95.
[42] 鲍晓磊,强志民,贲伟伟,等.磁性纳米复合材料CoFeM48对水中磺胺类抗生素的吸附去除研究[J].环境科学学报,2013,33(2).
[43] ZHANG X B,GUO W S,NGO H H,et al.Performance evaluation of powdered activated carbon for removing 28 types of antibiotics from water[J].Journal of Environmental Management,2016,172.
[44] SHIMABUKU K K,KEARNS J P,MARTINEZ J E,et al.Biochar sorbents for sulfamethoxazole removal from surface water,stormwater,and wastewater effluent[J].Water Research,2016,96:236-245.
[45] RAJAPAKSHA A U,VITHANAGE M,LEE S S,et al.Steam activation of biochars facilitates kinetics and pH-resilience of sulfamethazine sorption[J].Journal of Soils and Sediments,2016,16(3).
[46] LIAN F,SUN B B,XING B S.Physicochemical properties of herb-residue biochar and its sorption to ionizable antibiotic sulfamethoxazole[J].Chemical Engineering Journal,2014,247.
[47] 段伦超,王风贺,纪营雪,等.火力发电厂飞灰对抗生素磺胺的吸附性能[J].环境工程学报,2014,8(6).
[48] ZHENG H,WANG Z Y,ZHAO J,et al.Sorption of antibiotic sulfamethoxazole varies with biochars produced at different temperatures[J].Environmental Pollution,2013,181.
Researchprogressinpollutionstatusandtreatmenttechnologiesofsulfonamidesinaquaticenvironment
ZHAOTao1,QIUJinrong2,JIANGCheng’ai3,WANGXiujuan2.
(1.GuangdongEnvironmentalRadiationMonitoringCenter,GuangdongGuangzhou510300;2.SouthChinaInstituteofEnvironmentalSciences,MEP,GuangzhouGuangdong510655;3.CollegeofResourceandEnvironment,HuananAgricultureUniversity,GuangzhouGuangdong510642)
The increasing usage of sulfonamides in human medicine and livestock production system resulted in serious problems of environment pollution,which drew gradual attention all over the world. In order to better study sulfonamides and their treatment technologies,the hazards,used status and migration status of sulfonamides in aquatic environment were expounded. The current world-wide researches on treatment technologies of sulfonamides in aquatic environment were introduced,and the advantages and disadvantages of various treatment technologies were compared. Consequently,a systematic research on pollution status and treatment technologies of sulfonamides in aquatic environment was proposed.
sulfonamides; pollution; treatment technologies
10.15985/j.cnki.1001-3865.2017.10.022
赵 涛,男,1987年生,硕士,主要从事水污染控制技术研究。#
。
*国家水体污染控制与治理科技重大专项(No.2014ZX07206001);广东省自然科学基金资助项目(No.PM-zx018-201509-043)。
2016-07-14)
