生物阴极型微生物燃料电池处理氨氮有机废水及产电性能的研究*
2017-11-07金春姬杨远乐魏铭泽
李 英 金春姬 杨远乐 刘 明 鲁 静 魏铭泽
(中国海洋大学海洋环境与生态教育部重点实验室,山东 青岛 266100)
生物阴极型微生物燃料电池处理氨氮有机废水及产电性能的研究*
李 英 金春姬#杨远乐 刘 明 鲁 静 魏铭泽
(中国海洋大学海洋环境与生态教育部重点实验室,山东 青岛 266100)
将生物阴极型微生物燃料电池(BCMFC)阳极室的出水引进阴极,同时阴极采用间歇曝气的方式运行,以人工模拟的氨氮有机废水作为处理对象,探究外接电阻、DO、水力停留时间(HRT)以及碳氮质量比(C/N)对BCMFC的氨氮和有机物(以COD表征)去除效果以及产电性能的影响。结果表明:(1)开路以及50、100、500、1 000Ω条件下,最后出水中氨氮去除率分别为95.33%、86.12%、67.68%、100.00%、99.39%。外接电阻变化对COD的降解无太大的影响。500Ω条件下产电性能最佳。(2)DO为0.2、2.0、3.0、4.0、5.0、7.0mg/L条件下,最后出水中氨氮去除率分别为48.55%、56.56%、84.40%、93.25%、95.76%、97.01%,COD去除率分别为68%、96%、99%、99%、99%、99%。DO会影响整个电池的产电功率。DO设为4.0~5.0mg/L较合适。(3)C/N为8.3∶1.0、12.5∶1.0、25.0∶1.0、50.0∶1.0条件下,最后出水中氨氮去除率分别为74.68%、73.86%、94.07%、100.00%。C/N对COD的去除没有太大的影响。C/N为25.0∶1.0条件下最大产电功率密度最大。(4)HRT为8、10、13、20、24h条件下,最后出水的氨氮去除率分别为67.67%、79.01%、86.70%、92.72%、96.80%,COD去除率分别为96%、98%、98%、100%、100%。随着HRT的缩短,最大产电功率密度先增大后减小。HRT为20h时BCMFC性能较好。
生物阴极型微生物燃料电池 氨氮有机废水 氨氮COD产电功率密度
如今,化工行业迅速发展壮大,随之产生的氨氮废水也成为行业发展制约因素之一,未经处理的氨氮废水排入流域中易引起水中藻类及其他微生物大量繁殖,形成富营养化污染,除了会使自来水处理厂运行困难、造成饮用水的异味外,严重时会使水中DO下降,鱼类大量死亡,甚至会导致湖泊的干涸灭亡。目前,处理氨氮废水的方法很多,利用生物阴极型微生物燃料电池(BCMFC)处理氨氮废水是近年发展起来的一种新兴方法。
微生物燃料电池(MFC)是一种使用细菌作为催化剂,在降解有机和无机底物的同时回收电能的技术[1_5]。BCMFC是由MFC发展而来,它主要特点是阴极室与阳极室一样,接种功能型微生物,微生物接受来自电极的电子发生相应的生物电化学反应,利用微生物替代较昂贵的金属作为阴极催化剂,降低了构造成本,同时通过阴极室内硝化细菌的硝化作用能很好地处理氨氮废水。
CLAUWAERT等[6]以乙酸钠为阳极底物,在阴极接种厌氧微生物构建BCMFC,在去除有机物的同时实现了脱氮。李亮[7]构建了好氧/缺氧型MFC组合工艺,研究表明,在连续运行的情况下,当好氧型MFC外接电阻为20 Ω、缺氧型MFC外接电阻为5 Ω、进水流量比为1∶1、回流比为2∶1(体积比)时运行最优,能去除58.50 mg/L的氨氮。XIE等[8]利用好氧/缺氧BCMFC实现了同步脱氮除碳,COD、氨氮和总氮的总去除率分别为99%、97.40%和97.3%。VIRDIS等[9]2973使用特殊曝气方式在阴极实现了同步硝化反硝化,氮去除率达到94.1%±0.9%,出水氨氮降低至2.13 mg/L。CAI等[10]使用石墨棒作为电极,构建双室MFC,厌氧条件下去除硫化物和硝态氮的同时产电,而且厌氧条件下硫化物和硝态氮去除率都在90%以上。ZHANG等[11]采用双室好氧BCMFC,氨氮去除率达到84.00%~97.00%。JIA等[12]采用BCMFC进行反硝化,硝态氮最大去除速率达到0.084 mg/(cm2·d)。ZHANG等[13]将生物反应器与MFC相结合去除废水中的氨氮,98 h内,当进水氨氮为100 mg/L时,氨氮去除率可达90.20%。
从以上研究可看出,使用BCMFC能实现在去除氨氮和有机物的同时产电,但以上研究主要侧重于单个影响因素的研究,缺乏系统地探究外接电阻、DO、水力停留时间(HRT)以及碳氮质量比(C/N)对BCMFC同时去除氨氮和有机物及产电性能的影响。本研究构建了BCMFC,将阳极室的出水直接进入阴极室同时,阴极采用间歇曝气的方式运行,研究以上因素对氨氮有机废水处理及产电性能的影响。
1 材料和方法
1.1 实验装置
实验装置如图1所示,采用双室MFC,由两个长方形有机玻璃构成,两个极室净容积为0.5 L。阳极材料为碳布,表面积为35 cm2;阴极材料是表面积为35 cm2的光谱纯石墨板,阴极室中填充1 cm×1 cm×1 cm的碳毡,有效阴极体积约0.2 L。中间采用有效表面积为48 cm2的质子交换膜(PEM)将阳极室与阴极室分开。使用钛丝将电极相连接,外接22~22 000 Ω电阻箱。
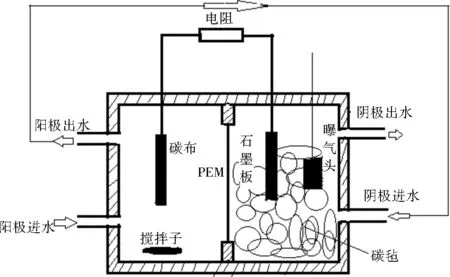
图1 BCMFC实验装置示意图Fig.1 Experimental schematic diagram of the BCMFC
1.2 实验方法
配制人工模拟的氨氮有机废水(以乙酸钠为碳源,氯化铵为氮源)。根据詹亚力等[14]的研究表明,乙酸钠初始浓度越高,微生物活性越高,输出最大电压越高,但乙酸钠浓度高于某一限值后,电极表面的微生物代谢反应速率达到峰值,单位时间内转移到电极表面的电子数量达到峰值,继续增大乙酸钠初始浓度,电池输出功率增长较小,故将COD初始质量浓度设为1 600 mg/L左右。而根据谢珊等[15]研究结果,氨氮初始浓度增高,好氧MFC的功率密度下降,同时为了维持微生物的正常生长,将氨氮初始质量浓度设为70 mg/L左右。
将该废水连续供给到MFC阳极,阳极出水进入密封装置中。生物阴极采用间歇曝气模式,反应周期共9.0 h,进水0.5 h,曝气6.0 h,停止曝气2.0 h,沉淀出水0.5 h。阴极每个周期的进水是阳极进入封闭装置后的出水。每个运行条件下,分别取阳极进水、阳极出水(即阴极进水)、曝气停止、最后出水4个不同阶段的水样,分别测定pH、电导率、COD和氨氮。水质分析指标测定后,开路6.0 h,测定极化曲线和产电功率密度曲线。每改变一次运行条件,使实验装置运行3个周期,达到稳定后再进行实验。
1.3 水质分析方法
pH使用雷磁PHS_3D型pH计测定;电导率使用DDS_312型精密电导率仪测定;COD根据《水质 化学需氧量的测定 快速消解分光光度法》(HJ/T 399—2007)测定;氨氮根据《水质 氨氮的测定 水杨酸分光光度法》(HJ 536—2009)测定。
2 结果与分析
2.1 外接电阻对BCMFC去除氨氮和有机物以及产电性能的影响
考察不同外接电阻(开路以及50、100、500、1 000 Ω)条件下BCMFC的氨氮和有机物(以COD表征)去除效果以及产电性能。废水水流速度为0.2 r/min,HRT为20 h。阴极室在曝气时保持进水DO为(7.0±0.5) mg/L。
不同外接电阻条件下氨氮质量浓度见图2。由图2可计算得出,开路以及50、100、500、1 000 Ω条件下,最后出水中氨氮去除率分别为95.33%、86.12%、67.68%、100.00%、99.39%。在阴极进水前,开路条件下的氨氮去除率高于500 Ω条件下;而500 Ω条件下曝气停止后氨氮去除率反而高于开路条件下。可能原因如下:在开路条件下,阳极室中产电微生物不传递电流,用于产电的微生物数量变少,多数是普通的微生物在起作用,所以氨氮去除率略高于500 Ω条件下。进入阴极室中后由于受到膜透过性的作用,形成了浓度梯度,使得极室中氨氮进入到阴极室中,增大了开路条件下最后出水中的氨氮浓度。
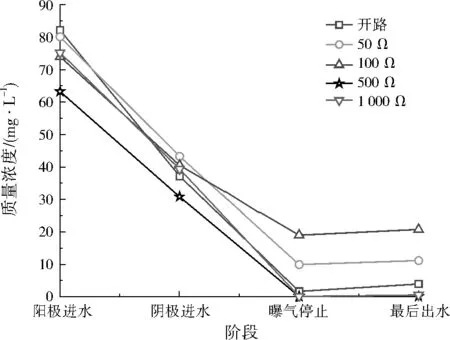
图2 不同外接电阻条件下氨氮质量浓度Fig.2 Concentration of ammonia nitrogen at the different resistance
不同外接电阻条件下COD质量浓度及去除率见图3。阴极进水时,开路条件下COD去除率最高,其次是1 000、500、100、50 Ω条件下。在未受到电流作用时,阳极微生物的代谢途径是产甲烷发酵,随着外接电阻的变化,受到电流的影响,阳极微生物的代谢途径发生变化,生物量随着电流强度增加而减少,COD去除能力下降,这与冯玉杰等[16]的研究相符。最后出水中COD去除率均在90%以上,开路和1 000 Ω条件下COD去除率达到了100%。比仅使用阳极去除有机物的普通双室MFC去除率[17]要高,将阳极未处理的有机物引入阴极,经过阴极好氧及反硝化作用,进一步降解有机物,从而达到COD较高的去除率。从整体看,外接电阻条件的变化对COD的降解无太大的影响。
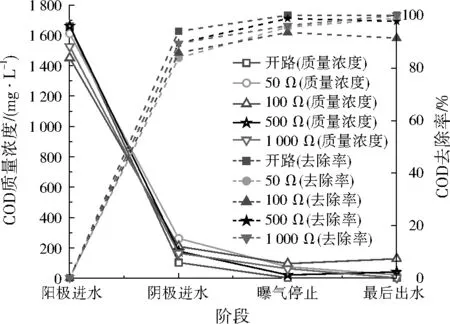
图3 不同外接电阻条件下COD质量浓度及去除率Fig.3 Concentration and removal rate of COD at the different resistance
根据欧姆定律可知,外接电阻改变,改变了电压与电流强度。电阻越小,阳极产生的电子就越易达到阴极,被阴极所利用,反之亦然。不同外接电阻条件下BCMFC的电压见图4。从图4可知,500、1 000 Ω以及开路条件下都有一个稳定阶段,大约1 h后电压趋于稳定化,稳定值分别为0.715、0.722、0.782 V。根据欧姆定律计算,500、1 000 Ω条件下相应稳定电流强度分别为1.430、0.722 mA(开路时电流强度为零)。结合产电性能认为,500 Ω条件下产电性能最佳,所以无特殊说明,后续实验外接电阻均为500 Ω。
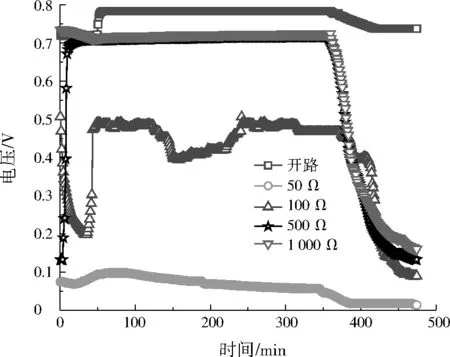
图4 不同外接电阻条件下BCMFC的电压Fig.4 Voltage of BCMFC at the different resistance
2.2 DO对BCMFC去除氨氮和有机物以及产电性能的影响
考察不同DO(0.2(即不曝气)、2.0、3.0、4.0、5.0、7.0 mg/L)条件下BCMFC的氨氮和有机物去除效果以及产电性能,其他步骤同2.1节。
不同DO条件下氨氮质量浓度的变化如图5所示。由图5可以计算得出,DO为0.2、2.0、3.0、4.0、5.0、7.0 mg/L条件下,最后出水中氨氮去除率分别为48.55%、56.56%、84.40%、93.25%、95.76%、97.01%。DO为4.0~7.0 mg/L条件下氨氮浓度相差较小,去除率也较接近;但DO为0.2、2.0 mg/L条件下氨氮去除效果不好。原因如下:HANAKI等[18]的研究表明,低DO的情况下,由于氨氧化菌增长速率加快,氨氧化速率并未受到很大的影响,并且氨氮经过硝化细菌的硝化作用转化为硝酸盐的过程需要在DO作用下进行新陈代谢活动,DO较低时,硝酸盐的活性受到抑制,而且能作为电子受体的氧气较少,所以硝化过程不明显,导致氨氮浓度较高。
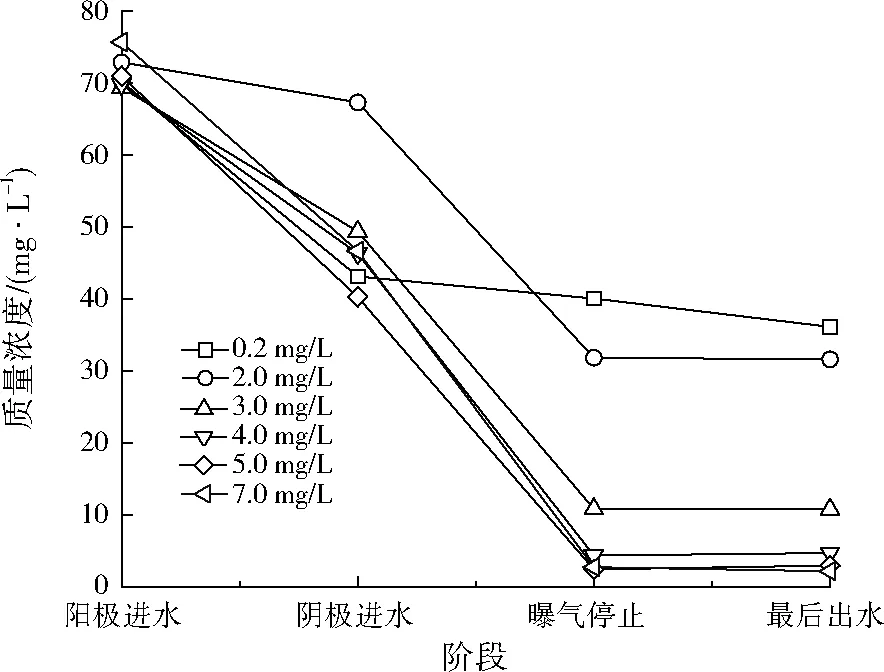
图5 不同DO条件下氨氮质量浓度Fig.5 Concentration of ammonia nitrogen at the different DO
不同DO条件下COD质量浓度及去除率的变化见图6。DO为0.2、2.0、3.0、4.0、5.0、7.0 mg/L条件下阴极进水的COD去除率分别为42%、56%、79%、92%、92%、93%。这与VIRDIS等[9]2973的研究结果类似。原因可能是DO较高时,一定量的DO通过PEM进入阳极室,这些氧气被兼性微生物所利用,而兼性微生物比厌氧微生物代谢有机物更彻底,故DO较高时阳极微生物处理高浓度有机物更彻底。DO为0.2、2.0、3.0、4.0、5.0、7.0 mg/L条件下最后出水的COD去除率分别为68%、96%、99%、99%、99%、99%,DO为3.0~7.0 mg/L条件下COD去除率较接近。这说明,DO为3.0~7.0 mg/L时,DO足够微生物的好氧呼吸。增加DO虽然能增加MFC产电所用的电子受体数量,但是DO越大,产生的硝态氮越多,不利于总氮的去除,再综合氨氮去除率,DO设为4.0~5.0 mg/L较合适。为了节省时间,产电性能实验时直接取DO为4.6 mg/L。
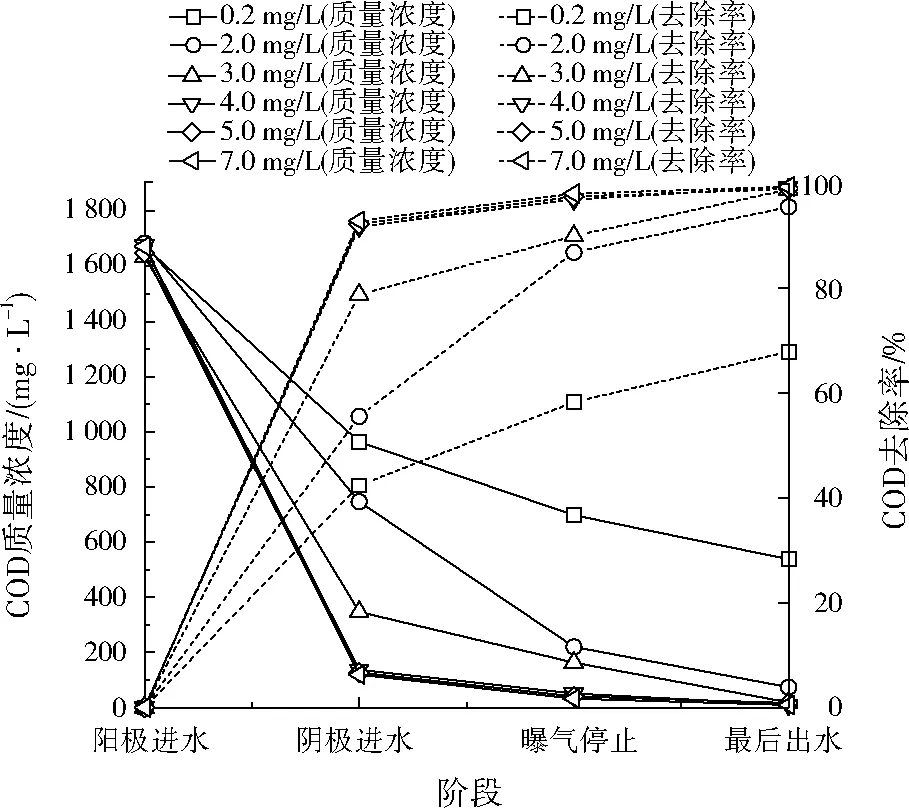
图6 不同DO条件下COD质量浓度及去除率的变化Fig.6 Concentration and removal rate of organic matter at the different DO
不同DO条件下BCMFC极化曲线及产电功率密度曲线见图7。DO为0.2、2.0、3.0、4.6、7.0 mg/L条件下,最大产电功率密度分别为57、103、370、983、2 500 mW/m3,对应的电流密度分别为214、287、860、2 560、5 000 mW/m3,相应的内阻分别为2 380、3 180、512、340、165 Ω。整体趋势是随着DO增多,最大产电功率密度增加,对应的电流密度增加、内阻下降。由于不同DO下,内阻从几千欧姆变化到165 Ω,说明最大产电功率密度的增加主要来源于内阻的减少。这说明,DO会影响整个电池的产电功率。
2.3 C/N对BCMFC去除氨氮和有机物以及产电性能的影响
固定进水COD为2 000 mg/L,分别添加不同质量的氮源,将C/N设为8.3∶1.0、12.5∶1.0、25.0∶1.0、50.0∶1.0以及未加氮源。考察不同C/N条件下,BCMFC的氨氮和有机物去除效果以及产电性能。其他步骤同2.1节。


图7 不同DO条件下BCMFC极化曲线及产电功率密度曲线Fig.7 Polarization and power density_current curve of BCMFC at the different DO
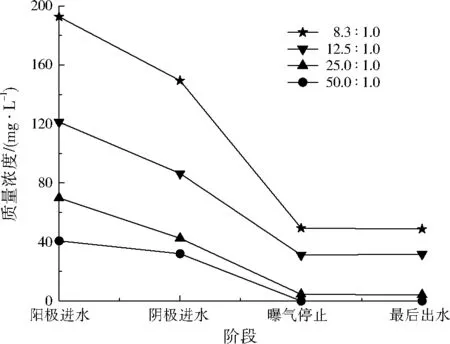
图8 不同C/N条件下氨氮质量浓度Fig.8 Concentration of ammonia nitrogen at the different C/N
不同C/N条件下COD质量浓度及去除率见图9。C/N为8.3∶1.0、12.5∶1.0、25.0∶1.0、50.0∶1.0以及未加氮源条件下,阴极进水的COD去除率分别为38%、72%、92%、91%、58%。COD去除率变化较大,未加氮源时阳极微生物缺少氮源而导致COD去除率偏低;C/N较低的条件下,加入的氮源较多,氯化铵中的氯离子浓度也较高,会对阳极微生物有毒害作用,所以COD去除率相对偏低。C/N为8.3∶1.0、12.5∶1.0、25.0∶1.0、50.0∶1.0以及未加氮源条件下,最后出水中COD去除率分别为99%、98%、99%、99%、90%。整体来讲,C/N的变化对COD的去除没有太大的影响。

图9 不同C/N条件下COD质量浓度及去除率Fig.9 Concentration and removal rate of organic matter at the different C/N
不同C/N条件下BCMFC的极化曲线和产电功率密度曲线见图10。C/N为8.3∶1.0、12.5∶1.0、25.0∶1.0、50.0∶1.0以及未加氮源条件下,最大产电功率密度分别为658、262、1 536、510、804 mW/m3,对应的电流密度分别为1 209、512、3 200、1 424、2 005 mW/m3,相应内阻分别为328、1 357、244、517、417 Ω。在未加氮源时,最大产电功率密度及对应的电流密度较高的原因是由于阴极室只需要降解COD,不存在去除氨氮,大量的DO提供电子受体,所以产电性能较高。C/N为25.0∶1.0、50.0∶1.0条件下,最大产电功率密度相差较大,原因是C/N为50.0∶1.0的条件下的内阻比C/N为25∶1.0条件下大,导致50.0∶1.0的最大产电功率密度变小。C/N小于25.0∶1.0条件下,当C/N变小时,氮素增多,相同开路时间内,剩余氮素不一样,这会导致在测定极化曲线过程中有一些氨氮没有被去除,争夺了用于产电的氧气,导致电池整体产电性能下降,最大产电功率密度变小。可见,C/N为25.0∶1.0条件下最大产电功率密度最大,对应的电流密度最大、内阻最小。

图10 不同C/N条件下BCMFC的极化曲线和产电功率密度曲线Fig.10 Polarization and power density_current curve of BCMFC at the different C/N
2.4 HRT对BCMFC去除氨氮和有机物以及产电性能的影响
本实验采用阳极室连续流供应废水。HRT关系到系统的处理效果与实验装置的容积。考察不同HRT(8、10、13、20、24 h)条件下,BCMFC的氨氮和有机物去除效果以及产电性能。其他步骤同2.1节。
不同HRT条件下氨氮质量浓度见图11。从图11可以计算得出,HRT为8、10、13、20、24 h条件下,阴极进水的氨氮去除率分别为19.22%、18.71%、10.19%、28.54%、53.45%,总体趋势是随着HRT的缩短,阴极进水的氨氮去除率降低;最后出水的氨氮去除率分别为67.67%、79.01%、86.70%、92.72%、96.80%,相差较大。原因可能如下:在阳极中相同氨氮浓度的进水,HRT越长,微生物与污水接触的时间越长,反应进行地越彻底;HRT越短,微生物与污水接触的时间越短,反应进行越不彻底,导致阴极进水中氨氮浓度增加。
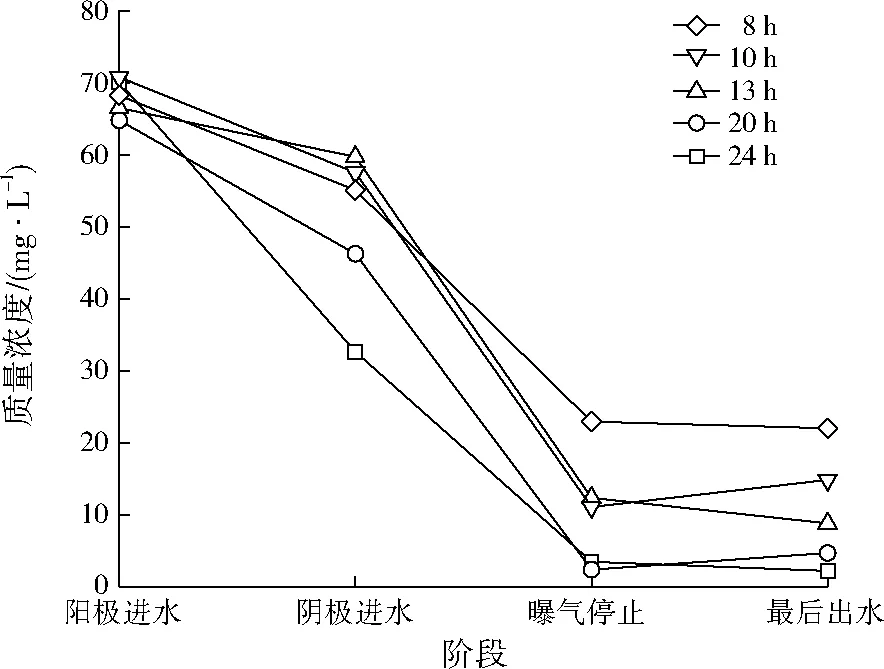
图11 不同HRT条件下氨氮质量浓度Fig.11 Concentration of ammonia nitrogen at the different HRT
阳极进水的HRT会影响阳极微生物与污染物质的接触有效性,HRT越大,接触时间越长,处理效果越好,但是接触时间过长会使得阳极微生物增殖速度变缓,而且增加运行成本及建筑成本;HRT过短,产生水利剪切,会对阳极上微生物产生流体力学影响使其脱落,影响污染物去除能力。不同HRT条件下COD质量浓度及去除率见图12。HRT为8、10、13、20、24 h条件下,COD去除变化较大,阴极进水的COD去除率分别为27%、27%、30%、92%、92%,明显看出HRT为20、24 h条件下的COD去除率最高,原因可能是:(1)微生物与有机物接触时间长,去除效果好;(2)因为本实验一直是在水流速度为0.2 r/min条件下供水的,所以HRT为20 h时微生物已完全适应了供水的浓度及水流速度。但是当供水的水流速度增加至0.3 r/min(即13 h),大量的有机物还不能被微生物所充分利用,所以出水中COD浓度很高,COD去除率下降。HRT为8、10、13、20、24 h条件下,最后出水的COD去除率分别为96%、98%、98%、100%、100%。COD去除率均在95%以上,出水COD符合《城镇污水处理厂污染物排放标准》(GB 18918—2002)中三级标准(≤120 mg/L)。
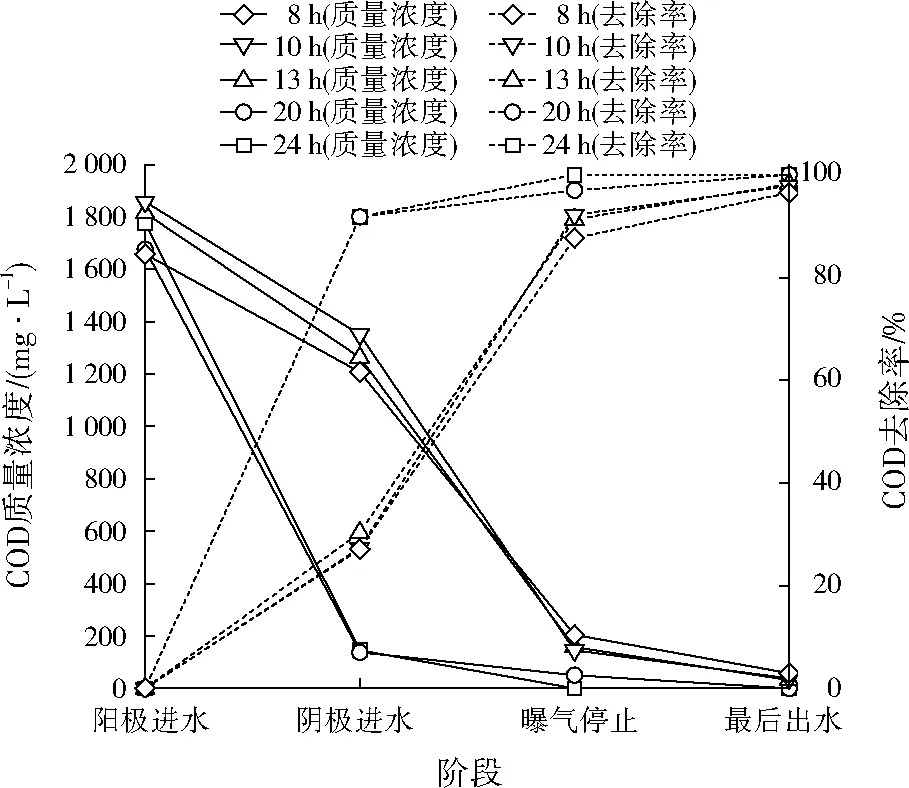
图12 不同HRT条件下COD质量浓度及去除率Fig.12 Concentration and removal rate of organic matter at the different HRT
不同HRT条件下BCMFC的极化曲线及产电功率密度曲线见图13。HRT影响着产电功率密度及内阻变化。HRT为8、10、13、20、24 h条件下,最大产电功率密度分别为909、918、1 344、983、543 mW/m3,对应的电流密度分别为1 611、2 473、2 993、2 560、2 330 mW/m3,对应内阻分别为494、376、219、340、437 Ω。随着HRT的缩短,最大产电功率密度和对应的电流密度均先增大后减小,对应的内阻则先下降后上升。原因是在阳极微生物与污染物质接触时间越长,消耗有机物越多,当有机物不足以支撑产电微生物对数期繁殖时,产电微生物进入稳定期,稳定期的活性小,阳极电势上升,输出电流变小,产电性能下降。但是并不是越短越好,HRT缩短,水力冲击对阳极微生物产生水利剪切作用,会破坏阳极电极膜上的产电微生物,所以产电功率密度下降。
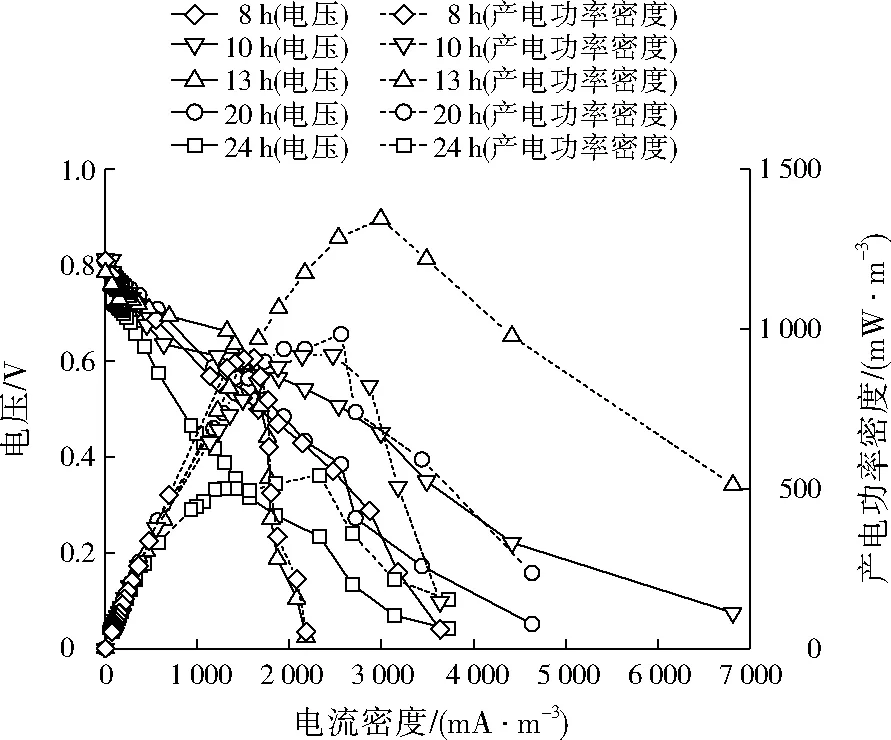
图13 不同HRT条件下BCMFC的极化曲线及产电功率密度曲线Fig.13 Polarization and power density_current curve of BCMFC at the different HRT
综合BCMFC在不同HRT条件下的脱氮除碳能力以及产电性能,其他运行条件不变情况下,当HRT为20 h时BCMFC性能较好。
3 讨 论
本实验在探究DO对BCMFC产电性能的影响时,得出DO为0.2、2.0、3.0、4.6、7.0 mg/L条件下的开路电压分别为0.445、0.702、0.708、0.808、0.828 V(见图7),开路电压随着DO的增加而增加,这是由于生物阴极表面富集的是好氧微生物,DO的增加有利于微生物生长,生物阴极性能就更好。但张金娜[21]认为,MFC由阴阳极室两部分构成,这两部分由PEM隔开,PEM对氧气又有一定的透过作用,因此阴极过量的曝气会加速氧气由阴极通过PEM扩散至阳极,破坏阳极的厌氧环境,进而影响阳极产电微生物的正常生长代谢,导致产电性能降低。本实验中并未出现因为DO过大而开路电压下降的现象,可能原因是文献[21]采用微孔曝气条曝气,曝气均匀稳定,测定的DO浓度基本与生物阴极表面的DO浓度一致。而本实验采用的是曝气头曝气,且将曝气头放置在碳毡中间,再者本实验测定DO是在碳毡中间近曝气头的部位,这就使得测得的DO浓度高于生物阴极表面的DO浓度,从而未出现DO过量导致开路电压降低的现象。
4 结 论
(1) 开路以及50、100、500、1 000 Ω条件下,最后出水中氨氮去除率分别为95.33%、86.12%、67.68%、100.00%、99.39%。外接电阻变化对COD的降解无太大的影响。500 Ω条件下产电性能最佳。
(2) DO为0.2、2.0、3.0、4.0、5.0、7.0 mg/L条件下,最后出水中氨氮去除率分别为48.55%、56.56%、84.40%、93.25%、95.76%、97.01%,COD去除率分别为68%、96%、99%、99%、99%、99%。DO会影响整个电池的产电功率。DO设为4.0~5.0 mg/L较合适。
(3) C/N为8.3∶1.0、12.5∶1.0、25.0∶1.0、50.0∶1.0条件下,最后出水中氨氮去除率分别为74.68%、73.86%、94.07%、100.00%。C/N对COD的去除没有太大的影响。C/N为25.0∶1.0条件下最大产电功率密度最大。
(4) HRT为8、10、13、20、24 h条件下,最后出水的氨氮去除率分别为67.67%、79.01%、86.70%、92.72%、96.80%,COD去除率分别为96%、98%、98%、100%、100%。随着HRT的缩短,随着HRT的缩短,最大产电功率密度先增大后减小。HRT为20 h时BCMFC性能较好。
[1] LOGAN B E,HAMELERS B,ROZENDAL R,et al.Microbial fuel cells:methodology and technology[J].Environmental Science & Technology,2006,40(17):5181_5192.
[2] RABAEY K,VERSTRAETE W.Microbial fuel cells:a novel biotechnology for energy generation[J].Trends in Biotechnology,2005,23(6):291_298.
[3] LOGAN B E,REGAN J M.Microbial fuel cells_challenges and applications[J].Environmental Science & Technology,2006,40(17):5172_5180.
[4] BERK R S,CANFIELD J H.Bioelectrochemical energy conversion[J].Applied Microbiology,1964,12(1):10_12.
[5] COHEN B.The bacterial culture as an electrical half_cell[J].Journal of Bacteriology,1931,21(1):18_19.
[6] CLAUWAERT P,RABAEY K,AELTERMAN P,et al.Biological denitrification in microbial fuel cells[J].Environmental Science & Technology,2007,41(9):3354_3360.
[7] 李亮.组合微生物燃料电池对废水的除碳脱氮产电性能研究[D].北京:中国地质大学(北京),2011.
[8] XIE Shan,LIANG Peng,CHEN Yang,et al.Simultaneous carbon and nitrogen removal using anoxic/anoxic_biocathode microbial fuel cells coupled system[J].Bioresource Technology,2011,102(1):348_354.
[9] VIRDIS B,RABAEY K,ROZENDAL R A,et al.Simultaneous nitrification,denitrification and carbon removal in microbial fuel cells[J].Water Research,2010,44(9).
[10] CAI Jing,ZHENG Ping,ZHANG Jiqiang,et al.Simultaneous anaerobic sulfide and nitrate removal coupled with electricity generation in Microbial Fuel Cell[J].Bioresource Technology,2013,129(2):224_228.
[11] ZHANG Fei,HE Zhen.Simultaneous nitrification and denitrification with electricity generation in dual_cathode microbial fuel cells[J].Journal of Chemical Technology and Biotechnology,2012,87(1):153_159.
[12] JIA Yuhong,TRAN H T,KIM D H,et al.Simultaneous organics removal and bio_electrochemical denitrification in microbial fuel cells[J].Bioprocess and Biosystems Engineering,2008,31(4):315_321.
[13] ZHANG Xiaoyan,ZHU Feng,CHEN Li,et al.Removal of ammonia nitrogen from wastewater using anaerobic cathode microbial fuel cell[J].Bioresource Technology,2013,146(10):161_168.
[14] 詹亚力,王琴,张佩佩,等.微生物燃料电池影响因素及作用机理探讨[J].高等学校化学学报,2008,29(1):144_148.
[15] 谢珊,梁鹏,李亮,等.好氧/缺氧生物阴极型微生物燃料电池组合工艺处理含氮废水的研究[J].广东化工,2011,38(6):126_127.
[16] 冯玉杰,王鑫,李贺,等.乙酸钠为基质的微生物燃料电池产电过程[J].哈尔滨工业大学学报,2008,39(12):1890_1894.
[17] 常继勇.微生物燃料电池处理生活污水特性研究[D].沈阳:沈阳建筑大学,2013.
[18] HANAKI K,WANTAWIN C,OHGAKI S.Nitrification at low levels of dissolved oxygen with and without organic loading in a suspended_growth reactor[J].Water Research,1990,24(3):297_302.
[19] BOND D,LOVELY D.Electricity production byGeobactersulfurreducensattached to electrodes[J].Applied and Environment Microbiology,2003,69(3):1548_1555.
[20] 郑平,胡宝兰,徐向阳.厌氧氨氧化菌好氧代谢特性的研究[J].浙江大学学报(农业与生命科学版),2000,26(5):521_526.
[21] 张金娜.三种不同阴极类型微生物燃料电池产电性能研究[D].哈尔滨:哈尔滨工业大学,2009.
Treatmentoforganicwasterwatercontainingammonianitrogenandelectricitygenerationusingabio_cathodemicrobialfuelcell
LIYing,JINChunji,YANGYuanle,LIUMing,LUJing,WEIMingze.
(KeyLaboratoryofMarineEnvironmentandEcology,MinistryofEducation,OceanUniversityofChina,QingdaoShandong266100)
BCMFC was constructed in this paper,the anode chamber effluent was into the cathode and cathodic operation was intermittent aeration. Taking organic wastewater with ammonia nitrogen as target pollutant,influence of external resistance, DO,hydraulic retention time (HRT) and carbon nitrogen ratio (C/N) were discussed on the removal rate of organic wastewater with ammonia nitrogen and the electricity generation in the BCMFC. The experimental results showed that: (1) when the conditions was open circuit and 50,100,500,1 000 Ω,the removal rate of ammonia nitrogen in the final water was 95.33%,86.12%,67.68%,100.00%,99.39%. The change of external resistance had no great influence on the degradation of COD. The best electricity generation performance was 500 Ω. (2) When DO was 0.2,2.0,3.0,4.0,5.0,7.0 mg/L,the removal rate of ammonia nitrogen were 48.55%,56.56%,84.40%,93.25%,95.76%,97.01%,the removal rate of COD were 68%,96%,99%,99%,99%,99%. DO would affect the whole battery power generation. DO of 4.0_5.0 mg/L was more appropriate. (3) When C/N was 8.3∶1.0,12.5∶1.0,25.0∶1.0,50.0∶1.0,the removal rate of ammonia nitrogen in the final effluent was 74.68%,73.86%,94.07%,100.00%. C/N had no significant effect on removaling COD. When C/N was 25.0∶1.0,the maximum power density was the best. (4) When HRT was 8,10,13,20 and 24 h,the removal rate of ammonia nitrogen in the final effluent was 67.67%,79.01%,86.70%,92.72%,96.80%. And COD removal rate was 96%,98%,98%,100%,100%. With the shortening of HRT,the current density maximum power density was firstly increased and then decreased. When HRT was 20 h,the performance of BCMFC was better.
bio_cathode microbial fuel cell; organic wasterwater containing ammonia nitrogen; ammonia nitrogen; COD; power density
10.15985/j.cnki.1001_3865.2017.01.014
2015_11_04)
李 英,女,1990年生,硕士研究生,研究方向为固体废弃物资源化。#
。
*山东省自然科学基金资助项目(No.ZR2011BM014)。
