重症肌无力-生活质量-15项评分在中国重症肌无力患者中的应用分析
2017-11-06刘潺潺李婷
刘潺潺 李婷
518000 深圳光明新区人民医院神经内科(刘潺潺);心内科[李婷(通信作者)]
重症肌无力-生活质量-15项评分在中国重症肌无力患者中的应用分析
刘潺潺 李婷
目的探讨重症肌无力-生活质量-15项评分(MG-QoL-15)在我国重症肌无力患者中的应用。方法收集2014年4月~2016年3月确诊MG患者,病情处于稳定期,记录包括年龄、性别、当前MGFA级、最差的MGFA及治疗方案,治疗性干预包括胸腺切除术、胆碱酯酶抑制剂、激素和其它免疫抑制剂;用MG-QOL-15中文版来评分,每个项目评分上标准是“0分”,“1分”,“2分”,“3分”和“4分”代表“完全没有”、“偶有”、“有一些”、“经常有”和“非常多”。结果共纳入65例患者,MGFA Ⅰ患者是13例,MGFA Ⅱ是17例,MGFA Ⅲ是14例,MGFA Ⅳ是21例,平均MG-QOL-15评分(7.22±6.44)分,当前等级MGFA和口服强的松与生活质量分数有关;性别、年龄>40岁、胸腺切除、口服溴吡斯的明的例数无显著差异(P>0.05)。结论MG-QOL-15评分是一种简单、快捷、人性化的工具,有利于更好地评估治疗效果。
重症肌无力 重症肌无力-生活质量-15项评分 生活质量
重症肌无力(MG)是一种神经肌肉接头自身免疫性疾病,病情往往迁延而有波动。生活质量(QOL)评估根据疾病相关症状和长期治疗效果来反映。生活质量是个人和社会的总体幸福感的测量。使用生活质量相关量表可以从患者的角度来评估各种疾病或治疗干预措施的影响。评分和身体健康、心理状态、独立的生活能力、社会关系以及对疾病的认识都有关系。它包含身体、心理、情感、社会和职业领域。重症肌无力(MG)特点是波动的骨骼肌无力或伴有吞咽困难或/和呼吸困难。主要的治疗方案有激素治疗、溴吡斯的明、胸腺切除、免疫抑制剂、急性期的血浆置换和丙种球蛋白。目前MG作为慢性疾病而无法根治,因而生活质量评分越来越受到各国医护人员的重视,从欧美发达国家到巴西、印度、土耳其发展中国家逐渐采用针对MG生活质量的新量表的评分,即MG-QOL-15评分[1-2]。本研究的目的是使用MG-QOL-15评分来评估MG临床症状稳定患者的生活质量,并对相关因素进行多元回归分析。
1 资料与方法
1.1 一般资料
收集2014年4月~2016年3月确诊MG患者,病情处于稳定期,诊断依据波动性骨骼肌无力、重复神经刺激阳性、新斯的明阳性。重症肌无力分类按照美国的重症肌无力基金会(MGFA)评分标准。根据医院赫尔辛基宣言和经医院伦理委员会批准。记录包括年龄、性别、当前MGFA级、最差的MGFA及治疗方案。治疗性干预包括胸腺切除术、胆碱酯酶抑制剂、激素和其它免疫抑制剂。
1.2 MG-QOL-15评分
生活质量使用MG-QOL-15量表中文版评价,总共有15项,每个项目评分上标准是“0分”,“1分”,“2分”,“3分”和“4分”代表“完全没有”、“偶有”、“有一些”、“经常有”和“非常多”。
1.3 统计学处理
采用SPSS19.0软件,进行多元Logistic回归分析。以P<0.05为差异有统计学意义。
2 结 果
共纳入65例患者。MGFA Ⅰ患者是13例,MGFA Ⅱ是17例,MGFA Ⅲ是14例,MGFA Ⅳ是21例(表1),平均MG-QOL-15水平是(7.22±6.436)分,当前等级MGFA与生活质量分数有关系。
性别、年龄>40岁、胸腺切除、口服溴吡斯的明的MG-QOL-15无显著差异(P>0.05),但是当前的 MGFA分组和口服激素患者明显影响了生活质量(表2)。

表1 MGFA分类与MG-QOL-15评分的关系(例)
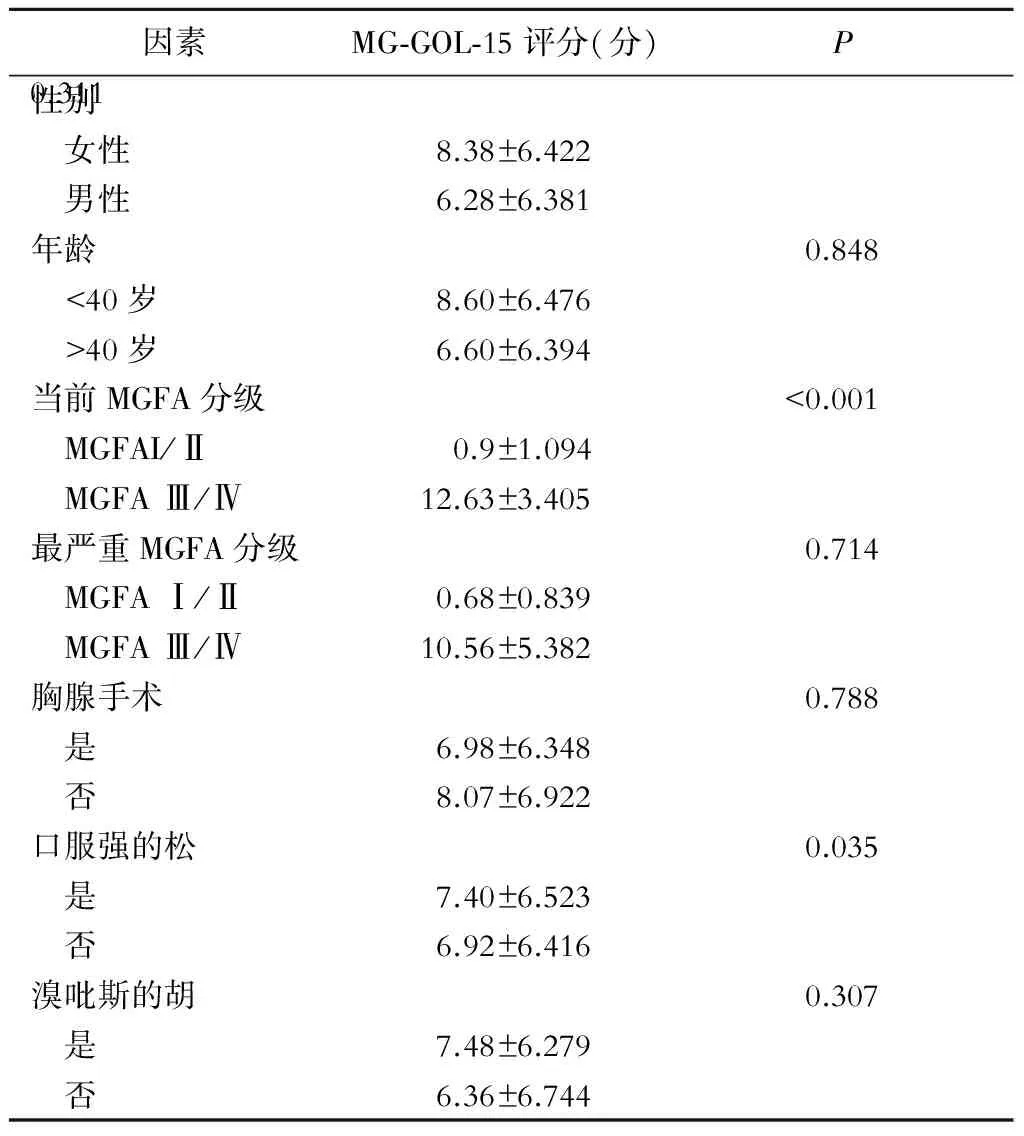
表2 MG-QOL-15评分多元回归分析
3 讨 论
MG是免疫介导的神经肌肉接头疾病,大部分患者表现为波动性的四肢无力,晨轻暮重,部分患者合并吞咽困难、呼吸肌无力,甚至重症肌无力危象而危及生命。虽然治疗方案在不断的优化,但是患者往往需要终生随访和治疗。MG患者因为肌无力而对生活和工作产生不利影响,需要监测患者生活质量。
之前与健康有关的生活质量(HR-QOL)、简明生活质量调查(SF-36)和世界卫生组织残疾评定表二(WHO-DAS Ⅱ)已被广泛用于评估MG生活质量[3],但是这些量表不是针对MG患者,比如一些疼痛的描述不适合MG,同时MG的症状波动也不适用于残疾量表来评估。MG日常生活评估量表(MG-ADL)是根据MG患者每天的日常活动如说话、咀嚼、吞咽、呼吸、刷洗/梳理、从椅子上站起、复视和眼睑下垂来制定,但是它不包含有关心理健康的项目。基于SF-36,国外采用了MG-QOL-60项生活质量评分,目的是为了比SF-36更好地评估疾病的变化情况。为了更方便临床使用,后来缩写为包括15个项目,涵盖身体状况、社会、生活功能、自理能力和心理成分。因此,MG-QOL-15评分具有了相应的优势,如简单快速、易于管理和解释,对临床改善灵敏度高[4-5]。同时这个量表容易翻译成其他语言并且文化差异影响比较小[5]。
年龄、教育状况、疾病的严重程度、用免疫抑制剂、胸腺切除术、社会支持、就业、共患疾病、焦虑、抑郁及体重都可能对生活质量产生影响[6]。年龄超过 40岁MG患者存在更多的问题,比如生活压力、共患疾病,但是本研究没有发现差异,可能需要更多的样本量。MG-QOL-15评分从患者角度设定评分标准,“完全没有”、“偶有”、“有一些”、 “经常有”和“非常多”,国际上认为患者从主观上进行自我判定可能更好地反应生活质量[7],一般认为得分<12分,表示症状有所改善[8]。
有研究认为MGFA严重程度对MG-QOL-15评分起决定作用,本研究也发现类似结果。这意味着当前疾病严重程度与生活质量有关[9]。本研究发现使用激素维持治疗的患者生活质量明显降低。这可能与患者受到激素的副作用的影响有关,比如向心性肥胖,同时这类患者也担心体重的进一步增加。国外研究认为免疫球蛋白或血浆治疗中的MG-QOL-15评分能显著改善[10],但本研究是调查稳定期的患者,急性期发病的患者没有纳入研究。共纳入65例MG稳定期的患者。MGFA Ⅰ患者是13例,MGFA Ⅱ是17例,MGFA Ⅲ是14例,MGFA Ⅳ是21例,平均MG-QOL-15评分(7.22±6.436)分,当前等级MGFA与生活质量分数有关系。
性别不是MG-QOL-15评分的决定因素。从长期来看胸腺切除对患者有益,但是部分患者胸腺切除后病情仍不能改善,所以生活质量不一定提高印度的研究表明口服溴吡斯的明是MG-QOL-15评分的决定因素[1-2],但本研究无显著差异,这一方面可能是溴吡斯的明的副作用较激素副作用小;另一方面就诊的患者总是对激素存在担心,比如激素可能产生的高血压病、高血糖、骨质疏松等。本研究口服激素明显影响了MG-QOL-15的评分。
MG-QOL-15评分比MG-ADL评分更好地评定心理状态,比如因为MG而感到挫折感、在公共场所感到麻烦、不知所措、郁闷。MG-ADL评分更多地评定MG患者生活处理能力,如从椅子上站起来、复视的时间、眼睑下垂的时间。本研究曾遇到这样1例MG患者,从小患有MG后双眼球固定,生活影响不大,后来积极治疗后一只眼球可以活动,患者反而容易出现复视,ADL评分显示病情加重,MG-QOL-15评分显示病情好转。这是因为ADL评分有一项专门评估复视严重程度的一项,以前没有复视现在有了,所以ADL评分增加了,但是MG患者自我评分认为用眼并没有感到麻烦加重,并对MG治疗充满了信心,郁闷少了,MG-QOL-15总体评分下降。从这个患者治疗中可以发现MG-QOL-15评分更能贴近患者生活和心理状态。
使用MG-QOL-15评分来评估MG的生活质量,可以更好地从以疾病为中心的模式转为以患者为中心的治疗模式,简明的评估方式适合临床医生使用,兼顾了患者的心理、生理、生活各方面。
[1] Kumar R,Nagappa M,Sinha S,et al.MG-QoL-15 scores in treated myasthenia gravis: Experience from a university hospital in India[J].Neurol India,2016,64(3):405-410.
[2] Mourão AM,Gomez RS,Barbosa LS,et al.Determinants of quality of Life in Brazilian patients with myasthenia gravis[J].Clinics (Sao Paulo),2016,71(7):370-374.
[3] Leonardi M,Raggi A,Antozzi C,et al.The relationship between health,disability and quality of Life in myasthenia gravis: results from an Italian study[J].J Neurol,2010,257(1):98-102.
[4] Burns TM,Graham CD,Rose MR,et al.Quality of Life and measures of quality of Life in patients with neuromuscular disorders[J].Muscle Nerve,2012,46(1):9-25.
[5] Masuda M,Utsugisawa K,Suzuki S,et al.The MG-QOL15 Japanese version: validation and associations with clinical factors[J].Muscle Nerve,2012,46(2):166-173.
[6] Padua L,Evoli A,Aprile I,et al.Health-related quality of Life in patients with myasthenia gravis and the relationship between patient-oriented assessment and conventional measurements[J].Neurol Sci,2001,22(5):363-369.
[7] Burns TM,Grouse CK,Wolfe GI,et al.The MG-QOL15 for following the health-related quality of Life of patients with myasthenia gravis[J].Muscle Nerve,2011,43(1):14-18.
[8] Burns TM,Conaway M,Sanders DB,et al.The MG composite: a valid and reliable outcome measure for myasthenia gravis[J].Neurology,2010,74(18):1434-1440.
[9] Utsugisawa K,Suzuki S,Nagane Y,et al.Health-related quality-of-life and treatment targets in myasthenia gravis[J].Muscle Nerve,2014,50(4):493-500.
[10] Barnett C,Wilson G,Barth D,et al.Changes in quality of Life scores with intravenous immunoglobulin or plasmapheresis in patients with myasthenia gravis[J].J Neurol Neurosurg Psychiatry,2013,84(1):94-97.
R746.1
A
1007-0478(2017)05-0458-03
10.3969/j.issn.1007-0478.2017.05.020
(2016-11-22收稿)
