在线固相萃取-高效液相色谱法检测碳酸饮料 中对羟基苯甲酸酯
2017-10-18蒋树新刘华良马永建阮丽萍
蒋树新, 刘华良 , 马永建*, 阮丽萍
(1.东南大学公共卫生学院,江苏南京 210009; 2.江苏省疾病预防控制中心,江苏南京 210009)
近年来,随着食品工业的迅速发展,各种防腐剂被广泛使用。对羟基苯甲酸酯与传统的苯甲酸、山梨酸防腐剂相比,具有低毒、高效、作用强、抑菌范围广、防腐效果不易随pH值变化而变化的优点[1]。有研究表明,对羟基苯甲酸酯具有雌激素活性[2 - 3],长期摄入会影响人体内分泌功能,甚至可能是乳房癌和男性不育的诱因[4 - 6]。因此,我国国家标准(GB 2760-2014)对食品中对羟基苯甲酸酯类防腐剂的添加规定了限量[7]。
目前,对食品中对羟基苯甲酸酯类的测定方法主要有高效液相色谱法[8 - 9]、气相色谱法[10 - 11]、气相色谱-质谱法[12 - 13]、薄层色谱法[14 - 15]、毛细管电泳法[16]。但这些测定方法的样品前处理多为离线前处理,操作复杂,溶剂消耗量大,费时费力。现行标准可同时测定对羟基苯甲酸乙酯和丙酯,但该方法样品前处理需乙腈提取三次,洗涤数次,耗时费力且产生大量废液[17]。本研究建立了碳酸饮料中对羟基苯甲酸乙酯和丙酯的在线分析方法,具有简单、快速、准确的特点,简化了分析步骤及有机溶剂的使用。
1 实验部分
1.1 仪器与试剂
双三元液相色谱系统(美国,Thermo Fisher 公司),配备DGP-3600RS泵、WPS-3000自动进样器、TCC-3X00(RS)柱温箱(配有一个六通阀)、VWD-3X00(RS)检测器和Chromeleon 7.0变色龙色谱管理软件;Mili-Q超纯水纯化系统(美国,Milipore公司);涡旋混合器(美国,Scientific Industries公司);分析天平(梅特勒-托利多仪器(上海)有限公司);超声波清洗器(德国,Elma 公司)。
甲醇为色谱纯(德国默克股份联合公司);乙酸铵为分析纯(南京化学试剂有限公司);水为超纯水;对羟基苯甲酸乙酯(Ethyl-paraben)和对羟基苯甲酸丙酯(Propyl-paraben)标准品(纯度≥99.5%,德国Laboratories of Dr.Ehrenstorfer)。
1.2 样品处理
称取碳酸饮料样品2.0 g(精确至0.01 g),样品需超声振荡去除CO2,用水稀释定容至10 mL,混匀后过0.45 μm微孔滤膜,待测。
1.3 在线固相萃取和色谱分离条件
在线萃取柱为Acclaim 120 C18柱(10×4.6 mm,5 μm),色谱柱分析为Agilent Extend-C18柱(250×4.6 mm,5 μm);进样量为10 μL,柱温25 ℃;右泵(Online-SPE pump)为净化泵,采用水(溶剂A)和甲醇(溶剂B)梯度洗脱;左泵( Analytical pump)为分析泵,采用水(溶剂A)和甲醇(溶剂B)等度洗脱。分别于5 min 和5.6 min处切换六通阀。六通阀切换程序及分析流路洗脱程序见表1,具体切换通路见图1和图2。

表1 在线净化与色谱分离的洗脱条件Table 1 Elution procedures of on-line SPE and chromatographic separation

图1 萃取阶段及分析阶段阀切换通路Fig.1 Column switching system in extraction and analytical periods
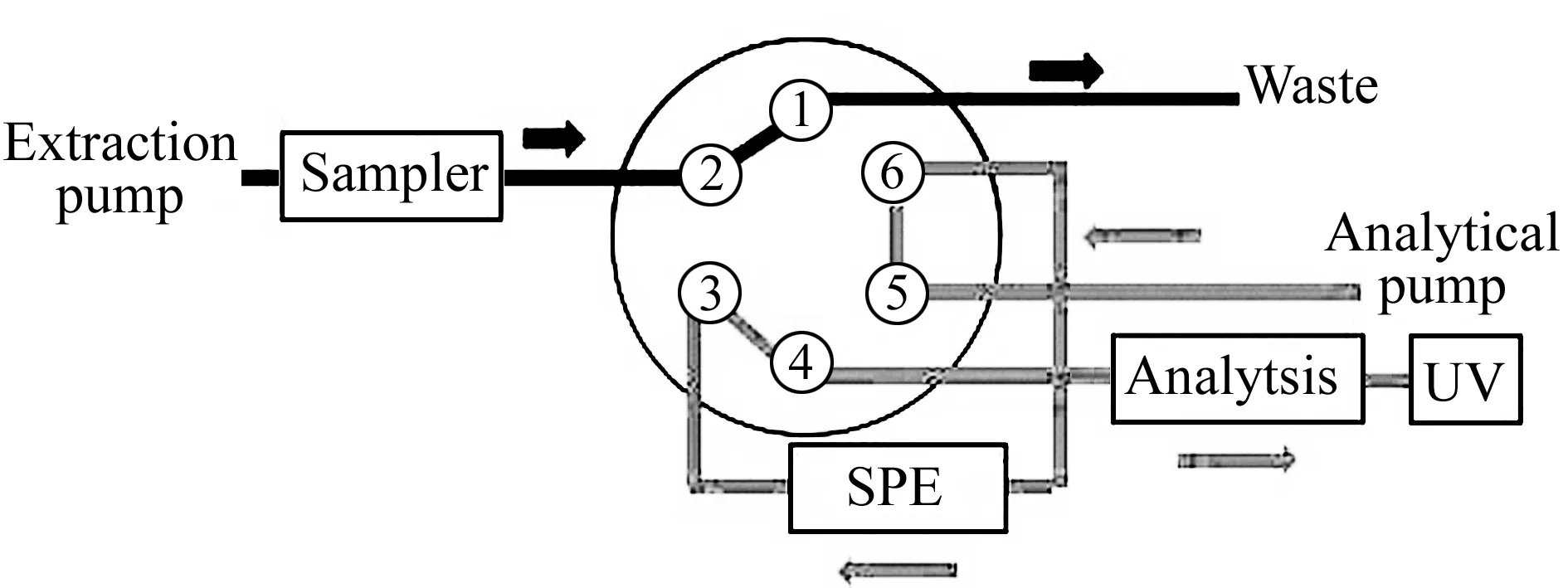
图2 转移阶段阀切换通路Fig.2 Column switching system in transfer period
2 结果与讨论
2.1 在线固相萃取条件优化
2.1.1在线萃取柱的选择实验比较了Oasis WAX、Acclaim 120 C18两种萃取柱的净化效果。结果表明:目标化合物经过Oasis WAX柱萃取后再洗脱到分析柱进行分离时无法基线分离、峰形矮胖和严重拖尾,改变色谱流动相成分或改变流动相中有机相比例均无法解决上述问题。Acclaim 120 C18柱具有极高的表面覆盖率和极低的金属含量,通过优化上样和净化条件可去除大量杂质,有效保留2种目标化合物,并获得良好分离度和峰形。因此,本研究选择Acclaim 120 C18柱作为在线萃取柱。
2.1.2淋洗液和洗脱液的选择比较了纯水、体积比分别为10∶90、20∶80、30∶70、40∶60的甲醇-水作为淋洗液的除杂效果。结果表明:30%体积比的甲醇除杂效果最佳,且能保留目标物;当甲醇比例达到40%时,目标物在上样后不能被保留在萃取柱上。将色谱流动相作为洗脱液可以简化实验步骤,缩短分析时间,本研究以乙腈-水(70∶30,V/V)作为洗脱溶液,可在短时间内将目标物洗脱。
2.2 分离条件优化
2.2.1流动相的选择分别比较了甲醇-水、甲醇-乙酸铵、乙腈-水、乙腈-乙酸铵的分析效果。结果表明这四种流动相均可以将目标物分离并获得良好峰形。考虑到乙腈毒性较大,色谱级乙腈价格较高以及缓冲盐对色谱柱和仪器有损伤,本研究选择甲醇-水作为流动相。研究还比较了流动相中甲醇比例对分离效果的影响,结果表明甲醇∶水=70∶30(V/V)为流动相时目标物分离度和峰形最好。
2.2.2色谱柱的选择比较了Agilent SB-C18柱、Agilent XDB-C18柱、迪马C18柱、Agilent Extend-C18柱对目标物的分离效果。在相同分离条件下,目标物除在Agilent SB-C18柱上有明显拖尾外,在其余三种色谱柱上均可以获得良好分离度和峰形。本研究选择柱压较小的Agilent Extend-C18柱作为分离柱。
2.2.3柱温和流速的选择本研究对柱温(25、30、35、40 ℃)和流速(0.6、0.8、1.0、1.2 mL/min)对分离效果的影响进行了考察。柱温对目标物分离度、保留值和峰形的影响不大,但柱温达到40 ℃时,Acclaim 120 C18萃取柱对对羟基苯甲酸乙酯保留能力明显减弱,对羟基苯甲酸乙酯和杂质一起在1 min左右被从萃取柱洗脱,造成其响应值明显减低。选择室温25 ℃作为检测柱温。流速主要影响的是柱压和保留值,为保护色谱柱和减少分析时间,选择1 mL/min作为检测流速。在已优化的萃取条件、分离条件和检测条件下,分别对两种对羟基苯甲酸甲酯的混合标准溶液和样品进行测定,所得图谱见图3和图4。
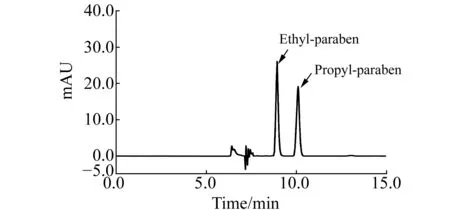
图3 对羟基苯甲酸酯标准混合溶液(5 μg/mL)色谱图Fig.3 Chromatograms of the mixed standard solution of 2 parabens(5 μg/mL)

图4 样品的色谱图(256 nm)Fig.4 Chromatogram of sample(256 nm)
2.3 方法的线性与定量限
用水配制系列浓度的标准混合溶液,并按上述优化后的条件进行分析。结果表明,2种对羟基苯甲酸酯在0.5~400 μg/mL浓度范围内线性良好,相关系数r2>0.9999。在空白样品中添加一系列低浓度的标准溶液,根据3倍信噪比计算检测限,结果见表2。

表2 2种对羟基苯甲酸酯线性方程与相关系数Table 2 Linear equations and correlation coefficients(r2) of 2 parabens
2.4 方法的回收率和精密度
称取适量碳酸饮料空白样品进行低、中、高3个水平加标(中水平加标量为GB 2760-2014[7]规定的最大限量值),每个水平重复测定6次,计算回收率和相对标准偏差(RSD)。结果见表3。

表3 回收率和精密度实验结果Table 3 Results of recovery and precision test
2.5 实际样品检测
从南京市鼓楼区的超市购买碳酸饮料样品共10份,采用本方法进行分析检测。检测结果均为阴性。
3 结论
本研究建立了在线固相萃取-高效液相色谱检测碳酸饮料中2种对羟基苯甲酸酯的分析方法。碳酸饮料样品经稀释过滤后可直接上样,无需其他前处理步骤。通过优化在线萃取条件和分离条件,可以实现2种对羟基苯甲酸酯的有效分离,并且可以获得较为理想的准确度和精密度。方法具有操作简单、快速简便、节省大量时间、重现性好等优点,能够满足碳酸饮料中对羟基苯甲酸酯的定量分析要求,具有实际应用价值。
