5-氟尿嘧啶聚乳酸缓释片的处方筛选及体外释药机制研究Δ
2017-10-13崔丽珺黄洁李兴华康前雁西安交通大学医学院第一附属医院眼科西安7006西安市食品药品检验所西安70054西安交通大学医学院第二附属医院药剂科西安70004
崔丽珺,黄洁,李兴华,康前雁(.西安交通大学医学院第一附属医院眼科,西安7006;.西安市食品药品检验所,西安 70054;.西安交通大学医学院第二附属医院药剂科,西安 70004)
5-氟尿嘧啶聚乳酸缓释片的处方筛选及体外释药机制研究Δ
崔丽珺1*,黄洁2,李兴华3,康前雁1(1.西安交通大学医学院第一附属医院眼科,西安710061;2.西安市食品药品检验所,西安 710054;3.西安交通大学医学院第二附属医院药剂科,西安 710004)
目的:筛选5-氟尿嘧啶(5-FU)聚乳酸(PLA)缓释片(5-FU-PLA-DS)的处方,研究其体外释药机制。方法:采用紫外分光光度法测定释放介质中5-FU含量,以模拟体液为释放介质,于37℃水浴中进行体外释放试验。以分子量分别为3 000、6 000、10 000、15 000和20 000的PLA,制备载药量分别为1.5、2.5、3.0 mg/片,直径3.0 mm、厚1.0 mm的15种圆形5-FU-PLA-DS;以有效浓度持续释放时间与累积释放度为指标,筛选最优处方。采用扫描电镜观察5-FU-PLA-DS释药后的形态,评价其释药机制。结果:最优处方中PLA的分子量为20 000,载药量为3.0 mg/片;所制5-FU-PLA-DS可释放119 d,累积释放度为100.63%,有效浓度持续释放91 d。扫描电镜观察显示,5-FU-PLA-DS表面的微球最先接触释放介质而进行蚀解、释放药物,待外层的微球和微球之间的PLA降解后才逐渐暴露出内层的微球进行释药,其释药机制主要为溶蚀和扩散。结论:成功制得5-FU-PLA-DS,其有效浓度持续释放时间长,能够由外向内有步骤地降解,实现不同层次微球的非同步释药。
5-氟尿嘧啶;聚乳酸;缓释片;体外释放度;扫描电镜
滤过性手术(Glaucoma filtration surgery,GFS)是治疗青光眼最常用的手术方式之一,但术后2年内的失败率仍达15%~25%,主要原因是成纤维细胞的增殖、细胞外间质中的胶原和葡糖胺聚糖大量合成,导致滤过道瘢痕化[1]。5-氟尿嘧啶(5-fluorouracil,5-FU)是临床上公认的、能有效抑制青光眼滤过泡纤维化的抗代谢药物[2],但是由于频繁结膜下注射,且单次注射造成结膜下药物浓度过高,易引起角膜、结膜毒性反应和滤过过畅。以可生物降解的生物材料为载体,包载抗代谢药物、抑制纤维血管增生关键因子或抗体的缓控释制剂,是目前青光眼抗瘢痕治疗研究的新趋势[3]。就5-FU这一经典的抗代谢药物来说,微球制剂的发展已经比较成熟,能够做到粒径均匀、缓释效果明显,但是总的载药量较少、释药时间短[4-6]。而报道的结膜下植入型片剂、膜剂,含药量虽然很高,但由于是采用单纯物理混合或压制而成,释药速度过快、释放时间亦短;此外释放速度快会造成局部药物浓度过高,增加并发症的发生率[7-9]。本研究以5-FU和不同分子量聚乳酸(Poly lactic acid,PLA)为原料,制备5-FU-PLA缓释片(5-FU-PLA sustained-release discs,5-FU-PLA-DS),并建立体外释放度的测定方法,考察其体外释药情况及释放后的形态变化,研究其释药机制。
1 材料
1.1 仪器
TU-1901型紫外-可见分光光度计(北京普析通用仪器有限公司);YKH-3型液体快速混合器(北京鸿泰顺达科技有限公司);DT5-4C型离心机(北京时代北利离心机有限公司);BSA124S-CW型万分之一天平[赛多利斯(中国)有限公司];MS105型十万分之一天平[梅特勒托利多(中国)有限公司];JSM-840型扫描电镜(日本Jeol公司)。
1.2 药品与试剂
外消旋PLA(山东省医疗器械研究所,批号:15031801、15031802、15031807、15031808、15031809,分子量:3 000、6 000、10 000、15 000、20 000);山梨糖醇酐单油酸酯(司盘80,上海纪宁生物科技有限公司,分析纯);5-FU对照品(中国食品药品检定研究院,批号:08052897,纯度:100%);5-FU原料药(上海瀚思化工有限公司,批号:A106011217,纯度:98.5%);二氯甲烷(天津基准化学试剂有限公司,分析纯);石油醚(天津市大茂化学试剂厂,分析纯);盐酸(西安市化学试剂厂,分析纯);其余试剂均为分析纯。
2 方法与结果
2.1 5-FU-PLA-DS的制备
将5-FU原料药充分研磨,200目筛网过筛后干燥备用。称取处理过的5-FU原料药,悬浮于含PLA及司盘80的二氯甲烷3 mL中,在液体快速混合器的高速搅拌下缓慢滴加石油醚15 mL(10~15滴/min);待过量载体使微球聚积沉淀而上层液变清透后,再加入石油醚15 mL,固化10 min。3 000 r/min(离心半径10 cm)离心15 min,将白色糊状、质地均匀的沉淀物取出,置于表面涂有少许甘油的玻璃模具(3.0 cm×2.5 cm×1.0 mm)中,稍微加压使其充满模具。表面干燥后,以直径3.0 mm的管状模具进行切割,50℃烘箱干燥。同时,按照上述方法制作与5-FU-PLA-DS规格相同,但不含5-FU的PLA空白缓释片(PLA-DS)。分别用5种分子量(3 000、6 000、10 000、15 000、20 000)的PLA制备不同载药量(1.5、2.5、3.0 mg/片)的5-FU-PLA-DS,为方便描述和记录,以代称表示15种缓释片,如1.5P3表示5-FU载药量1.5 mg/片,PLA分子量3 000;3.0P20表示5-FU载药量3.0 mg/片,PLA分子量20 000;以此类推。不同载药量的5-FU-PLA-DS的处方组成见表1。
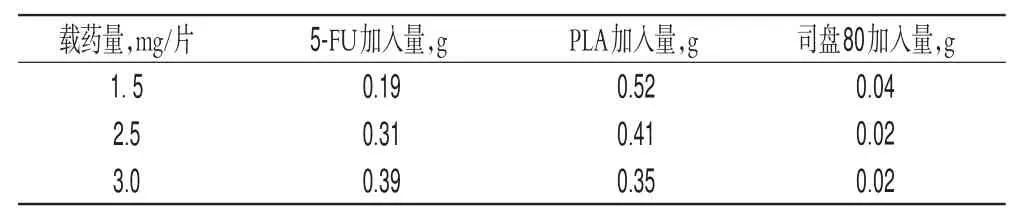
表1 不同载药量的5-FU-PLA-DS的处方组成Tab 1 Formulation composition of 5-FU-PLA-DS with different drug loading amount
2.2 体外释放度的测定
2.2.1 模拟体液(Simulated body fluid,SBF)的制备 烧杯中加入750 mL纯化水,36.5℃保温,依次加入7.996 g NaCl、0.350 g NaHCO3、0.224 g KCl、0.228 g K2HPO4·2H2O、0.305 g MgCl2·6H2O、40 mL 1 mol/L的HCl溶液、0.278 g CaCl2、0.071 g Na2SO4,逐个加入,待一种完全溶解后再加入下一种;最后加入6.057 g(CH2OH)3CNH2,加入时应一点一点加,每次不超过1 g,避免局部pH值增加;搅拌均匀,36.5℃时调节pH至7.5左右,然后再用1 mol/L的HCl溶液将pH调至7.25;转移到1 000 mL量瓶中,用纯化水定容至刻度,摇匀,5~10℃冰箱储存备用。
2.2.2 对照品溶液的制备 精密称取5-FU对照品2.5 mg,置于10 mL量瓶中,加SBF使溶解并定容至刻度,制备成0.25 mg/mL的对照品贮备液。移取对照品贮备液0.1、0.2、0.3、0.4、0.6、0.8、1.0、1.2 mL,分别置于5 mL量瓶中,加SBF定容至刻度,制备成0.005、0.010、0.015、0.020、0.030、0.040、0.050、0.060 mg/mL的对照品溶液。2.2.3 检测波长的选择 取1片5-FU-PLA-DS,溶于二氯甲烷中,振荡摇匀,SBF萃取。取SBF溶液层,在200~400 nm波长范围内进行紫外扫描。结果,5-FU在203 nm和265.5 nm波长处均有最大吸收。考虑到SBF的截止波长,最终选择265.5 nm为5-FU的检测波长,与《中国药典》(二部)规定[10]一致。同样取1片PLA-DS,按上述方法处理后紫外扫描,结果上清液在265.5 nm波长处几乎没有紫外吸收,表明其对5-FU的测定不造成干扰。2.2.4 线性关系考察 以PLA-DS的SBF萃取液为空白对照,在265.5 nm波长处依次测定“2.2.2”项下对照品溶液的吸光度(A),并以5-FU的质量浓度(x)对A进行线性回归,得回归方程为A=45.496x+0.147 5(r=0.999 9)。结果表明,5-FU检测质量浓度的线性范围为0.005~0.060 mg/mL。
2.2.5 精密度试验 取0.010、0.030、0.050 mg/mL(低、中、高质量浓度)的5-FU对照品溶液,在265.5 nm波长处测定吸光度,第1天内测定5次,之后每天测定1次,连续测定5 d,考察日内、日间精密度。结果低、中、高质量浓度对照品溶液的日内RSD分别为0.698%、0.641%、0.509%(n=5),日间 RSD 分别为 1.534%、1.205%、1.214%(n=5),满足相关规定要求。
2.2.6 准确度试验 取0.010、0.030、0.050 mg/mL(低、中、高质量浓度)的5-FU对照品溶液,分别在265.5 nm波长处测定吸光度,根据标准曲线回归方程计算浓度。以测定值与真实值之间的比值计算回收率。结果,低、中、高质量浓度对照品溶液的平均回收率分别为100.01%、98.87%、99.90%,RSD均小于1%(n=3)。
2.2.7 稳定性试验 制备5-FU质量浓度为0.030 mg/mL的SBF溶液(pH 7.4),置于具塞锥形瓶中,37℃恒温水浴孵育,每天定时取样,在265.5 nm波长处测定吸光度,连续测定7 d。结果,7 d后SBF中5-FU的相对含量仍维持在99.03%,吸光度的RSD=0.36%(n=7),表明5-FU在SBF中是比较稳定的。
2.3 体外释放试验
2.3.1 5-FU饱和溶解度测定 取2 mL SBF置于具塞离心管中,加入过量的5-FU原料药,超声使其分散均匀,37℃水浴磁力搅拌。30 min后取样,经0.45µm滤膜过滤,弃初滤液,取续滤液稀释后测定其吸光度。根据标准曲线回归方程计算5-FU在SBF中的饱和溶解度,结果为35.16 mg/mL。所以试验设计中设定的释放介质的体积,完全可以满足“漏槽”条件。
2.3.2 体外释放度测定 15种5-FU-PLA-DS随机选取6片,称质量后置于一端封口的管状释放装置底部,分别加入SBF释放介质5 mL,37℃水浴中进行释放,定时取样并补充新鲜SBF。将取出的溶液适当稀释,以PLADS的SBF萃取液作为空白对照,在265.5 nm波长处测定吸光度,根据标准曲线回归方程计算5-FU的含量,再计算累积释放度,绘制体外释放曲线。每周测定标准溶液并校正标准曲线。取样时间点为:第1天的2、4、8、16、24 h;第1周每日1次;第2周隔日1次;第3~5周每4 d 1次;第6周之后每周1次。第1天2、4、8 h取样后分别补充新鲜SBF 0.3、0.6、1.0 mL,之后各时间点取样后均补充新鲜SBF 1.0 mL。最低有效浓度设定为10 μg/mL[11],如果日平均释放浓度<5 μg/mL并持续2个时间点,且累积释放量大于含药量的90%,则停止取样。15种5-FU-PLA-DS的体外释放曲线见图1,主要体外释放参数见表2。
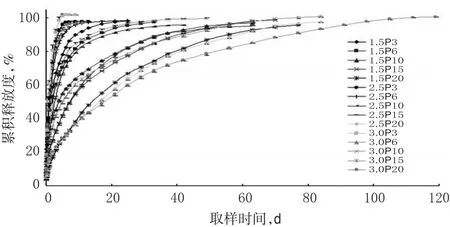
图1 15种5-FU-PLA-DS的体外释放曲线(n=6)Fig 1 The in vitro release curves of 15 species of 5-FU-PLA-DS(n=6)
从表2可以看出,对于PLA分子量小(3 000、6 000)的缓释片,载药量越高,释放速度越快,有效浓度持续时间越短,突释效应越明显(第1天累积释放度越大);而PLA分子量大(20 000)的缓释片,随着载药量的增高,有效浓度持续时间明显延长且释放更彻底,突释效应不明显。综合考虑,确定5-FU-PLA-DS处方为5-FU载药量3.0 mg/片,PLA分子量20 000。所制5-FU-PLA-DS可持续释药119 d,有效浓度持续时间91 d。

表2 15种5-FU-PLA-DS的主要体外释放参数Tab 2 Main in vitro release parameters of 15 species of 5-FU-PLA-DS
2.3.3 释药形态观察 观察释放后5-FU-PLA-DS的表面形态。按“2.3.2”确定的处方制备5-FU-PLA-DS 6片进行体外释放,分别于释放前和释药14、28、56、84 d及释药结束(释药119 d)时各取出1片,经清洗、烘干,进行扫描电镜观察其形态变化,扫描电镜图见图2。
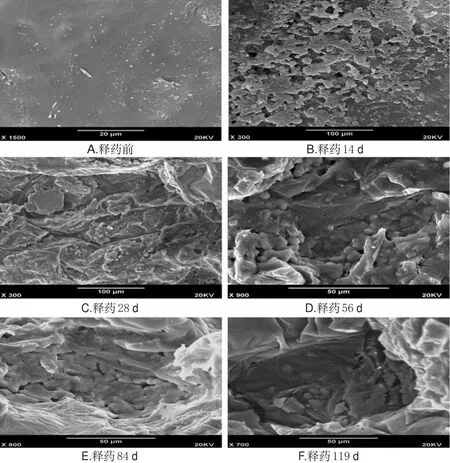
图2 最优处方5-FU-PLA-DS体外释药不同时期的扫描电镜图Fig 2 Scanning electron microscopy of in vitro release of 5-FU-PLA-DS with optimal formulation in different drug-release time
由图2可以看出,5-FU-PLA-DS释药前表面平整;释药14 d表层微球开始蚀解、脱落,留下圆形的空隙;释药28 d表层微球完全降解,暴露出深层的微球;释药56 d暴露出深层密集的聚积微球和基质,并可见裂隙、孔洞向内部延伸深;释药84 d表面形成许多较大的孔洞,孔洞间通过许多裂隙和通道相互连接;释药119 d孔洞内的聚积微球消失,孔内深部仍有少数聚积微球。由此推测5-FU-PLA-DS是由聚积的微球构成,其释药机制主要为溶蚀和扩散。
2.3.4 缓释片残余药量测定 将体外释放后的缓释片用二氯甲烷溶解,经HCl萃取后,于265.5 nm波长处测定吸光度,计算残余药量。结果测得残余药量为(72±6)µg(n=6),残余百分数为2.35%。由此可见,所选处方5-FU-PLA-DS的释放都是比较完全的。
3 讨论
5-FU是目前青光眼滤过术的经典辅助用药,可以明显提高青光眼手术的成功率[7],但频繁结膜下注射使患者痛苦,单次注射药物浓度过高,在抑制滤过泡瘢痕形成的同时,必然不同程度地影响眼部其他代谢旺盛组织,易引起角膜、结膜毒性反应[12]。已有不少学者致力于研究5-FU生物可降解缓控释制剂,并进行兔眼、猴眼等活体研究,但缺乏以最低有效浓度进行长期、稳定的释药研究。
PLA是合成高分子材料中的一种新型聚合物,具有良好的生物相容性和可降解吸收性,通过调节分子量、结构和组成等手段可改变其力学性能和降解速度,生物可塑性强,目前已经广泛应用于医学的基础研究和临床[13]。PLA类载体材料的释药主要与药物分子量及分子量的分布,药物与PLA的比例,制剂形状、大小、厚薄、体积及药物的极性等因素有关[14]。从笔者研究中也可以看出,随着PLA分子量增加,有效浓度持续时间逐渐延长,平均日释药浓度降低,突释效应减小;随着5-FU的载药量增加,释药速度加快,突释效应明显。
当5-FU-PLA-DS接触SBF后,表层微球首先暴露并降解、释放药物,药物溶解扩散后留下的通道使微球更容易降解;而间隔于微球之中的PLA并不含药或含药较少,降解速度明显较慢。从扫描电镜图可以证实,整个5-FU-PLA-DS的降解过程是从外向内逐层进行:当表层微球降解、脱落,遇到过量PLA形成的间隔后,要等待PLA降解暴露出内层的微球,再开始溶解释放药物。正是这种由外向内有步骤地降解、不同层次微球逐渐释药,使得5-FU以有效浓度缓慢、平稳、长期地释放,而PLA的分子量控制了整个缓释片的释药速度和时间。
综上所述,本研究成功制得5-FU-PLA-DS,其有效浓度持续释放时间长,能够由外向内有步骤地降解,实现不同层次微球的非同步释药。
[1] Sharma A,Anumanthan G,Reyes M,et al.Epigenetic modification prevents excessive wound healing and scar formation after glaucoma filtration surgery[J].Invest Ophthalmol Vis Sci,2016,57(7):3381-3389.
[2] Amoozgar B,Lin SC,Han Y,et al.A role for antimetabolites in glaucoma tube surgery:current evidence and future directions[J].Curr Opin Ophthalmol,2016,27(2):164-169.
[3] Xu Y,Lyu L.Progression of drug delivery system for glaucoma[J].Zhonghua Yan Ke Za Zhi,2014,50(12):946、951.
[4] 黎靖,魏郁梦,杨红茹,等.氟尿嘧啶中空微球的制备、表征及释药性能[J].重庆医科大学学报,2016,41(5):448-452.
[5] 黄慧玲,李益,王玥,等.5-FU-PLGA复乳微球的制备及体外释放[J].化学工业与工程,2016,33(1):76-81.
[6] Huang Y,Wei Y,Yang H,et al.A 5-fluorouracil-loaded floating gastroretentive hollow microsphere:development,pharmacokinetic in rabbits,and biodistribution in tumor-bearing mice[J].Drug Des Devel Ther,2016,3(10):997-1008.
[7] Huhtala A,Rönkkö S,Teräsvirta M,et al.The effects of 5-fluorouracil on ocular tissues in vitro and in vivo after controlled release from a multifunctional implant[J].Invest Ophthalmol Vis Sci,2009,50(5):2216-2223.
[8] Rodríguez-Agirretxe I,Vega SC,Rezola R,et al.The PLGA implant as an antimitotic delivery system after experimental trabeculectomy[J].Invest Ophthalmol Vis Sci,2013,54(8):5227-5235.
[9] Wu Z,Li S,Wang N,et al.A comparative study of the safety and efficacy effect of 5-fluorouracil or mitomycin C mounted biological delivery membranes in a rabbit model of glaucoma filtration surgery[J].Clin Ophthalmol,2013,doi:10.2147/OPTH.S34200.
[10] 国家药典委员会.中华人民共和国药典:二部[S].2015年版.北京:中国医药科技出版社,2015:751.
[11] Masoumpour MB,Nowroozzadeh MH,Razeghinejad MR.Current and future techniques in wound healing modulation after glaucoma filtering surgeries[J].Open Ophthalmol J,2016,10(9):68-85.
[12] Na JH,Sung KR,Shin JA,et al.Antifibrotic effects of pirfenidone on Tenon’s fibroblasts in glaucomatous eyes:comparison with mitomycin C and 5-fluorouracil[J].Graefes Arch Clin Exp Ophthalmol,2015,253(9):1537-1545.
[13] 齐雪飞,庞秀炳,吴侃.聚乳酸及其共聚物在医疗器械领域内的应用[J].中国医疗器械杂志,2014,38(4):274-277.
[14] 罗宇燕,成晓岚,郭喆霏,等.微球中聚乳酸羟基乙酸共聚物浓度与微球结构、释药、降解的关系研究[J].中国药房,2015,26(7):986-990.
Formulation Screening of 5-fluorouracil Polylactic Acid Sustained-release Tablet and Study on Its in vitro Drug-release Mechanism
CUI Lijun1,HUANG Jie2,LI Xinghua3,KANG Qianyan1(1.Dept.of Ophthalmology,the First Affiliated Hospital of Medical College,Xi’an Jiaotong University,Xi’an 710061,China;2.Institute for Food and Drug Control of Xi’an,Xi’an 710054,China;3.Dept.of Pharmacy,the Second Affiliated Hospital of Medical College,Xi’an Jiaotong University,Xi’an 710004,China)
OBJECTIVE:To screen the formulation of 5-fluorouracil(5-FU)polylactic acid(PLA)sustained-release discs(5-FU-PLA-DS),and study its in vitro drug-release mechanism.METHODS:UV spectrophotometry was used to determine the 5-FU content in the release medium.Using simulate body fluid as release medium,in vitro drug-release test was conducted under 37℃ water bath.Using PLA with molecular weight of 3 000,6 000,10 000,15 000,20 000,15 species of round 5-FU-PLA-DS with drug containing of 1.5,2.5,3.0 mg/piece and 3.0 mm in diameter and 1.0 mm in thickness were prepared.Using effective concentration sustained release time and cumulative release rate as indexes,the optimal formulation was screened.The form of 5-FU-PLA-DS was observed by scanning electron microscopy after release,and its release mechanism was evaluated.RESULTS:In the optimal formulation,the PLA molecular weight was 20 000 and drug containing was 3.0 mg/piece.The prepared 5-FU-PLA-DS can release for 119 d,with cumulative release degree of 100.63%and effective concentration sustained for 91 d.Scanning electron microscopy showed that the microspheres at the surface were degraded to the release medium first,and then the microspheres of inner layer exposed and release drug gradually after PLA degraded.The main mechanism of drug-release was melting and diffusion.CONCLUSIONS:5-FU-PLA-DS is successfully prepared,with long release time in effective concentration,can be degraded step by step from outside to inside and achieve non-synchronous drug-release of microspheres at different layers.
5-fluorouracil;Polylactic acid;Sustained-release tablet;in vitro drug-release rate;Scanning electron microscopy
R943
A
1001-0408(2017)28-3969-04
2017-05-11
2017-08-07)
(编辑:邹丽娟)
国家自然科学基金资助项目(No.81300765)
*主治医师,博士。研究方向:青光眼、白内障。电话:029-85323960。E-mail:cuilijun@mail.xjtu.edu.cn
DOI 10.6039/j.issn.1001-0408.2017.28.22
