生活中常见的两种有机物
2017-10-12郑良周
郑良周
摘要:针对实验课的教学进行设计,即在完成必须的基础实验课内容后,以学生感兴趣的微生物学问题为主体,让学生自己设置实验内容,建立实验方案,并在教师的指导下从事科学研究,在探索中掌握知识、培养技能,激发他们探索问题、渴求知识的欲望和学习兴趣[1]。
关键词:乙酸的结构;乙酸的性质;乙酸乙酯的制取;酯化反应的特点
一、教学目标
1、了解乙酸的主要用途。
2、掌握乙酸的组成与主要性质。
3、学会分析官能团与物质性质关系的方法。
二、教学重点
乙酸的结构和性质是本课时的教学重点,特别是酯化反应的特点和过程分析即对酯化反应演示实验的观察和有关问题及数据分析、推理又是性质教学中的重点。
三、教学难点
酯反应的反应原理。
课堂教学设计。
[引入]插播电影《天下无贼》片断剥鸡蛋思考:结合现象及生活中已有的知识,你能猜出使鸡蛋“脱去外衣”的物质是什么?
上节课我们学习乙醇的结构和一些重要的性质,知道它是酒的主要成分,那你又是否知道:为什么酒的年份越长味道就越香?厨师烧鱼时加醋并加点酒,鱼的味道就变得无腥、鲜美?通过本节课的学习我们就能够知道其中的奥妙。
[板书]生活中两种常见的有机物—乙酸。
[展示]无水乙酸样品,让学生观察并总结乙酸的物理性质(颜色、状态和气味)。
[板书]物理性质。
①无色有强烈刺激性气味的液体。
②易溶于水乙醇等溶剂。
③沸点:117.9℃熔点:16.6℃。
[讲述]当温度低于16.6℃时无水乙酸易凝结成冰一样的晶体,所以无水乙酸又称为冰醋酸。
思考:冰醋酸为混合物吗?
[过渡]刚才我们已经了解了乙酸的一些外观特征,为什么酒的年份越长味道就越香?厨师烧鱼时加醋并加点酒,鱼的味道就变得无腥、鲜美?让我们看看它到底发生了什么反应?
[展示]乙酸分子的球棍模型,让学生总结乙酸的化学式、结构式和结构简式。
[板书]分子组成与结构。
①化学式:C2H4O2。②结构式:③结、构简式。④官能团。
[讲述]乙酸可以看作是甲基和羧基组成的。
[板书]化学性质。
实验探究一:乙酸具有酸性吗?
请利用下列药品设计实验方案来证明乙酸具有酸性。
镁条、乙酸溶液、石蕊试液、碳酸钠粉末。[板书]弱酸性。
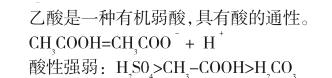
[归纳]通过前面几个小实验可以证明乙酸具有酸的通性:能与活泼金属、碱、盐等物质发生反应。乙酸的酸性比硫酸、盐酸等的酸性弱,但比碳酸的酸性强。
[观看“除去水垢”漫画,说出其中的道理]。
[投影]乙酸除去水垢的原理。
[思考]你知道吗?
厨师烧鱼时常加醋并加点酒,这样鱼的味道就变得无腥、香醇,特别鲜美。
[阅读思考]课本第148页—第149页,
①什么是酯化反应?有何特点?
②实验5—7中,反应所需的药品是什么?各起什么作用?药品的添加顺序如何?
③实验装置有何特点?
[讲解]酯化反应的概念(由学生回答)
实验探究二:乙酸乙酯的制取(教材P15)。
观察与讨论。
①图中发生装置有何特点?为什么使用长导管?导管口为什么要在溶液的液面上方?
注意:不能伸到液面以下(防倒吸)。
②药品的添加顺序如何?
③浓硫酸的作用是什么?
④得到的产物是否纯净?
主要杂质有哪些?
投影出示下表。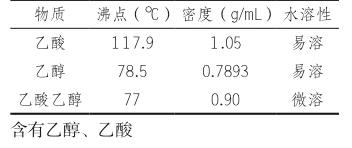
⑤为什么要用饱和的碳酸钠溶液来吸收产品?
除去乙酸、溶解乙醇,降低乙酸乙酯在水中的溶解度
2酯化反應(学生完成化学方程式)
定义:酸和醇起作用,生成酯和水的反应叫做酯化反应。
思考:酯化反应中酸和醇分子内的化学键怎样断裂?
同位素示踪法:—研究有机反应机理常用的方法。
实质:酸脱羟基、醇脱氢(羟基上的)注意:可逆反应。
反应类型:取代反应。
通过这种层层递进式的教学,可培养学生科学的思维方法,亲身感知和体验化学实验在科学探索过程中的作用和地位。
[板书]酯化反应的实质:酸脱羟基、醇脱氢(羟基上的)。
强调:羧基的存在使得乙酸即具有酸性,又能够发生酯化反应
[过渡]结构决定性质,性质决定用途。
[板书]乙酸的重要用途。
乙酸是一种重要的有机化工原料。可用于生产醋酸纤维、合成纤维、喷漆溶剂、香料、染料、医药以及农药等。同时,乙酸是食醋的重要成分,也可用于杀菌消毒。
当堂练习:
(1)分别将一小块钠投入下列物质中,能生成氢气,但生成氢气的速率最慢的是( )。
A.乙酸 B.碳酸
C.乙醇 D.水
(2)在3支试管中从左至右分别放有:①1mL乙酸乙酯和3mL水 ②1mL溴苯和3mL水 ③1mL乙酸和3mL水。下图中3支试管从左到右的排列顺序为( )。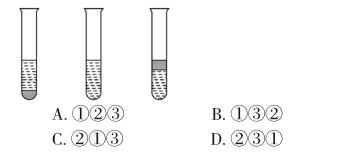
(3)酯类物质广泛存在于香蕉、梨等水果中。某实验小组从梨中分离出一种酯,然后将分离出的酯水解,得到乙酸和另一种分子式为C6H13OH的物质。下列分析不正确的是( )。
A.C6H13OH分子中含有羟基
B.实验小组分离出的酯可表示为CH3COOC6H13
C.C6H13OH可与金属钠发生反应
D.这种酯易溶于水
参考文献
[1] 葛秋莲.初中化学实验课的过程探索[J].吉林教育:教研,2010(5):49-49.endprint
