密蒙花颗粒的急性毒性实验研究
2017-10-11彭晓芳覃艮艳张又玮彭清华
彭晓芳,王 英,覃艮艳,张又玮,彭 俊,彭清华
(湖南中医药大学中医眼科学重点学科,湖南 长沙 410208)
·方药研究·
密蒙花颗粒的急性毒性实验研究
彭晓芳,王 英,覃艮艳,张又玮,彭 俊,彭清华*
(湖南中医药大学中医眼科学重点学科,湖南 长沙 410208)
目的 观察密蒙花颗粒对小鼠的急性毒性反应及死亡情况,为临床应用安全性提供依据。方法 将30只小鼠分别用不同浓度及最大浓度密蒙花颗粒混悬液灌胃进行预实验,观察7 d未见小鼠死亡,无法测出LD50,故进行最大耐受量(MTD)的测定。将40只小鼠随机分为给药组和空白对照组,根据小鼠可承受的最大体积分别用最大混悬浓度的密蒙花颗粒和蒸馏水1 d内灌胃2次,连续观察14 d,每天记录小鼠的一般状况、体质量,14 d后处死动物,测定小鼠的血常规指标,肝、脾、肾等主要脏器指数,观察解剖学及病理组织学改变情况。结果 给药组小鼠无死亡,与空白对照组比较,给药组小鼠的体质量变化无显著差异(P>0.05),血常规指标与空白对照组亦无显著差异(P>0.05),小鼠密蒙花颗粒日最大耐受量为114 g/kg。结论 急性毒性结果表明,密蒙花颗粒临床常用量是安全的。
密蒙花颗粒;急性毒性试验;半数致死量;最大耐受量
随着现代生活习惯及自然环境的改变,干眼症的发病率越来越高,湖南中医药大学第一附属医院眼科专家彭清华教授经过长期的临床实践,组方密蒙花颗粒,该药由密蒙花、枸杞子等六味药组成,对于干眼症有良好的临床疗效,为进一步开发该特色制剂,评价其安全性,我们对密蒙花颗粒进行急性毒性实验研究,以期为临床安全应用提供实验依据。
1 材料
1.1 实验材料
1.1.1 受试药物 密蒙花颗粒,主要成分为密蒙花、枸杞子等,购于湖南中医药大学第一附属医院门诊部药房,将单味中药免煎颗粒组配。密蒙花颗粒每日临床推荐用量为18 g,实验前将本品配制成可供小鼠灌胃的最大浓度混悬液,每毫升相当于0.95 g生药。
1.1.2 试验动物 昆明种小鼠,70只,清洁级,18~24 g,雌雄各半,由湖南斯莱克景达实验动物有限公司提供, 许可证号:SYXK (湘)2011-0003,SYXK (湘)2013-0004,小鼠用塑料盒群养,雌雄分笼,每箱≤11只,每天喂饲鼠用配合饲料,自由饮水,视情况更换笼具和垫料。饲料来源于湖南斯莱克景达实验动物有限公司。
1.2 主要仪器
C0006型电子分析天平 (日本AND公司),XN9000型希森美康XN全自动血液分析流水线(日本Sysmex公司),4062型石蜡切片机(德国SLEE),CM1850型恒冷箱切片机(德国LEICA)水合氯醛(上海国药集团生产),罗氏Cobas8000 CCM全自动生化免疫流水线(瑞士罗氏公司),真空采血管、一次性采血针,止血钳、组织剪、有齿镊等。
2 实验方法
参照文献[1-4]及《中药药理实验方法学》的急性毒性实验方法[5]。
2.1 预实验
按照半数急性毒性实验要求先进行毒性实验预实验预测本品的致死量 (LD50)[6],取体质量18~24 g小鼠30只,随机分3个组,每组10只,雌、雄各半,动物适应饲养3 d后,禁食不禁水12 h后,分别灌胃给予浓度 0.950 g/mL、0.475 g/mL、0.238 g/mL的密蒙花颗粒,小鼠灌胃可承受的最大体积(40 mL/kg),1 d给药3次,相当于三组小鼠日给药剂量分别为 114 g/kg、57 g/kg、28.5 g/kg。 给药后自由进食和饮水,连续观察7 d,记录小鼠死亡数。计算出零致死量(Dn)和全致死量(Dm),进而计算出半数致死量[7-9]。
2.2 最大耐受量的测定
KM清洁级小鼠40只,试养1周后,按体质量随机分为空白对照组和给药组(每组20只),每组雌雄各半,禁食不禁水12 h后,给药组以本品可供灌胃的最大浓度0.95 g/mL,小鼠灌胃可承受的最大体积 (40 mL/kg),灌胃给药1 d,24 h内给药3次,经计算,最大耐受量倍数=(每只小鼠的耐受量/小鼠平均体质量20 g)×(成人平均体质量50 kg/成人每日用量18 g),相当于成人临床用量的317倍左右,给药间隔时间4 h,间隔期间不供食,末次给药4 h后自由进食和饮水,空白对照组给予等容积的蒸馏水,连续观察14 d。
2.3 指标测定
观察行为活动、肌肉运动、植物神经系统反应、呼吸及心血管、胃肠方面、皮肤颜色、眼及泌尿生殖系统等。
小鼠14 d观察期结束后,摘除眼球取血,分别进行血常规白细胞(WBC)、红细胞(RBC)、血红蛋白(HGB)、血小板(PLT)、淋巴细胞比率(LYM%)的检测。
取血完毕,解剖取肝、脾、肾等主要脏器精密称质量,计算脏器指数:脏器指数(mg/g)=脏器质量/体质量;取脑、心、肝、脾、肺、肾、卵巢、睾丸、胃、小肠、视网膜等主要脏器,多聚甲醛固定,HE染色,进行组织病理学检查。
2.4 统计学处理
3 结果
3.1 半数致死量实验
在灌胃后7 d观察时间内,小鼠一般状态、行为活动、饮食情况、分泌物和排泄物等均未见明显异常,未见小鼠死亡;7 d后,处死小鼠,肉眼观察其脑、心、肝、脾、肺、肾、睾丸卵巢等主要脏器,均未见明显的病理学变化。因无法测出密蒙花颗粒的半数致死量,故进行其最大耐受量实验。
3.2 指标测定结果
3.2.1 小鼠一般情况观察 小鼠一般状况观察实验结果表明,实验小鼠以密蒙花颗粒最大混悬浓度和可承受的最大体积1 d 3次灌胃给药后,大部分小鼠出现喜静卧,活动量减少、闭目、反应迟钝、大便稍湿,但无竖毛、抽搐、翻倒等异常情况,对照组与给药组情况类似,于第2天恢复正常,连续观察14 d,小鼠无死亡情况出现。
3.2.2 对小鼠体质量的影响 小鼠体质量变化:给药前,给药组与对照组比较,雌、雄性小鼠体质量差异无统计学意义。给药后,雄性小鼠,给药组与对照组相比,体质量差异无统计学意义(P均>0.05);雌性小鼠,给药组与对照组比较,体质量差异无统计学意义(P均>0.05),说明给药后,密蒙花颗粒对小鼠体质量无影响,详见表1。
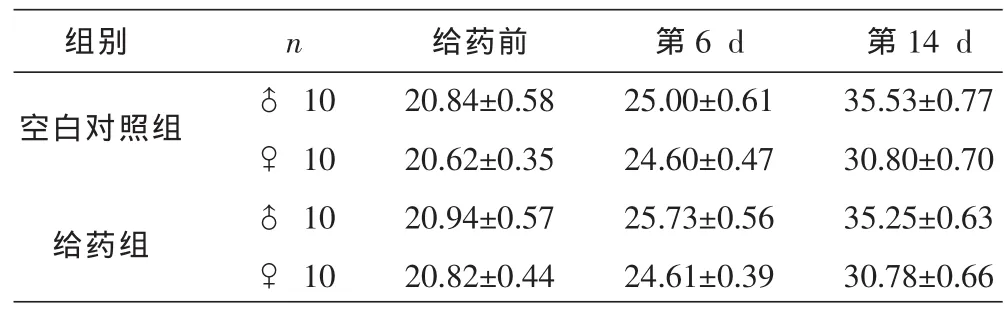
表1 给药后小鼠体质量的变化 (g)
3.2.3 对小鼠血液学指标的影响 对小鼠血液学指标的影响由表2可知,给药组小鼠血液学指标与对照组比较无显著性差异(P>0.05)。实验结果表明,密蒙花颗粒以最大耐受量灌胃给药对实验小鼠血液学指标变化无明显影响。
表2 两组小鼠血常规相关指标的比较 (±s)

表2 两组小鼠血常规相关指标的比较 (±s)
组别空白对照组给药组n♂10♀10♂10♀10 WBC/×109·L-12.19±1.36 2.08±0.36 1.48±0.51 2.10±0.86 RBC/×1012·L-16.89±0.12 8.04±0.37 7.55±0.47 8.02±0.37 HGB/g·L-1103.33±6.89 124.00±4.44 117.00±9.45 126.00±5.96 PLT 239±159.21 330±171.86 464.33±194 260±147.29 LYM%67.7±5.93 53.88±18.21 44.33±20.54 59.88±18.21
3.2.4 对小鼠重要脏器系数的影响 给药组肝体比值、脾体比值、肾体比值与对照组比较,差异均无统计学意义(P>0.05),见表 3,表明密蒙花颗粒对大鼠的脏器重量及脏器/体质量比值无明显影响。
表3 两组小鼠给药后肝脏、肾脏和脾脏与体质量的比值 (±s)

表3 两组小鼠给药后肝脏、肾脏和脾脏与体质量的比值 (±s)
组别n空白对照组给药组♂10♀10♂10♀10肝体比0.057 9±0.005 1 0.060 6±0.004 5 0.056 7±0.003 1 0.065 2±0.003 7脾体比0.007 2±0.001 9 0.003 9±0.000 6 0.003 9±0.000 4 0.004 5±0.000 9肾体比0.019 0±0.001 5 0.014 8±0.000 7 0.019 3±0.002 3 0.016 4±0.001 1
3.2.5 病理组织学检查 各组动物的脑、心、肝[10]、脾、肺、肾、卵巢、睾丸、胃、小肠、视网膜等脏器,肉眼观察均未见明显异常。部分脏器病理组织学切片镜下检查结果表明,给药组与对照组上述脏器均未见明显病变,详见图1-8。
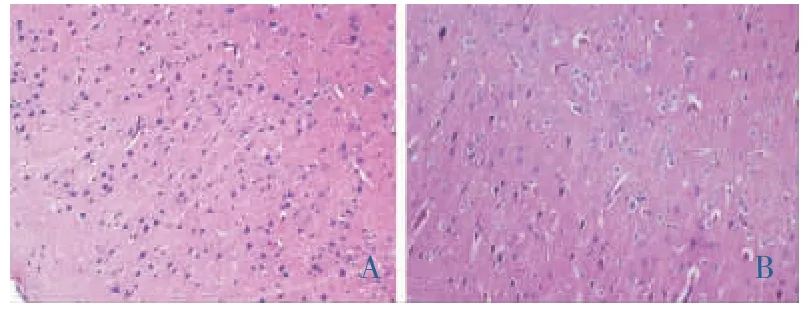
图1 小鼠急性毒性脑皮质组织病理变化(HE×400)
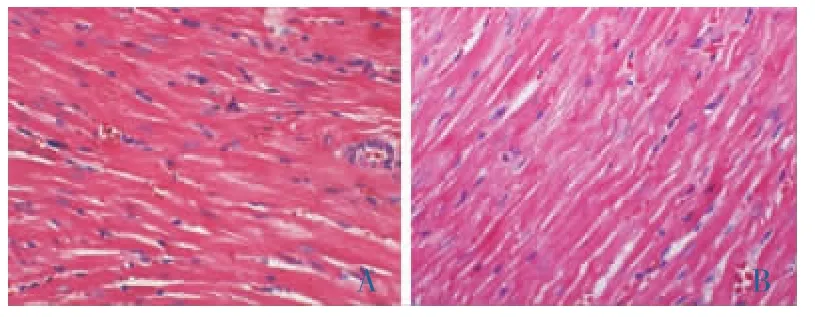
图2 小鼠急性毒性心组织病理变化(HE×400)
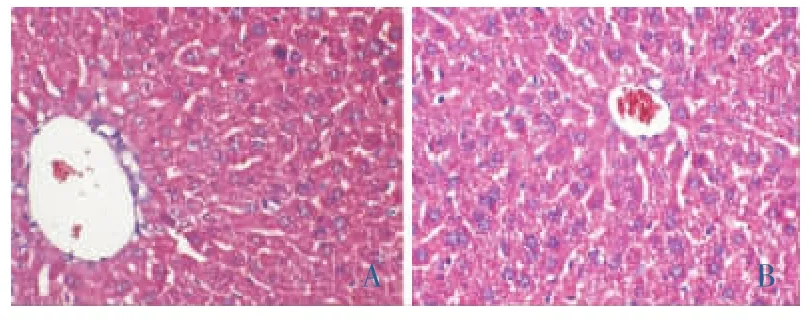
图3 小鼠急性毒性肝组织病理变化(HE×400)
4 讨论

图4 小鼠急性毒性脾组织病理变化(HE×400)
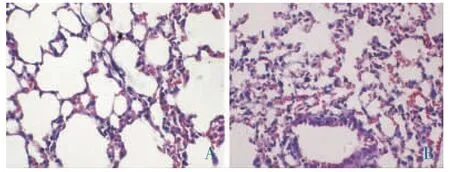
图5 小鼠急性毒性肺组织病理变化(HE×400)

图6 小鼠急性毒性肾组织病理变化(HE×400)
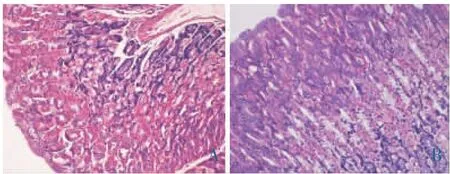
图7 小鼠急性毒性胃组织病理变化(HE×400)

图8 小鼠急性毒性视网膜组织病理变化(HE×400)
一般情况下,传统中药毒性很低,无法按常规方法测定LD50,故以最大给药量进行急毒实验。我们对密蒙花颗粒进行急性毒性试验,观察其对小鼠体质量的影响以及其对小鼠神经、胃肠、泌尿生殖、皮肤、毛及眼等的影响,给药后连续观察14 d,小鼠血液学指标及主要脏器指数与对照组比较无显著差异,主要脏器的病理组织学亦未见明显毒副反应。一般认为,按体质量计算,小鼠1日最大给药量相当于临床日用量的100倍以上则较为安全,可以提供临床研究试用[11]。本实验设计的小鼠日最大给药量为114 g/kg,相当于临床成人剂量的约317倍,本研究结果表明密蒙花颗粒毒性较小,在常规剂量下服用时安全可靠的。
[1]崔明超,欧阳强,潘金火.鸦胆子油亚纳米乳注射液的急性毒性及长期毒性实验[J].中国药师,2014,17(2):305-307.
[2]陈晓军,李燕婧,谭建宁.复方龙脷胶囊急性毒性实验研究[J].中国药师,2014,17(8):1414-1415.
[3]史传道,张荣强,张志刚,等.抗疏健骨颗粒急性毒性实验研究[J].实用中医药杂志,2016,32(6):521-522.
[4]赵 岩,妙志岩,郜玉钢,等.人参茸芝胶囊的急性毒性实验研究[J].食品安全质量检测学报,2015(2):614-618.
[5]李仪奎.中药药理实验方法学[M].2版.上海:上海科学技术出版社,2006:1001-1007.
[6]李飞艳,李福元,陈 斌,等.补肾温肺合剂的急性毒性实验研究[J].内蒙古中医药,2014,33(8):41-42.
[7]阳 敬,兰 慧,李安华,等.不同制备工艺的柴藿颗粒急性毒性实验比较研究[J].世界临床医学,2016,10(8):191-193.
[8]杜正彩,郝二伟,黄 庆,等.复方绞股蓝益智颗粒急性毒性与慢性毒性实验研究[J].当代医学,2012,18(19):1-3.
[9]王京霞,张 琦,陈 琳.复方大青颗粒急性毒性实验研究[J].浙江中西医结合杂志,2014(6):496-498.
[10]Olorunnisola O,Bradley G,Afolayan AJ.Acute and subchronic toxicity studiesof methanolic extract of Tulbaghia violacea rhizomes in Wistarrats.[J].Biotechnol,2012,11:14934-14940.
[11]谢秀琼.中药新制剂开发与应用[M].2版.北京:人民卫生出版社,2000:540.
(本文编辑 杨 瑛)
Acute Toxicity Test of Flos Buddlejae Granules
PENG Xiaofang,WANG Ying,QIN Genyan,ZHANG Youwei,PENG Jun,PENG Qinghua*
(Hunan University of Chinese Medicine,Changsha,Hunan 410208,China)
Objective To observe the acute toxic reaction of Flos Buddlejae granules and the situation of mice's death,to provide basis for the clinical safety of medication.Methods Having preliminary experiment on thirty mice with different concentrationsofsuspension liquid.Therewasnomice'sdeath in 7 days,LD50could notbeen detcted.Therefore,the maximum tolerance (MTD)was measured.Forty mice were randomly divided into the medicated group and the control group.In line with the maximum volume of the mice,the maximal suspension concentration of the Flos Buddlejae granules and the distilled water were separately given twice daily.Keeping the observation for 14 days,and recording the general condition and body mass in mice every day.After 14 days,the mice were killed.The blood routine indexes,and the major organs indexes of liver,spleen,kidneys and so on,the change of anatomy and pathological histology were observed.ResultsTherewasnomicedeath in medicated group.Compared with thecontrolgroup,thebodyweightofmice in medicated group had no significant changes (P>0.05).The routine blood indexes in the medicated group were not significantly different (P>0.05).The maximum tolerance dose of Flos Buddlejae granules in mice was 114 g/kg daily.Conclusion The acute toxicity result shows that the clinical dose of Flos Buddlejae granules is safe.
Flos Buddlejae granules;acute toxicity test;median lethal dose;maximum of tolerance dose
R285.5;R965.3
A
10.3969/j.issn.1674-070X.2017.09.003
本文引用:彭晓芳,王 英,覃艮艳,张又玮,彭 俊,彭清华.密蒙花颗粒的急性毒性实验研究[J].湖南中医药大学学报,2017,37(9):931-934.
2017-04-01
国家自然科学基金面上资助项目(30772824,81574031);湖南省高层次卫生人才“225”工程培养项目资助;湖南省科技厅科研基金资助项目(2015SF2016-6);湖南省发展改革委科研基金资助项目(湘发改投资[2014]658号);长沙市科技计划重大专项(K1501014-31);湖南中医药大学研究生创新课题项目(2016CX19)。
彭晓芳,女,在读硕士研究生,研究方向:眼表疾病。
* 彭清华,男,二级教授,主任医师,博士研究生导师,E-mail:pqh410007@126.com。
